16. Elektrický proud v elektrolytech, plynech a ve vakuu
16. Elektrický proud v elektrolytech, plynech a ve vakuu
16. Elektrický proud v elektrolytech, plynech a ve vakuu
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>16.</strong> Elektrický <strong>proud</strong> v <strong>elektrolytech</strong>, <strong>plynech</strong> a <strong>ve</strong> <strong>vakuu</strong><br />
Kapaliny<br />
Kovy – – elektronová vodivost – pi prchodu <strong>proud</strong>u nedochází k chemickým<br />
zmnám ani k penosu látky.<br />
Kapaliny<br />
1) neelektrolyty – ne<strong>ve</strong>dou el. <strong>proud</strong> ( alkoholy, sacharidy, aldehydy, estery,<br />
vtšina kapalin v chemicky istém stavu)<br />
2) elektrolyty – – pi prchodu <strong>proud</strong>u dochází k chemickým<br />
zmnám i k penosu látky (vodné roztoky kyselin, solí a zásad, rozta<strong>ve</strong>né<br />
soli,…)<br />
Elektrolytická disociace – dj štpení polárních molekul elektrolytu na ionty pod vli<strong>ve</strong>m<br />
polárních molekul vody (rozpouštdla)<br />
Elektrolýza - dj usmrnného pohybu iont, k nmuž dojde po ponoení elektrod do<br />
elektrolytu. Ty na elektrodách odevzdají el. náboj, mní se v neutrální atomy i skupiny<br />
atom a vyluují se nebo reagují s materiálem elektrod nebo s elektrolytem.<br />
V-A charakteristika elektrolytu:<br />
I<br />
<br />
U r – rozkladné naptí<br />
<br />
U r<br />
U<br />
:<br />
Pozn. Na katod se vždy vyluuje vodík nebo kov.<br />
. Hmotnost m látky vylouené na elektrodách je pímo úmrná náboji, který prošel<br />
elektrolytem: m = A.Q = A.I.t , kde A je elektrochemický ekvivalent látky (pro danou látku<br />
konstantní)<br />
. Hmotnosti rzných prvk (nebo radikál) vylouených pi elektrolýze stejným nábojem<br />
jsou chemicky ekvivalentní (mohou se vzájemn zastupovat i beze zbytku sluovat).<br />
M m<br />
A = , kde F = 9,65.10 4 C.mol -1 , z je nábojové íslo iontu a pedstavuje poet<br />
F.<br />
z<br />
elektron nutných k vylouení jedné molekuly.<br />
Užití elektrolýzy:<br />
1) Chemické zdroje naptí<br />
Je-li kov <strong>ve</strong> styku s roztokem, vytváí se na rozhraní elektrická dvojvrstva (ionty kovu<br />
pecházejí do elektrolytu nebo se ionty elektrolytu vyluují na elektrod – naptí mezi<br />
povrchem kovu elektrody a obklopujícím elektrolytem je elektrolytický potenciál.<br />
Jeho absolutní hodnotu nelze urit. Urují se jen pomrné hodnoty (základní je<br />
vzhledem k dohodou stano<strong>ve</strong>né vodíkové elektrod s potenciálem oznaeným za<br />
nulový). Rznou kombinací elektrod a elektrolyt vznikne zdroj stejnosmrného<br />
naptí.<br />
a) galvanické lánky – primární (nelze je nabíjet, prchodem el. <strong>proud</strong>u se povrch<br />
elektrod pokrývá produkty elektrolýzy, mní se kvalita povrchu, vznikají nové dvojvrsty –<br />
polarizace elektrod. Pvodní naptí postupn klesá až na nulu (technickými úpravami lze<br />
vliv polarizace omezit)).<br />
P. Voltv lánek, Danielv lánek, suchý lánek (plochá baterie), plošný lánek,<br />
knoflíkový lánek,…
Primární lánky<br />
Nejjednodušší galvanický lánek se skládá z elektrolytu a dvou elektrod(1800<br />
Alessandro Volta ).<br />
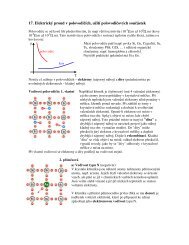
P.: Voltv lánek Zn - | H2S04 | Cu + : Elektrolytem je zedná kyselina sírová, kladná<br />
elektroda je z mdi a záporná elektroda je zinková. Elektromotorické naptí lánku<br />
je asi 1,1 V.<br />
Ponoením elektrod do elektrolytu se<br />
zinková elektroda zane rozpouštt a do<br />
elektrolytu se dostávají kladné ionty<br />
zinku. V elektrod zstanou volné<br />
elektrony a proto se zinková elektroda<br />
nabíjí záporn. M se v roztoku kyseliny<br />
rozpouští mén než zinek a proto je<br />
"mén záporná" než zinková elektroda -<br />
je vi ní kladná. Mezi obma elektrodami<br />
se objeví naptí o <strong>ve</strong>likosti 1,05 V.<br />
Jestliže pipojíme k elektrodám spotebi<br />
(nap. žárovku), pecházejí nadbytené<br />
elektrony ze zinkové elektrody pes<br />
spotebi k mdné elektrod a ást jejich<br />
energie se <strong>ve</strong> spotebii mní napíklad<br />
na svtlo nebo teplo. Obvodem zane procházet elektrický <strong>proud</strong>: <strong>ve</strong> vnjším obvodu<br />
je zpsoben pohybem volných elektron v kovových vodiích, v elektrolytu pohybem<br />
kladných a záporných iont. Na elektrodách pitom dochází k chemickým reakcím a<br />
jejich zplodiny by brzy pokryly povrch elektrod a lánek by se brzy znehodnotil. Tento<br />
nepíznivý jev se odstrauje depolarizátorem, který zabrauje usazování zplodin na<br />
elektrodách.<br />
Dalším píkladem primárního lánku je lánek Danielv Zn - | ZnSO4 | |CuSO4 | Cu + .<br />
Je tvoen dvma elektrodami, které jsou umístné v elektrolytu. Zinková<br />
elektroda je v roztoku ZnSO 4 , mdná v roztokuCuSO 4 . Oba roztoky jsou od<br />
sebe oddleny membránou, kterou mže procházet voda, náboje, ale nikoliv<br />
samotný roztok. Elektromotorické naptí je asi1,1 V.<br />
Nejpoužívanjší jsou tzv. suché lánky Leclanchéovy Zn - | NH4Cl (MnO2) | C +<br />
- kladnou elektrodou je uhlíková tyinka, zápornou je zinkový kalíšek, elektrolytem je<br />
pasta chloridu amonného a depolarizátorem sms oxidu manganiitého a grafitu.<br />
Naptí mezi elektrodami je 1,5V. Výkonnjší, ale dražší jsou lánky alkalické nebo<br />
rtuové. Potebujeme-li vtší naptí, spojujeme jednotlivé lánky sériov a vytvoíme z<br />
nich baterii lánk, napíklad bžná plochá baterie s naptím 4,5 V je tvoena temi<br />
sériov zapojenými lánky (4,5 V = 3 x 1,5 V).<br />
b) akumulátory – sekundární (lze je znovu nabíjet)<br />
P. Olovný akumulátor: V nabitém stavu aktivní hmotu záporné elektrody tvoí<br />
houbovité olovo (Pb), u kladné elektrody je to oxid oloviitý (PbO 2 ). Elektrolytem v<br />
olovných akumulátorech je vodou zedná kyselina sírová (H 2 SO 4 ) o koncentraci<br />
pibližn 35% u pln nabitého akumulátoru. Tento roztok mže být z technických<br />
dvod nasáknutý do vaty ze skelných vláken (AGM) nebo ztužený do formy gelu.<br />
Vybíjením se aktivní hmota záporné i kladné elektrody pemuje na síran olovnatý<br />
(PbSO 4 ) a elektrolyt je ochuzován o kyselinu sírovou a obohacován o vodu. Pi<br />
vybíjení tedy klesá koncentrace elektrolytu a naopak pi nabíjení jeho koncentrace<br />
roste.<br />
Chemické reakce pi nabíjení:<br />
Olovo se na vzduchu pokrývá vrstvou oxidu olovnatého PbO. Po ponoení do roztoku<br />
H 2 SO 4 dojde na obou elektrodách k reakci PbO + H 2 SO 4 PbSO 4 + H 2 O, takže se<br />
ob elektrody pokryjí vrstvou PbSO 4 . Uvážíme-li, že se elektrolytickou disociací
kyseliny sírové vytvoí <strong>ve</strong> vodném roztoku H 2 SO 4 ionty 2H + a SO 2- 4 , dojde pi<br />
nabíjení na jednotlivých elektrodách k následujícím reakcím (reakce jsou<br />
zjednodušené, nebo kationt H + nemže v roztoku existovat samostatn - vytváí tzv.<br />
oxoniový ion H 3 O + s molekulou vody, což skutené reakce komplikuje):<br />
anoda: PbSO 4 + SO 2- 4 - 2e - + 2H 2 O PbO 2 + 2H 2 SO 4<br />
katoda: PbSO 4 + 2H + + 2e - Pb + H 2 SO 4<br />
Jakmile se spotebuje všechen PbSO 4 na elektrodách, zane se vyluovat na katod<br />
vodík a na anod kyslík (akumulátor „vaí“).<br />
Chemické reakce pi vybíjení:<br />
K akumulátoru je pipojen spotebi. Reakce na elektrodách probíhají „opan“ než<br />
pi nabíjení.<br />
Pozn.: Naptí na jeden lánek olovného akumulátoru:<br />
minimální naptí - 1,75 V<br />
jmenovité naptí - 2 V<br />
(Jmenovité naptí, jinak též nominální naptí, je vhodn zvolená íselná<br />
hodnota naptí, která zastupuje skutenou hodnotu naptí, které nemá jednu<br />
konkrétní <strong>ve</strong>likost, ale nabývá hodnot z uritého ne<strong>ve</strong>lkého rozmezí.<br />
Jmenovité naptí je voleno uvnit tohoto rozmezí.)<br />
maximální naptí - 2,7 V teoreticky, 2,4 V prakticky<br />
Další akumulátory: oceloniklový (NiFe) akumulátor, niklkadmiový (NiCd)<br />
akumulátor,…<br />
2) Elektrometalurgie – získávání kov z roztok díky vyluování kov na katod pi<br />
elektrolýze<br />
3) Galvanostegie – pokovování<br />
4) Galvanoplastika – vytváení odlitk, matric,…<br />
5) Elektrolytické kondenzátory (dielektrikem je <strong>ve</strong>lmi tenká (10 -4 mm) vrstva nevodivého<br />
Al 2 O 3 )<br />
…<br />
Plyny<br />
Plyny jsou za normálních podmínek nevodie.<br />
Ionizace – dj, pi nmž se vnjším zásahem ionizátoru (plamen, rtg. záení, UV-záení,<br />
katodové záení, silné el. pole,…) z pvodn neutrálních atom a molekul tvoí elektricky<br />
nabité ástice.<br />
Vedení el. <strong>proud</strong>u v plynu – výboj.<br />
Výboj - (probíhá pouze za pítomnosti ionizátoru)<br />
- (trvá i po odstranní ionizátoru) – el. pole je tak silné, že se ionty samy<br />
pi své <strong>ve</strong>lké rychlosti stávají ionizaním inidlem – ionizace nárazem – lavinovitá<br />
ionizace (na tomto principu založen nap. Geiger-Müllerv poíta).<br />
V-A charakteristika výboje:<br />
I<br />
I n – nasycený <strong>proud</strong><br />
U z – zápalné naptí<br />
I n A B úsek OAB – nesamostatný výboj<br />
O U n U z U
Samostatný výboj v plynu:<br />
1. za normálních podmínek<br />
a) výboj – plynem prochází znaný <strong>proud</strong>vysoká teplota plynu i<br />
elektrod (až 6000 o C) pispívá k ionizaci nárazem (pozn. elektrody uhoívají –<br />
záporná pomaleji, zahrocuje se, v kladné se tvoí kráter).<br />
Užití: obloukové pece, obloukové svaování, osvtlovací výbojky – intenzivní<br />
zdroj svtla,…<br />
b) výboj – krátkodobý.<br />
Užití: elektrojiskrové obrábní (obrábná souástka – anoda), elektrické svíky<br />
v zážehových spalovacích motorech, v pírod blesk mezi mrakem a zemí nebo<br />
mezi dvma mraky (I 10kA až 30kA, U 10MV až 1GV),…<br />
c) (tichý) – malé hodnoty <strong>proud</strong>u – vznik v okolí hran,<br />
hrot, tenkých vodi (dosáhne-li el pole intenzity dostaující k ionizaci<br />
molekul)<br />
Užití (projevy): Elektrofiltry, Eliášovo svtlo, vysokonapová <strong>ve</strong>dení –<br />
nežádoucí (ztráty),…<br />
2. za sníženého tlaku<br />
v závislosti na tlaku vzduchu (plynu) v trubici se mní jeho vzhled i barva (pi<br />
poklesu tlaku z 10 5 Pa na 1Pa: er<strong>ve</strong>ný vlnící se pruh z anody – anodové svtlo<br />
vyplní trubici–zvrství se – odstoupí od katody – katodové svtlo (zelené).<br />
Katodové záení – vzniká <strong>ve</strong> výbojové trubici pi <strong>ve</strong>lmi nízkém tlaku (pod 2Pa) a dostaten<br />
vysokém naptí na elektrodách (ádov 10 4 V). Jedná se o tok elektron emitovaných pímo<br />
z kovu katody. Jeho základní vlastnosti:<br />
- šíí se pímoae, není-li pod vli<strong>ve</strong>m elektrického nebo magnetického pole<br />
- v elektrickém a magnetickém poli se vychyluje<br />
- zpsobuje pi interakci s nkterými látkami jejich zahívání a svtélkování; má<br />
chemické úinky<br />
- proniká <strong>ve</strong>lmi tenkými materiály a rozptyluje se<br />
- vyvolává rtg. záení, dopadá-li na kovové materiály s <strong>ve</strong>lkou relativní atomovou<br />
hmotností<br />
Užití katodového záení v obrazových elektronkách (osciloskopu, televizní obrazovce):<br />
Zdrojem katodového záení je rozžha<strong>ve</strong>né vlákno katody obklopené ídicí elektrodou<br />
(Wehneltovým válcem) s malým kruhovým otvorem. Jím vyletují elektrony v podob<br />
elektronového paprsku a jsou urychlovány el. polem mezi katodou a anodami.<br />
V osciloskopu se pak dvma páry vychylovacích destiek elektronový paprsek vychyluje<br />
<strong>ve</strong> svislém a vodorovném smru. Dopadem na stínítko obrazovky vyvolávají elektrony<br />
luminiscenní záení (stínítko je opateno vrstvou ZnS s nepatrným množstvím Ag). Zmnou<br />
hodnot naptí a polarity vychylovacích destiek se stopa paprsku pohybuje po stínítku –<br />
vzniká obraz nap. asových závislostí naptí nebo fyz. <strong>ve</strong>liin, které lze na naptí pevést.<br />
V televizní obrazovce se získaný demodulovaný a zesílený videosignál pivádí na ídicí<br />
elektrodu obrazovky, její potenciál se tím mní a dsledkem je mnící se tok a energie<br />
elektron dopadajících na stínítko. Elektronový paprsek je vychylován magnetickým polem<br />
dvojice vychylovacích cí<strong>ve</strong>k a pohybuje se po stínítku v ádcích (625 ádk se napisuje 25krát<br />
za sekundu).<br />
Pozn. barevná televize – kamera barevné televize obsahuje ti snímací optoelektrické mnie<br />
pro získání tí základních barevných signál obrazu (z nich se získává i signál jasový).<br />
Obrazovka barevné televize má pak ti zdroje elektron pro vytváení obrazu z jednotlivých<br />
barevných složek na stínítku pokrytém luminofory záícími pi dopadu elektron svtly<br />
základních barev (míšením tchto barev se získá libovolná barva libovolné intenzity).