Elektrochemische Thermodynamik
Elektrochemische Thermodynamik
Elektrochemische Thermodynamik
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Thermodynamik</strong><br />
(1)<br />
(2)<br />
(1-2)<br />
Pt, H<br />
Pt, H<br />
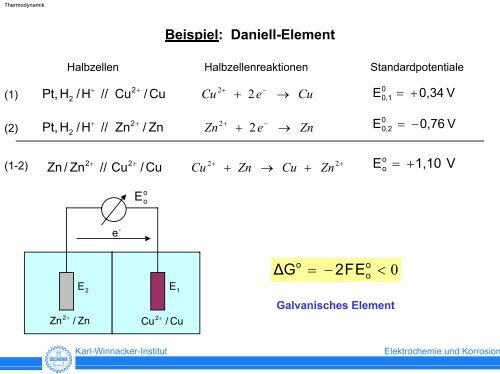
Beispiel: Daniell-Element<br />
Halbzellen Halbzellenreaktionen Standardpotentiale<br />
2<br />
2<br />
/ H<br />
/ H<br />
Zn / Zn<br />
Zn 2+<br />
E2<br />
/ Zn<br />
+<br />
+<br />
//<br />
//<br />
//<br />
Cu<br />
Zn<br />
Cu<br />
2+<br />
2+<br />
2 + 2+<br />
-<br />
e<br />
/ Cu<br />
/ Zn<br />
/ Cu<br />
o<br />
Eo<br />
E1<br />
Cu / Cu<br />
2+<br />
Cu<br />
2+<br />
−<br />
Cu + 2e<br />
→<br />
2+<br />
−<br />
Zn + 2e<br />
→<br />
2+<br />
+<br />
Zn<br />
→<br />
Cu<br />
∆G<br />
+ 0,34 V<br />
Karl-Winnacker-Institut Elektrochemie und Korrosion<br />
Cu<br />
o<br />
Zn<br />
+<br />
=<br />
Zn<br />
−<br />
2+<br />
2FE<br />
o<br />
o<br />
E 0<br />
0,1<br />
E 0<br />
0,2<br />
E o<br />
o<br />
<<br />
Galvanisches Element<br />
=<br />
0<br />
=<br />
=<br />
−0,76<br />
V<br />
+ 1,10<br />
V