Hereditäre Tubulopathien mit Diuretika-ähnlichem Salzverlust
Hereditäre Tubulopathien mit Diuretika-ähnlichem Salzverlust
Hereditäre Tubulopathien mit Diuretika-ähnlichem Salzverlust
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
M E D I Z I N<br />
AKTUELL<br />
kum Infektionskrankheiten maskieren<br />
kann. Zusätzlich zur Therapie <strong>mit</strong><br />
COX-Inhibitoren ist in jedem Lebensalter<br />
auf eine ausreichende Flüssigkeitszufuhr<br />
und Elektrolytsubstitution<br />
<strong>mit</strong> NaCl und gegebenenfalls auch KCl<br />
zu achten. In der Dauerbetreuung der<br />
FSLT-Patienten sind mindestens halbjährliche<br />
Verlaufskontrollen zur Therapieüberwachung<br />
(unter anderem renale<br />
Prostaglandin-Ausscheidung<br />
und Indometacin-Serumspiegel)<br />
erfor-<br />
Grafik 2<br />
derlich (49). Da die Nebenwirkungen<br />
einer lebenslangen<br />
Indometacinbehandlung,<br />
insbesondere<br />
in Hinsicht auf eine Analgetika-Nephropathie,<br />
bei<br />
FSLT-Patienten bisher<br />
nicht bekannt sind, sollte<br />
die Indometacindosis so<br />
niedrig wie möglich liegen<br />
und regelmäßig den individuellen<br />
Bedürfnissen angepaßt<br />
werden.<br />
Die Prognose einer<br />
FSLT hängt derzeit wesentlich<br />
vom Grad der<br />
Frühgeburtlichkeit und<br />
von der Optimierung des<br />
perinatalen Managements<br />
ab. Postpartale Entgleisungen<br />
des Salz- und Wasserhaushalts<br />
sowie allgemeine<br />
Probleme der extremen<br />
Frühgeburtlichkeit<br />
sind wahrscheinliche<br />
Ursachen für eine psychomotorische<br />
Retardierung<br />
bei einigen FSLT-Patienten<br />
(46, 47, 49). Bei Jugendlichen<br />
und jungen Erwachsenen<br />
wurde vereinzelt<br />
über eine chronisch<br />
progrediente Niereninsuffizienz<br />
berichtet (2, 46, 60). Dabei<br />
bleibt allerdings unklar, ob diese durch<br />
die Langzeitbehandlung <strong>mit</strong> COX-<br />
Inhibitoren oder primär durch die<br />
Grunderkrankung verursacht wurde.<br />
Thiazid-Typ<br />
Prävention<br />
eines Hypotonus<br />
Der Thiazid-Typ (TSLT: Thiazide-like<br />
salt-losing tubulopathy) ist<br />
bisher unter den Bezeichnungen<br />
Gitelman-Syndrom, Hypokalziurisches<br />
Bartter-Syndrom oder familiäre<br />
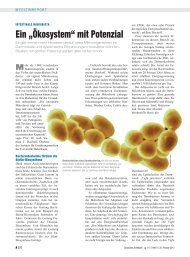
Tubulärer Transportdefekt (NKCC2/ROMK)<br />
Verminderte Reabsorption von Chlorid, Natrium, Kalzium<br />
<strong>Salzverlust</strong><br />
TGF<br />
Volumenkontraktion<br />
Abfall von<br />
GFR RBF<br />
PGE 2<br />
Renin-Angiotensin-Aldosteron<br />
Korrektur der<br />
Hyponatriämie<br />
Hyperkaliurie<br />
Hypokaliämie<br />
Isosthenurie<br />
„ADH-Antagonist“<br />
hypokaliämische Hypomagnesiämie<br />
bekannt (Tabelle 1) (18, 42, 44, 59). Im<br />
Gegensatz zur FSLT wird die Erkrankung<br />
häufig erst im späten Kindesoder<br />
frühen Erwachsenenalter diagnostiziert<br />
und zeigt in der Regel einen<br />
milderen Verlauf. Die Patienten<br />
fallen durch Müdigkeit, Obstipation,<br />
Muskelschwäche oder -krämpfe, Gelenkbeschwerden<br />
(Chondrokalzinose)<br />
und gelegentlich durch einen Minderwuchs<br />
auf (49, 56). In anderen Fällen<br />
wird die Diagnose beispielsweise<br />
bei einer präoperativen Elektrolyt-<br />
Bestimmung oder im Rahmen einer<br />
Enuresis-Abklärung gestellt. Die typische<br />
Konstellation von Laborparametern<br />
liegt jedoch bereits im Säuglingsalter<br />
vor (Tabelle 2). Bei nur<br />
leichtem renalem Kochsalzverlust ist<br />
die tubuläre Konzentrationsfähigkeit<br />
fast vollständig erhalten. Die Diurese<br />
ist nur mäßig erhöht oder sogar normal.<br />
Pathognomonisch ist eine Hypokalziurie<br />
(< 0,1 mol/mol Kreatinin) in<br />
Kombination <strong>mit</strong> einer hypermagnesiurischen<br />
Hypomagnesiämie (5, 49).<br />
Letztere ist für das Auftreten muskulärer<br />
Symptome verantwortlich,<br />
kann aber selbst bei sehr niedrigen Serumkonzentrationen<br />
(Mg ++ ✜ 0,3<br />
mmol/l) asymptomatisch bleiben.<br />
Ähnlich wie bei der FSLT findet man<br />
auch hier eine sekundäre hypokaliämische<br />
Alkalose als Zeichen<br />
einer Stimulation<br />
des Renin-Angiotensin-<br />
Aldosteron-Systems. Dagegen<br />
ist die renale Prostaglandinexkretion<br />
bei<br />
der TSLT häufig nur<br />
leicht oder mäßig erhöht<br />
(19, 35).<br />
Als primärer Defekt<br />
konnten bei Patienten<br />
<strong>mit</strong> TSLT verschiedene<br />
Mutationen im Thiazidsensitiven<br />
Na + -Cl - -Kotransporter<br />
(NCCT-Gen<br />
auf Chromosom 16q13)<br />
identifiziert werden (55).<br />
Diese gehen <strong>mit</strong> einer gestörten<br />
Kochsalzresorption<br />
im distalen Tubulus<br />
einher. Im Detail basiert<br />
dieser epitheliale Transport<br />
auf folgenden Mechanismen<br />
(Grafik 3).<br />
Ähnlich wie in den<br />
übrigen Tubulusabschnitten<br />
hält die basolaterale<br />
Na + -K + -ATPase die intrazelluläre<br />
Na + -Konzentration<br />
niedrig und trägt<br />
zur Aufrechterhaltung des<br />
Membranpotentials bei.<br />
Nephrokalzinose<br />
Hyposthenurie<br />
Schematische Darstellung der pathophysiologischen Abläufe bei der FSLT. TGF: tubuloglomeruläres<br />
Feedback; GFR: glomeruläre Filtrationsrate; RBF: renaler Blutfluß; ADH:<br />
antidiuretisches Hormon.<br />
Der elektrochemische<br />
Gradient für Natrium von<br />
extra- nach intrazellulär<br />
ist wiederum Antriebskraft<br />
für die luminale Kochsalzaufnahme<br />
durch den Thiazid-sensitiven Na + -<br />
Cl - -Kotransporter (20). Ein Defekt<br />
dieses Kotransporters resultiert nicht<br />
nur in einer verminderten NaCl-Resorption,<br />
sondern immer auch in einer<br />
gesteigerten Kalziumresorption (16).<br />
Anders als in der Henleschen Schleife<br />
erfolgt die Kalziumresorption im distalen<br />
Tubulus transzellulär (Grafik 3).<br />
Kalzium strömt durch spannungsabhängige<br />
Ca ++ -Kanäle aus dem Lumen<br />
in die Zelle und wird basolateral im<br />
Austausch gegen Natrium in das Inter-<br />
A-1844<br />
(36) Deutsches Ärzteblatt 95, Heft 30, 24. Juli 1998