7.3.6: 4-Methoxysalicylaldehyd
7.3.6: 4-Methoxysalicylaldehyd
7.3.6: 4-Methoxysalicylaldehyd
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
7. Substitutionen an Aromaten und Heterocyclen www.ioc-praktikum.de<br />
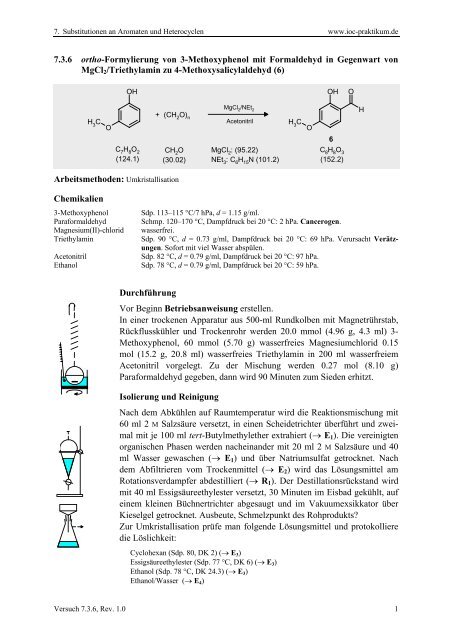
<strong>7.3.6</strong> ortho-Formylierung von 3-Methoxyphenol mit Formaldehyd in Gegenwart von<br />
MgCl 2 /Triethylamin zu 4-<strong>Methoxysalicylaldehyd</strong> (6)<br />
OH<br />
OH<br />
O<br />
C H 3<br />
O<br />
C 7<br />
H 8<br />
O 2<br />
(124.1)<br />
+ (CH 2<br />
O) n<br />
CH 2<br />
O<br />
(30.02)<br />
MgCl 2<br />
/NEt 2<br />
Acetonitril<br />
MgCl 2<br />
: (95.22)<br />
NEt 3<br />
: C 6<br />
H 15<br />
N (101.2)<br />
C H 3<br />
O<br />
6<br />
C 8<br />
H 8<br />
O 3<br />
(152.2)<br />
H<br />
Arbeitsmethoden: Umkristallisation<br />
Chemikalien<br />
3-Methoxyphenol<br />
Paraformaldehyd<br />
Magnesium(II)-chlorid<br />
Triethylamin<br />
Acetonitril<br />
Ethanol<br />
Sdp. 113–115 °C/7 hPa, d = 1.15 g/ml.<br />
Schmp. 120–170 °C, Dampfdruck bei 20 °C: 2 hPa. Cancerogen.<br />
wasserfrei.<br />
Sdp. 90 °C, d = 0.73 g/ml, Dampfdruck bei 20 °C: 69 hPa. Verursacht Verätzungen.<br />
Sofort mit viel Wasser abspülen.<br />
Sdp. 82 °C, d = 0.79 g/ml, Dampfdruck bei 20 °C: 97 hPa.<br />
Sdp. 78 °C, d = 0.79 g/ml, Dampfdruck bei 20 °C: 59 hPa.<br />
Durchführung<br />
Vor Beginn Betriebsanweisung erstellen.<br />
In einer trockenen Apparatur aus 500-ml Rundkolben mit Magnetrührstab,<br />
Rückflusskühler und Trockenrohr werden 20.0 mmol (4.96 g, 4.3 ml) 3-<br />
Methoxyphenol, 60 mmol (5.70 g) wasserfreies Magnesiumchlorid 0.15<br />
mol (15.2 g, 20.8 ml) wasserfreies Triethylamin in 200 ml wasserfreiem<br />
Acetonitril vorgelegt. Zu der Mischung werden 0.27 mol (8.10 g)<br />
Paraformaldehyd gegeben, dann wird 90 Minuten zum Sieden erhitzt.<br />
Isolierung und Reinigung<br />
Nach dem Abkühlen auf Raumtemperatur wird die Reaktionsmischung mit<br />
60 ml 2 M Salzsäure versetzt, in einen Scheidetrichter überführt und zweimal<br />
mit je 100 ml tert-Butylmethylether extrahiert (→ E 1 ). Die vereinigten<br />
organischen Phasen werden nacheinander mit 20 ml 2 M Salzsäure und 40<br />
ml Wasser gewaschen (→ E 1 ) und über Natriumsulfat getrocknet. Nach<br />
dem Abfiltrieren vom Trockenmittel (→ E 2 ) wird das Lösungsmittel am<br />
Rotationsverdampfer abdestilliert (→ R 1 ). Der Destillationsrückstand wird<br />
mit 40 ml Essigsäureethylester versetzt, 30 Minuten im Eisbad gekühlt, auf<br />
einem kleinen Büchnertrichter abgesaugt und im Vakuumexsikkator über<br />
Kieselgel getrocknet. Ausbeute, Schmelzpunkt des Rohprodukts?<br />
Zur Umkristallisation prüfe man folgende Lösungsmittel und protokolliere<br />
die Löslichkeit:<br />
Cyclohexan (Sdp. 80, DK 2) (→ E 3 )<br />
Essigsäureethylester (Sdp. 77 °C, DK 6) (→ E 3 )<br />
Ethanol (Sdp. 78 °C, DK 24.3) (→ E 3 )<br />
Ethanol/Wasser (→ E 4 )<br />
Versuch <strong>7.3.6</strong>, Rev. 1.0 1
7. Substitutionen an Aromaten und Heterocyclen www.ioc-praktikum.de<br />
Das Rohprodukt unter leichtem Erwärmen (Badtemperatur 40 °C) in etwa 5<br />
ml Ethanol gelöst. Nach Zugabe von 2 ml Wasser wird langsam auf Raumtemperatur<br />
abgekühlt und der verschlossene Kolben über Nacht zur<br />
Kristallisation in den Kühlschrank gestellt. Das kristalline Produkt wird auf<br />
einem Hirschtrichter abgesaugt, mit ca. 2 ml eiskaltem 50-proz. wässrigen<br />
Ethanol nachgewaschen (Mutterlauge → E 4 ) und im Vakuumexsikkator<br />
über Silicagel getrocknet. Man bestimme Ausbeute und Schmelzpunkt der<br />
reinen Verbindung. Ausbeute an 6: 55–60%, Schmp. 42–43 °C.<br />
Hinweise zur Entsorgung (E), Recycling (R) der Lösungsmittel<br />
E 1 : Wässrige Phasen: Neutralisation mit Natronlauge → Entsorgung (H 2 O mit RHal/Halogenid).<br />
E 2 : Trockenmittel → Entsorgung (Anorg. Feststoffe).<br />
E 3 : Wasserfreie Mutterlaugen → Entsorgung (RH).<br />
E 4 : Wässrige Mutterlauge → Entsorgung (H 2 O mit RH).<br />
R 1 : Abdestilliertes Lösungsmittel → Recycling (tert-Butylmethylether).<br />
Auswertung des Versuchs<br />
1 H-NMR-Spektrum von 6 (300 MHz, CDCl 3 ): δ = 3.85 (3 H), 6.42 (1 H), 6.54 (1 H), 7.43 (1 H), 9.71 (1 H),<br />
11.49 (1 H).<br />
LM<br />
7.5 7.0<br />
6.5<br />
12.0 10.0<br />
8.0<br />
6.0<br />
4.0 2.0 [ppm] 0.0<br />
13 C-NMR Spektrum von 6 (75.5 MHz, CDCl 3 ): δ = 55.72 (CH 3 ), 110.65 (CH), 108.38 (CH), 115.16 (C),<br />
135.27 (CH), 164.51 (C), 166.83 (C), 194,42 (CH).<br />
LM<br />
200 180 160 140<br />
120<br />
100<br />
80<br />
60 40 20 [ppm] 0<br />
Versuch <strong>7.3.6</strong>, Rev. 1.0 2
7. Substitutionen an Aromaten und Heterocyclen www.ioc-praktikum.de<br />
IR-Spektrum von 6 (KBr):<br />
100<br />
T [%]<br />
50<br />
2844<br />
1505<br />
1575<br />
1650<br />
1635<br />
0<br />
~<br />
4000 3000 2000 1500 1000 ν [cm -1 ]<br />
* Formulieren Sie den zu 6 führenden Reaktionsmechanismus (Siehe auch Einführung zu Kap. 7.3).<br />
Weitere denkbare Reaktionsprodukte:<br />
OH<br />
OH<br />
OH<br />
H<br />
H<br />
H<br />
H<br />
CH 2<br />
OH<br />
HOCH 2<br />
O<br />
OH<br />
O<br />
O<br />
MeO<br />
MeO<br />
CH 2<br />
OH<br />
MeO<br />
MeO<br />
MeO<br />
OMe<br />
A B C D E<br />
* Mit welchen spektroskopischen Daten und einfachen Versuchen lassen sich A–E ausschließen?<br />
* Diskutieren Sie die denkbaren Reaktionsmechanismen.<br />
Literatur, allgemeine Anwendbarkeit der Methode<br />
Diese Methode erlaubt die selektive ortho-Formylierung einer Vielzahl substituierter Phenole (z.B. 2-Naphthol,<br />
2-, 3- und 4-Alkylphenol, 2-, 3- und 4-Chlorphenol).<br />
[1] N.U. Hofslǿken, L. Skattebǿl, Acta Chem. Scand. 1999, 53, 258–262.<br />
Versuch <strong>7.3.6</strong>, Rev. 1.0 3