Lösung Aufgabe 6.2.2 ”Otto-Prozess” 1 − 2 isentrope Kompression ...
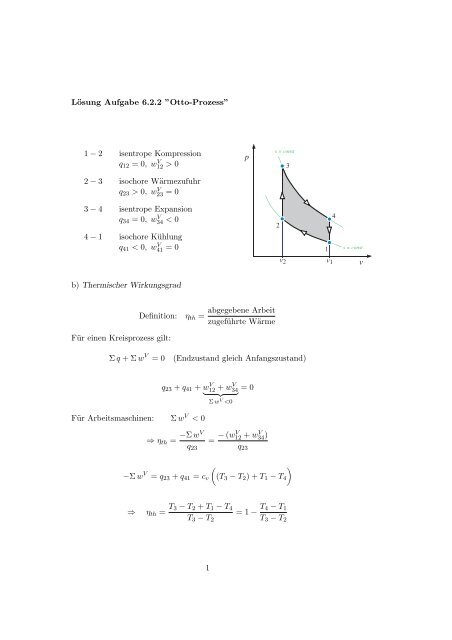
Lösung Aufgabe 6.2.2 ”Otto-Prozess” 1 − 2 isentrope Kompression ...
Lösung Aufgabe 6.2.2 ”Otto-Prozess” 1 − 2 isentrope Kompression ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Lösung</strong> <strong>Aufgabe</strong> <strong>6.2.2</strong> <strong>”Otto</strong>-<strong>Prozess”</strong><br />
1 <strong>−</strong> 2 <strong>isentrope</strong> <strong>Kompression</strong><br />
q 12 = 0, w V 12 > 0<br />
2 <strong>−</strong> 3 isochore Wärmezufuhr<br />
q 23 > 0, w V 23 = 0<br />
3 <strong>−</strong> 4 <strong>isentrope</strong> Expansion<br />
q 34 = 0, w V 34 < 0<br />
4 <strong>−</strong> 1 isochore Kühlung<br />
q 41 < 0, w V 41 = 0<br />
p<br />
s = const<br />
3<br />
4<br />
2<br />
1 s = const<br />
v 2 v 1 v<br />
b) Thermischer Wirkungsgrad<br />
Definition:<br />
η th =<br />
abgegebene Arbeit<br />
zugeführte Wärme<br />
Für einen Kreisprozess gilt:<br />
Σ q + Σ w V = 0<br />
(Endzustand gleich Anfangszustand)<br />
Für Arbeitsmaschinen: Σ w V < 0<br />
q 23 + q 41 + w12 V + w34<br />
V = 0<br />
} {{ }<br />
Σ w V
Isentrope <strong>Kompression</strong>, ideales Gas: T 2 /T 1 = ( V 1 /V 2 ) κ<strong>−</strong>1 = ε n<strong>−</strong>1<br />
} {{ }<br />
ε<br />
Isentrope Expansion, ideales Gas: T 3 /T 4 = ( V 4 /V 3 ) κ<strong>−</strong>1 = ε n<strong>−</strong>1<br />
} {{ }<br />
ε<br />
Eingesetzt:<br />
η th = 1 <strong>−</strong><br />
T 4 <strong>−</strong> T 1<br />
(T 4 <strong>−</strong> T 1 )ε κ<strong>−</strong>1 = 1 <strong>−</strong> 1<br />
ε κ<strong>−</strong>1 mit κ = c p<br />
,<br />
c v<br />
c p <strong>−</strong> c v = R L<br />
Zahlenwert: Mit κ =<br />
c p<br />
c p <strong>−</strong> R L<br />
= 1, 4 folgt η th = 0, 5902<br />
c) Abgegebene spezifische Nettoarbeit<br />
<strong>−</strong>Σ w v = η th q 23<br />
Zahlenwert:<br />
<strong>−</strong>Σ w v = 0, 5902 · 1400 kJ kJ<br />
= 826, 28<br />
kg kg<br />
e) Modifizierter Prozess<br />
q 2 ∗ 3 ∗ = u 3 ∗ <strong>−</strong> u 2 ∗, wV 2 ∗ 3 ∗ = 0<br />
= c v (ϑ 3 ∗ <strong>−</strong> ϑ 2 ∗)<br />
p<br />
ϑ 3 ∗ = ϑ 2 ∗ + q 23<br />
c v<br />
Isentrope Zustandsänderung:<br />
( )<br />
T 2 ∗<br />
κ<strong>−</strong>1 ( ) κ<strong>−</strong>1<br />
V1 V1<br />
=<br />
=<br />
T 1 V 2 ∗ αV 2<br />
( ) ε κ<strong>−</strong>1<br />
= = (ε ∗ ) κ<strong>−</strong>1<br />
α<br />
s = const<br />
3*<br />
4*<br />
2<br />
2*<br />
1 s = const<br />
v 2 v 1 v<br />
2
Zahlenwerte:<br />
ε ∗ = 6, 643<br />
⇒ T 2 ∗ = T 1 ε ∗(κ<strong>−</strong>1) = 298, 15 K 6, 643 0,4 = 635, 89 K<br />
T 3 ∗ = T 2 ∗ + q 23<br />
c v<br />
= 2587, 11 K (c v = c p<br />
κ )<br />
T 2 = T 1 ε κ<strong>−</strong>1 = 747, 48 K<br />
T 3 = 2678, 71 K<br />
⇒ T 3 ∗ <strong>−</strong> T 3 = <strong>−</strong>91, 60 K<br />
f) Thermischer Wirkungsgrad des mod. Prozesses<br />
η th = 1 <strong>−</strong><br />
1<br />
(ε ∗ = 0, 5311<br />
) κ<strong>−</strong>1<br />
3