Destillation und Rektifikation Teil 2 (detaillierter) - Institut für ...
Destillation und Rektifikation Teil 2 (detaillierter) - Institut für ...
Destillation und Rektifikation Teil 2 (detaillierter) - Institut für ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Destillation</strong> <strong>und</strong> <strong>Rektifikation</strong>: Zusammenfassung des zweiten <strong>Teil</strong>s<br />
Allgemeine Bemerkung zu den Berechnungen <strong>und</strong> Ableitungen der Formeln: Die Vorgänge werden in<br />
der Regel für ideale Zustände beschrieben <strong>und</strong> abgeleitet. Die realen Verhältnisse werden später<br />
bzw. in der Praxis üblicherweise mit Hilfe von Korrekturformeln <strong>und</strong> -termen für Realität in die<br />
Beschreibung eingeführt, wie typischerweise beim Aktivitätskoeffizient.<br />
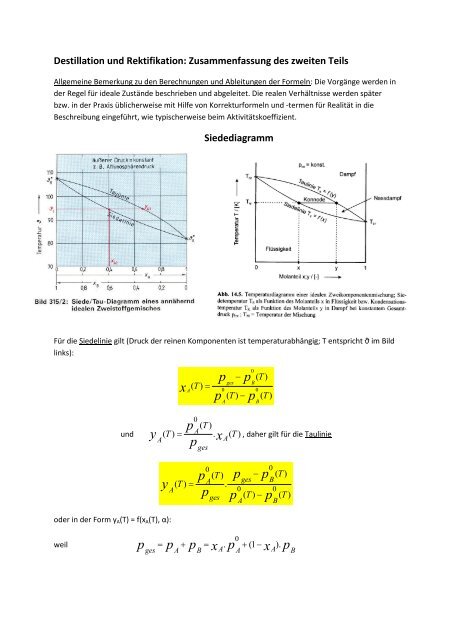
Siedediagramm<br />
Für die Siedelinie gilt (Druck der reinen Komponenten ist temperaturabhängig; T entspricht ϑ im Bild<br />
links):<br />
x<br />
A<br />
p<br />
p<br />
0<br />
p<br />
p<br />
− ( T)<br />
ges B<br />
( T)<br />
=<br />
0<br />
0<br />
( T)<br />
− ( T)<br />
A<br />
0<br />
p ( T )<br />
<strong>und</strong> y ( T ) = A . x ( T ) , daher gilt für die Taulinie<br />
A<br />
A<br />
pges<br />
B<br />
y<br />
A<br />
( T ) =<br />
0<br />
p<br />
p<br />
A<br />
( T)<br />
.<br />
ges<br />
p<br />
p<br />
ges<br />
0<br />
A<br />
−<br />
( T ) −<br />
p<br />
0<br />
B<br />
0<br />
p<br />
( T)<br />
B<br />
( T )<br />
oder in der Form y A (T) = f(x A (T), α):<br />
weil<br />
p<br />
ges<br />
=<br />
p<br />
A<br />
+<br />
p<br />
B<br />
=<br />
x<br />
A<br />
.<br />
p<br />
0<br />
A<br />
+ (1 −<br />
x<br />
A<br />
).<br />
p<br />
B
ist<br />
y<br />
A<br />
( T )<br />
x<br />
A<br />
p<br />
0<br />
=<br />
A , <strong>und</strong> da<br />
0<br />
0<br />
xA<br />
p + (1 − x ).<br />
A p<br />
A<br />
B<br />
p<br />
p<br />
0<br />
( T)<br />
α =<br />
A (Trennfaktor), gilt für die Taulinie<br />
0<br />
( T)<br />
B<br />
y<br />
α ⋅x<br />
A<br />
1+<br />
x ⋅<br />
A ( α −1)<br />
( T ) =<br />
wobei der Trennfaktor α auch von der Temperatur (wenig) <strong>und</strong> vom<br />
A<br />
Druck (viel) abhängig ist. Diese Form eignet sich für die Darstellung im Zusammensetzungsdiagramm<br />
(auch genannt Gleichgewichtsdiagramm), y = f(x):<br />
McCabe-Thiele-Diagramm (Zusammensetzungs- oder Gleichgewichtsdiagramm)<br />
Bei idealen Mischungen ist die<br />
Kurve y = f(x) eine Hyperbel, bei<br />
realen Mischungen kann sie fast<br />
beliebige Formen annehmen,<br />
abhängig von den konkreten<br />
Komponenten. Die Dampfphase<br />
ist im Normalfall an der<br />
leichterflüchtigen Komponente<br />
angereichert. Je größer ist die<br />
relative Flüchtigkeit<br />
(Trennfaktor), desto höher ist<br />
der Gehalt an der<br />
leichterflüchtigen Komponente<br />
in der Dampfphase bei<br />
gegebenem x, <strong>und</strong> desto besser (vollständiger) läuft die Trennung. Bei α = 1 erfolgt keine Trennung,<br />
da die Zusammensetzung der flüssigen <strong>und</strong> der gasförmigen Phase gleich ist. Dies ist z.B. der Fall bei<br />
realen Mischungen, wenn die Zusammensetzung einem Azeotrop entspricht.<br />
Umgekehrt, bei bekannten x A <strong>und</strong> y A ist der Trennfaktor α :<br />
α =<br />
y<br />
x<br />
A<br />
A<br />
(1−<br />
x<br />
(1−<br />
y<br />
⋅<br />
⋅<br />
A<br />
A<br />
)<br />
)<br />
<strong>Destillation</strong> binärer Gemische, das Hebelgesetz:<br />
Im Dampfdruckdiagramm, P = f(x), oder im Siedediagramm, T = g(x)<br />
Konnode ist eine Verbindungslinie zwischen zwei übereinstimmenden Zuständen, siedende<br />
Flüssigkeit <strong>und</strong> kondensierender Dampf; verläuft im Dampfdruck-oder Siedediagramm horizontal <strong>und</strong><br />
entspricht einer Isobare bzw. einer Isoterme.<br />
Das Hebelgesetz im Siedediagramm: Bei Temperatur über der Taulinie existiert nur Dampf, bei<br />
Temperatur unter der Siedelinie (fast) nur Flüssigkeit. Beim Entspannen (oder Erhitzen) der
Flüssigkeit oder beim Komprimieren (oder Abkühlen) des Dampfes zerfällt die Mischung zwischen der<br />
Siede- <strong>und</strong> Taulinie in die flüssige <strong>und</strong> gasförmige Phase (der Nassdampfbereich). Der Zustandspunkt<br />
(P) unterteilt die durch ihn verlaufende Konnode in zwei Äste, deren Längen im gleichen Verhältnis<br />
zueinander stehen wie die molaren Anteile der Flüssigkeit <strong>und</strong> des Dampfs. Je näher der Mischpunkt<br />
P zur Taulinie kommt, desto mehr Dampf <strong>und</strong> weniger Flüssigkeit liegt im Zweiphasengemisch vor.<br />
Wird auf der Siedelinie Gasphase isobar entfernt, steigt die Temperatur, das System siedet <strong>und</strong> x A,0<br />
wandert auf der Siedelinie in Richtung der schwererflüchtigen Komponente. Jedem x A,i entspricht die<br />
Zusammensetzung der Gasphase y A,i .<br />
P<br />
Molverhältnis in der Gas- <strong>und</strong> Flüssigkeitsphase:<br />
n<br />
n<br />
g<br />
l<br />
=<br />
x<br />
y<br />
−<br />
A,0<br />
−<br />
A,1<br />
x<br />
x<br />
A,1<br />
A,0<br />
=<br />
a<br />
b<br />
x A,0<br />
Gesamtzusammensetzung, n 0 = n l + n g<br />
x A,1 , y A,1<br />
Zusammensetzung n l <strong>und</strong> n g<br />
(Ableitung: n 0 = n l + n g ; n 0 *x A,0 = n l *x A,1 + n g *y A,1 ; n l *(x A,0 – x A,1 ) = n g *(y A,1 – x A,0 ))<br />
( (a) (b) )
Azeotropie: reale Gemische<br />
0<br />
p A = γ A * x A * p A<br />
Positive Abweichung des Aktivitätskoeffizienten γ -> Siedetemperaturminimum, Minimumazeotrop<br />
Dampfdruck der azeotropen Mischung > Dampfdruck der leichterflüchtigen Komponente<br />
Beispiel: EtOH+Wasser, Isopropanol+Isopropylether<br />
Negative Abweichung des Aktivitätskoeffizienten γ -> Siedetemperaturmaximum, Maximumazeotrop<br />
Dampfdruck der azeotropen Mischung < Dampfdruck der schwererflüchtigen Komponente<br />
Beispiel: Chloroform+Aceton, Wasser+HNO 3
Trennung der Azeotrope:<br />
- Druckänderung (Druckerniedrigung): der azeotrope Punkt wird verschoben<br />
- Extraktive <strong>Rektifikation</strong>: Zugabe einer schwerflüchtigen Komponente verschiebt die<br />
Aktivitätskoeffiziente <strong>und</strong> damit den azeotropen Punkt. Der Hilfsstoff bildet meist selbst ein<br />
azeotropes Gemisch mit einer der Mischungskomponenten, <strong>und</strong> lässt die zweite<br />
Komponente leicht abdestillieren, da ihr Trennfaktor steigt. Die Hilfsstoffe werden auch<br />
Schleppmittel (entrainer) genannt, da sie eine der Azeotropkomponenten<br />
„herausschleppen“. Der Hilfsstoff-Siedepunkt sollte mindestens um 40 °C höher liegen als die<br />
Siedepunkte der zu trennenden Komponenten, so dass er sich in einer weiteren Kolonne<br />
leicht trennen lässt. Beispiel: Trennung von Benzen <strong>und</strong> Cyclohexan durch Zusatz von Anilin.<br />
- Azeotrope <strong>Rektifikation</strong>: ein leichtflüchtiger Hilfsstoff wird zum Azeotrop zugegeben, der mit<br />
einer oder beiden der Komponenten ein leichtsiedendes Azeotrop bildet. Der Hilfsstoff<br />
(Azeotropbildner bei eng siedenden Gemischen, Azeotropwandler bei Azeotropen) muss<br />
dann leicht vom gewünschten Produkt abzutrennen sein (schwer mischbare Stoffe).<br />
Beispiel: Absolutierung von EtOH mit Hilfe von Kohlenwasserstoffen (Benzen, Toluen,<br />
Cyclohexan, Pentan)
Wasserdampfdestillation<br />
(Trägerdampfdestillation: auch andere Stoffe als Wasser)<br />
Zwei ineinander unlösliche Komponenten, jede Komponente entwickelt p i 0 (T):<br />
Dalton: p ges = p A 0 + p w<br />
0<br />
y A = (p A 0 )/(p A 0 + p w 0 )<br />
Das Gemisch siedet, wenn p ges >= p atm -> Minimumazeotrop (T S < (T A , T B ))<br />
Wird verwendet für Stoffe mit hohem Siedepunkt oder Zersetzung beim Sieden (ätherische Öle,<br />
Alkaloide, halogenierte Aromate etc.).
Notwendige Wassermenge, um Stoffmenge m Org abzudestillieren (p * ≡ p 0 ):
<strong>Rektifikation</strong><br />
(Z = Zulauf (Feed), E = Erzeugnis (Destillat))<br />
Praktischer <strong>Teil</strong> der Berechnung einer <strong>Rektifikation</strong>skolonne:<br />
- minimale Bodenzahl für (x Z , x S , x E )<br />
- minimales <strong>und</strong> optimales Rücklaufverhältnis V min , V opt<br />
- Lage <strong>und</strong> Zustand des Zulaufs (Dampf, siedende Flüssigkeit usw.)<br />
x E , E - Erzeugnisstrom<br />
V - Rücklaufverhältnis<br />
Zulauf<br />
x Z , Z<br />
x S , S - Sumpfstrom
Berechnung des Rücklaufverhältnisses V: Verstärkungsgerade = Bilanzgerade im Verstärkungsteil<br />
Bei der Zugabe sowohl unten im Sumpf oder mittig in der Kolonne<br />
- x Z , Z: Zulauf (Feed) [mol/h]<br />
- x E , E: Erzeugnistrom (Destillat) [mol/h]<br />
- y, D: Dampffstrom [mol/h]<br />
- x, F: Flüssigkeitsstrom [mol/h]<br />
E, x E<br />
D<br />
F<br />
y x Bilanz am Kolonnenkopf: D = F + E<br />
y*D = x*F + x E *E<br />
Rücklaufverhältnis:<br />
V = F/E<br />
V -> ∞ (E = 0): kein Destillat<br />
V -> 0 (F = 0): <strong>Destillation</strong><br />
V = V min : minimales V zum Erreichen von x E<br />
y = x*F/(F + E) + x E *E/(F + E) -><br />
V 1<br />
y = ⋅ x + ⋅ xE<br />
V + 1 V + 1<br />
Verstärkungsgerade<br />
Steigung:<br />
V/(V+1)<br />
Abschnitt auf der y-Achse: x E *(1/(V + 1))<br />
Verläuft durch die Punkte: (x E ;x E ) <strong>und</strong> (0; x E *(1/(V + 1))<br />
(Im Bild: x D ≡ x E )
Analog, Berechnung der Abtriebsgerade = Bilanzgerade im Abtriebsteil (falls Zugabe mittig in der<br />
Kolonne):<br />
- y, D: Dampffstrom [mol/h]<br />
- x, F: Flüssigkeitsstrom [mol/h]<br />
- x S , S: Sumpfstrom [mol/h]<br />
D<br />
y<br />
F<br />
x<br />
S, x S<br />
Bilanz am Sumpf:<br />
Abtriebsverhältnis:<br />
V<br />
V<br />
D = F + E<br />
x*F = y*D + x S *S<br />
V A = F/S<br />
y = x*F/(F - S) - x S *S/(F - S) -> A 1<br />
y = ⋅ x − ⋅<br />
−1<br />
−1<br />
xS<br />
A<br />
A<br />
V<br />
Abtriebsgerade<br />
Steigung: V A /(V A -1)<br />
Verläuft durch den Punkt: (x S ;x S ) (y(x = x S ) = x S )
Schnittpunkt Verstärkungsgerade x Abtriebsgerade muss unterhalb der Gleichgewichtslinie liegen,<br />
sonst ist keine Trennung auf Ströme mit der Zusammensetzung x E <strong>und</strong> x S möglich.<br />
Schnittpunktgerade: der Schnittpunkt der beiden Bilanzgeraden (Verstärkungs- <strong>und</strong> Abtriebsgerade)<br />
ist durch den thermischen Zustand des Zulaufs gegeben.<br />
Die Steigung der Schnittpunktgerade: q/(q - 1), q - siehe Tabelle 15.2:
Für Zulauf als siedende Flüssigkeit: q = 1, Steigung = ∞ (Vertikale): wenn der Zulauf im flüssigen<br />
Zustand, auf Siedetemperatur erhitzt zugeführt wird (häufig in der Praxis), verläuft die<br />
Schnittpunktsgerade senkrecht durch den Punkt x = x Z .<br />
Wie aus der obigen Abb. 15.7 ersichtlich, kann man z.B bei gegebenen x Z , x S , x E (gewünschte<br />
Trennung von x Z ), gewähltem Zulaufzustand <strong>und</strong> Abtriebsverhältnis das dazu notwendige<br />
Rücklaufverhältnis graphisch bestimmen (aus der Steigung der Verstärkungsgerade).<br />
Berechnung der minimalen Bodenzahl (Trennstufenzahl) zur Trennung von Zulauf der<br />
Zusammensetzung x Z in x E <strong>und</strong> x S : die geringste Zahl von Trennstufen ist erforderlich, wenn kein<br />
Erzeugnis- <strong>und</strong> Sumpfstrom abgezogen werden, also V = ∞. Die minimale Bodenzahl ist nicht von<br />
praktischer Bedeutung (kein Destillat), liefert aber erste Anhaltspunkte für den erforderlichen<br />
Trennaufwand (Investitionskosten).<br />
Hier:<br />
x B ≡ x S (im Text)<br />
x D ≡ x E (im Text)<br />
Berechnung des minimalen Rücklaufverhältnisses V min (d.h., das minimal notwendige V für die<br />
Produktion von E mit der Zusammensetzung x E aus Zulauf der Zusammensetzung x Z <strong>und</strong> gewähltem<br />
Zustand (z.B. siedend) im Auftriebsteil der Kolonne) :<br />
Das minimale Rücklaufverhältnis wird bei unendlicher Bodenzahl erreicht, wenn die Steigung der<br />
Verstärkungsgeraden ein Minimum besitzt. Die Verstärkungsgerade <strong>und</strong> die Abtriebsgerade<br />
schneiden sich auf der Gleichgewichtskurve, die Lage des Schnittpunktes ist durch den thermischen<br />
Zustand des Zulaufs über die Schnittpunktgerade gegeben.<br />
Hier:<br />
x F ≡ x Z (im Text)<br />
x D ≡ x E (im Text)
Hier:<br />
z F ≡ x Z (im Text)<br />
x D ≡ x E (im Text)<br />
In Abb. 4.12, für jeden Erzeugnis-Molenbruch (Destilat) x E , x E ' gilt ein anderes<br />
Minimalrücklaufverhältnis. Allgemein gilt:<br />
y min = x E /(V min + 1) -> V min = x E /y min + 1<br />
Berechnung der Trennstufenzahl<br />
Die Anzahl der notwendigen Trennstufen folgt aus einer Stufenkonstruktion zwischen den<br />
Bilanzgeraden <strong>und</strong> der Gleichgewichtslinie im McCabe-Thiele-Diagramm. Die Stufenkonstruktion<br />
beginnt bei x S <strong>und</strong> endet bei x E , die Anzahl der Stufen ergibt die Anzahl der Verdampfungs- <strong>und</strong><br />
Kondensationsvorgänge bzw. die minimale Anzahl der theoretisch benötigten Trennstufen. Die Höhe<br />
des Zulaufs (auf welchem Trennboden) wird dann direkt bei x Z abgelesen.
Hier:<br />
x F ≡ x Z (im Text)<br />
x D ≡ x E (im Text)
Optimales Rücklaufverhältnis<br />
Ist der Rücklauf klein, braucht die Kolonne viele Trennstufen <strong>und</strong> wird höher, d.h. höhere<br />
Investitionskosten. Ist der Rücklauf groß, fließt viel Flüssigkeit in den Sumpf <strong>und</strong> muss wieder<br />
verdampft werden, d.h. höhere Betriebskosten. Das wirtschaftliche Minimum der Gesamtkosten liegt<br />
bei V = 1.2 bis 4 V min , je nach Häufigkeit der Produktion.
Vorgehen bei der Berechnung einer <strong>Rektifikation</strong>skolonne<br />
1. Gleichgewichtskurve der Mischung, x E , x S , x Z -> minimale theoretische Stufenzahl<br />
2. Zustand von Zulauf -> Schnittpunktgerade<br />
3. Bestimmung von V min -> V (Rücklaufverhältnis)<br />
4. Verstärkungs- <strong>und</strong> Abtriebgerade<br />
5. Trennstufenzahl, Platzierung von Zulauf (auf welchem Boden)<br />
Berechnung der <strong>Rektifikation</strong>sanlagen: z.B. ASPEN (Software zur Simulation chemischer Anlagen)<br />
Literatur<br />
1. Daniel S. Christen, Praxiswissen der chemischen Verfahrenstechnik, Springer-Verlag Berlin<br />
Heidelberg 2005<br />
2. Jürgen Gmehling, Axel Brehm, Gr<strong>und</strong>operationen. Lehrbuch der Technischen Chemie Band 2,<br />
Georg Thieme Verlag 1996