s - KemnitzLab
s - KemnitzLab
s - KemnitzLab
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
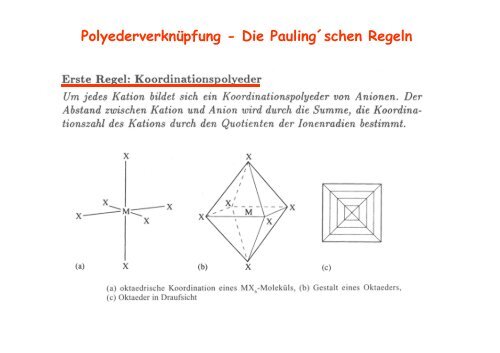
Polyederverknüpfung - Die Pauling´schen Regeln
Zwei Seiten dieser Regel:<br />
i) Kationen-zentrierte Polyeder (geometrisch, aber konzentriert elektronischen<br />
Fokus auf Kationen obwohl Elektronen mehr am Anion konzentriert sind.<br />
ii) Zweiter Teil reflektiert Idee der Ionenradien<br />
Kann daraus geschlussfolgert werden, dass Mg 2+ größer als Ni 2+ oder<br />
Mg 2+ größer als Fe 2+ ist?<br />
Konstante Ionenradien ein und desselben Ions in verschiedenen<br />
Verbindungen sind offensichtlich zweifelhaft!
iii) Idee der Radienquotienten als die Strukturen kontrollierender Faktor ist<br />
mehr als jede andere Regel (obwohl in allen Büchern zitiert) zweifelhaft<br />
r + /r - = 0,732<br />
r + /r - = 0,414<br />
Von 98 Punkten fallen 38 in<br />
die falsche Region!<br />
Damit stellt sich die Frage<br />
nach der Haltbarkeit<br />
dieser Regel<br />
Probleme resultieren aus<br />
dem rein geometrischen<br />
Ansatz
Es sollten besser die energetischen Aspekte in den Vordergrund gestellt werden<br />
Die elektrostatischen Energien zweier Strukturen (i,j) entsprechen<br />
E i /E j = (M i /M j ) n/(n-1) (Q j /Q i ) 1/(n-1) mit<br />
Dieses Modell beinhaltet die Madelung-Konstante (M) für jede Struktur sowie<br />
Repulsionskräfte nächster Nachbarn<br />
wenn der Born-Exponent (n) groß ist, verhalten sich Ionen hart und umgekehrt<br />
bei γ + r(γ - r) gibt es m + (m - ) dichteste Kationen-Kationen (Anionen-Anionen)-Abstände<br />
(darin gibt r die Kationen-Anionen-Abstände an), p ist der Radienquotient und n die KZ<br />
des Anions durch das Kation und umgekehrt.<br />
Der spezielle Paulingsche Wert 0,414 ist bedeutungslos<br />
für harte Schalen ist 0,325 ein limitierender Wert<br />
n für Separation KZ=6 von KZ=8 liegt so hoch, dass es<br />
hier nicht eingezeichnet werden kann!<br />
Zum LiF: egal wie p gewählt wird, diese Struktur fällt<br />
niemals in den korrekten Bereich � d.h., das ionische<br />
Modell ist fragwürdig zur richtigen Vorhersage
Das Pseudopotential beschreibt das<br />
Potentialfeld durch ein äußeres, oder Valenz-<br />
Elektron in einem Atom oder Festkörper. Die<br />
inneren Elektronen werden als „eingefroren“<br />
angenommen, und wegen des Pauli-Prinzips<br />
heben die abstoßenden Kräfte die Anziehung des<br />
Kerns auf die äußeren Elektronen nahezu auf.<br />
Der Radius ist der Punkt, an dem die Pseudo-<br />
Wellenfunktion ihr Maximum erreicht. D.h., die<br />
Radien sind nicht konstant.
Satz von Daten, die nach dem<br />
Pseudopotentialmodell für s- und<br />
p-AOs genutzt werden.<br />
Wichtig: diese Radien sind<br />
atomare Parameter und als<br />
solche unabhängig von der Natur<br />
der chemischen Umgebung
s = Größenangabe = Summe der s und p-Pseudopotential-Orbital-Radien<br />
Die Linien separieren 4-, 6- und 8-fach koordinierte Strukturen, aber sind nicht berechnete Daten<br />
sondern gezogen, um „bestmögliche Separation dieser Strukturen zu erreichen.<br />
1/r l korreliert mit der Energie � gute Korrelation zwischen 1/r l und Ionisierungsenergie<br />
EN Mulliken = Summe der IE = (1/r s + (1/r p ) χ A,B -Plot in Part B (Abb)<br />
Es bleibt ein<br />
„philosophisches“<br />
Problem:<br />
a) zeigt, dass die<br />
Größe wichtig ist<br />
b) suggeriert, die<br />
relativen Orbitallagen<br />
sind wichtig<br />
Deshalb ist sichere<br />
Vorhersage der KZ in<br />
einer Struktur unsicher
MX 2 (KZ M2+ = 6) � s = 2/6 = 1/3, nur wenn KZ des Anions a = 3 ist ergibt sich<br />
die richtige Ladung für das Anion (-1)<br />
MX 4 (KZ M4+ = 6) � s = 4/6 = 2/3: für Anion X - mit a = 2 �<br />
Σs i = 2/3 + 2/3 = 4/3, für X - mit a = 1 � Σs i = 2/3<br />
Andere Werte für KZ ergeben noch stärker vom Sollwert abweichende Werte!<br />
Also wird die Struktur Anionen mit a = 2 und a = 1 im Verhältnis 1:1 enthalten!<br />
Besonders hilfreich zur Unterscheidung von O 2- , OH - und H 2 O (in Röntgen-<br />
Strukturbestimmung nicht unterscheidbar) – ihre Ladung muß aber zur Summe p j<br />
der elektrostatischen Bindungsstärke der umgebenden Kationen passen.<br />
Bsp: Al 2 Si 2 O 5 (OH) 4 = „Al 2 O 3 . 2SiO2 . 2H2 O“ KZ Al = 6, KZ Si = 4<br />
s Al3+ = 3/6 = 0,5 s Si4+ = 4/4 = 1<br />
Schichtabfolge in diesem Schichtsilicat ist O(1)-Al-O(2)-Si-O(3)
O1<br />
O2<br />
O3<br />
O(2) verknüpft Oktaeder mit Tetraedern KZ = 3 (2xAl, 1xSi)<br />
Die anderen O haben KZ = 2<br />
Berechnung der Summe der elektrostatischen Bindungsstärken:<br />
O(1): p 1 = 2·s Al3+ = 2·0,5 = 1<br />
O(2): p 2 = 2·s Al3+ + 1·s Si4+ = 2·0,5 + 1 = 2<br />
O(3): p 3 = 2·s Si4+ = 2·1 = 2<br />
Also müssen sich OH - auf der O(1)-Position und O 2- auf den anderen<br />
Positionen befinden
CaCO 3<br />
Ca 2+ KZ = 6 s = 1/3<br />
C 4+ KZ = 3 s = 4/3<br />
Für O 2- erhalten wir dann den richtigen Wert für z,<br />
wenn jedes davon zwei Ca- und einem C-Atom<br />
angehört: z = -[2s(Ca 2+ ) + s(C 4+ )] = -2
Diese Regel ist eigentlich eine<br />
„Spielart“ der dritten Regel
d(MX(j)) = d(MX) + bΔp j
Polyederverknüpfung
Eckenverknüpfte Oktaeder<br />
[M 2 F 11 ] -
Verknüpfungen in MX 5
Verknüpfungen in MX 4
Verknüpfungen in MX 3
3 , 6 = 2:1, d.h., 1/3 besetzbar<br />
x ≤ 0,33<br />
Strukturen von Wolfram-Bronzen<br />
3,4,5 = 2:1:2, d.h., 3/5 besetzbar<br />
x ≤ 0,6
Kantenverknüpfte Oktaeder
MX 3
MX 2
Flächenverknüpfte Oktaeder
Oktaeder mit gemeinsamen Ecken und Kanten
Oktaeder mit gemeinsamen Kanten und Flächen
Verknüpfte trigonale Prismen
Eckenverknüpfte Tetraeder
Verknüpfung von Tetraedern über<br />
alle 4 Ecken
Zeolithe
Kantenverknüpfte Tetraeder