Spiropyran - Kantonsschule Trogen
Spiropyran - Kantonsschule Trogen
Spiropyran - Kantonsschule Trogen
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
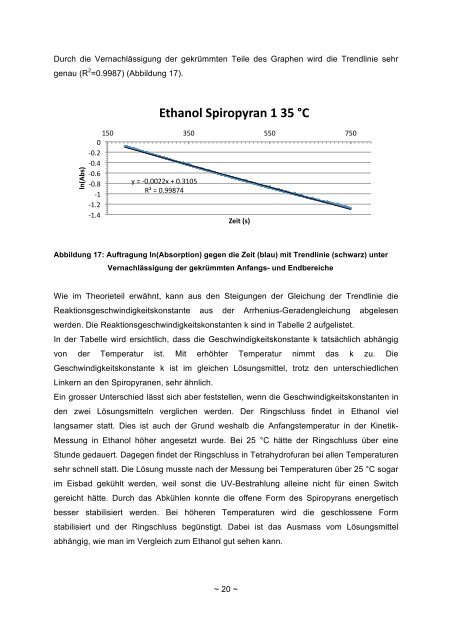
Durch die Vernachlässigung der gekrümmten Teile des Graphen wird die Trendlinie sehrgenau (R 2 =0.9987) (Abbildung 17).ln(Abs) 0 -‐0.2 -‐0.4 -‐0.6 -‐0.8 -‐1 -‐1.2 -‐1.4 Ethanol <strong>Spiropyran</strong> 1 35 °C 150 350 550 750 y = -‐0.0022x + 0.3105 R² = 0.99874 Zeit (s) Abbildung 17: Auftragung ln(Absorption) gegen die Zeit (blau) mit Trendlinie (schwarz) unterVernachlässigung der gekrümmten Anfangs- und EndbereicheWie im Theorieteil erwähnt, kann aus den Steigungen der Gleichung der Trendlinie dieReaktionsgeschwindigkeitskonstante aus der Arrhenius-Geradengleichung abgelesenwerden. Die Reaktionsgeschwindigkeitskonstanten k sind in Tabelle 2 aufgelistet.In der Tabelle wird ersichtlich, dass die Geschwindigkeitskonstante k tatsächlich abhängigvon der Temperatur ist. Mit erhöhter Temperatur nimmt das k zu. DieGeschwindigkeitskonstante k ist im gleichen Lösungsmittel, trotz den unterschiedlichenLinkern an den <strong>Spiropyran</strong>en, sehr ähnlich.Ein grosser Unterschied lässt sich aber feststellen, wenn die Geschwindigkeitskonstanten inden zwei Lösungsmitteln verglichen werden. Der Ringschluss findet in Ethanol viellangsamer statt. Dies ist auch der Grund weshalb die Anfangstemperatur in der Kinetik-Messung in Ethanol höher angesetzt wurde. Bei 25 °C hätte der Ringschluss über eineStunde gedauert. Dagegen findet der Ringschluss in Tetrahydrofuran bei allen Temperaturensehr schnell statt. Die Lösung musste nach der Messung bei Temperaturen über 25 °C sogarim Eisbad gekühlt werden, weil sonst die UV-Bestrahlung alleine nicht für einen Switchgereicht hätte. Durch das Abkühlen konnte die offene Form des <strong>Spiropyran</strong>s energetischbesser stabilisiert werden. Bei höheren Temperaturen wird die geschlossene Formstabilisiert und der Ringschluss begünstigt. Dabei ist das Ausmass vom Lösungsmittelabhängig, wie man im Vergleich zum Ethanol gut sehen kann.~ 20 ~