Zellbiologie & Imaging - Laborwelt
Zellbiologie & Imaging - Laborwelt
Zellbiologie & Imaging - Laborwelt
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Blitzlicht Zellbasierte Assays<br />
A B<br />
C<br />
5x<br />
Das Problem Meniskusbildung<br />
Sowohl Tube Formation- als auch Sprouting-<br />
Assays werden auf Gelmatrizes durchgeführt,<br />
wobei meist BD Matrigel TM von Becton Dickinson<br />
verwendet wird. Aufgrund der hohen Kosten<br />
für die Gelmatrix und der Parallelisierung<br />
wird angestrebt, den Test in möglichst kleinen<br />
Wells durchzuführen.<br />
Allerdings tritt im Fall kleiner Wells ein<br />
störender Meniskus auf. Dieser führt einerseits<br />
zu einer ungleichmäßigen Zellverteilung<br />
durch Zellkonzentration in der Mitte<br />
des Wells. Andererseits liegen die Zellen<br />
auf einer gekrümmten Oberfläche, was eine<br />
scharfe mikroskopische Abbildung aller Zellen<br />
zugleich unmöglich macht (Abb. 2). Die automatisierte<br />
Bildverarbeitung wird dadurch<br />
drastisch aufwendiger.<br />
Ein möglicher Lösungsansatz ist es, Bilder<br />
in verschiedenen Fokusebenen aufzunehmen,<br />
um danach die jeweils scharfen Bereiche der<br />
Bilder zu einem Bild zusammenzusetzen. Um<br />
das Meniskusproblem selbst zu verringern,<br />
bleibt bisher nur die Verwendung von größeren<br />
Wells, zum Beispiel von 6 Well- oder<br />
35 mm-Petrischalen. In diesem Fall vergrößert<br />
sich allerdings der Matrigeleinsatz pro Well<br />
–in 96-Well-Platten ca. 100 µl – um ein Vielfaches.<br />
Bei der Verwendung von 100 µl pro Well<br />
entstehen bereits Matrigelkosten von rund<br />
300 Euro für eine 96-Well-Platte. Hier gilt es,<br />
zwischen hohen Kosten einerseits und starker<br />
5x<br />
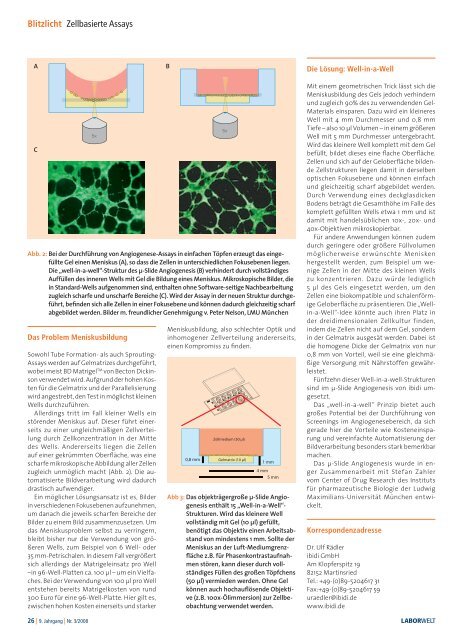
Abb. 2: Bei der Durchführung von Angiogenese-Assays in einfachen Töpfen erzeugt das eingefüllte<br />
Gel einen Meniskus (A), so dass die Zellen in unterschiedlichen Fokusebenen liegen.<br />
Die „well-in-a-well“-Struktur des µ-Slide Angiogenesis (B) verhindert durch vollständiges<br />
Auffüllen des inneren Wells mit Gel die Bildung eines Meniskus. Mikroskopische Bilder, die<br />
in Standard-Wells aufgenommen sind, enthalten ohne Software-seitige Nachbearbeitung<br />
zugleich scharfe und unscharfe Bereiche (C). Wird der Assay in der neuen Struktur durchgeführt,<br />
befinden sich alle Zellen in einer Fokusebene und können dadurch gleichzeitig scharf<br />
abgebildet werden. Bilder m. freundlicher Genehmigung v. Peter Nelson, LMU München<br />
0,8 mm<br />
5x<br />
5x<br />
Meniskusbildung, also schlechter Optik und<br />
inhomogener Zellverteilung andererseits,<br />
einen Kompromiss zu finden.<br />
Zellmedium (50 µl)<br />
Gelmatrix (10 µl)<br />
4 mm<br />
5 mm<br />
26 | 9. Jahrgang | Nr. 3/2008 LABORWElT<br />
1 mm<br />
Abb 3: Das objekträgergroße µ-Slide Angiogenesis<br />
enthält 15 „Well-in-a-Well“-<br />
Strukturen. Wird das kleinere Well<br />
vollständig mit Gel (10 µl) gefüllt,<br />
benötigt das Objektiv einen Arbeitsabstand<br />
von mindestens 1 mm. Sollte der<br />
Meniskus an der Luft-Mediumgrenzfläche<br />
z.B. für Phasenkontrastaufnahmen<br />
stören, kann dieser durch vollständiges<br />
Füllen des großen Töpfchens<br />
(50 µl) vermieden werden. Ohne Gel<br />
können auch hochauflösende Objektive<br />
(z.B. 100x-Ölimmersion) zur Zellbeobachtung<br />
verwendet werden.<br />
Die Lösung: Well-in-a-Well<br />
Mit einem geometrischen Trick lässt sich die<br />
Meniskusbildung des Gels jedoch verhindern<br />
und zugleich 90% des zu verwendenden Gel-<br />
Materials einsparen. Dazu wird ein kleineres<br />
Well mit 4 mm Durchmesser und 0,8 mm<br />
Tiefe – also 10 µl Volumen – in einem größeren<br />
Well mit 5 mm Durchmesser untergebracht.<br />
Wird das kleinere Well komplett mit dem Gel<br />
befüllt, bildet dieses eine flache Oberfläche.<br />
Zellen und sich auf der Geloberfläche bildende<br />
Zellstrukturen liegen damit in derselben<br />
optischen Fokusebene und können einfach<br />
und gleichzeitig scharf abgebildet werden.<br />
Durch Verwendung eines deckglasdicken<br />
Bodens beträgt die Gesamthöhe im Falle des<br />
komplett gefüllten Wells etwa 1 mm und ist<br />
damit mit handelsüblichen 10x-, 20x- und<br />
40x-Objektiven mikroskopierbar.<br />
Für andere Anwendungen können zudem<br />
durch geringere oder größere Füllvolumen<br />
möglicherweise erwünschte Menisken<br />
hergestellt werden, zum Beispiel um wenige<br />
Zellen in der Mitte des kleinen Wells<br />
zu konzentrieren. Dazu würde lediglich<br />
5 µl des Gels eingesetzt werden, um den<br />
Zellen eine biokompatible und schalenförm -<br />
ige Geloberfläche zu präsentieren. Die „Wellin-a-Well“-Idee<br />
könnte auch ihren Platz in<br />
der dreidimensionalen Zellkultur finden,<br />
indem die Zellen nicht auf dem Gel, sondern<br />
in der Gelmatrix ausgesät werden. Dabei ist<br />
die homogene Dicke der Gelmatrix von nur<br />
0,8 mm von Vorteil, weil sie eine gleichmäßige<br />
Versorgung mit Nährstoffen gewähr -<br />
leistet.<br />
Fünfzehn dieser Well-in-a-well-Strukturen<br />
sind im µ-Slide Angiogenesis von ibidi umgesetzt.<br />
Das „well-in-a-well“ Prinzip bietet auch<br />
großes Potential bei der Durchführung von<br />
Screenings im Angiogenesebereich, da sich<br />
gerade hier die Vorteile wie Kosteneinsparung<br />
und vereinfachte Automatisierung der<br />
Bildverarbeitung besonders stark bemerkbar<br />
machen.<br />
Das µ-Slide Angiogenesis wurde in enger<br />
Zusammenarbeit mit Stefan Zahler<br />
vom Center of Drug Research des Instituts<br />
für pharmazeutische Biologie der Ludwig<br />
Maximilians-Universität München entwickelt.<br />
Korrespondenzadresse<br />
Dr. Ulf Rädler<br />
ibidi GmbH<br />
Am Klopferspitz 19<br />
82152 Martinsried<br />
Tel.: +49-(0)89-5204617 31<br />
Fax:+49-(0)89-5204617 59<br />
uraedler@ibidi.de<br />
www.ibidi.de