GIÁO ÁN HÓA 9 CHUẨN 5 BƯỚC TUẦN 1 TUẦN 13 (2018)
https://app.box.com/s/aszr4wi4p3bwibzunsnfdgbi3sj10cph
https://app.box.com/s/aszr4wi4p3bwibzunsnfdgbi3sj10cph
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
https://twitter.com/daykemquynhon<br />
plus.google.com/+DạyKèmQuyNhơn<br />
www.facebook.com/daykem.quynhon<br />
https://daykemquynhon.blogspot.com<br />
Hóa học 9<br />
http://daykemquynhon.ucoz.com<br />
Nơi bồi dưỡng kiến thức Toán - Lý - Hóa cho học sinh cấp 2+3 /<br />
Diễn Đàn Toán - Lý - Hóa Quy Nhơn 1000B Trần Hưng Đạo Tp.Quy Nhơn Tỉnh Bình Định<br />
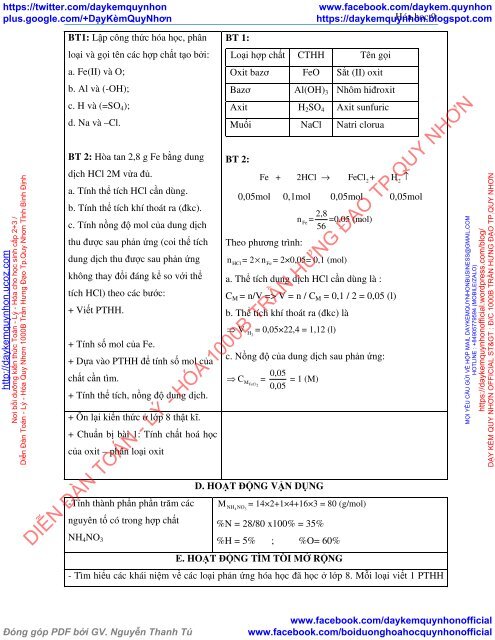
BT1: Lập công thức hóa học, phân<br />
loại và gọi tên các hợp chất tạo bởi:<br />
a. Fe(II) và O;<br />
b. Al và (-OH);<br />
c. H và (=SO 4 );<br />
d. Na và –Cl.<br />
BT 2: Hòa tan 2,8 g Fe bằng dung<br />
dịch HCl 2M vừa đủ.<br />
a. Tính thể tích HCl cần dùng.<br />
b. Tính thể tích khí thoát ra (đkc).<br />
c. Tính nồng độ mol của dung dịch<br />
thu được sau phản ứng (coi thể tích<br />
dung dịch thu được sau phản ứng<br />
không thay đổi đáng kể so với thể<br />
tích HCl) theo các bước:<br />
+ Viết PTHH.<br />
+ Tính số mol của Fe.<br />
+ Dựa vào PTHH để tính số mol của<br />
chất cần tìm.<br />
+ Tính thể tích, nồng độ dung dịch.<br />
+ Ôn lại kiến thức ở lớp 8 thật kĩ.<br />
+ Chuẩn bị bài 1: Tính chất hoá học<br />
của oxit – phân loại oxit<br />
-Tính thành phần phần trăm các<br />
nguyên tố có trong hợp chất<br />
NH 4 NO 3<br />
BT 1:<br />
Loại hợp chất CTHH Tên gọi<br />
Oxit bazơ FeO Sắt (II) oxit<br />
Bazơ<br />
Al(OH) 3 Nhôm hiđroxit<br />
Axit H 2 SO 4 Axit sunfuric<br />
Muối NaCl Natri clorua<br />
BT 2:<br />
Fe + 2HCl → FeCl + H<br />
0,05mol 0,1mol 0,05mol 0,05mol<br />
Theo phương trình:<br />
HCl<br />
a. Thể tích dung dịch HCl cần dùng là :<br />
C M = n/V => V = n / C M = 0,1 / 2 = 0,05 (l)<br />
b. Thể tích khí thoát ra (đkc) là<br />
c. Nồng độ của dung dịch sau phản ứng:<br />
D. HOẠT ĐỘNG VẬN DỤNG<br />
M<br />
%N = 28/80 x100% = 35%<br />
2,8<br />
n<br />
Fe<br />
= =0,05 (mol)<br />
56<br />
n = 2×<br />
n = 2×0,05= 0,1 (mol)<br />
H 2<br />
%H = 5% ; %O= 60%<br />
E. HOẠT ĐỘNG TÌM TÒI MỞ RỘNG<br />
2 2<br />
- Tìm hiểu các khái niệm về các loại phản ứng hóa học đã học ở lớp 8. Mỗi loại viết 1 PTHH<br />
Fe<br />
⇒ V = 0,05×22,4 = 1,12 (l)<br />
0,05<br />
⇒ C<br />
M FeCl2<br />
= = 1 (M)<br />
0,05<br />
NH4NO3<br />
= 14×2+1×4+16×3 = 80 (g/mol)<br />
DIỄN ĐÀN TO<strong>ÁN</strong> - LÝ - <strong>HÓA</strong> 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
↑<br />
MỌI YÊU CẦU GỬI VỀ HỘP MAIL DAYKEMQUYNHONBUSINESS@GMAIL.COM<br />
HOTLINE : +84905779594 (MOBILE/ZALO)<br />
https://daykemquynhonofficial.wordpress.com/blog/<br />
DẠY KÈM QUY NHƠN OFFICIAL ST> : Đ/C 1000B TRẦN HƯNG ĐẠO TP.QUY NHƠN<br />
Đóng góp PDF bởi GV. Nguyễn Thanh Tú<br />
www.facebook.com/daykemquynhonofficial<br />
www.facebook.com/boiduonghoahocquynhonofficial