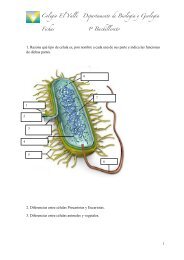
TEMA 12. CATABOLISMO
TEMA 12. CATABOLISMO
TEMA 12. CATABOLISMO
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>TEMA</strong> <strong>12.</strong> <strong>CATABOLISMO</strong> AERÓBICO Y ANAERÓBICO <br />
<strong>CATABOLISMO</strong> AERÓBICO <br />
Está formado por varias rutas metabólicas que conducen a la obtención de moléculas de ATP <br />
que podrán ser empleadas en otros procesos que necesiten un aporte energético. La energía <br />
que no se almacena se disipa en forma de calor. <br />
GLUCÓLISIS (RUTA DE EMBDEN-MEYERHOF) <br />
Tiene lugar en el citosol sin necesidad de oxígeno. Se trata de una secuencia de reacciones <br />
químicas donde una molécula de glucosa de (6C) se va a transformar en dos moléculas de ácido <br />
pirúvico (3C). <br />
http://1.bp.blogspot.com/_FigIDhaqGWI/Sw8LUYhqMDI/AAAAAAAAAEE/z0HftqsYpnw/s1600/glucólisis.gif <br />
Balance energético <br />
Glucosa + 2 ADP + 2 P i + 2 NAD + → 2 Ácido pirúvico + 2 ATP + 2 NADH + 2 H + + 2 H 2O <br />
Etapas clave de la glucólisis <br />
• En condiciones aerobias, el NADH extramitocondrial cede sus electrones a la cadena <br />
transportadora a través de la dihidroxiacetona fosfato, que se reduce a glicerol fosfato, <br />
el cual entra en la mitocondria, se reoxida mediante la reducción de un FAD, y sale de <br />
nuevo al citosol como dihidroxiacetona fosfato. Este proceso se denomina lanzadera de <br />
dihidroxiacetona <br />
• En condiciones anaerobias, el NADH extramitocondrial se oxida a NAD + , <br />
reduciéndose el ácido pirúvico. Se obtiene energía de forma anaeróbica y las reacciones <br />
se llaman fermentaciones. <br />
<br />
1
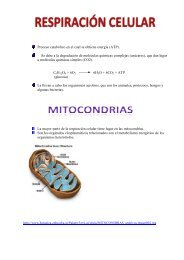
RESPIRACIÓN CELULAR <br />
1. CICLO DE KREBS <br />
• Oxidación del piruvato. <br />
El ácido pirúvico formado en la glucólisis, en el citoplasma celular, va a pasar a la matriz <br />
mitocondrial atravesando las membranas mitocondriales externa e interna. <br />
El ácido pirúvico se oxida, liberándose una molécula de CO 2 y un grupo acetilo <br />
(CH 3-‐CO -‐ ), en una reacción catalizada por la piruvato-deshidrogenasa, que es un complejo <br />
enzimático de gran tamaño. Dos molécula de NAD + se reducen, con lo que se obtienen dos <br />
NADH por cada glucosa. <br />
Cada grupo acetilo se une momentáneamente a un compuesto llamado coenzima A, <br />
formándose acetil-CoA, el cual une los procesos de oxidación del piruvato y el ciclo de <br />
Krebs. <br />
http://html.rincondelvago.com/000639872.jpg <br />
• Ciclo de Krebs <br />
Tiene lugar en la matriz mitocondrial, siempre que haya suficiente oxígeno. <br />
http://3.bp.blogspot.com/_CshA7oEPtGQ/RprXHMy6v4I/AAAAAAAAAJo/C2F3mM8Ko-‐0/s400/CicloDeKrebs.gif <br />
Balance energético del ciclo de Krebs <br />
2 Acetil-‐CoA + 6 NAD + + 2 FAD + 2 GDP + 2 P i → 2 CoA + 6 NADH + 2 FADH 2 + 2 GTP + 2 ATP <br />
Se obtiene poca energía en forma de moléculas fosforiladas, pero mucha en forma de núcleotidos <br />
reducidos. <br />
<br />
2
2. CADENA TRANSPORTADORA DE ELECTRONES <br />
Parte de la energía procedente de la degradación de la molécula de glucosa se ha utilizado en la <br />
síntesis de ATP, pero la mayor parte de la energía se encuentra en los electrones que fueron <br />
aceptados por el NAD + y el FAD. Estos electrones están en un nivel energético alto. <br />
Durante el transporte electrónico, los electrones son transportados a través de una serie de <br />
aceptores de distinto potencial de reducción. Según se avanza en la cadena, los aceptores se <br />
encuentran en un nivel energético ligeramente menor. <br />
Cada par redox sólo puede recibir electrones de otro par que tenga un potencial de reducción <br />
más negativo, y sólo puede cederlos a otro par redox que lo tenga menos negativo. El potencial <br />
mas negativo de la cadena respiratoria es el NAD + con -‐0,32 voltios. En el otro extremo está el <br />
agua con +0,82 voltios. <br />
http://recursos.cnice.mec.es/biosfera/alumno/2bachillerato/Fisiologia_celular/imagenes/transporte_completo.jpg <br />
Cuando los electrones se mueven por la cadena transportadora salen a niveles energéticos <br />
inferiores y van liberando energía. Esta energía se emplea para fabricar ATP, a partir de ADP, <br />
en el proceso de fosforilación oxidativa, propuesto por un bioquímico británico llamado <br />
Peter Mitchell. Este proceso depende de la generación de un gradiente de protones a través de <br />
la membrana mitocondrial interna. <br />
-‐<br />
-‐<br />
Por cada dos electrones que pasan del NADH al oxígeno se forman 3 moléculas de ATP. <br />
Por cada dos electrones que pasan desde el FADH 2 al oxígeno forman 2 de ATP. El <br />
mecanismo por el cual se produce ATP se explica por la teoría del acoplamiento <br />
quimiosmótico. <br />
Acoplamiento quimiosmótico <br />
La membrana mitocondrial interna es impermeable a los protones, luego su bombeo permite <br />
que exista un gradiente electroquímico entre la matriz y el espacio intermembrana. De esta <br />
forma, se genera energía aprovechable para hacer funcionar procesos acoplados a canales por <br />
los que circulan protones a favor de gradiente hacia la matriz mitocondrial. <br />
Estos canales los conforman las partículas F, formados por una ATP-‐sintetasa con una porción <br />
F 0 integrada en la membrana de la cresta mitocondrial, y una porción F 1 que sobresale hacia la <br />
matriz. <br />
Cuando los protones atraviesan esta bomba, la partícula F rota y cataliza la hidrólisis de ATP a <br />
partir de ADP y fosfato. Por cada tres protones que fluyen a través de la ATP-‐sintetasa, se <br />
forma una molécula de ATP. Como el flujo de protones es impulsado por un gradiente <br />
electroquímico, este proceso tiene carácter quimiosmótico. <br />
<br />
3
BALANCE ENERGÉTICO DE LA RESPIRACIÓN CELULAR <br />
• La glucólisis rinde dos moléculas de ATP y dos de NADH fuera de la mitocondria. En <br />
presencia de oxígeno, los electrones del NADH extramitocondrial entran en la cadena <br />
transportadora de electrones, gracias a la dihidroxiacetona fosfato, y son cedidos al FAD <br />
en la cadena transportadora de electrones, donde el rendimiento es de dos moléculas de <br />
ATP por cada FADH 2. El rendimiento en la glucólisis es de 6 ATP. <br />
• La conversión de ácido pirúvico en acetil-‐CoA rinde dos moléculas de NADH por cada <br />
molécula de glucosa, y cuando sus electrones se transfieren a la cadena respiratoria se <br />
forman 6 ATP. <br />
• En el ciclo de Krebs se introducen dos moléculas de acetil-‐CoA y se forman dos de GTP <br />
(cada uno de ellos origina 2 moléculas de ATP), seis de NADH y dos de FADH 2. Por lo tanto, <br />
por cada molécula de glucosa se formarán 24 ATP en el ciclo de Krebs y en las cadenas <br />
respiratorias asociadas a él. <br />
El rendimiento total que produce la degradación de una molécula de glucosa es de 36 ATP. <br />
PROCESO <br />
CITOPLASMA <br />
MATRIZ <br />
MITOCONDRIAL <br />
TRANSPORTE <br />
ELECTRÓNICO <br />
TOTAL <br />
Glucólisis <br />
2 ATP <br />
2 NADH <br />
2 (2 ATP) <br />
2 FADH 2 <br />
2 ATP <br />
4 ATP <br />
Respiración <br />
Piruvato a <br />
Acetil-‐CoA <br />
Ciclo de Krebs <br />
2 (1 NADH) 2 (3 ATP) 6 ATP <br />
2 (1 ATP) <br />
2 (3 NADH) <br />
2 (FADH 2) <br />
6 (3 ATP) <br />
2 (2 ATP) <br />
2 ATP <br />
18 ATP <br />
4 ATP <br />
BALANCE ENERGÉTICO GLOBAL (por molécula de glucosa) <br />
36 ATP <br />
<br />
4
<strong>CATABOLISMO</strong> ANAERÓBICO: FERMENTACIONES <br />
Cuando el catabolismo ocurre en condiciones anaerobias, es decir, el último aceptor de <br />
electrones no es el oxígeno, las rutas de degradación de la glucosa se llaman fermentaciones. <br />
En un mismo organismo pueden tener lugar rutas aerobias y anaerobias, según las condiciones <br />
ambientales de sus células. Ocurre en muchas células vegetales y en la fibra muscular estriada <br />
de vertebrados. <br />
Aparecen varios tipos de fermentaciones: <br />
1. FERMENTACIÓN ETÍLICA. <br />
Ocurre en vegetales, hongos y bacterias, ya que la alcohol deshidrogenasa cataliza la <br />
reducción del gliceraldehido a etanol. Ejemplo: Saccharomyces cerevisiae. <br />
- Efecto Pasteur: Se inhibe la fermentación cuando hay presencia de oxígeno. Tiene lugar en <br />
organismos anaerobios facultativos, como las levaduras. El balance energético en condiciones <br />
aerobias es mucho más favorable, obteniéndose 36 ATP frente a los 2 ATP obtenidos en las <br />
fermentaciones. <br />
NAD + <br />
NADH <br />
2. FERMENTACIÓN LÁCTICA. <br />
Se origina ácido láctico a partir del ácido pirúvico procedente de la glucólisis, regenerándose el <br />
NAD + para que pueda proseguir la glucólisis. <br />
Este tipo de fermentación la llevan a cabo bacterias Gram positivas del grupo de los <br />
lactobacilos, las cuales son anaerobias facultativas. Al ser heterótrofas requieren medios de <br />
cultivo ricos en biomoléculas, y por eso no se encuentran en el suelo ni en el agua, sino en la <br />
leche, el intestino… <br />
a. Bacterias homofermentativas: Sólo producen ácido láctico. <br />
-‐ Producen los derivados lácteos. Ejemplo: Lactobacillus lactis, L. casei. <br />
-‐ Otros viven en el intestino humano. Ejemplo: Streptococcus faecalis. <br />
b. Bacterias heterofermentativas: Producen otras sustancias a demás del ácido láctico. <br />
Ejemplo: Lactobacillus brevis, <br />
<br />
5
OTRAS RUTAS CATABÓLICAS <br />
1. OXIDACIÓN DE LOS ÁCIDOS GRASOS <br />
-‐ En primer lugar, los triacilglicéridos se van a hidrolizar en el citoplasma celular, gracias a las <br />
lipasas presentes en la bilis y a las enzimas pancreáticas, formándose glicerol y ácidos grasos, <br />
los cuales pasan a la β-‐oxidación. <br />
-‐ Los fosfolípidos también se hidrolizan , formando glicerol, ácido fosfórico y ácidos grasos. <br />
El glicerol resultante se fosforila y se oxida a dihidroxiacetona fosfato, la cual puede <br />
isomerizarse a gliceraldehído-‐3-‐fosfato, el cual se incorpora a la glucólisis. <br />
β- oxidación de los ácidos grasos <br />
Los ácidos grasos se activan en la membrana mitocondrial externa, uniéndose a la CoA en una <br />
reacción catalizada por la acil-‐CoA sintetasa. Se forma un compuesto llamado Acil-‐CoA, que <br />
traspasa la membrana mitocondrial al unirse a la carnitina, que actúa como lanzadera por la <br />
acción de una translocasa. <br />
1. Oxidación del acil-‐CoA, reacción catalizada por la acil-‐CoA-‐deshidrogenasa, en la cual se <br />
forma un compuesto llamado enoil-CoA. En este proceso se forma una molécula de FADH 2 <br />
gracias a la reducción de un FAD + . <br />
2. Hidratación del doble enlace presente en el enoil-‐CoA en una reacción catalizada por una <br />
enzima llamada enoil-‐CoA-‐hidratasa, para formar β-hidroxiacil-CoA. <br />
3. Oxidación catalizada por la β-‐hidroxiacil-‐CoA-‐deshidrogenasa, que convierte el grupo OH -‐<br />
del C 3 en un grupo ceto, formándose NADH y β-cetoacil-CoA. <br />
4. Escisión y tiólisis del β-‐cetoacil-‐CoA en una reacción catalizada por la tiolasa, originándose <br />
un acetil-CoA y un acil-CoA acortado en dos átomos de carbono. <br />
El acetil-‐CoA se incorpora al ciclo de Krebs y el acil-‐CoA acortado sigue un nuevo ciclo de <br />
oxidación. <br />
La β oxidación consigue, en el interior de la mitocondria, que de un ácido graso saturado se <br />
liberen tantas unidades de acetil-‐CoA como permita su número par de átomos de carbono. <br />
<br />
6
2. OXIDACIÓN DE LOS AMINOÁCIDOS <br />
Los aminoácidos que superan las necesidades metabólicas no pueden ser almacenados ni <br />
excretados, sino que se emplean como reserva energética. <br />
El grupo α-‐amino de los aminoácidos se separa, transformándose en urea que será excretada, <br />
mientras que el resto de la cadena carbonada formará intermediarios metabólicos que se <br />
incorporarán al las principales rutas catabólicas. <br />
• El grupo α-amino se transfiere al ácido-‐α-‐cetoglutárico para formar ácido glutámico, <br />
que se va a desaminar formando amonio (NH 4<br />
+). En los mamíferos, el ión amonio se <br />
transforma en urea mediante el ciclo de la urea, para ser excretado posteriormente. <br />
• El esqueleto carbonado de los aminoácidos forma intermediarios del ciclo del Krebs. <br />
Dependiendo del tipo de metabolito que originen, los aminoácidos se clasifican en: <br />
Aminoácidos cetogénicos: Leucina y lisina. Originan compuestos como el acetil-‐ <br />
CoA o el acetoacetil-‐CoA, que pueden transformarse en cuerpos cetónicos en el <br />
hígado. <br />
Aminoácidos glucogénicos: Alanina, glicina, cisteína, serina, treonina, asparagina, <br />
ácido aspártico, metionina, ácido glutámico, glutamina, histidina, prolina y valina. <br />
Al degradarse originan ácido pirúvico, ácido-‐α-‐cetoglutárico, succinil-‐CoA, ácido <br />
fumárico y ácido oxalacético. <br />
Aminoácido mixtos. Isoleucina, fenilalanina, triptófano y tirosina. Son aquellos <br />
que pueden formar compuestos cetogénicos y glucogénicos. <br />
<br />
7