Ja conseguimos razoavelmente distinguir ostres estados ffsicos,mas ha materiais onde 0 estadoffsico pode ser discutido: uma geleia pode serconsiderada um solido amorfo limftrofe ao estadoIfquido.o vidro nao tem propriamente temperatura defusao: a medida que 0 aquecemos ele se tornamenos'viscoso (mais fluido) e sua organizac;:ao emais aparentada com 0 estado Iiquido do que como estado solido. Oiz-se que ele e um Iiquido superresfriado,ou seja, um Iiquido que deveria ter-secristalizado mas isto nao ocorreu.Nas mudanc;:asde e~tado em que h8 aumentoda organizac;:aodo sistema, pode ocorrer um retardamento,isto e, a mudanc;:ade estado pode naoocorrer na temperatura esperada. Assim, a aguao-10pode ser resfriada ate -100e sem que se inicie acristalizac;:ao. No entanto, apos esta ter-se iniciado,a temperatura sobe ate ooe e se mantem durante asolidificac;:ao.Por que isso acontece? Bem, para se iniciar acristalizac;:ao da agua e preciso que algumas moleculasse arranjem convenientemente, formando um"molde" onde se depositem novas moleculas. Assim,0 cristal cresce e 0 processo de cristalizac;:aose desenvolve por todo 0 material. Mas, as vezes,as moleculas da agua nao formam esse "molde" eo Iiquido pode ser resfriado abaixo do ponto desolidificac;:ao, formando um sistema meta-estavel.Quando um material tem a sua temperaturadiminufda alem do seu ponto de liquefac;:aoou desolidificac;:ao e a mudanc;:ade estado nab ocorre, 0sistema e chamado meta-estavel e tende a passaresp.ontaneamente para uma situac;:aomais estavel.Se cedemos bruscamente calor a agua nessascondic;:6es, perturbamos a organizac;:ao metaestavel,0 arranjo molecular e alterado e pode seiniciar a cristalizac;:ao. Af,enfim, 0 processo de solidificac;:aotoma conta de todo 0 material.Quando colocamos garrafas de refrigerantesou de cerveja no congelador, a temperatura podedescer abaixo do ponto de solidificac;:ao. Quandopegamos uma dessas garrafas, cedemos calor aomaterial, desarranjando 0 sistema meta-estavel,e acristalizac;:ao tem infcio; a bebida, antes Iiquida,agora se apresenta em parte congelada.Algumas experiencias sobre mudanc;asde estadoUma pedra, um pedac;:ode madeira sao bansexemplos de solidos. Agua e alcool sac Iiquidos euma bexiga de borracha ou uma camara de ar depneu servem para conter porc;:6esde gas.Mude os solidos de um lugar para outro eassim voce pode fixar as noc;:6esde que as solid osmantem volume e forma.Mude a agua de um recipiente para outro, demaneira que os alunos percebam que a forma variamas nao 0 volume.Use uma seringa de injec;:ao(fechada na pontacom 0 dedo) e comprima 0 embolo; depois, puxe 0embolo de forma a ficar claro que 0 gas tem seuvolume e sua forma determinados pelo recipienteque a contem.Mostre agora um pouco de sal ou de ac;:ucarformando um pequeno monte; a seguir, coloquenum tuba de ensaio ou espalhe 0 material pelopapel. A forma e 0 volume mudaram?A mudanc;:a de forma do solido nesse casopode ser facilmente explicada: 0 solido e formadopor pequenos cristais que individualmente mantemvolume e forma, mas que no conjunto podem apresentarforma e volume variaveis·
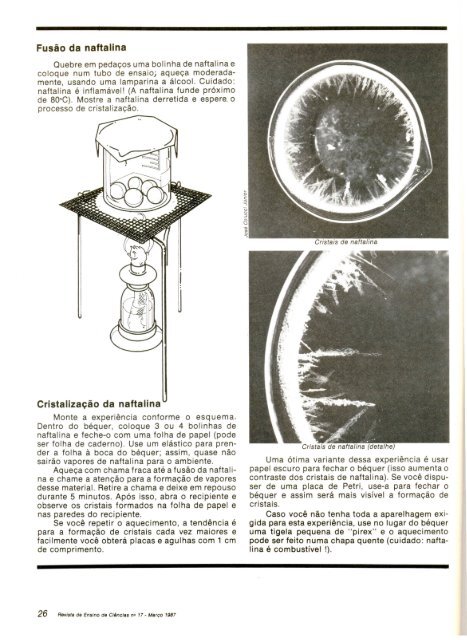
Quebre em pedac;:os uma bolinha de naftalina ecoloque num tubo de ensaioj aquec;:a moderadamente,usando uma lamparina a alcool. Cuidado:naftalina e inflamavel! (A naftalina funde pr6ximode 80 a C). Mostre a naftalina derretida e espere. 0processo de cristalizac;:ao.Cristaliza~ao da naftalinaMonte a experi€mcia conforme 0 esquema.Dentro do bequer, coloque 3 ou 4 bolinhas denaftalina e feche-o com uma folha de papel (podeser folha de caderno). Use um elastico para prendera folha a boca do bequer; assim, quase naosairao vapores de naftalina para 0 ambiente.Aquec;:a com chama fraca ate a fusao da naftalinae chame a atenc;:ao para a formac;:ao de vaporesdesse material. Retire a chama e deixe em repousodurante 5 minutos. Ap6s isso, abra 0 recipiente eobserve os cristais formados na folha de papel enas paredes do recipiente.Se voce repetir 0 aquecimento, a tendencia epara a formac;:ao de cristais cad a vez maiores efacilmente voce obtera placas e agulhas com 1 cmde comprimento.Crista is de naftalina(detalhe)Uma 6tima variante dessa experiencia e usarpapel escuro para fechar 0 bequer (isso aumenta 0contraste dos cristais de naftalina). Se voce dispuserde uma placa de Petri, use-a para fechar 0bequer e assim sera mais visivel a formac;:ao decristais.Caso voce nao tenha toda a aparelhagem ex i-gida para esta experiencia, use no lugar do bequeruma tigela pequena de "pi rex" e 0 aquecimentopode ser feito numa chapa quente (cuidado: nafta-Iina e combustivel I).