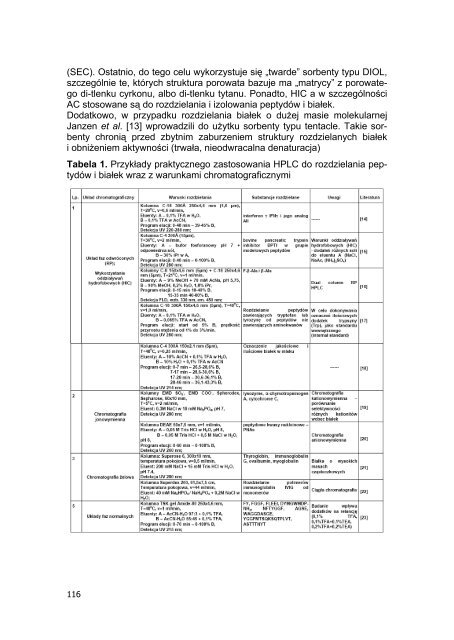
(SEC). Ostatnio, do tego celu wykorzystuje się „twarde” sorbenty typu DIOL,szczególnie te, których struktura porowata bazuje ma „matrycy” z porowategodi-tlenku cyrkonu, albo di-tlenku tytanu. Ponadto, HIC a w szczególnościAC stosowane są do rozdzielania i izolowania peptydów i białek.Dodatkowo, w przypadku rozdzielania białek o dużej masie molekularnejJanzen et al. [13] wprowadzili do użytku sorbenty typu tentacle. Takie sorbentychronią przed zbytnim zaburzeniem struktury rozdzielanych białeki obniżeniem aktywności (trwała, nieodwracalna denaturacja)Tabela 1. Przykłady praktycznego zastosowania HPLC do rozdzielania peptydówi białek wraz z warunkami chromatograficznymi116
ROZDZIELANIE PEPTYDÓW I BIAŁEK W UKŁADACHFAZ ODWRÓCONYCHMetody RP-HPLC są powszechnie stosowane do rozdzielania peptydówi białek w szczególności do celów analitycznych, a także w proteomice.Rozdzielanie peptydów i białek w układach faz odwróconych odbywa się napowierzchni fazy stacjonarnej o określonym stopniu hydrofobowości [18],z zastosowaniem sorbentów typu C18, C8, C4 (C5, C6), C2, fenyl, alkilofenyl,alkilonitryl i inne. Z reguły rozdzielanie peptydów i białek przeprowadzasię w warunkach elucji gradientowej. Faza ruchoma bardzo często zawierawodę i acetonitryl z dodatekiem kwasu trifluorooctowego (TFA), zarównow eluencie A (niższe stężenie acetonitrylu 5 – 25%) jak i w eluencie B (wyższestężenie acetonitrylu 75 – 95%).Rozdzielane cząsteczki peptydów i białek są złożone z różnych aminokwasów(hydrofobowych lub hydrofilowych), ułożonych w zróżnicowanejkombinacji. Retencja zależy od wynikowej hydrofobowości rozdzielanychcząsteczek, albo ich solwatów, tzn. zarówno od struktury i rozkładu hydrofobowościw cząsteczkach, jak i od hydrofobowości solwatów istniejącychw równowadze ze składnikami eluentu.Podczas rozdzielania dużych cząsteczek polipeptydów i białekw układach faz odwróconych dość często obserwowane są niekorzystneprzypadki zmian konformacyjnych łańcucha aminokwasowego [24] i w konsekwencjidenaturacja produktu [25]. Nie polarna faza stacjonarna, organicznafaza ruchoma i kwaśne, albo alkaliczne dodatki do fazy ruchomej(kwas trifluorooctowy (TFA) lub inny, albo amina) – to czynniki mające potencjalnedziałanie denaturujące, a nawet hydrolityczne. Denaturacja objawiasię najczęściej zmianą, retencji substancji, a hydroliza - zwiększeniemilości pików. Aby uniknąć hydrolizy trzeba kontrolować pH i temperaturę rozdzielania[26]. Denaturacji można, także uniknąć przez dodatek do eluentusoli stabilizujących strukturę białka (np. NaCl, AcNa, (NH 4 ) 2 SO 4 ). Trzeba się,jednak, liczyć się z tym, że taki dodatek często modyfikuje retencję substancji[15].Najczęściej do rozdzielania peptydów i białek w układach faz odwróconychsą stosowane sorbenty siloksanowe modyfikowane grupami alkilowymi,fenylowymi i difenylowymi Wśród grup alkilowych najczęściej wykorzystujesię grupę butylową (C4), kolejno pentylową (C5) i oktylową (C8).Wiele jest też zastosowań oktadecylowych (C18) faz stacjonarnych. Rys. 1przedstawia przykład rozdzielania 9 białek w kolumnie wypełnionej sorbentemtypu C5, [27], a chromatogram na rys. 2 to przykład rozdzielania 8 peptydówi białek z wykorzystaniem kolumny C8.117
- Page 1 and 2:
POSTĘPY CHROMATOGRAFIIPraca zbioro
- Page 3:
SPIS TREŚCIPrzedmowa..............
- Page 7 and 8:
Piotr M. SŁOMKIEWICZ 1 , Zygfryd W
- Page 9 and 10:
W komorze 2 znajduje się pojemnik
- Page 11 and 12:
czyna przypływać przez komorę 2
- Page 13 and 14:
4Cnapięcie [mV]3Rys. 6. Chromatogr
- Page 15 and 16:
Bronisław K. GŁÓD 1 , Paweł PIS
- Page 17 and 18:
Rys. 1. Metabolizm dopaminyL-dopa p
- Page 19 and 20:
Dopamina, której niedobór w czę
- Page 21 and 22:
katecholowej oraz kompleksowaniu ż
- Page 23 and 24:
typu skonstruowano w Instytucie Ele
- Page 25 and 26:
takich jak zmęczenie czy stres. Dr
- Page 27 and 28:
CPA SUROWICY KRWI PACJENTÓW Z CHOR
- Page 29 and 30:
mo wyższych stężeń w surowicy e
- Page 31:
LITERATURA1. C. Courderot-masuyer,
- Page 34 and 35:
dopuszczające leki jak np. FDA nie
- Page 36 and 37:
W przypadku przeprowadzania analizy
- Page 38 and 39:
pompaHPLCkolumna chiralnakolumnarea
- Page 40 and 41:
25. K. Lorenz, E. Yashima, Y. Okamo
- Page 42 and 43:
Tlen, chociaż jest konieczny do ż
- Page 44 and 45:
σ2∗pπ * 2pπ 2pσ 2psingletowy
- Page 46 and 47:
Rozpuszczalność tlenku azotu w wo
- Page 48 and 49:
nia wolnych rodników. Dlatego nie
- Page 50 and 51:
na do nich również poliaminy biog
- Page 52 and 53:
trwały rodnik, możliwy do oznacze
- Page 54 and 55:
cej zmiany stężenia detektora lub
- Page 56 and 57:
Rodniki hydroksylowe są wyjątkowo
- Page 58 and 59:
COOHOCOCH3aspirynahydrolizaCOOHCOC
- Page 60 and 61:
W statycznej, chromatograficznej me
- Page 62 and 63:
sowej. Warto zwrócić w tym przypa
- Page 64 and 65:
35. W. Pakszys, B.K. Głód, P.P. L
- Page 66 and 67: 95. A. Ghiselli, M. Serafini, F. Na
- Page 68 and 69: nych umożliwiających oznaczanie f
- Page 70 and 71: W monitoringu wód powierzchniowych
- Page 72: RT: 4.01 - 19.97IntensityIntensity1
- Page 75 and 76: Ciekawą rolę pełnią zbiorniki w
- Page 77: Stosowana w badaniach procedura ana
- Page 80 and 81: wania substancji, zwłaszcza, w ska
- Page 82 and 83: - Kolumnowa, elucyjna chromatografi
- Page 84 and 85: Przykłady a, a’, b, b’, c, c
- Page 86 and 87: ZJAWISKA PRZEŁADOWANIA KOLUMNY (PO
- Page 88 and 89: ZASADY OPTYMALNEGO STOSOWANIA PREPA
- Page 90 and 91: - przeładowanie objętościoweW ch
- Page 92 and 93: Średnica kolumnyNajbardziej celowe
- Page 94 and 95: Średnica ziaren wypełnienia kolum
- Page 96 and 97: RetencjaSilna retencja składników
- Page 98 and 99: OPERACJE JEDNOSTKOWE I TECHNOLOGIA
- Page 100 and 101: Rys. 10. Schemat ideowy chromatogra
- Page 102 and 103: Na rys. 13 pokazano kilka chromatog
- Page 104 and 105: fizycznych i hydrodynamicznych w ko
- Page 106 and 107: Nie opanowany do końca problem sta
- Page 108 and 109: Rys. 18. Przykłady reprezentowanyc
- Page 110 and 111: LITERATURA UZUPEŁNIAJĄCA (pozycje
- Page 112 and 113: 14. Hupe K.P. and Lauer H.H., J. Ch
- Page 114 and 115: stość izolowanych substancji. Pep
- Page 118 and 119: 51243678 90 2 4 6 8 10 12 14 16Rys.
- Page 120 and 121: jące długie łańcuchy alkilowe,
- Page 122 and 123: Tabela 2. Modyfikatory fazy ruchome
- Page 124 and 125: nowymiennych, równorzędnie kation
- Page 126 and 127: UKŁADY ADSORPCYJNE I ADSORPCYJNO-J
- Page 128 and 129: CHROMATOGRAFIA ŻELOWAChromatografi
- Page 130 and 131: CHROMATOGRAFIA ODDZIAŁYWAŃ HYDROF
- Page 132 and 133: związków. Połączenie elektrofor
- Page 134 and 135: METODY DETEKCJI W CHROMATOGRAFII PE
- Page 136 and 137: [25] S.U. Sane, S.M. Cramer, T.M. P