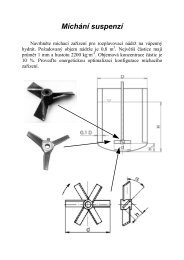
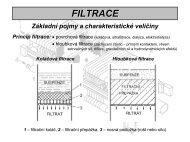
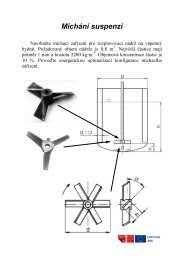
PÅednáška odsiÅovánà 2012-13
PÅednáška odsiÅovánà 2012-13
PÅednáška odsiÅovánà 2012-13
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Odsiřování<br />
Ochrana ovzduší<br />
ZS <strong>2012</strong>/20<strong>13</strong><br />
1
Úvod<br />
• Produkce emisí SO 2<br />
– antropogenní zdroje:<br />
• zejména spalování fosilních paliv obsahujících síru<br />
• různé průmyslové procesy<br />
– přírodní zdroje:<br />
• bakteriální činnost, vulkanická činnost, požáry vegetace,<br />
aerosoly z mořské tříště<br />
2
Oxid siřičitý SO 2 a oxid sírový SO 3<br />
Oxid siřičitý<br />
• Bezbarvý, nehořlavý plyn se štiplavým zápachem<br />
• M mol,SO2 = 64,06 kg/kmol<br />
• V mol,SO2,N = 21,89 m 3 /kmol<br />
• ρ SO2,N = 2,93 kg/m 3<br />
• Čichový práh<br />
• V ovzduší přechází na oxid sírový SO 3<br />
– bezbarvý plyn<br />
– ρ SO3,N = 1,995 kg/m 3<br />
3
Oxid siřičitý SO 2 a oxid sírový SO 3<br />
• Hydratace vzdušnou vlhkostí<br />
• Oxidy síry – součást „londýnského smogu“<br />
Zdravotní účinky SO 2<br />
• akutní<br />
• při dlouhodobé expozici a vyšších koncentracích<br />
Negativní účinky SO 2<br />
4
Legislativa<br />
Imise (dle zákona č. 201/<strong>2012</strong> Sb.)<br />
• Imisní limity pro SO 2 jako součást limitů pro ochranu zdraví<br />
• Imisní limit pro ochranu ekosystémů a vegetace<br />
Emise (dle zákona č. 201/<strong>2012</strong> Sb.)<br />
• Emisní limity – obecné<br />
– specifické<br />
• E.L. budou vydány vyhláškou MŽP<br />
• Dle předchozí legislativy:<br />
– pro ZV, V a S zdroje<br />
– podle druhu paliva<br />
– podle data uvedení do provozu<br />
5
Emise SO 2<br />
• Významný pokles v 90. letech min. století<br />
• Po r. 2000 okolo 220 kt/rok<br />
• V r. 2008: 174 kt, většina jsou emise ze stacionárních zdrojů,<br />
hlavně ZV a V<br />
6
• Vznik emisí<br />
Metody snižování emisí síry<br />
• S → SO 2 → SO 3 (2%)<br />
• Při spalování tuhých paliv – většina S přechází na SO 2<br />
• Při spalování kapalných a plynných paliv – veškerá S přechází<br />
na SO 2<br />
• Závislost množství emisí na měrné sirnatosti paliva<br />
S<br />
m<br />
( g<br />
síry<br />
S<br />
/ MJ ) =<br />
Q<br />
r<br />
p<br />
(%) ⋅10<br />
( MJ<br />
/ kg)<br />
• ČR H.U.: S p = 0,5 až 1,4 %, Q r = 10 až 20 MJ/kg,<br />
S m = 0,4 až 1,3 g síry /MJ<br />
7
Metody snižování emisí síry<br />
• Požadavky na kvalitu paliv z hlediska ochrany ovzduší pro M<br />
a S zdroje<br />
• Primárně – snižování spotřeby paliv<br />
• Základní způsoby odsíření spalin:<br />
• spalování nízkosirnatých paliv<br />
• odsiřování uhlí<br />
• odsiřování spalin<br />
8
Odsiřování uhlí<br />
• Problematické<br />
• Metody:<br />
– mechanické<br />
– chemické<br />
– biologické<br />
• Síra je v uhlí ve 3 formách:<br />
– pyritická<br />
– síranová<br />
– organická<br />
9
Mechanické postupy<br />
• Separace pyritické síry<br />
Chemické postupy<br />
Odsiřování uhlí<br />
• Převedení uhlí do kapalné nebo plynné fáze a následné snížení<br />
obsahu S<br />
Biologické postupy<br />
• Loužení uhlí vodou<br />
• Snižování obsahu pyritické síry pomocí bakterií<br />
• Nevýhody<br />
• Obecně – nízká účinnost, komplikované, drahé, nevyužívají se<br />
10
Odsiřování uhlí<br />
Tlakové zplyňování uhlí<br />
• Chemický postup<br />
• Tlakové zplyňování uhlí kyslíkem a vodní párou v tlakovém<br />
generátoru<br />
• Produktem energoplyn<br />
• Využití energoplynu<br />
• Tlaková plynárna ve Vřesové<br />
– 26 tlakových generátorů se sesuvným ložem Lurgi<br />
– paroplynový dvojblok o výkonu 2 x 185 MW<br />
11
• Tlaková plynárna ve Vřesové<br />
Odsiřování uhlí<br />
12
Odsiřování spalin<br />
• Jediná široce aplikovaná metoda<br />
• Nezbytná pro dodržení E.L.<br />
• Charakteristické rysy odsiřování<br />
<strong>13</strong>
Odsiřování spalin<br />
• Řada způsobů odsiřování<br />
• Dělení podle hlediska regenerace činidla:<br />
– metody regenerativní<br />
– metody neregenerativní<br />
• Dělení podle hlediska fáze:<br />
– suché metody<br />
– polosuché metody<br />
– mokré metody<br />
• Dělení podle hlediska místa procesu odsiřování:<br />
– odsiřování přímo v kotli<br />
– odsiřování za kotlem<br />
14
Odsiřování spalin<br />
• Kritéria pro výběr odsiřovací metody:<br />
– splnění emisních limitů,<br />
– složitost technologie,<br />
– prostorová náročnost,<br />
– provozní spolehlivost,<br />
– investiční a provozní náklady,<br />
– vyřešení problematiky likvidace produktu odsiřování<br />
15
Suchá aditivní vápencová metoda<br />
• Nástřik suchého aditiva do ohniště nad zónu plamene<br />
• Aditiva:<br />
– CaCO 3<br />
– CaMg(CO 3 ) 2<br />
– CaO<br />
• Kalcinace vápence<br />
– při t = 900 °C<br />
• Reakce CaO s SO 2<br />
– při t = 600 až 1000 °C<br />
CaO + SO<br />
1<br />
2<br />
+ 2 O2<br />
→ CaSO4<br />
CaCO → CaO +<br />
CaO<br />
CaSO<br />
3<br />
CO 2<br />
+ SO 2<br />
→ CaSO 3<br />
1<br />
3<br />
+ 2 O2<br />
→ CaSO4<br />
16
• Schéma<br />
Suchá aditivní vápencová metoda<br />
• CaSO 4 – odloučen s popílkem v EO<br />
• Účinnost závisí na: t, τ, jemnosti mletí, a<br />
a =<br />
M<br />
M<br />
CaO<br />
CaO,min<br />
17
Suchá aditivní vápencová metoda<br />
• Účinnost odsiřování η SO2<br />
η<br />
SO<br />
2<br />
=<br />
C<br />
SO , výstup<br />
2<br />
( bez odsirovani) − CSO<br />
( s odsirovanim)<br />
2 , výstup<br />
C ( bez odsirovani)<br />
SO , výstup<br />
2<br />
• Při obvyklém a = 2 je η SO2 = maximálně 50 %<br />
• Výhody<br />
• Nevýhody<br />
18
• Využití<br />
Suchá aditivní vápencová metoda<br />
• Schéma – el. Tisová I (do r. 1997)<br />
19
Fluidní spalování s aditivy<br />
• Fluidní kotle – vyšší účinnost suché aditivní metody<br />
• Vhodná pracovní teplota 850 °C<br />
• Dostatečná doba setrvání aditiva<br />
• Výhody<br />
• Nevýhody<br />
20
Fluidní spalování s aditivy<br />
• Kotle se stacionární fluidní vrstvou<br />
– Citlivé na zrnitost aditiva<br />
– η SO2 = 60 % při a = 2<br />
• Kotle s bublající fluidní vrstvou<br />
– vyšší η SO2<br />
• Kotle s cirkulující fluidní vrstvou<br />
– nejdokonalejší<br />
– horký primární odlučovač<br />
– η SO2 = 80 až 85 % při a = 1,5, η SO2 = přes 90 % při a = 2<br />
21
Fluidní spalování s aditivy<br />
• Kotel s cirkulující fluidní vrstvou a přidáváním aditiva<br />
22
Intenzifikace suché aditivní metody<br />
• Schopnost hydratovaného CaO, tj. Ca(OH) 2 vázat SO 2 při<br />
nízkých teplotách blízkých rosnému bodu t r<br />
• Teplota spalin na výstupu z odsiřovací komory – alespoň o<br />
10°C vyšší než t r<br />
V – výstup<br />
blízko φ = 1 ∆t r<br />
=&<br />
∆t ad<br />
23
Intenzifikace suché aditivní metody<br />
• Odsiřovací komora<br />
CaO +<br />
O → Ca( ) 2<br />
( OH )<br />
2<br />
→ CaSO3<br />
H O<br />
( OH ) +<br />
1 O → CaSO H O<br />
H 2<br />
OH<br />
SO2 + Ca<br />
+<br />
2<br />
SO2 + Ca<br />
2 2<br />
4<br />
+<br />
2<br />
2<br />
( OH ) → CaSO H O<br />
SO3 + Ca<br />
4<br />
+<br />
2<br />
2<br />
• Suché produkty<br />
24
Intenzifikace suché aditivní metody<br />
25
Intenzifikace suché aditivní metody<br />
• Recyklace nezreagovaného CaO<br />
• Suchá a mokrá recyklace<br />
• LIFAC (fa Tampella)<br />
suchá recyklace suchá a mokrá recyklace<br />
26
Intenzifikace suché aditivní metody<br />
• Účinnost odsiřování je silně závislá na rozdílu mezi t spalin a t r<br />
• Řízení teploty<br />
• η SO2 = 75 až 80 % při a = 2<br />
27
Polosuchá (mokrosuchá) vápenná metoda<br />
• Rozprašovací sušárna<br />
• Nástřik vodní suspenze Ca(OH) 2<br />
Reaktor od fy<br />
Niro Atomizer<br />
s rotačním rozprašovačem<br />
28
Polosuchá (mokrosuchá) vápenná metoda<br />
• Aditivum:<br />
– CaO<br />
– Ca(OH) 2<br />
• Reakce: SO2 + Ca( OH )<br />
2<br />
→ CaSO3<br />
+ H<br />
2O<br />
SO2 + Ca OH +<br />
1 2 O2<br />
→ CaSO4<br />
+ H<br />
2<br />
( )<br />
2<br />
O<br />
( OH ) → CaSO H O<br />
SO3 + Ca<br />
4<br />
+<br />
2<br />
2<br />
• Výborná účinnost při odstraňování chlorovodíku HCl a<br />
flurovodíku HF<br />
• η HCl, HF = přes 90 % při a = Ca : HCl (HF) = 1<br />
( OH )<br />
2<br />
→ CaCl2<br />
+ 2 H O<br />
( OH ) → CaF + H O<br />
HCl + Ca<br />
2<br />
HF + Ca<br />
2 2<br />
2<br />
2<br />
29
Polosuchá (mokrosuchá) vápenná metoda<br />
• Produkt<br />
• Omezená využitelnost<br />
Účinnost odsiřování<br />
• Tím vyšší, čím je t výstup blíže t ad<br />
• Vyšší lepivost<br />
∆t ad = 10 až 20 °C<br />
• Recirkulace produktu<br />
• η SO2 = 75 % při a = Ca:S = 1,5<br />
• η SO2 = 80 % při a = Ca:S = 1,7<br />
30
Polosuchá (mokrosuchá) vápenná metoda<br />
• Účinnost odsiřování<br />
• Nebezpečí kondenzace spalin za reaktorem<br />
• Koncový odlučovač<br />
31
Polosuchá (mokrosuchá) vápenná metoda<br />
Schéma<br />
32
Polosuchá (mokrosuchá) vápenná metoda<br />
• Využití<br />
• Výhody<br />
• Nevýhody<br />
33
Mokrá vápencová vypírka<br />
• V současnosti nejužívanější metoda při odsiřování velkých<br />
zdrojů<br />
• Vývoj – rozdělení podle produktu<br />
– získávání využitelného energosádrovce CaSO 4·2H 2 O<br />
– získávání nevyužitelného kalu<br />
34
Mokrá vápencová vypírka<br />
• SO 2 se vypírá vodní suspenzí uhličitanu vápenatého CaCO 3<br />
nebo vodní suspenzí vápna Ca(OH) 2<br />
SO +<br />
SO H<br />
2<br />
2<br />
+ CaCO3<br />
→ CaSO3<br />
CO2<br />
2<br />
+ Ca OH<br />
2<br />
→ CaSO3<br />
+<br />
( ) O<br />
• Další reakce CaSO 3<br />
CaSO3 + SO2<br />
+ H<br />
2O<br />
→ Ca HSO<br />
3)<br />
2<br />
+ CaCO3<br />
→ 2<br />
(<br />
3<br />
) 2<br />
Ca ( HSO<br />
CaSO + H O + CO<br />
• Oxidace CaSO 3 a Ca(HSO 3 ) 2 při pH opt = 5 až 6, při nižším pH<br />
vyšší tvorba úsad<br />
CaSO3 + 2 H<br />
2O<br />
+<br />
1 2 O2<br />
→ CaSO4<br />
⋅ 2 H<br />
2O<br />
Ca HSO + 2 H O +<br />
1 O → CaSO ⋅ H O + H SO<br />
(<br />
3<br />
)<br />
2 2 2<br />
4<br />
2<br />
2 2 3<br />
2<br />
3<br />
2<br />
2<br />
35
Mokrá vápencová vypírka<br />
• Sumární vyjádření procesu:<br />
SO 2 H O + CO<br />
1<br />
2<br />
+ CaCO3<br />
+ 2 O2<br />
+ H<br />
2O<br />
→ CaSO4<br />
⋅ 2<br />
2<br />
2<br />
• Sorbernt<br />
– většinou vápenec CaCO 3<br />
– mletí<br />
• Aditiva<br />
36
Mokrá vápencová vypírka<br />
• Účinnost odsiřování η SO2 = 95 % a více při<br />
a = CaCO 3 : SO 2 = 1,02 až 1,07<br />
• Účinné zachytávání HCl a HF s účinností nad 90 %<br />
2 HCl + CaCO3<br />
→ CaCl2<br />
+ CO2<br />
+ H<br />
2O<br />
2 HF + CaCO3<br />
→ CaF2<br />
+ CO2<br />
+ H<br />
2O<br />
• Proces odsíření v absorbéru<br />
• Úprava spalin<br />
• Nutná ochrana proti korozi<br />
37
Mokrá vápencová vypírka<br />
Protiproudý bezvýplňový absorbér<br />
• Nejčastější<br />
• Vstup spalin ve spodní části nad jímkou absorbéru<br />
• Absorpční zóna<br />
• t opt = 60 °C, chlazení spalin<br />
• Odlučovač kapek<br />
• Jímka absorbéru<br />
– oxidační zóna<br />
– neutralizační zóna<br />
38
Mokrá vápencová vypírka<br />
Protiproudý bezvýplňový absorbér Babcock & Wilcox<br />
39
Mokrá vápencová vypírka<br />
Souproudý absorbér<br />
• Menší rozměry<br />
• Přívod spalin a absorpční suspenze vrchem absorbéru<br />
• Umělohmotná výplň<br />
40
Mokrá vápencová vypírka<br />
Souproudo-protiproudý absorbér<br />
• Kombinace protiproudého a souproudého absorbéru<br />
Absorbér SHL<br />
41
Mokrá vápencová vypírka<br />
Tryskově-bublinový absorbér<br />
• Přívod spalin do absorpční suspenze řadou trubek<br />
• Tvorba bublin a pěny<br />
42
Mokrá vápencová vypírka<br />
Protiproudý absorbér se dvěma okruhy<br />
• Hasicí okruh<br />
• Absorpční okruh<br />
protiproudý<br />
43
Mokrá vápencová vypírka<br />
Ochlazení neodsířených a dohřev odsířených spalin<br />
• Regenerativní výměníky tepla<br />
• Rekuperativní výměníky tepla<br />
• Menší zdroje – ve výměníku tepla vnějšími zdroji<br />
Chladicí věže s přirozeným tahem<br />
• Bez dohřevu spalin, spalinového ventilátoru a komína<br />
• Odpar skrápěcí vody<br />
44
Mokrá vápencová vypírka<br />
• Regenerativní výměník tepla (REGAVO)<br />
45
Mokrá vápencová vypírka<br />
• Rekuperativní výměník tepla (EKOGAVO)<br />
46
Mokrá vápencová vypírka<br />
• Produkt: energosádrovec CaSO 4·2H 2 O<br />
• Odvod z jímky absorbéru → hydrocyklóny → pásové n.<br />
bubnové filtry → dosušení → příp. briketování<br />
• Využití<br />
• Výroba sádry CaSO 4·½H 2 O<br />
– kalcinací<br />
CaSO H O CaSO<br />
1<br />
H O<br />
3<br />
4<br />
⋅2<br />
2<br />
↔<br />
4<br />
⋅ 2 2<br />
+ 2 H<br />
2O<br />
– využití ve stavebnictví<br />
47
Mokrá vápencová vypírka<br />
• Problém tvorby úsad a nánosů<br />
• Nánosy – měkké<br />
– tvrdé<br />
• Odstraňování<br />
• Omezení vzniku – konstrukce, technologie<br />
48
Mokrá vápencová vypírka<br />
Výhody<br />
Nevýhody<br />
49
Schéma<br />
Mokrá vápencová vypírka<br />
50
Mokrá vápencová vypírka<br />
Schéma odsiřování v el. Chvaletice s chladicími věžemi<br />
51
Mokrá vápencová vypírka<br />
• Nejrozšířenější metoda odsiřování<br />
• V ČR využití technologií řady firem<br />
Parametry odsiřovacího zařízení elektrárny Chvaletice<br />
počet a výkon odsiřovaných bloků<br />
počet absorbérů<br />
objem spalin do jednoho absorbéru<br />
obsah SO 2<br />
v nevyčištěných spalinách<br />
koncentrace popílku na vstupu do absorbéru<br />
obsah SO 2<br />
v čistých spalinách<br />
koncentrace TZL v čistých spalinách<br />
účinnost odsíření<br />
4 x 200 MW e<br />
2<br />
583 200 až 2 174 400 Nm 3 /h<br />
7 000 mg/Nm 3<br />
max. 200 mg/Nm 3<br />
garantováno 400, běžně do 200 mg/Nm 3<br />
garantováno 50, běžně do 20 mg/Nm 3<br />
94,3 % a vyšší<br />
52
Odsiřování<br />
Způsob odsíření z kotlů Skupiny ČEZ<br />
elektrárna<br />
Elektrárna Dětmarovice<br />
Elektrárna Hodonín<br />
Elektrárna Chvaletice<br />
Elektrárna Ledvice<br />
Elektrárna Mělník II<br />
Elektrárna Mělník III<br />
Elektrárna Počerady<br />
Elektrárna Poříčí II<br />
Elektrárna Prunéřov I<br />
Elektrárna Prunéřov II<br />
Elektrárna Tisová I<br />
Elektrárna Tisová II<br />
Elektrárna Tušimice II<br />
bloky<br />
4 x 200 MW<br />
50 MW, 55 MW<br />
4 x 200 MW<br />
3 x 110 MW<br />
2 x 110 MW<br />
500 MW<br />
5 x 200 MW<br />
3 x 55 MW<br />
4 x 110 MW<br />
5 x 210 MW<br />
2 bloky pro<br />
3 x 57 MW + 1 x 12,8 MW<br />
112 MW<br />
4 x 200 MW<br />
metoda odsiřování<br />
mokrá vápencová<br />
fluidní spalování<br />
mokrá vápencová<br />
2 x polosuchá metoda<br />
1 fluidní kotel<br />
mokrá vápencová<br />
mokrá vápencová<br />
mokrá vápencová<br />
fluidní spalování<br />
mokrá vápencová<br />
mokrá vápencová<br />
fluidní spalování<br />
mokrá vápencová<br />
mokrá vápencová<br />
53
• Regenerace činidla<br />
• Malé rozšíření<br />
Regenerativní metody<br />
Natrium-sulfitová metoda (metoda Wellmann-Lord)<br />
• Reakce v absorbéru<br />
Na<br />
2SO3<br />
+ SO2<br />
+ H<br />
2O<br />
→ 2 NaHSO3<br />
• Regenerace<br />
• Využití SO 2<br />
• Vstupní suroviny: NaOH nebo Na 2 CO 3<br />
• Nejrozšířenější regenerativní metoda<br />
• Výhody<br />
• Nevýhody<br />
54
Regenerativní metody<br />
Schéma natrium-sulfitové metody<br />
55
Regenerativní metody<br />
Magnezitová metoda<br />
• Vypírka SO 2 ve vodní suspenzi MgO<br />
• Reaktor za odlučovačem popílku<br />
• Konečný produkt MgSO 3<br />
– rozklad při vysokých T<br />
• Nežádoucí produkt MgSO 4<br />
• Výhody<br />
• Nevýhody<br />
56
Katalytické metody<br />
• Suché metody<br />
• Regenerativní i neregenerativní<br />
• Katalytická oxidace SO 2 na SO 3<br />
• Výhody<br />
• Nevýhody<br />
• Většinou v kombinaci s denitrifikací spalin<br />
57
Katalytické metody<br />
Proces Cat-ox<br />
• Oxidace SO 2 na SO 3 na katalyzátoru V 2 O 5 při T = 450 °C<br />
• Vypírání SO 3 kyselinou sírovou v absorbéru<br />
58
Proces Haldor-Topsøe<br />
Katalytické metody<br />
• Oxidace SO 2 na SO 3 na katalyzátoru V 2 O 5<br />
• Při chlazení kondenzována kyselina sírová ve skleněném<br />
chladiči<br />
Proces Kyioura, proces Chiyoda<br />
59
Adsorpční metody<br />
• Suché metody<br />
• Adsorpce SO 2 na aktivním uhlí nebo koksu<br />
• Většinou regenerace činidla<br />
• Proces Sulfacid, proces Bergau-Forschung<br />
60