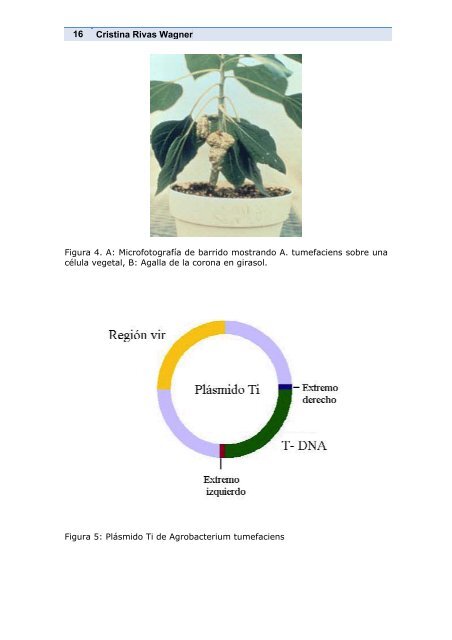
16 Cristina Rivas Wagner Figura 4. A: Microfotografía de barrido mostrando A. tumefaciens sobre una célula vegetal, B: Agalla de la corona en girasol. Figura 5: Plásmido Ti de Agrobacterium tumefaciens
<strong>Plantas</strong> y <strong>cultivos</strong> <strong>transgénicos</strong> 17 II) Transformación de células de Agrobacterium con el / los genes de interés. Veamos ahora como podemos introducir los plásmidos que contienen los genes de interés, en las células de Agrobacterium (transformación). Pese a que los oncogenes son los responsables de la producción de tumores, las únicas regiones del T- ADN esenciales para su transferencia son las secuencias de aproximadamente 25 pb localizadas en sus extremidades. De este modo, los genes presentes en el T - ADN pueden ser eliminados y sustituidos, sin alterar el proceso de transferencia. Además de las extremidades del T - ADN, la región vir también es esencial para la transferencia. La preparación de un linaje de Agrobacterium para ser utilizado como vector para la transformación de plantas transgénicas, incluye dos etapas: En la primera etapa, se debe obtener un “linaje desarmado”, en el cual el T-ADN original, con sus oncogenes fue eliminado por un proceso de doble recombinación. Actualmente disponemos de linajes desarmados, obtenidos a partir de linajes salvajes de diferentes orígenes. La segunda etapa, implica la preparación de un vector conteniendo el T- ADN con los genes de interés. Debido a su gran tamaño (aproximadamente 200 kb), el plásmido Ti no puede ser manipulado directamente, por lo que se emplean plásmidos más pequeños (vectores), que resultan fáciles de manipular. Estos vectores contienen las extremidades del T-ADN, entre las cuales se clonan los genes de interés. Una vez obtenido el vector, este debe ser transferido al Agrobacterium mediante un proceso que se conoce con el nombre de transformación. Se han desarrollado tres métodos de transformación: conjugación, electroporación y shock térmico: a) Conjugación: se trata de un método simple y eficiente que no requiere de equipamiento específico y prescinde de la preparación de ADN plasmidial de E. coli. En el protocolo más común, se realiza un cocultivo de dos l inajes de E. coli (“helper” y “donante”) y un linaje de Agrobacterium (receptora), según puede apreciarse en la Figura 6. El linaje “helper” suministra las funciones de movilización (mob) y transferencia ( tra) de plásmidos, entre bacterias compatibles, mientras que el linaje “donante”, contiene el vector que será transferido. Durante la conjugación, el plásmido ‘helper” es transferido al linaje donante, promoviendo posteriormente su movilización hacia Agrobacterium, junto con el vector. El plásmido “helper” no se replica en Agrobacterium, y por lo tanto es eliminado. Luego de la transferencia, se seleccionan los linajes recombinates de Agrobacterium mediante el uso de antibióticos apropiados. La principal desventaja de la conjugación es la posibilidad de que ocurran alteraciones en el plásmido introducido, debido a la recombinación con el plásmido ‘helper”.