actualizaciones farmacológicas - Aula de la Farmacia
actualizaciones farmacológicas - Aula de la Farmacia
actualizaciones farmacológicas - Aula de la Farmacia
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
ACTUALIZACIONES FARMACOLÓGICAS<br />
Hiperp<strong>la</strong>sia benigna <strong>de</strong> próstata<br />
Antonio Barbero González<br />
Farmacéutico Comunitario. Miembro <strong>de</strong> SEFaC. Miembro <strong>de</strong> <strong>la</strong> REAP.<br />
Patrono Fundación Pharmaceutical Care<br />
1. Síntesis <strong>de</strong> testosterona<br />
Para enten<strong>de</strong>r tanto el <strong>de</strong>sarrollo <strong>de</strong> <strong>la</strong> hiperp<strong>la</strong>sia<br />
benigna <strong>de</strong> próstata, como los mecanismos<br />
<strong>de</strong> acción <strong>de</strong> los medicamentos utilizados<br />
en su tratamiento, conviene que previamente<br />
estudiemos cómo es el ciclo <strong>de</strong> <strong>la</strong> síntesis<br />
y regu<strong>la</strong>ción <strong>de</strong> <strong>la</strong>s hormonas masculinas<br />
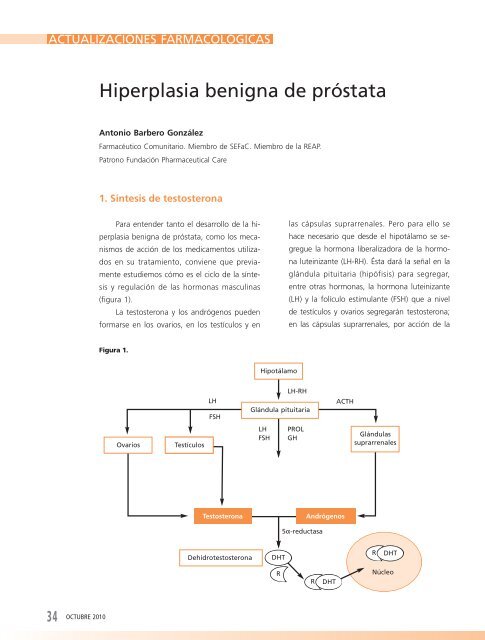
(figura 1).<br />
La testosterona y los andrógenos pue<strong>de</strong>n<br />
formarse en los ovarios, en los testículos y en<br />
<strong>la</strong>s cápsu<strong>la</strong>s suprarrenales. Pero para ello se<br />
hace necesario que <strong>de</strong>s<strong>de</strong> el hipotá<strong>la</strong>mo se segregue<br />
<strong>la</strong> hormona liberalizadora <strong>de</strong> <strong>la</strong> hormona<br />
luteinizante (LH-RH). Ésta dará <strong>la</strong> señal en <strong>la</strong><br />
glándu<strong>la</strong> pituitaria (hipófisis) para segregar,<br />
entre otras hormonas, <strong>la</strong> hormona luteinizante<br />
(LH) y <strong>la</strong> folículo estimu<strong>la</strong>nte (FSH) que a nivel<br />
<strong>de</strong> testículos y ovarios segregarán testosterona;<br />
en <strong>la</strong>s cápsu<strong>la</strong>s suprarrenales, por acción <strong>de</strong> <strong>la</strong><br />
Figura 1.<br />
Hipotá<strong>la</strong>mo<br />
LH<br />
FSH<br />
LH-RH<br />
Glándu<strong>la</strong> pituitaria<br />
ACTH<br />
Ovarios<br />
Testículos<br />
LH<br />
FSH<br />
PROL<br />
GH<br />
Glándu<strong>la</strong>s<br />
suprarrenales<br />
Testosterona<br />
Andrógenos<br />
5α-reductasa<br />
Dehidrotestosterona<br />
DHT<br />
R<br />
DHT<br />
R<br />
R<br />
DHT<br />
Núcleo<br />
34<br />
OCTUBRE 2010
hormona adrenocorticotropa (ACTH), se sintetizarán<br />
andrógenos, especialmente androstenodiona.<br />
La testosterona y los andrógenos no son<br />
<strong>la</strong>s verda<strong>de</strong>ras hormonas activas, sino que tienen<br />
que ser transformados por medio <strong>de</strong>l enzima<br />
5α-reductasa en <strong>la</strong> <strong>de</strong>hidrotestosterona<br />
(DHT), que es <strong>la</strong> verda<strong>de</strong>ra hormona sexual activa.<br />
La DHT formada se une a su receptor específico<br />
y <strong>de</strong>ntro <strong>de</strong>l núcleo <strong>de</strong> <strong>la</strong>s célu<strong>la</strong>s facilitará<br />
<strong>la</strong> síntesis proteica para dar lugar al efecto<br />
sexual masculino correspondiente.<br />
Existen dos tipos <strong>de</strong> 5α-reductasa:<br />
• Tipo I. Se localiza en los folículos pilosos,<br />
glándu<strong>la</strong>s sebáceas <strong>de</strong>l cuero cabelludo frontal,<br />
hígado y piel. La DHT producida en<br />
estos tejidos es responsable <strong>de</strong>l acné, incremento<br />
<strong>de</strong>l pelo corporal y facial y <strong>la</strong> calvicie<br />
androgénica.<br />
• Tipo II. Se localiza en <strong>la</strong> próstata, tejido genital<br />
y cuero cabelludo. La DHT producida<br />
en <strong>la</strong> próstata es <strong>la</strong> responsable <strong>de</strong>l agrandamiento<br />
y crecimiento <strong>de</strong> <strong>la</strong> misma.<br />
2. Hiperp<strong>la</strong>sia benigna <strong>de</strong><br />
próstata (HBP)<br />
Figura 2. Aparato reproductor masculino vejiga<br />
Próstata<br />
Uretra<br />
Pene<br />
Epididimo<br />
Vejiga<br />
Algunos autores <strong>la</strong> <strong>de</strong>nominan hipertrofia<br />
benigna <strong>de</strong> próstata. Sin embargo, <strong>la</strong> mayoría<br />
prefieren el término <strong>de</strong> hiperp<strong>la</strong>sia benigna <strong>de</strong><br />
próstata, ya que <strong>de</strong>scribe mejor el proceso que<br />
se produce cuando se visualizan <strong>la</strong>s célu<strong>la</strong>s<br />
epiteliales a través <strong>de</strong>l microscopio electrónico.<br />
El término hiperp<strong>la</strong>sia pue<strong>de</strong> indicar <strong>la</strong> formación<br />
<strong>de</strong> un tejido nuevo a expensas <strong>de</strong> tejido<br />
sano, no diferenciándose en nada, ni en su<br />
forma ni en sus funciones, <strong>de</strong> sus generadores;<br />
<strong>la</strong> segunda acepción indica un <strong>de</strong>sarrollo<br />
exagerado <strong>de</strong> un tejido o <strong>de</strong> un órgano.<br />
Sin embargo, <strong>la</strong> hipertrofia indica un aumento<br />
<strong>de</strong> nutrición <strong>de</strong> un órgano. Es <strong>de</strong>cir,<br />
aumento <strong>de</strong> gasto en el consumo <strong>de</strong> nutrientes,<br />
aunque se emplea normalmente como sinónimo<br />
<strong>de</strong> aumento <strong>de</strong> volumen <strong>de</strong> un órgano.<br />
Otro término mal utilizado es el <strong>de</strong> prostatitis.<br />
Este término implica una inf<strong>la</strong>mación <strong>de</strong><br />
<strong>la</strong> glándu<strong>la</strong> prostática, pero el origen en algunos<br />
casos son infecciones bacterianas y se conoce<br />
como prostatitis bacteriana; <strong>la</strong> prostatitis<br />
no bacteriana es un proceso que cursa con<br />
dolor y es conocido también como síndrome<br />
<strong>de</strong> dolor crónico pélvico.<br />
2.1. ¿Qué es <strong>la</strong> próstata?<br />
Ano<br />
Conductos <strong>de</strong>ferentes<br />
Testículo<br />
Escroto<br />
Facia espermática<br />
La próstata es una glándu<strong>la</strong> sexual masculina<br />
que tiene dos funciones: segregar fluidos<br />
que forman una parte, hasta un 20-40%,<br />
<strong>de</strong>l volumen total <strong>de</strong>l líquido <strong>de</strong> <strong>la</strong> eyacu<strong>la</strong>ción,<br />
y dar lugar a secreciones con un posible<br />
efecto antibacteriano <strong>de</strong>bido a <strong>la</strong>s altas concentraciones<br />
<strong>de</strong> zinc.<br />
La próstata se encuentra situada <strong>de</strong>trás<br />
<strong>de</strong> <strong>la</strong> vejiga urinaria y ro<strong>de</strong>ando a <strong>la</strong> uretra<br />
(ver figura 2) Al nacer, <strong>la</strong> próstata pesa 1 g<br />
aproximadamente. En <strong>la</strong> pubertad aumenta el<br />
volumen hasta llegar a los 15-20 g. Des<strong>de</strong> <strong>la</strong><br />
Vesícu<strong>la</strong>s<br />
Seminales<br />
Recto<br />
OCTUBRE 2010 35
ACTUALIZACIONES FARMACOLÓGICAS<br />
edad <strong>de</strong> 25-30 años, <strong>la</strong> próstata permanece<br />
en ese tamaño hasta los 40 años que comienza<br />
su segundo crecimiento que continúa hasta<br />
que el hombre tiene 70-80 años. Durante este<br />
período, el tamaño <strong>de</strong> <strong>la</strong> próstata pue<strong>de</strong> dob<strong>la</strong>rse<br />
o incluso triplicarse.<br />
La glándu<strong>la</strong> prostática está formada por<br />
tres tipos <strong>de</strong> tejidos: tejido epitelial, estroma<br />
(músculo liso) y cápsu<strong>la</strong>. Al tejido epitelial también<br />
se le conoce como tejido g<strong>la</strong>ndu<strong>la</strong>r, y es<br />
el que produce <strong>la</strong>s secreciones prostáticas.<br />
Estas secreciones se eliminan a <strong>la</strong> uretra durante<br />
<strong>la</strong> eyacu<strong>la</strong>ción y contribuyen al volumen<br />
<strong>de</strong>l líquido eyacu<strong>la</strong>torio, que se compone <strong>de</strong><br />
este fluido y el que se produce en <strong>la</strong>s vesícu<strong>la</strong>s<br />
seminales y los espermatozoi<strong>de</strong>s <strong>de</strong> los testículos.<br />
El tejido epitelial se encuentra bajo el<br />
control <strong>de</strong> andrógenos, es <strong>de</strong>cir, los andrógenos<br />
estimu<strong>la</strong>n el crecimiento <strong>de</strong> tejido epitelial.<br />
El tejido <strong>de</strong>l estroma, formado por tejido<br />
muscu<strong>la</strong>r liso, es abundante en receptores α-<br />
adrenérgicos. La estimu<strong>la</strong>ción <strong>de</strong> estos receptores<br />
por noradrenalina da a lugar a una contracción<br />
<strong>de</strong>l músculo liso produciéndose una<br />
compresión <strong>de</strong> <strong>la</strong> uretra, reduciéndose <strong>la</strong> luz<br />
<strong>de</strong>l lumen y disminuyendo el vaciado <strong>de</strong> <strong>la</strong> vejiga<br />
urinaria.<br />
La cápsu<strong>la</strong>, o capa externa <strong>de</strong> <strong>la</strong> próstata,<br />
está compuesta por tejido conectivo fibroso y<br />
músculo liso que también está lleno <strong>de</strong> receptores<br />
α-adrenérgicos. Por lo tanto, cuando es<br />
estimu<strong>la</strong>do por noradrenalina, <strong>la</strong> cápsu<strong>la</strong> también<br />
se contrae alre<strong>de</strong>dor <strong>de</strong> <strong>la</strong> uretra.<br />
2.2. ¿Cómo se produce <strong>la</strong> hiperp<strong>la</strong>sia<br />
benigna <strong>de</strong> próstata?<br />
Durante <strong>la</strong> primera fase <strong>de</strong> <strong>la</strong> HBP, <strong>de</strong>bido<br />
a <strong>la</strong> edad y por estimu<strong>la</strong>ción androgénica, el<br />
tejido prostático crece produciendo un agrandamiento<br />
(aumento <strong>de</strong>l tamaño) <strong>de</strong> <strong>la</strong> próstata.<br />
Esto provoca una presión sobre <strong>la</strong> uretra,<br />
disminuyendo <strong>la</strong> luz <strong>de</strong> <strong>la</strong> misma, como resultado<br />
<strong>de</strong> <strong>la</strong> obstrucción mecánica. Si <strong>la</strong> presión<br />
se incrementa, los pacientes pue<strong>de</strong>n experimentar<br />
dificultad para comenzar a orinar o<br />
pue<strong>de</strong> dar lugar a una disminución <strong>de</strong>l flujo<br />
urinario. Algunos pacientes tienen que presionar<br />
ellos mismos <strong>la</strong> vejiga para comenzar a<br />
orinar. A medida que los síntomas empeoran,<br />
<strong>la</strong> vejiga urinaria podría hacerse más reactiva.<br />
Esto da lugar a <strong>la</strong> siguiente fase <strong>de</strong> <strong>la</strong> HBP, en<br />
<strong>la</strong> que siempre queda un remanente <strong>de</strong> orina<br />
en <strong>la</strong> vejiga que pue<strong>de</strong> causar que este órgano<br />
se haga hipersensible. Es <strong>de</strong>cir, que incluso pequeñas<br />
restos <strong>de</strong> orina, junto con <strong>la</strong> presión<br />
<strong>de</strong>l agrandamiento <strong>de</strong> <strong>la</strong> próstata, hace que<br />
los pacientes experimenten poliuria (sensación<br />
<strong>de</strong> tener ganas <strong>de</strong> orinar muy a menudo).<br />
Por otro <strong>la</strong>do, un excesivo tono α-adrenérgico<br />
bloquea el cuello <strong>de</strong> <strong>la</strong> vejiga urinaria<br />
y <strong>la</strong> uretra posterior, dando lugar a una contracción<br />
<strong>de</strong> <strong>la</strong> glándu<strong>la</strong> prostática alre<strong>de</strong>dor <strong>de</strong><br />
<strong>la</strong> uretra estrechando el lumen uretral.<br />
2.3. Signos y síntomas<br />
Es necesario comentar que existen hombres<br />
que, aunque tienen agrandamiento <strong>de</strong> <strong>la</strong><br />
próstata, no llegan a tener síntomas significativamente<br />
molestos. Sin embargo, lo normal es<br />
lo contrario. Los signos y síntomas más característicos<br />
<strong>de</strong> <strong>la</strong> hiperp<strong>la</strong>sia benigna <strong>de</strong> próstata<br />
(HBP) son:<br />
Síntomas obstructivos:<br />
• Retraso en el inicio <strong>de</strong> <strong>la</strong> micción.<br />
• Disminución <strong>de</strong>l calibre y fuerza <strong>de</strong>l chorro.<br />
• Micción intermitente o prolongada.<br />
• Goteo postmiccional.<br />
• Sensación <strong>de</strong> micción incompleta.<br />
• Retención urinaria.<br />
36<br />
OCTUBRE 2010
Figura 3.<br />
HBP<br />
Síntomas leves<br />
Síntomas<br />
mo<strong>de</strong>rados<br />
Síntomas severos<br />
y complicados<br />
Esperar y ver<br />
Antagonistas α-adrenérgicos<br />
o Inhibidor 5α-reductasa<br />
Antagonistas α-adrenérgicos<br />
e Inhibidor 5α-reductasa<br />
CIRUGÍA<br />
Si respon<strong>de</strong>, continuar<br />
Si no respon<strong>de</strong><br />
• Incontinencia por rebosamiento.<br />
Síntomas irritativos:<br />
• Po<strong>la</strong>quiuria.<br />
• Nicturia.<br />
• Urgencia miccional.<br />
• Incontinencia por urgencia.<br />
Evi<strong>de</strong>ntemente estos síntomas pue<strong>de</strong>n ser<br />
indicativos <strong>de</strong> otros problemas <strong>de</strong> salud: prostatitis,<br />
cáncer <strong>de</strong> próstata e infección <strong>de</strong>l tracto<br />
urinario. Para realizar un diagnóstico diferencial,<br />
el médico tendrá que realizar algunos<br />
procedimientos como el examen rectal digital<br />
y <strong>la</strong> <strong>de</strong>terminación <strong>de</strong> <strong>la</strong> PSA (antígeno específico<br />
<strong>de</strong> <strong>la</strong> próstata) para <strong>de</strong>scartar otras condiciones.<br />
2.4. Tratamiento <strong>de</strong> <strong>la</strong> hiperp<strong>la</strong>sia<br />
benigna <strong>de</strong> próstata<br />
El objetivo principal <strong>de</strong>l tratamiento <strong>de</strong> <strong>la</strong><br />
hiperp<strong>la</strong>sia benigna <strong>de</strong> próstata es aliviar o<br />
mejorar los síntomas, a<strong>de</strong>más <strong>de</strong> parar <strong>la</strong> progresión<br />
y prevenir <strong>la</strong>s complicaciones. En líneas<br />
generales, lo que se busca es mejorar <strong>la</strong> calidad<br />
<strong>de</strong> vida <strong>de</strong> estos pacientes. Por ello, los<br />
tratamientos que se p<strong>la</strong>ntean <strong>de</strong>berían ser<br />
aceptados también por los pacientes.<br />
El algoritmo que aparece en <strong>la</strong> figura 3 es<br />
quizás el más utilizado entre los médicos a <strong>la</strong><br />
hora <strong>de</strong> <strong>de</strong>cidir el tratamiento <strong>de</strong> estos pacientes.<br />
El médico, para po<strong>de</strong>r discernir entre síntomas<br />
leves, síntomas mo<strong>de</strong>rados o síntomas severos,<br />
utiliza cuestionarios validados que intentan<br />
c<strong>la</strong>sificar a los pacientes <strong>de</strong> acuerdo a los<br />
síntomas que presentan. El cuestionario más<br />
utilizado y validado en España es el Baremo Internacional<br />
<strong>de</strong> los Síntomas Prostáticos (IPSS)<br />
(Figura 4). En él se pregunta al paciente por<br />
síntomas que haya pa<strong>de</strong>cido en el mes anterior<br />
y se le indica que lo c<strong>la</strong>sifique en una esca<strong>la</strong> <strong>de</strong><br />
0 a 5. Posteriormente se sumarán los puntos<br />
obtenidos y se c<strong>la</strong>sificarán los síntomas en<br />
leves, mo<strong>de</strong>rados y severos según <strong>la</strong>s puntuaciones:<br />
OCTUBRE 2010 37
ACTUALIZACIONES FARMACOLÓGICAS<br />
Figura 4. Baremo Internacional <strong>de</strong> los síntomas prostáticos (IPSS)<br />
Ninguna<br />
Menos <strong>de</strong> 1 vez<br />
cada 5 veces<br />
Menos <strong>de</strong> <strong>la</strong> mitad<br />
<strong>de</strong> <strong>la</strong>s veces<br />
Alre<strong>de</strong>dor <strong>de</strong> <strong>la</strong><br />
mitad <strong>de</strong> <strong>la</strong>s veces<br />
Más <strong>de</strong> <strong>la</strong> mitad<br />
<strong>de</strong> <strong>la</strong>s veces<br />
Casi<br />
siempre<br />
1. Durante el último mes ¿con<br />
qué frecuencia ha tenido <strong>la</strong><br />
sensación <strong>de</strong> no vaciar<br />
completamente su vejiga al<br />
acabar <strong>de</strong> orinar?<br />
2. Durante el último mes, ¿con<br />
qué frecuencia ha tenido que<br />
orinar <strong>de</strong> nuevo en menos <strong>de</strong><br />
2 horas <strong>de</strong>spués <strong>de</strong> haberlo<br />
acabado <strong>de</strong> hacer?<br />
3. Durante el último mes, ¿con<br />
qué frecuencia ha<br />
interrumpido y reanudado<br />
varias veces el chorro<br />
mientras orinaba?<br />
4. Durante el último mes,<br />
¿con qué frecuencia ha<br />
tenido dificultad para<br />
retrasar o aguantar<br />
<strong>la</strong>s ganas <strong>de</strong> orinar?<br />
5. Durante el último mes,<br />
¿con qué frecuencia ha<br />
tenido un chorro con menos<br />
fuerza <strong>de</strong> lo habitual?<br />
0<br />
0<br />
0<br />
0<br />
0<br />
1 2 3 4 5<br />
1 2 3 4 5<br />
1 2 3 4 5<br />
1 2 3 4 5<br />
1 2 3 4 5<br />
6. Durante el último mes, ¿con<br />
qué frecuencia ha tenido que<br />
esforzarse o apretar para<br />
comenzar a orinar?<br />
7. Durante el último mes,<br />
¿Cuántas veces ha tenido<br />
que levantarse para orinar<br />
<strong>de</strong>s<strong>de</strong> que se acuesta por <strong>la</strong><br />
noche hasta que se levanta<br />
por <strong>la</strong> mañana?<br />
0<br />
0<br />
1 2 3 4 5<br />
1 2 3 4 5<br />
Entre aceptable<br />
P<strong>la</strong>centero Agradable Aceptable<br />
e inaceptable<br />
Inaceptable Desgraciado Terriblemente<br />
mal<br />
Si tuviera que pasar el resto<br />
<strong>de</strong> su vida con los problemas<br />
urinarios que ahora tiene,<br />
¿cómo se sentiría?<br />
0 1 2 3 4 5 6<br />
38<br />
OCTUBRE 2010
• 0-7 puntos: síntomas leves<br />
• 8-19 puntos: síntomas mo<strong>de</strong>rados<br />
• 20-35 puntos: síntomas severos<br />
Existe una última pregunta que tiene que<br />
ver con <strong>la</strong> calidad <strong>de</strong> vida <strong>de</strong>l paciente y que<br />
sirve para <strong>de</strong>cidir si es conveniente dar o no<br />
tratamiento al paciente según <strong>la</strong> puntuación<br />
obtenida:<br />
• 0-2 puntos: ligera<br />
• 3 puntos: mo<strong>de</strong>rada<br />
• 4-6 puntos: severa<br />
Para aquellos pacientes cuyos síntomas<br />
son muy leves o poco molestos (ver figura 3), lo<br />
que se propone es no dar tratamiento y hacer<br />
lo que se l<strong>la</strong>ma espera vigi<strong>la</strong>nte o esperar y ver.<br />
Es <strong>de</strong>cir, que al paciente se le recomienda visitas<br />
al médico cada 6-12 meses para revisión. En<br />
estas revisiones se hará el examen rectal digital<br />
y <strong>la</strong> <strong>de</strong>terminación <strong>de</strong>l PSA. En estas consultas<br />
se aprovecha para dar educación sanitaria al<br />
paciente, ampliando los conocimientos <strong>de</strong>l paciente<br />
sobre su enfermedad y <strong>la</strong> modificación<br />
<strong>de</strong> los estilos <strong>de</strong> vida. Entre éstos po<strong>de</strong>mos<br />
citar: restricción <strong>de</strong> ingesta <strong>de</strong> líquidos antes <strong>de</strong><br />
acostarse; evitar <strong>la</strong>s bebidas con cafeína y alcohol;<br />
orinar frecuentemente durante <strong>la</strong>s horas<br />
<strong>de</strong>l día para evitar <strong>la</strong> incontinencia por <strong>de</strong>sbordamiento<br />
y por urgencia; evitar medicamentos<br />
que pue<strong>de</strong>n empeorar los síntomas <strong>de</strong> <strong>la</strong> hiperp<strong>la</strong>sia<br />
benigna <strong>de</strong> próstata. Entre estos últimos<br />
po<strong>de</strong>mos citar:<br />
• Aporte externo <strong>de</strong> testosterona (<strong>la</strong> propia<br />
testosterona, anabolizantes, etc.).<br />
• Agonistas α-adrenérgicos utilizados como<br />
<strong>de</strong>scongestionantes nasales: pseudroefedrina,<br />
efedrina y fenilefrina. Estos medicamentos<br />
pue<strong>de</strong>n estimu<strong>la</strong>r los receptores α-adrenérgicos<br />
<strong>de</strong> <strong>la</strong> próstata produciendo contracción<br />
y por lo tanto provocarán una disminución<br />
<strong>de</strong>l calibre <strong>de</strong> <strong>la</strong> uretra, impidiendo<br />
el normal vaciamiento <strong>de</strong> <strong>la</strong> vejiga urinaria.<br />
• Medicamentos con efecto anticolinérgico.<br />
Entre ellos po<strong>de</strong>mos citar: antihistamínicos<br />
<strong>de</strong> primera generación, fenotiazinas, anti<strong>de</strong>presivos<br />
tricíclicos, anticolinérgicos utilizados<br />
como antiespasmódicos (butilescopo<strong>la</strong>mina)<br />
y los medicamentos para el tratamiento <strong>de</strong>l<br />
Parkinson.<br />
Para el tratamiento <strong>de</strong> <strong>la</strong> HBP existen<br />
principalmente los siguientes tratamientos:<br />
• Antagonistas α-adrenérgicos (alfa-bloqueantes).<br />
• Inhibidores <strong>de</strong> <strong>la</strong> 5α-reductasa.<br />
• Combinaciones <strong>de</strong> los grupos anteriores.<br />
• Antimuscarínicos: tolterodina y oxibutinina.<br />
• Fitoterapia: Serenoa repens y Pygeum Africanum.<br />
2.4.1. ANTAGONISTAS ALFA-ADRENÉRGICOS<br />
Estos medicamentos evitan que <strong>la</strong> noradrenalina<br />
se una al receptor α-adrenérgico y <strong>de</strong> esta<br />
manera disminuya el tono vascu<strong>la</strong>r <strong>de</strong> <strong>la</strong> próstata<br />
y <strong>de</strong> <strong>la</strong> uretra. Son muy utilizados como primera<br />
opción, ya que su efectividad es muy rápida. Su<br />
acción se basa en re<strong>la</strong>jar <strong>la</strong> muscu<strong>la</strong>tura, pero no<br />
disminuyen el tamaño <strong>de</strong> <strong>la</strong> próstata.<br />
Existen dos subtipos <strong>de</strong> receptores α-<br />
adrenérgicos: el alfa 1, que se subdivi<strong>de</strong> en<br />
1a, 1b y 1d; y el alfa 2.<br />
En <strong>la</strong>s célu<strong>la</strong>s prostáticas humanas el más<br />
prevalente es el alfa 1a, siendo el objetivo <strong>de</strong> los<br />
tratamientos. Históricamente los antagonistas α-<br />
adrenérgicos <strong>de</strong> primera generación, como fenoxibenzamina,<br />
bloqueaban ambos subtipos<br />
alfa-1 y alfa-2. De esta manera producían efectos<br />
adversos importantes: hipotensión ortostática,<br />
taquicardia refleja, arritmias cardíacas. Por<br />
eso se limitó su uso y se <strong>de</strong>secharon.<br />
Los <strong>de</strong> 2ª generación tienen más afinidad<br />
por el receptor alfa-1 que por el alfa-2. De<br />
OCTUBRE 2010 39
ACTUALIZACIONES FARMACOLÓGICAS<br />
esta manera han mejorado consi<strong>de</strong>rablemente<br />
su perfil toxicológico. Estos <strong>de</strong> 2ª generación<br />
incluyen los siguientes medicamentos: prazosina,<br />
terazosina, doxazosina y alfuzosina. De<br />
todas maneras todavía siguen produciendo los<br />
efectos hipotensores. Estos efectos se pue<strong>de</strong>n<br />
minimizar comenzando con dosis bajas e incrementándo<strong>la</strong>s<br />
poco a poco durante varias semanas<br />
y tomando estas dosis a <strong>la</strong> hora <strong>de</strong> acostarse<br />
para prevenir <strong>la</strong> inci<strong>de</strong>ncia <strong>de</strong> síncopes.<br />
También es necesario hacer seguimiento <strong>de</strong> los<br />
efectos sinérgicos que se producen cuando se<br />
aña<strong>de</strong>n medicamentos antihipertensivos que<br />
tome el paciente. Otros efectos adversos <strong>de</strong><br />
estos compuestos <strong>de</strong> 2ª generación son: mareos,<br />
astenia, hipotensión postural, síncope, dolor <strong>de</strong><br />
cabeza, rinitis y disfunciones sexuales. El mareo<br />
y <strong>la</strong> astenia son los más frecuentes.<br />
En un metanálisis <strong>de</strong> ensayos clínicos contro<strong>la</strong>dos<br />
con p<strong>la</strong>cebo con 6333 pacientes,<br />
tanto <strong>la</strong> terazosina, doxazosina, alfuzosina y<br />
tamsulosina mostraron igual eficacia en mejorar<br />
los síntomas y en incrementar el flujo urinario.<br />
La tasa <strong>de</strong> discontinuación <strong>de</strong>bido a<br />
efectos adversos cardiovascu<strong>la</strong>res (efecto <strong>de</strong> 1ª<br />
dosis, hipotensión ortostática y mareos) fue<br />
más alta con terazosina, doxazosina y alfuzosina<br />
(liberación inmediata). Los efectos adversos<br />
fueron menores con alfuzosina <strong>de</strong> liberación<br />
retardada y tamsulosina, medicamentos que<br />
pertenecen ya a <strong>la</strong> 3ª generación 1,2 .<br />
Las características farmacocinéticas, dosificación<br />
y marcas comerciales existentes en<br />
nuestro país <strong>la</strong>s po<strong>de</strong>mos ver en <strong>la</strong> tab<strong>la</strong> 1.<br />
Prazosín<br />
Fue el primer medicamento <strong>de</strong> <strong>la</strong> segunda<br />
generación <strong>de</strong> antagonistas α-adrenérgicos.<br />
Su empleo se vio muy limitado <strong>de</strong>bido a su<br />
corta vida media (t1/2=2.5 h), lo que requería<br />
administrarlo varias veces al día (tres veces) y<br />
por otro <strong>la</strong>do por sus habituales reacciones<br />
adversas: hipotensión ortostática, mareos y<br />
síncope, náuseas, vómitos, vértigo. Hoy día no<br />
se utiliza.<br />
Terazosina<br />
También como <strong>la</strong> prazosina es un antagonista<br />
selectivo <strong>de</strong>l receptor α1-adrenérgico. Se<br />
ha convertido en el medicamento <strong>de</strong> elección<br />
en aquellos hombres con hipertensión e hiperp<strong>la</strong>sia<br />
benigna <strong>de</strong> próstata. Los efectos secundarios<br />
más comunes son: vértigos, mareos,<br />
sueño, dolor <strong>de</strong> cabeza, estreñimiento, pérdida<br />
<strong>de</strong> apetito, fatiga, congestión nasal y ojos<br />
secos. Apenas se producen efectos secundarios<br />
<strong>de</strong> tipo sexual.<br />
Se <strong>de</strong>be tener precaución en pacientes<br />
con insuficiencia cardíaca e insuficiencia renal.<br />
Se han notificado interacciones con propanolol,<br />
verapamilo e inhibidores <strong>de</strong> <strong>la</strong> fosfodiesterasa,<br />
aumentando el efecto <strong>de</strong> hipotensión<br />
ortostática.<br />
Doxazosina<br />
Está indicado tanto para <strong>la</strong> hipertensión<br />
como para <strong>la</strong> HBP. Tiene un efecto muy favorable<br />
sobre el perfil lipídico: aumenta el índice<br />
HDL-colesterol/colesterol total y disminuye los<br />
niveles <strong>de</strong> triglicéridos, colesterol total y LDLcolesterol.<br />
Sólo <strong>de</strong>ben utilizarse <strong>la</strong>s formu<strong>la</strong>ciones<br />
retard <strong>de</strong>bido al potente efecto <strong>de</strong> hipotensión<br />
ortostática. Por este motivo se <strong>de</strong>ben<br />
tener precauciones con el uso simultáneo <strong>de</strong><br />
antagonistas <strong>de</strong> calcio, especialmente nifedipino,<br />
betabloqueantes (propanolol) e inhibidores<br />
<strong>de</strong> <strong>la</strong> fosfodiesterasa.<br />
Sin embargo, en el estudio ALLHAT<br />
2009 3 , <strong>la</strong> rama <strong>de</strong> pacientes en tratamiento<br />
con doxazosina fue interrumpida <strong>de</strong>bido a importantes<br />
reacciones adversas cardiovascu<strong>la</strong>res:<br />
25% más alto que con <strong>la</strong> clortalidona y dos<br />
40<br />
OCTUBRE 2010
Tab<strong>la</strong> 1 Antagonistas α-adrenérgicos<br />
Farmacocinética Posología Marcas comerciales<br />
PRAZOSIN<br />
Biodisponibilidad: 40-70%<br />
Unión a proteínas: 90-95%<br />
Vd: 0.63 l<br />
Metabolismo: hepático amplio<br />
T1/2= 2-4 h<br />
Biodisponibilidad:<br />
60-70% (liberac. rápida)<br />
Unión a proteínas: 98%<br />
Metabolismo: hepático intenso<br />
T1/2= 18-22 h<br />
Biodisponibilidad: 90%<br />
Unión a proteínas: 90-94%<br />
Metabolismo: hepático escaso<br />
Eliminación: heces: 40 %;<br />
orina: 60%<br />
T1/2 = 10-18 h<br />
Biodisponibilidad: 64%<br />
Unión a proteínas: 87%<br />
Metabolismo: hepático<br />
Eliminación: heces: 75-91%,<br />
orina: 11%<br />
T1/2 = 3-5 h<br />
Biodisponibilidad: 57%<br />
Unión a proteínas: 99%<br />
Metabolismo: parcialmente<br />
hepático<br />
T1/2 = 14-15 h<br />
FORMAS RETARD<br />
Biodisponibilidad: 32%<br />
Unión a proteínas: 97%<br />
Metabolismo: hepático intenso<br />
Eliminación orina: 76%<br />
T1/2 = 13 h<br />
0.5 mg/12 h<br />
1 mg/12 h<br />
Dosis mantenimiento: 2-3 mg/día<br />
DOXAZOSINA<br />
Las formas <strong>de</strong> liberación inmediata<br />
ya no se utilizan.<br />
Dosis máxima:16 mg<br />
Liberación modificada:<br />
4 mg/24 h---8 mg/24 h<br />
TERAZOSINA<br />
Empezar con 1 mg/ 24 h al acostarse.<br />
Cada 3-4 días ir aumentando <strong>la</strong><br />
dosis:<br />
2 mg/ 24 h,<br />
luego 5 mg/ 24 h<br />
Liberación normal: 2.5 mg/8 h<br />
Max: 10 mg/24h<br />
Formu<strong>la</strong>ción retard:<br />
5 mg/ 12 h ó 10 mg/24 h<br />
0,4 mg/24 h<br />
ALFUZOSINA<br />
Presentaciones:<br />
Cápsu<strong>la</strong>s retard<br />
Comprimidos OCAS<br />
0.4 mg/12 h<br />
0.8 mg/24 h<br />
TAMSULOSINA<br />
SILODOSINA<br />
Minipres 1 mg<br />
Minipres 2 mg<br />
Minipres 5 mg<br />
Carduran neo 4 mg<br />
Carduran neo 8 mg<br />
Doxazosina (EFG) 2 mg<br />
Doxazosina (EFG) 4 mg<br />
Deflox 2 mg<br />
Deflox 5 mg<br />
Magnurol 2 mg<br />
Magnurol 5 mg<br />
Terazosina (EFG): 2 mg, 5 mg<br />
Benestan 5 mg retard<br />
Unibenestan 10 mg retard<br />
Alfuzosina (EFG) 2,5 mg<br />
Alfuzosina (EFG) 5 mg<br />
Alfuzosina (EFG) 10 mg<br />
Omnic 0.4 mg cap<br />
Omnic 0.4 mg OCAS<br />
Urolosin 0.4 mg cap<br />
Urolosin 0.4 mg OCAS<br />
Urolosin 0.4 mg (EFG) cap<br />
No comercializado aún en España<br />
veces más insuficiencias cardíacas que con diuréticos.<br />
Por todo ello, no es un medicamento<br />
que se recomien<strong>de</strong> como <strong>de</strong> primera línea <strong>de</strong><br />
tratamiento.<br />
Los efectos adversos más notificados son<br />
dolor abdominal, dispepsia, sequedad <strong>de</strong><br />
boca, náuseas, palpitaciones, taquicardia, hipotensión,<br />
prurito y vértigo.<br />
Alfuzosina<br />
Está c<strong>la</strong>sificado como un bloqueante α1<br />
selectivo 4 . Al absorberse se produce una distri-<br />
OCTUBRE 2010 41
ACTUALIZACIONES FARMACOLÓGICAS<br />
bución alta <strong>de</strong>l medicamento en <strong>la</strong> próstata.<br />
Alfuzosina re<strong>la</strong>ja el músculo en <strong>la</strong> próstata y<br />
cuello <strong>de</strong> <strong>la</strong> vejiga, permitiendo <strong>de</strong> esta manera<br />
orinar. Los efectos secundarios más importantes<br />
son los mareos, <strong>de</strong>bidos a <strong>la</strong> hipotensión<br />
postural, infección <strong>de</strong>l tracto respiratorio<br />
superior, dolor <strong>de</strong> cabeza y fatiga. Los efectos<br />
secundarios menos frecuentes (0,6-7%) son<br />
astenia y eyacu<strong>la</strong>ciones anormales.<br />
Lo <strong>de</strong>ben tomar con precaución aquellos<br />
pacientes con insuficiencia renal y está contraindicado<br />
en pacientes con historia conocida<br />
<strong>de</strong> prolongación <strong>de</strong>l intervalo QT en el electrocardiograma.<br />
Alfuzosina se metaboliza extensamente<br />
en hígado, por los que aquellos pacientes<br />
con insuficiencia hepática <strong>de</strong>berían comenzar<br />
con dosis lo más bajas posibles y realizar<br />
seguimientos <strong>de</strong> <strong>la</strong>s enzimas hepáticas.<br />
Diltiazem enlentece el metabolismo hepático<br />
<strong>de</strong> alfuzosina y éste provoca aumento <strong>de</strong><br />
los niveles séricos <strong>de</strong> diltiazem. A<strong>de</strong>más los inhibidores<br />
<strong>de</strong>l citocromo P450 3A4 (ketoconazol,<br />
itraconazol, ritonavir) aumentan los niveles<br />
séricos <strong>de</strong> <strong>la</strong> alfuzosina.<br />
Tamsulosina<br />
Pertenece a <strong>la</strong> 3ª generación <strong>de</strong> antagonistas<br />
α-adrenérgicos. Es un bloqueador selectivo<br />
con gran afinidad por los receptores α-1a<br />
y α-1d <strong>de</strong> <strong>la</strong> próstata especialmente. Este mecanismo<br />
único comparado con los anteriores<br />
compuestos hace que se reduzca <strong>la</strong> inci<strong>de</strong>ncia<br />
<strong>de</strong> efectos vascu<strong>la</strong>res. Por eso es rara <strong>la</strong> hipotensión<br />
como efecto adverso.<br />
El uso conjunto con antihipertensivos no da<br />
lugar a un riesgo significativo <strong>de</strong> hipotensión.<br />
Hay que tener precauciones en:<br />
• Anestesia general: se requiere una vigi<strong>la</strong>ncia<br />
especial en estos pacientes.<br />
• Insuficiencia renal grave: no requiere ajuste<br />
<strong>de</strong> dosis.<br />
• Insuficiencia hepática grave: no requiere<br />
ajuste <strong>de</strong> dosificación.<br />
Los efectos adversos más comunes <strong>de</strong>scritos<br />
<strong>de</strong> <strong>la</strong> tamsulosina son:<br />
• Síndrome <strong>de</strong>l iris flácido intraoperatorio. En<br />
aquellos pacientes que van a ser operados<br />
<strong>de</strong> cataratas, convendría que <strong>de</strong>jaran <strong>la</strong> tamsulosina<br />
2 semanas antes <strong>de</strong> <strong>la</strong> operación,<br />
ya que se han observado problemas durante<br />
<strong>la</strong> operación quirúrgica y complicaciones en<br />
el postoperatorio. Este efecto pue<strong>de</strong> ser extensible<br />
a todos los antagonistas alfa adrenérgicos.<br />
• Disfunciones sexuales: eyacu<strong>la</strong>ción retrógrada<br />
unida a <strong>la</strong> dosis: 8,4% con dosis <strong>de</strong> 0,4<br />
mg; 18,1% con 0,8 mg. A<strong>de</strong>más ocurre<br />
más frecuentemente que con p<strong>la</strong>cebo en los<br />
estudios llevados a cabo (4,5% con tamsulosina<br />
0,4 mg vs 0,5% con p<strong>la</strong>cebo).<br />
• Los efectos <strong>de</strong> hipotensión postural ocurren<br />
menos frecuentemente con tamsulosina.<br />
La tamsulosina se encuentra comercializada<br />
en dos formas retard: cápsu<strong>la</strong>s <strong>de</strong> liberación<br />
retardada y comprimidos <strong>de</strong> liberación<br />
gradual (OCAS). Las cápsu<strong>la</strong>s retard pue<strong>de</strong>n<br />
ver alterada su absorción por los alimentos,<br />
mientras que esto parece que no ocurre con<br />
los comprimidos OCAS. Por ello, se aconseja<br />
tomar <strong>la</strong>s cápsu<strong>la</strong>s siempre 30 minutos <strong>de</strong>spués<br />
<strong>de</strong>l <strong>de</strong>sayuno o <strong>de</strong> <strong>la</strong> comida, pero siempre<br />
a <strong>la</strong> misma hora.<br />
Finalmente comentar que existen estudios<br />
que <strong>de</strong>muestran <strong>la</strong> efectividad <strong>de</strong> tamsulosina<br />
0,4 mg tomándo<strong>la</strong> en días alternos 5 .<br />
Silodosina (aún no comercializado en España)<br />
Estructuralmente muy parecido a <strong>la</strong> tamsulosina<br />
6 . Comparado con otros antagonistas α-<br />
adrenérgicos (terazosina y doxazosina), silodosina<br />
es 1400 veces más selectivo sobre los receptores<br />
α1A y 40 veces más que <strong>la</strong> tamsulosina.<br />
42<br />
OCTUBRE 2010
Figura 5.<br />
Testosterona<br />
Célu<strong>la</strong><br />
prostática<br />
En los estudios clínicos ha <strong>de</strong>mostrado<br />
una efectividad simi<strong>la</strong>r a <strong>la</strong> tamsulosina.<br />
Se metaboliza a través <strong>de</strong> <strong>la</strong> citocromo<br />
P450 3A4 por lo que está contraindicado su<br />
uso junto a inhibidores potentes <strong>de</strong> esta enzima<br />
(ketoconazol, itraconazol, c<strong>la</strong>ritromicina, ritonavir),<br />
ya que se produce un aumento <strong>de</strong> 3,8<br />
veces <strong>de</strong> silodosina en p<strong>la</strong>sma. También está<br />
contraindicado su uso junto con ciclosporina.<br />
Las principales reacciones adversas son alteraciones<br />
en <strong>la</strong> eyacu<strong>la</strong>ción, mareos y diarreas.<br />
Al igual que otros antagonistas α-adrenérgicos,<br />
pue<strong>de</strong> llegar a producir el síndrome <strong>de</strong>l<br />
iris flácido intraoperatorio.<br />
Si<strong>la</strong>dosina se encuentra contraindicado en<br />
pacientes con grave insuficiencia renal (ac<strong>la</strong>ramiento<br />
<strong>de</strong> creatinina < 30 ml/min).<br />
2.4.2. INHIBIDORES DE LA 5-ALFA REDUCTASA<br />
Según se pue<strong>de</strong> ver en <strong>la</strong> figura 5, <strong>la</strong> testosterona,<br />
que no es <strong>la</strong> hormona activa, necesita<br />
transformarse en <strong>de</strong>hidrotestosterona<br />
(hormona activa) por efecto <strong>de</strong>l enzima 5 α-<br />
reductosa. La <strong>de</strong>hidrotestosterona tiene un<br />
papel importante en el <strong>de</strong>sarrollo normal <strong>de</strong><br />
<strong>la</strong>s célu<strong>la</strong>s <strong>de</strong> <strong>la</strong> próstata. A<strong>de</strong>más está asociada<br />
con <strong>la</strong> hiperp<strong>la</strong>sia benigna <strong>de</strong> próstata y<br />
con <strong>la</strong> alopecia androgénica.<br />
Existen dos isoformas <strong>de</strong> <strong>la</strong> 5α-reductasa:<br />
tipo I y tipo II. La inhibición <strong>de</strong> ambos tipos en<br />
los hombres con hiperp<strong>la</strong>sia benigna <strong>de</strong> próstata<br />
lleva a un resultado más satisfactorio en<br />
el tratamiento <strong>de</strong> <strong>la</strong> misma.<br />
Los inhibidores <strong>de</strong> <strong>la</strong> 5α-reductasa interfieren<br />
con el efecto estimu<strong>la</strong>torio <strong>de</strong> <strong>la</strong> testosterona<br />
sobre el agrandamiento <strong>de</strong> <strong>la</strong> próstata y <strong>de</strong><br />
esta manera se produce una disminución <strong>de</strong>l tamaño<br />
<strong>de</strong> <strong>la</strong> misma, llevando a una reducción<br />
efectiva <strong>de</strong> los síntomas, disminuyendo el riesgo<br />
<strong>de</strong> retención urinaria y evitando en muchos<br />
casos <strong>la</strong> intervención quirúrgica. Pero estos medicamentos<br />
para ser <strong>de</strong>l todo efectivos y po<strong>de</strong>r<br />
observar resultados requieren que su utilización<br />
se realice durante varios meses (6 meses). Los<br />
efectos no son inmediatos.<br />
Finasteri<strong>de</strong><br />
R<br />
5α-reductasa<br />
DHT<br />
Núcleo<br />
( - )<br />
Es un antiandrógeno que actúa más específicamente<br />
sobre <strong>la</strong> 5α-reductasa tipo II.<br />
Este medicamento está c<strong>la</strong>sificado como <strong>de</strong><br />
categoría X en mujeres embarazadas, por lo<br />
que ninguna mujer en estado fértil <strong>de</strong>be manipu<strong>la</strong>r<br />
ni tocar trozos <strong>de</strong> un comprimido roto.<br />
Las tabletas enteras no tienen este problema<br />
<strong>de</strong>bido al <strong>la</strong>cado <strong>de</strong>l comprimido.<br />
En un estudio <strong>de</strong> 4 años <strong>de</strong> duración 7 , los<br />
pacientes recibieron 5 mg <strong>de</strong> finasteri<strong>de</strong> frente a<br />
p<strong>la</strong>cebo. El estudio encontró una reducción significativa<br />
en el riesgo <strong>de</strong> retención urinaria y <strong>de</strong><br />
operaciones quirúrgicas en los pacientes tratados<br />
con finasteri<strong>de</strong> en comparación con p<strong>la</strong>cebo.<br />
En otro estudio se comprobó el efecto <strong>de</strong><br />
<strong>la</strong> dosis (<strong>de</strong> 1 a 5 mg) en <strong>la</strong> reducción <strong>de</strong> síntomas<br />
y en el flujo urinario en cualquiera <strong>de</strong><br />
<strong>la</strong>s dosis, siendo más efectiva <strong>la</strong> disminución<br />
<strong>de</strong> los síntomas con dosis <strong>de</strong> 5 mg, <strong>de</strong>jando <strong>la</strong><br />
<strong>de</strong> 1 mg para el tratamiento <strong>de</strong> <strong>la</strong> alopecia 8 , 9 .<br />
El estudio PROWESS midió el efecto a<br />
Dehidrotestosterona (DHT)<br />
R<br />
Finasteri<strong>de</strong><br />
Dutasteri<strong>de</strong><br />
R<br />
DHT<br />
OCTUBRE 2010 43
ACTUALIZACIONES FARMACOLÓGICAS<br />
<strong>la</strong>rgo p<strong>la</strong>zo <strong>de</strong> finasteri<strong>de</strong> 5 mg diarios versus<br />
p<strong>la</strong>cebo en más <strong>de</strong> 3000 hombres con HBP<br />
durante 2 años 10 . Finasteri<strong>de</strong> mostró una mejora<br />
más gran<strong>de</strong> y significativa en <strong>la</strong> disminución<br />
<strong>de</strong> los síntomas que el p<strong>la</strong>cebo a los 4 y a<br />
los 24 meses. Los efectos secundarios re<strong>la</strong>cionados<br />
con el sexo, como cambios en <strong>la</strong> libido,<br />
alteraciones <strong>de</strong> <strong>la</strong> eyacu<strong>la</strong>ción, impotencia y<br />
disfunción en el orgasmo fueron experimentados<br />
por 273 pacientes (165 en el grupo <strong>de</strong> finasteri<strong>de</strong><br />
y 108 en el grupo p<strong>la</strong>cebo).<br />
En el estudio PROSPECT 11 se evaluó el uso<br />
<strong>de</strong> finasteri<strong>de</strong> en el tratamiento <strong>de</strong> <strong>la</strong> HBP mo<strong>de</strong>rada<br />
durante 2 años. Los pacientes (613) estuvieron<br />
un mes con p<strong>la</strong>cebo para posteriormente<br />
aleatorizarse a recibir 5 mg <strong>de</strong> finasteri<strong>de</strong><br />
o continuar con el p<strong>la</strong>cebo. El principal objetivo<br />
<strong>de</strong>l estudio fue ver cambios en los síntomas <strong>de</strong><br />
HBP, cambios en el flujo urinario y cambios en el<br />
volumen <strong>de</strong> <strong>la</strong> próstata. Los cambios en los síntomas<br />
fueron más significativos a los 12 y a los<br />
16 meses <strong>de</strong> <strong>la</strong> terapia. Los pacientes que recibieron<br />
finasteri<strong>de</strong> mostraron una mayor y más<br />
significativa mejora en los síntomas que en los<br />
pacientes tratados con p<strong>la</strong>cebo. Después <strong>de</strong> dos<br />
años, el volumen medio <strong>de</strong> <strong>la</strong> próstata se había<br />
reducido en un 21% en el grupo <strong>de</strong> finasteri<strong>de</strong><br />
y un incremento <strong>de</strong>l 8,4% en el grupo p<strong>la</strong>cebo.<br />
Ambos valores fueron estadísticamente significativos.<br />
Más pacientes en el grupo <strong>de</strong> finasteri<strong>de</strong><br />
tuvieron efectos secundarios <strong>de</strong> tipo sexual: alteraciones<br />
en <strong>la</strong> eyacu<strong>la</strong>ción e impotencia.<br />
Últimamente a finasteri<strong>de</strong> se le ha puesto en<br />
duda al re<strong>la</strong>cionar su uso con una potenciación<br />
<strong>de</strong> tumores <strong>de</strong> próstata más agresivos que si no<br />
se utiliza este tratamiento 12 y también el que se<br />
han empezado a dar casos <strong>de</strong> cánceres <strong>de</strong> mama<br />
en hombres tratados con este fármaco.<br />
Dutasteri<strong>de</strong><br />
Inhibidor potente y selectivo irreversible<br />
<strong>de</strong> los dos subtipos <strong>de</strong> <strong>la</strong> 5α-reductasa, tipo I<br />
y tipo II. Sin embargo, es menos rápido y selectivo<br />
que finasteri<strong>de</strong>. Se utiliza una dosis <strong>de</strong><br />
0,5 mg diarios.<br />
En un estudio <strong>de</strong> 24 semanas, dutasterida<br />
0,5 mg diarios mostró una mayor reducción<br />
<strong>de</strong> <strong>de</strong>hidrotestosterona sérica comparado con<br />
finasteri<strong>de</strong> 5 mg diarios (95% frente a 71%<br />
respectivamente; P
2.4.3. TERAPIA COMBINADA<br />
Normalmente es utilizada esta opción terapéutica<br />
cuando a pesar <strong>de</strong> usar un antagonista<br />
α-adrenérgico a dosis máxima, se observa que<br />
todavía no se consigue disminuir los síntomas<br />
<strong>de</strong> obstrucción urinaria. En estos casos se<br />
aña<strong>de</strong> un inhibidor <strong>de</strong> <strong>la</strong> 5α-reductasa.<br />
El estudio MTOPS 17 mostró un incremento<br />
<strong>de</strong> <strong>la</strong> eficacia en aliviar los síntomas y reducir<br />
<strong>la</strong> progresión <strong>de</strong> <strong>la</strong> enfermedad con <strong>la</strong> utilización<br />
<strong>de</strong> ambos tipos <strong>de</strong> medicamentos citados<br />
anteriormente, comparándolo con <strong>la</strong> utilización<br />
<strong>de</strong> una so<strong>la</strong> c<strong>la</strong>se <strong>de</strong> medicamentos. En<br />
este caso se utilizó <strong>la</strong> combinación <strong>de</strong> doxazosina<br />
y finasteri<strong>de</strong>. Los efectos adversos aumentan,<br />
pero los pacientes obtienen un beneficio<br />
palpable por ellos mismos.<br />
En un estudio don<strong>de</strong> se estudió <strong>la</strong> combinación<br />
<strong>de</strong> dutasterida y tamsulosina 18 frente a<br />
cada uno <strong>de</strong> ellos por separado, <strong>la</strong> combinación<br />
obtenía un beneficio mayor que <strong>la</strong> <strong>de</strong><br />
cada medicamento por separado. También observaron<br />
que <strong>la</strong>s reacciones adversas que se<br />
producían con <strong>la</strong> combinación eran muy simi<strong>la</strong>res<br />
a <strong>la</strong>s que se producían para cada medicamento<br />
por separado.<br />
En un estudio multicéntrico aleatorizado<br />
no se evi<strong>de</strong>nció un efecto aditivo con <strong>la</strong> combinación<br />
<strong>de</strong> terazosina y finasterida 19 .<br />
En el estudio PREDICT, se evaluó doxazosina,<br />
finasterida y <strong>la</strong> combinación <strong>de</strong> ambos<br />
durante 1 año. Se valoró el flujo urinario y el<br />
cuestionario específico para <strong>la</strong> HBP, el IPSS (Baremo<br />
Internacional <strong>de</strong> Síntomas Prostáticos).<br />
Los pacientes que recibieron doxazosina y<br />
aquellos que recibieron <strong>la</strong> combinación mostraron<br />
mejoras significativas en el cuestionario<br />
IPSS y en el flujo urinario comparado con <strong>la</strong> finasterida<br />
so<strong>la</strong>. No obstante, no se pudieron<br />
observar diferencias estadísticamente significativas<br />
entre <strong>la</strong> doxazosina y <strong>la</strong> terapia combinada<br />
20 . Sin embargo, como ya hemos comentado<br />
antes, en el estudio ALLHAT 3 , el grupo <strong>de</strong> doxazosina<br />
tuvo que interrumpirse <strong>de</strong>bido a que<br />
el medicamento no reducía <strong>la</strong> enfermedad coronaria,<br />
ni <strong>la</strong> mortalidad total, sino que existía<br />
un 80% <strong>de</strong> incremento en el riesgo <strong>de</strong> <strong>de</strong>sarrol<strong>la</strong>r<br />
insuficiencia cardíaca en los pacientes en<br />
tratamiento con dicha doxazosina.<br />
En el estudio SMART-1 21 se quiso estudiar<br />
<strong>la</strong> efectividad <strong>de</strong> utilizar <strong>la</strong> combinación <strong>de</strong> dutasterida<br />
y tamsulosina y posteriormente <strong>de</strong>jar<br />
sólo <strong>la</strong> dutasterida. Se llevó a cabo un estudio<br />
aleatorizado en el que se valoró o utilizar dutasterida<br />
y tamsulosina durante 36 semanas<br />
(DT36), o bien, utilizar <strong>la</strong> dutasterida y tamsulosina<br />
durante 24 semanas seguido sólo <strong>de</strong> dutasterida<br />
y p<strong>la</strong>cebo otras 12 semanas<br />
(DT24+D12). Se observó que en los pacientes<br />
con síntomas mo<strong>de</strong>rados, se podría prescindir<br />
<strong>de</strong>l antagonista α-adrenérgico, y el alivio <strong>de</strong> los<br />
síntomas continuaba. Sin embargo, en los pacientes<br />
con síntomas severos, no se mantenía el<br />
alivio <strong>de</strong> los síntomas, por lo que se podría continuar<br />
con <strong>la</strong> combinación durante más tiempo.<br />
Como conclusión, po<strong>de</strong>mos <strong>de</strong>cir que,<br />
cuando los síntomas no son muy severos, los<br />
bloqueantes α-adrenérgicos <strong>de</strong> tercera generación<br />
(alfuzosina retard y tamsulosina) serían los<br />
más recomendables. Cuando los síntomas sean<br />
más severos, <strong>la</strong> combinación <strong>de</strong> medicamentos<br />
antagonistas α-adrenérgicos y los inhibidores<br />
5α-reductasa no han <strong>de</strong>mostrado su efectividad.<br />
Sin embargo, para los pacientes <strong>la</strong> mejora es<br />
apreciable, ya que mejoran algunos síntomas. Se<br />
requerirían más estudios para verificar esto.<br />
2.4.4. ANTIMUSCARÍNICOS<br />
(ANTIESPASMÓDICOS)<br />
Actúan sobre <strong>la</strong>s fibras <strong>de</strong>l músculo <strong>de</strong> <strong>la</strong><br />
pared <strong>de</strong> <strong>la</strong> vejiga urinaria y bloquean los efectos<br />
muscarínicos <strong>de</strong> <strong>la</strong> acetilcolina sobre el<br />
OCTUBRE 2010 45
ACTUALIZACIONES FARMACOLÓGICAS<br />
músculo <strong>de</strong> <strong>la</strong> vejiga, lo que origina una re<strong>la</strong>jación<br />
<strong>de</strong>l <strong>de</strong>trusor, aumentando, en los pacientes<br />
con vejiga inestable, <strong>la</strong> capacidad <strong>de</strong> <strong>la</strong> vejiga<br />
y disminuyendo <strong>la</strong> frecuencia <strong>de</strong> <strong>la</strong>s contracciones<br />
espontáneas <strong>de</strong>l <strong>de</strong>trusor y por<br />
tanto <strong>de</strong> <strong>la</strong>s emisiones <strong>de</strong> orina 22,23 .<br />
No son medicamentos que se puedan utilizar<br />
en todos los pacientes, porque estará<br />
contraindicada en muchos <strong>de</strong> ellos, especialmente<br />
aquellos que tengan obstrucción urinaria.<br />
Según los citados estudios, estos compuestos<br />
se utilizan en aquellos pacientes con síntomas<br />
irritativos, junto con medicamentos antagonistas<br />
α-adrenérgicos y vigi<strong>la</strong>ndo estrechamente<br />
los síntomas <strong>de</strong> obstrucción.<br />
Los principios activos utilizados son:<br />
• Tolterodina. Las dosis más utilizadas son 2<br />
mg/12 h, o bien, 4 mg/24 h.<br />
• Oxibutinina. Se utiliza en dosis <strong>de</strong> 5 mg/8 h.<br />
2.4.5. FITOTERAPIA<br />
Existen dos tipos <strong>de</strong> medicamentos a<br />
base <strong>de</strong> p<strong>la</strong>ntas medicinales que son:<br />
• Serenoa Repens<br />
• Pigeum Africanum<br />
Serenoa Repens<br />
Se piensa que inhibe <strong>la</strong> 5α-reductasa bloqueando<br />
<strong>la</strong> conversión <strong>de</strong> testosterona a <strong>de</strong>hidrotestosterona<br />
que es <strong>la</strong> responsable <strong>de</strong>l estímulo<br />
<strong>de</strong>l crecimiento <strong>de</strong> <strong>la</strong> glándu<strong>la</strong> prostática 24 .<br />
Entre los efectos secundarios se incluyen<br />
dolor <strong>de</strong> cabeza y malestar gastrointestinal.<br />
En algunos estudios han encontrado que<br />
el tratamiento con esta p<strong>la</strong>nta aumenta el<br />
flujo máximo urinario 24,25 . Sin embargo, en un<br />
estudio doble ciego, aleatorizado frente a p<strong>la</strong>cebo,<br />
225 hombres con HBP tomaron 160 mg<br />
<strong>de</strong> Serenoa Repens o p<strong>la</strong>cebo dos veces al día<br />
durante 1 año 26 . No se observaron diferencias<br />
significativas entre el tratamiento con <strong>la</strong> p<strong>la</strong>nta<br />
y el grupo p<strong>la</strong>cebo en cuanto al flujo urinario,<br />
tamaño <strong>de</strong> próstata, calidad <strong>de</strong> vida o niveles<br />
<strong>de</strong> PSA.<br />
Parecidos resultados se obtuvieron en un<br />
estudio <strong>de</strong> Mark y cols. 27 . Los pacientes con<br />
HBP fueron tratados durante seis meses o con<br />
Serenoa Repens o con p<strong>la</strong>cebo. Serenoa Repens<br />
no produjo diferencias significativas en<br />
cuanto a los parámetros clínicos, volumen<br />
prostático y PSA frente a p<strong>la</strong>cebo.<br />
Sin embargo, en un metaanálisis se sugería<br />
que esta p<strong>la</strong>nta produciría mejoras en aliviar<br />
los síntomas <strong>de</strong> HBP sólo a corto p<strong>la</strong>zo 28 .<br />
Pygeum Africanum<br />
El concentrado <strong>de</strong> extracto ha sido estudiado<br />
por su eficacia en HBP 29 . Sin embargo,<br />
problemas <strong>de</strong> metodología (poco tiempo, evaluación<br />
incompleta <strong>de</strong> resultados, falta <strong>de</strong> estandarización<br />
<strong>de</strong>l extracto, etc.) han impedido<br />
sacar conclusiones válidas.<br />
Bibliografía<br />
1. Djavan B, Marberger M. A meta-analysis on the efficacy and tolerability of alpha1 adrenoceptor antagonists in patients<br />
with lower urinary tract symptoms suggestive of benign prostatic obstruction. Eur Urol 1999;36:1-13.<br />
2. Lukacs B. Using a <strong>la</strong>rge clinical database to assess the effectiveness of alfuzosin. Eur Urol 1997;32(suppl 2):45-47.<br />
3. ALLHAT Col<strong>la</strong>borative Research Group. Major cardiovascu<strong>la</strong>r events in hypertensive patients randomized to doxazosin<br />
vs chlorthalidone: the antihypertensive and lipid-lowering treatment to prevent heart attack trial (ALLHAT).<br />
JAMA 2000;283:1967-1975.<br />
4. Kirby RS. Clinical uroselectivity of alfuzosin in the treatment of benign prostatic hyper-p<strong>la</strong>sia. Eur Urol<br />
1998;33(suppl 2):19-27.<br />
5. Yanardag H, Goktas S, Kibar Y, Kilic S, Erduran D. Intermittent tamsulosin therapy in men with lower urinary tract<br />
46<br />
OCTUBRE 2010
symptoms. J Urol 2005;173:155-7.<br />
6. Cantrell MA, Bream-Rouwenhorst HR, Hemerson P, Magera JS. Silodosin for benign prostatic hyperp<strong>la</strong>sia. Ann<br />
Pharmacother 2010;44:302-10.<br />
7. McConnell JD, Bruskewitz R, Walsh P, et al. The effect of finasteri<strong>de</strong> on the risk of acute urinary retention and the<br />
need for surgical treatment among men with benign prostatic hyperp<strong>la</strong>sia. N Engl J Med 1998;338:557-563.<br />
8. Gormley GJ, Stoner E, Bruskewitz RC, et al. The effect of finasteri<strong>de</strong> in men with benign prostatic hyperp<strong>la</strong>sia. N<br />
Engl J Med 1992;327:1185-1191.<br />
9. The Finasteri<strong>de</strong> Study Group. Finasteri<strong>de</strong> (MK-906) in the treatment of benign prostatic hyperp<strong>la</strong>sia. Prostate<br />
1993;22:291-299.<br />
10. Marberger MJ. Long-term effects of finasteri<strong>de</strong> in patients with benign prostatic hyper-p<strong>la</strong>sia: a double-blind, p<strong>la</strong>cebo-controlled,<br />
multicenter study. Urology 1998;51:677-686.<br />
11. Nickel JC, Fra<strong>de</strong>t Y, Boake RC, et al. Efficacy and safety of finasteri<strong>de</strong> therapy for benign prostatic hyperp<strong>la</strong>sia: results<br />
of a 2-year randomized controlled trial (the PROSPECT study). Can Med Assoc J 1996;155:1251-1259.<br />
12. Rubin MA, Kantoff PW, Roehrborn CG, Burke HB, Schwartz DT, Ross RK, Skinner E, Cote RJ, Lee SC, Ellis RJ, Barzell<br />
WE, Thompson IM Jr, Goodman PJ, Coltman CA Jr. Prevention of prostate cancer with Finasteri<strong>de</strong>. N Engl J<br />
Med 2003;349:1569.<br />
13. C<strong>la</strong>rk RV, Hermann DJ, Cunningham GR, et al. Marked suppression of dihydrotestosterone in men with benign prostatic<br />
hyperp<strong>la</strong>sia by dutasteri<strong>de</strong>, a dual 5alpha-reductase inhibitor. J Clin Endocrinol Metab 2004;89:2179-2184.<br />
14. Gilling PJ, Jacobi G, Tamme<strong>la</strong> TL, van Erps P. Efficacy of dutasteri<strong>de</strong> and finasteri<strong>de</strong> for the treatment of benign<br />
prostate hyperp<strong>la</strong>sia: results of the 1-year En<strong>la</strong>rged Prostate International Comparator Study (EPICS). J Urol<br />
2004;171(suppl 4):356. Abstract 1353.<br />
15. Roehrborn CG, Boyle P, Nickel JC, et al. Efficacy and safety of a dual inhibitor of 5-alpha-reductase types 1 and 2<br />
(dutasteri<strong>de</strong>) in men with benign prostatic hyperp<strong>la</strong>sia. ARIA 3001, ARIA 3002 and ARIA 3003 study investigators.<br />
Urology 2002;60:434-441.<br />
16. Roehrborn CG, Boyle P, Gould AL, Waldstreicher J. Serum prostate-specific antigen as a predictor of prostate volume<br />
in men with benign prostatic hyperp<strong>la</strong>sia. Urology 1999;53:581-589.<br />
17. Andriole GL, Kirby R. Safety and tolerability of the dual 5alpha-reductase inhibitor dutasteri<strong>de</strong> in the treatment of<br />
benign prostatic hyperp<strong>la</strong>sia. Eur Urol 2003;44:82-88.<br />
18. Roehrborn CG, Siami, P, Barkin J, Damiao R, Major-Walker K, Nandy I, Morrill B, GagnierR, Montorsi F. The effects<br />
of combination therapy with dutasteri<strong>de</strong> and Tamsulosin on clinical outcomes in men with syntomatic benign prostatic<br />
hyperp<strong>la</strong>sia: 4-year results from the CombAT Study. Eur Urol 2010;57:123-131.<br />
19. Lepor H, Williford WO, Barry MJ et al. The efficacy of terazosin, finasteri<strong>de</strong>, or both in benign prostatic hyperp<strong>la</strong>sia.<br />
N Engl J Med 1996;335:533-539.<br />
20. McConnell JD, Roehrborn CG, Bautista OM, et al. The long-term effect of doxazosin, finasteri<strong>de</strong>, and combination<br />
therapy on the clinical progression of benign prostatic hyperp<strong>la</strong>sia. N Engl J Med 2003;349:2387-2398.<br />
21. Barkin J, Guimarães M, Jacobi G, et al. Alpha-blocker therapy can be withdrawn in the majority of men following<br />
initial combination therapy with the dual 5alpha-reductase inhibitor dutasteri<strong>de</strong>. Eur Urol 2003;44:461-466.<br />
22. Kap<strong>la</strong>n SA, Walmsley K, Te AE. Tolterodine exten<strong>de</strong>d release attenuates lower urinary tract symptoms in men with<br />
benign prostatic hyperp<strong>la</strong>sia. J Urol 2005;174:2273-2276.<br />
23. MacDiarmid SA, Peters KM, Chen A, Armstrong RB, Orman C, Aquilina JW, Nitti VW. Efficacy and safety of exten<strong>de</strong>d-release<br />
oxybutynin in combination with tamsulosin for treatment of lower urinary tract symptoms in men: randomized,<br />
double-blind, p<strong>la</strong>cebo-controlled study. Mayo Clin Proc 2008;83:1002-1010.<br />
24. Wilt T, Ishani A, Stark G, et al. Saw palmetto extracts for treatment of benign prostatic hyperp<strong>la</strong>sia: a systematic review.<br />
JAMA 1998;280:1604-1609.<br />
25. Gordon AE, Shaughnessy AF. Saw palmetto for prostate disor<strong>de</strong>rs. Am Fam Physician 2003;67:1281-1286.<br />
26. Bent S, Kane C, Shinohara K, et al. Saw palmetto for benign prostatic hyperp<strong>la</strong>sia. New Eng J Med. 2006;354:557-<br />
566.<br />
27. Marks LS, Partin AW, Epstein JI, et al. Effects of a saw palmetto herbal blend in men with symptomatic benign<br />
prostatic hyperp<strong>la</strong>sia. J Urol 2000;163:1451-1456.<br />
28. Ernst E. The risk-benefit profile of commonly used herbal therapies: ginkgo, St. John's wort, ginseng, echinacea,<br />
saw palmetto, and kava. Ann Intern Med 2002;136:42-53.<br />
29. Ishani A, MacDonald R, Nelson D, et al. Pygeum africanum for the treatment of patients with benign prostatic<br />
hyperp<strong>la</strong>sia: a systematic review and quantitative meta-analysis. Am J Med 2000;109:654-664.<br />
OCTUBRE 2010 47