Pathologie acquise de la jonction dermo-épidermique - iPubli-Inserm
Pathologie acquise de la jonction dermo-épidermique - iPubli-Inserm
Pathologie acquise de la jonction dermo-épidermique - iPubli-Inserm
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
-<br />
376<br />
SYNTHÈSE<br />
mé<strong>de</strong>cine/sciences 1993 ; 9 : 3 76-86<br />
Jean-François Nico<strong>la</strong>s<br />
Hélène Micha<strong>la</strong>ki<br />
,<br />
Eric Peyron<br />
Paulo Machado<br />
Emmanuel Cozzani<br />
Daniel Schmitt<br />
ADRESSE<br />
J.-F. Nico<strong>la</strong>s : directeur <strong>de</strong> recherche à l'<strong>Inserm</strong>.<br />
H. Micha<strong>la</strong>ki : chercheur post-doctoral. E. Peyron<br />
: chercheur pré-doctoral. P. Machado : <strong>de</strong>rmatologue<br />
hospitalier. E. Cozzani : chercheur prédoctoral.<br />
D. Schmitt : directeur <strong>de</strong> recherche, directeur<br />
<strong>de</strong> l'U. 316 <strong>de</strong> l'<strong>Inserm</strong>. <strong>Inserm</strong> U. 346,<br />
clinique <strong>de</strong>rmatologique, pavillon R, univers)<br />
té C<strong>la</strong>u<strong>de</strong>-Bernard, Lyon I, hôpital<br />
Edouard-Herriot, 69437 Lyon Ce<strong>de</strong>x 03,<br />
France.<br />
Hélène Micha<strong>la</strong>ki, Paulo Machado et<br />
Emmanuel Cozzani ont été aidés par une<br />
bourse <strong>de</strong> <strong>la</strong> Fondation Mérieux (H.M.),<br />
une bourse <strong>de</strong> <strong>la</strong> Fondation pour <strong>la</strong> recherche<br />
médicale (P.M.) et une bourse <strong>de</strong> l'Universita<br />
<strong>de</strong>gli studi di Genova (E. C.).<br />
<strong>Pathologie</strong> <strong>acquise</strong><br />
<strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
La <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique et les <strong>de</strong>smosomes coo<br />
pèrent pour assurer <strong>la</strong> résistance <strong>de</strong> <strong>la</strong> peau, <strong>la</strong> première<br />
en ancrant soli<strong>de</strong>ment l'épi<strong>de</strong>rme au <strong>de</strong>rme et les seconds<br />
en liant les kératinocytes entre eux. Or, les <strong>de</strong>smosomes<br />
et <strong>de</strong>s constituants <strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique (les<br />
hémi<strong>de</strong>smosomes et les fibrilles d'ancrage) sont fortement<br />
antigéniques et <strong>de</strong>viennent <strong>la</strong> cible d'auto-anticorps dans<br />
les trois principales <strong>de</strong>rmatoses auto-immunes bulleuses :<br />
les pemphigus, <strong>la</strong> pemphigoï<strong>de</strong> bulleuse et l' épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong>. Les antigènes reconnus par les auto<br />
anticorps <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong> bulleuse et <strong>de</strong> l' épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong> sont maintenant bien caractérisés et<br />
leurs gènes sont clonés. De ce fait, <strong>de</strong>s progrès très<br />
importants ont été faits dans <strong>la</strong> compréhension <strong>de</strong> <strong>la</strong><br />
physiopathologie <strong>de</strong> ces ma<strong>la</strong>dies et dans leur diagnostic.<br />
es structures qui assurent <strong>la</strong><br />
L<br />
résistance <strong>de</strong> <strong>la</strong> peau sont<br />
schématiquement <strong>de</strong> <strong>de</strong>ux<br />
types : les <strong>de</strong>smosomes et <strong>la</strong><br />
<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
(ou membrane basale <strong>de</strong>rmoépi<strong>de</strong>rmique).<br />
Les <strong>de</strong>smosomes permettent<br />
l'adhérence <strong>de</strong>s cellules épi<strong>de</strong>rmiques,<br />
les kératinocytes, entre<br />
eux. La <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
représente l'interface entre l'épi<strong>de</strong>rme<br />
et le <strong>de</strong>rme, et doit être considérée<br />
comme une structure macromolécu<strong>la</strong>ire<br />
complexe dont le but principal<br />
est d'assurer une bonne adhérence <strong>de</strong><br />
l'épi<strong>de</strong>rme au <strong>de</strong>rme. Les connaissances<br />
récentes <strong>de</strong> <strong>la</strong> pathogénie <strong>de</strong>s<br />
ma<strong>la</strong>dies auto-immunes bulleuses, et<br />
en particulier les recherches orientées<br />
vers <strong>la</strong> compréhension <strong>de</strong> <strong>la</strong> perte <strong>de</strong><br />
<strong>la</strong> cohésion et du défaut d'attachement<br />
cellu<strong>la</strong>ire, ont permis <strong>de</strong> montrer<br />
que trois structures cutanées<br />
étaient fortement antigéniques (les<br />
<strong>de</strong>smosomes, les hémi<strong>de</strong>smosomes et<br />
les fibrilles d'ancrage) et étaient <strong>la</strong><br />
cible <strong>de</strong> <strong>la</strong> réponse auto-immune dans<br />
les trois principales <strong>de</strong>rmatoses autoimmunes<br />
bulleuses : les pemphigus,<br />
<strong>la</strong> pemphigoï<strong>de</strong> bulleuse et l'épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong>.<br />
Les <strong>de</strong>rmatoses auto-immunes bulleuses<br />
comprennent un ensemble <strong>de</strong><br />
ma<strong>la</strong>dies caractérisées par <strong>la</strong> perte <strong>de</strong><br />
<strong>la</strong> cohésion <strong>de</strong>s constituants cutanés<br />
à <strong>la</strong> suite d'une réaction autoimmune,<br />
aboutissant à <strong>la</strong> formation<br />
<strong>de</strong> bulles. Deux grands groupes <strong>de</strong><br />
<strong>de</strong>rmatoses auto-immunes bulleuses<br />
peuvent être individualisés en fonction<br />
du site <strong>de</strong> survenue <strong>de</strong> <strong>la</strong> bulle<br />
et en fonction <strong>de</strong>s antigènes cibles <strong>de</strong><br />
<strong>la</strong> réponse auto-immune (Tableau !) .<br />
1. Les <strong>de</strong>rmatoses auto-immunes<br />
bulleuses épi<strong>de</strong>rmiques qui regroupent<br />
les pemphigus, définis par <strong>la</strong><br />
perte <strong>de</strong> <strong>la</strong> cohésion <strong>de</strong>s kératinocytes<br />
entre eux, secondaire à <strong>la</strong> perte<br />
mis n ° 4 vol. 9, avril 93
Tableau 1<br />
STRUCTURES CUTANÉES ET ANTIGÈNES CIBLES<br />
DES DERMATOSES BULLEUSES AUTO-IMMUNES<br />
Structure Antigène Ma<strong>la</strong>die<br />
Desmosomes Desmogléines Pemphigus<br />
Desmop<strong>la</strong>kines<br />
Cadhérine (P. vulgaire)<br />
Desmocollines<br />
Hémi<strong>de</strong>smosomes BP Ag1<br />
BP Ag2<br />
Fibrilles Col<strong>la</strong>gène<br />
d'ancrage<br />
d'intégrité <strong>de</strong>s <strong>de</strong>smosomes ; les <strong>de</strong>smosomes<br />
sont <strong>la</strong> cible <strong>de</strong>s autoanticorps<br />
dans les pemphigus autoimmuns<br />
; plusieurs antigènes <strong>de</strong>smosomiaux<br />
différents peuvent être en<br />
cause avec génération d'une réponse<br />
inf<strong>la</strong>mmatoire aboutissant à <strong>de</strong>s<br />
tableaux cliniques distincts.<br />
2. Les <strong>de</strong>rmatoses auto-immunes<br />
bulleuses sous-épi<strong>de</strong>rmiques, qui seules<br />
nous intéressent dans ce travail,<br />
sont liées à <strong>la</strong> perte d'intégrité <strong>de</strong> <strong>la</strong><br />
<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique ou <strong>de</strong> <strong>la</strong><br />
zone <strong>de</strong>rmique superficielle sousbasale.<br />
Les <strong>de</strong>rmatoses auto-immunes<br />
bulleuses sous-épi<strong>de</strong>rmiques comportent<br />
les ma<strong>la</strong>dies du groupe <strong>de</strong> <strong>la</strong><br />
pemphigoï<strong>de</strong> bulleuse, les ma<strong>la</strong>dies<br />
du groupe <strong>de</strong> l'épi<strong>de</strong>rmolyse bulleuse<br />
<strong>acquise</strong> et les <strong>de</strong>rmatoses à IgA<br />
linéaire [ 1). Les hémi<strong>de</strong>smosomes<br />
sont <strong>de</strong>s structures du pôle basal <strong>de</strong><br />
<strong>la</strong> membrane cytop<strong>la</strong>smique <strong>de</strong>s kératinocytes<br />
basaux ; ils sont <strong>la</strong> cible <strong>de</strong><br />
<strong>la</strong> réponse auto-immune dans les<br />
ma<strong>la</strong>dies du groupe <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong><br />
bulleuse. Les fibrilles d'ancrage<br />
sont <strong>de</strong>s composés <strong>de</strong> <strong>la</strong> zone sousbasale<br />
et sont <strong>la</strong> cible <strong>de</strong>s autoanticorps<br />
dans les ma<strong>la</strong>dies du groupe<br />
<strong>de</strong> l'épi<strong>de</strong>rmolyse bulleuse <strong>acquise</strong>.<br />
Les acquisitions récentes dans le<br />
domaine <strong>de</strong>s <strong>de</strong>rmatoses autoimmunes<br />
bulleuses <strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique concernent avant<br />
tout <strong>la</strong> pemphigoï<strong>de</strong> bulleuse et l'épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong>. Les progrès<br />
portent sur <strong>la</strong> nosologie <strong>de</strong>s différentes<br />
ma<strong>la</strong>dies grâce à <strong>la</strong> caractérisation<br />
<strong>de</strong>s auto-antigènes, sur les<br />
métho<strong>de</strong>s diagnostiques et sur <strong>la</strong><br />
Pemphigoï<strong>de</strong><br />
VIl EBA<br />
Lupus bulleux<br />
1 Morphologie<br />
<strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
La <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique est<br />
une structure complexe macromolécu<strong>la</strong>ire<br />
<strong>de</strong> 100 nm d'épaisseur, qui<br />
constitue une interface épithéliummésenchyme<br />
aux multiples fonctions<br />
[2, 3). La <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
est le fon<strong>de</strong>ment <strong>de</strong><br />
l'organisation tissu<strong>la</strong>ire <strong>de</strong>s <strong>de</strong>ux composants<br />
principaux <strong>de</strong> <strong>la</strong> peau (épi<strong>de</strong>rme,<br />
<strong>de</strong>rme) et <strong>de</strong> <strong>la</strong> cicatrisation.<br />
C'est un substrat d'adhérence cellu<strong>la</strong>ire,<br />
un lieu <strong>de</strong> stockage <strong>de</strong> cytokines,<br />
et une barrière chimique et<br />
physique. Cette <strong>de</strong>rnière fonction est<br />
particulièrement importante, car c'est<br />
par <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
que <strong>la</strong> cohésion entre l'épi<strong>de</strong>rme et le<br />
<strong>de</strong>rme s'effectue, ce qui permet une<br />
résistance aux forces <strong>de</strong> traction cutanée<br />
externes.<br />
Pour que cette cohésion soit forte, <strong>la</strong><br />
<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique est constituée<br />
d'un réseau <strong>de</strong> macromolécules<br />
qui forment <strong>la</strong> membrane basale<br />
et <strong>de</strong> structures d'adhérence<br />
particulières.<br />
En microscopie électronique à transmission,<br />
<strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
apparaît constituée <strong>de</strong><br />
trois couches (figure 1). De l'épi<strong>de</strong>rme<br />
vers le <strong>de</strong>rme, on trouve : (1) <strong>la</strong><br />
membrane cellu<strong>la</strong>ire du pôle basal<br />
<strong>de</strong>s kératinocytes basaux qui contient<br />
les hémi<strong>de</strong>smosomes ; (2) <strong>la</strong> membrane<br />
basale proprement dite, faite <strong>de</strong><br />
<strong>de</strong>ux feuillets : un feuillet c<strong>la</strong>ir aux<br />
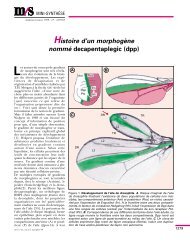
Figure 1. Aspect ultrastructural <strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique <strong>de</strong> <strong>la</strong><br />
peau humaine normale. La partie supérieure correspond à une partie d'un<br />
kératinocyte basal (KJ avec ses tonofi<strong>la</strong>ments <strong>de</strong> kératine (-.), séparé du <strong>de</strong>rme<br />
(D) par <strong>la</strong> membrane basale ou <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique. On distingue nettement<br />
<strong>la</strong> membrane p<strong>la</strong>smique du kératinocyte avec les hémi<strong>de</strong>smosomes ( ,.. ),<br />
<strong>la</strong> <strong>la</strong>mina lucida c<strong>la</strong>ire aux électrons r-J. <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa opaque aux électrons<br />
(). et les fibrilles d'ancrage du <strong>de</strong>rme superficiel (_..) . Dans le <strong>de</strong>rme<br />
pathogénie. (0) on distingue les fibres <strong>de</strong> col<strong>la</strong>gène fibril<strong>la</strong>ire (types 1 et Ill) (o). -<br />
mis n ° 4 vol. 9, avn·l 93<br />
377
RÉFÉRENCES ---- -- -<br />
1. Ortonne JP. La <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
et sa pathologie <strong>acquise</strong> et héréditaire.<br />
Path Biol 1992 ; 40 : 121-32.<br />
2. Verrando P. La <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique.<br />
ln : Thivolet J, Faure M,<br />
Schmitt D, eds. Biologie <strong>de</strong> <strong>la</strong> peau, 6• cours<br />
.francophon_e annuel. Colloque <strong>Inserm</strong>, vol. 214.<br />
Paris : Editions <strong>Inserm</strong>, 1991 : 83- 100.<br />
3. Bruckner-Tu<strong>de</strong>rman L. Col<strong>la</strong>gens of the<br />
<strong>de</strong>rmal-epi<strong>de</strong>rmal junction : role in bullous<br />
disor<strong>de</strong>rs. Eur J Dennatol 1991 ; 1 : 89-1 00.<br />
4. Staquet MJ , Le Varlet B, Dezutter<br />
Dambuyant C, Schmitt D, Thivolet J. I<strong>de</strong>ntification<br />
of specifie human epithelial cell<br />
integrin receptors as VLA proteins. Exp Cel/<br />
Res 1990 ; 187 : 277-83 .<br />
5. Sonnenberg A, Ca<strong>la</strong>fat J, Janssen H,<br />
Daams H, van <strong>de</strong>r Raaij-Helmer LMH,<br />
Falcioni R; Kennel SJ , Apl in JD, Baker J,<br />
Loizidou M, Garrod D. lntegrin a6{34 complex<br />
is located in hemi<strong>de</strong>smosomes, suggesting<br />
a major role in epi<strong>de</strong>rmal cell-basement<br />
membrane adhesion. J Cel/ Biol 1991 ; 113 :<br />
907-17.<br />
6. Carter WG, Ryan MC, Gahr PJ . Epiligrin,<br />
a new ccli adhesion ligand for integrin<br />
a3{31 in epithelial basement membranes. Cel/<br />
1991 ; 65 : 599-610.<br />
7. Stanley JR. Pemphigus and pemphigoid<br />
as paradigms of organ-specifie, autoantibody<br />
mediated diseases. J Clin lnvesl<br />
1991 ; 83 : 1443-8.<br />
8. Domloge-Hultsch N. Gammon WR,<br />
Briggaman RA, Gil SG, Carter WC, Yancey<br />
KB. Epiligrin, the major human keratinocyte<br />
integrin ligand, is the target in both<br />
and acquired autoimmune and an inherited<br />
subepi<strong>de</strong>rmal blistering skin disease. J Clin<br />
Invesl 1992 ; 90 : 1628-33.<br />
9. Thivolet J, Barthélemy H. Bullous pemphigoid.<br />
Sernin Dennatol 1988 ; 7 : 91-103.<br />
10. C<strong>la</strong>udy AL. La pemphigoï<strong>de</strong> gestationis :<br />
un modèle unique d'auto-immunité spécifique<br />
d'organe. Ann Dennatol Venerol 1991 ;<br />
118 : 323-7.<br />
11. Prost C, Labeille B, Chaussa<strong>de</strong> V,<br />
Guil<strong>la</strong>ume JC, Martin N, Dubertret L.<br />
Immunoelectron microscopy in subepi<strong>de</strong>rmal<br />
autoimmune bullous diseases : a prospective<br />
study of IgG and C3 bound in vivo in 32<br />
patients. J lnvesl Dennatol 1987 ; 89 : 567-73.<br />
12. Gammon WR, Briggaman RA, Inman<br />
AO, Queen LL, Wheeler CE. Differentiating<br />
anti-/amina lucida and anti-sub/amina <strong>de</strong>nsa<br />
anti-BMZ antibodies by indirect immunofluorescence<br />
on 1.0 M sodium chlori<strong>de</strong>separated<br />
skin. J lnvest Dennatol 1984 ; 82 :<br />
- 139-44.<br />
378<br />
électrons, <strong>la</strong> <strong>la</strong>mina lucida , et un feuillet<br />
<strong>de</strong>nse aux électrons, <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa. Les fi<strong>la</strong>ments d'ancrage amarrent<br />
les hémi<strong>de</strong>smosomes à <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa en traversant <strong>la</strong> <strong>la</strong>mina lucida ;<br />
(3) <strong>la</strong> région située sous <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa (sub<strong>la</strong>mina <strong>de</strong>nsa), qui contient les<br />
fibrilles d'ancrage et les faisceaux <strong>de</strong><br />
col<strong>la</strong>gènes microfibril<strong>la</strong>ires et<br />
interstitiels.<br />
Deux structures fonctionnelles apparaissent<br />
plus spécialement responsables<br />
<strong>de</strong> <strong>la</strong> cohésion <strong>de</strong> 1 'épi<strong>de</strong>rme au<br />
<strong>de</strong>rme : (1) le complexe hémi<strong>de</strong>smosomes/fùaments<br />
d'ancrage qui amarre<br />
le pôle basal <strong>de</strong>s kératinocytes basaux<br />
à <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa et les fibrilles<br />
d'ancrage qui amarrent <strong>la</strong> <strong>la</strong>mina<br />
1<br />
<strong>de</strong>nsa au <strong>de</strong>rme (figure 2) .<br />
Molécules ·<br />
<strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
Tous les composants <strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique ne sont probable-<br />
Epi<strong>de</strong>rme<br />
F.t. ---+-+<br />
HO, P.A. ----+ rT1r-,_,...<br />
P. O.S. B. ---•<br />
Derme<br />
c--.<br />
ment pas encore connus. Néanmoins,<br />
un grand nombre <strong>de</strong> molécules ont<br />
été i<strong>de</strong>ntifiées, caractérisées et localisées<br />
ces <strong>de</strong>rnières années grâce à<br />
1 'immunomicroscopie électronique<br />
(figure 3) . Ainsi, les hémi<strong>de</strong>smosomes<br />
contiennent les antigènes <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong><br />
bulleuse (BP Ag 1 et 2) et<br />
<strong>la</strong> molécule a6/34, une intégrine spécifique<br />
<strong>de</strong>s épithéliums [ 4]. La <strong>la</strong>minine<br />
est l'un <strong>de</strong>s constituants principaux<br />
<strong>de</strong> <strong>la</strong> <strong>la</strong>mina lucida, qui contient<br />
aussi <strong>de</strong>s molécules dont les dénominations<br />
différentes (nicéine, kalinine<br />
et épiligrine) sont probablement <strong>de</strong>s<br />
éponymes d'une même protéine.<br />
Le col<strong>la</strong>gène <strong>de</strong> type IV, l'entactine/nidogène,<br />
les héparan-sulfate<br />
protéoglycanes et <strong>la</strong> molécule BM-40<br />
sont <strong>de</strong>s constituants <strong>de</strong> <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa. Le col<strong>la</strong>gène <strong>de</strong> type VII est<br />
associé aux fibrilles d'ancrage dans <strong>la</strong><br />
sub<strong>la</strong>mina <strong>de</strong>nsa.<br />
Beaucoup <strong>de</strong> progrès ont été accomplis<br />
ces <strong>de</strong>rnières années en ce qui<br />
concerne l'organisation supramolécu-<br />
C.B.<br />
L.L.<br />
L.D.<br />
S.L.D.<br />
Figure 2. Jonction <strong>de</strong>rmo-épi<strong>de</strong>rmique : aspects morphologiques. 0: <strong>de</strong>smosomes<br />
; N : noyau ; F. l. : fi<strong>la</strong>ments intermédiaires ; C. B. : kératinocytes <strong>de</strong><br />
<strong>la</strong> couche basale <strong>de</strong> l'épi<strong>de</strong>rme ; HO : hémi<strong>de</strong>smosomes ; P.A. : p<strong>la</strong>ques d'attachement<br />
; P.D.S.B. : p<strong>la</strong>ques <strong>de</strong>nses sub-basales ; F. I.A. : fi<strong>la</strong>ments d'ancrage ;<br />
F. A. : fibrilles d'ancrage ; C: col<strong>la</strong>gène ; L.L. : <strong>la</strong>mina lucida ; L.D. : <strong>la</strong>mina<br />
<strong>de</strong>nsa ; S.L.D. : sub<strong>la</strong>mina <strong>de</strong>nsa ; J. O. E. :<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique ; F.E. :<br />
pseudofibrilles é<strong>la</strong>stiques ; P.An. : p<strong>la</strong>que d'ancrage.<br />
J.<br />
D.<br />
E.<br />
mis n ° 4 vol. 9, avril 93
<strong>la</strong>ire <strong>de</strong>s constituants <strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique. Il semble que les<br />
molécules hémi<strong>de</strong>smosomiales a6/34<br />
interagissent avec les antigènes BP,<br />
eux-mêmes associés aux fùaments<br />
intermédiaires du cytosquelette. Ces<br />
molécules a6/34 formeraient un complexe<br />
d'adhérence stable, qui aurait<br />
pour ligand dans <strong>la</strong> <strong>la</strong>mina lucida <strong>la</strong><br />
nicéine/épiligrine, elle-même ancrée<br />
dans <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa (5] (figure 4).<br />
L'adhésine a3/31 exprimée par les<br />
cellules épi<strong>de</strong>rmiques aurait pour<br />
ligand l'épiligrine (6]. Ces hypothèses<br />
d'interactions molécu<strong>la</strong>ires suggérées<br />
par les résultats <strong>de</strong> travaux réalisés in<br />
vitro méritent d'être confirmées.<br />
La connaissance précise <strong>de</strong>s molécules<br />
composant <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
et <strong>de</strong> leur distribution<br />
dans ses différentes couches présente<br />
non seulement un intérêt fondamental<br />
en biologie cellu<strong>la</strong>ire, mais aussi<br />
un intérêt diagnostique et pathogénique<br />
dans les ma<strong>la</strong>dies <strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique. Plusieurs ma<strong>la</strong>dies<br />
génétiques et <strong>acquise</strong>s se caractérisent<br />
par une fragilité cutanée due<br />
à un défaut d'adhérence <strong>de</strong> l'épi<strong>de</strong>rme<br />
au <strong>de</strong>rme par l'intermédiaire<br />
<strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique [ 1].<br />
La connaissance précise <strong>de</strong> <strong>la</strong> distribution<br />
<strong>de</strong>s principales molécules <strong>de</strong> <strong>la</strong><br />
<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique peut être<br />
appliquée utilement à l'immunolocalisation<br />
<strong>de</strong>s antigènes lors <strong>de</strong> décollement<br />
bulleux cutanés. Le marquage<br />
d'une peau bulleuse avec <strong>de</strong>s anticorps<br />
dirigés contre <strong>de</strong>s constituants<br />
<strong>de</strong>s hémi<strong>de</strong>smosomes (BP Ag), <strong>de</strong> <strong>la</strong><br />
<strong>la</strong>mina lucida (<strong>la</strong>minine), <strong>de</strong> <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa (col<strong>la</strong>gène <strong>de</strong> type IV) ou <strong>de</strong> <strong>la</strong><br />
zone <strong>de</strong> <strong>la</strong> sub<strong>la</strong>mina <strong>de</strong>nsa (col<strong>la</strong>gène<br />
<strong>de</strong> type VII), permet <strong>de</strong> préciser rapi<strong>de</strong>ment<br />
le niveau du clivage . Les<br />
techniques immunochimiques permettant<br />
<strong>de</strong> mettre en évi<strong>de</strong>nce l'existence<br />
d'auto-anticorps dirigés contre <strong>de</strong>s<br />
constituants <strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
ont permis <strong>de</strong> préciser<br />
les critères diagnostiques <strong>de</strong> certaines<br />
ma<strong>la</strong>dies auto-immunes bulleuses, et<br />
<strong>de</strong> définir les antigènes cibles <strong>de</strong>s<br />
réponses inf<strong>la</strong>mmatoires au taimmunes<br />
[7]. Enfm, certaines <strong>de</strong>rmatoses<br />
bulleuses héréditaires se caractérisent<br />
par l'absence ou l'expression<br />
anormale <strong>de</strong> certains composants <strong>de</strong><br />
<strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique [ 1].<br />
Parmi <strong>la</strong> vingtaine <strong>de</strong> molécules constituant<br />
<strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique<br />
mis n ° 4 uol. 9, aoril 93<br />
H.D.<br />
L.L.<br />
L.D.<br />
Figure 3. Jonction <strong>de</strong>rmo-épi<strong>de</strong>rmique : aspects molécu<strong>la</strong>ires. Coll. IV : col<strong>la</strong>gène<br />
IV ; Coll. VI/ : col<strong>la</strong>gène VI/ ; Ag : antigène ; BPA : antigène(s) <strong>de</strong> <strong>la</strong><br />
pemphigoï<strong>de</strong> bulleuse. Pour les autres abréviations, voir légen<strong>de</strong> <strong>de</strong> <strong>la</strong> figure 2.<br />
L.L.<br />
L.D.<br />
S.L.D.<br />
Kératinocytes<br />
basaux<br />
Figure 4. Molécules <strong>de</strong>s hémi<strong>de</strong>smosomes. BPA : antigènes <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong><br />
bulleuse. Pour les autres abréviations, voir légen<strong>de</strong> <strong>de</strong> <strong>la</strong> figure 2. -<br />
379
RÉFÉRENCES<br />
13. Kelly SE, Wojnarowska F. The use of<br />
chemically split tissue in the <strong>de</strong>tection of circu<strong>la</strong>ting<br />
anti-basement membrane zone antibodies<br />
in bullous pempbigoid and cicatricial<br />
pemphigoid. Br J Dermatol 1988 ; 118 :<br />
31-40.<br />
14. Mueller S, K<strong>la</strong>us-Kovtun V, Stanley<br />
JR. A 230-kD basic protein is the major<br />
bullous pempbigoid antigen. J lnvest Dermatol<br />
1989 ; 92 : 33-8.<br />
15. Sarret Y, Reano A, Nico<strong>la</strong>s JF, Su H,<br />
Tbivolet J. Bullous pempbigoid and cicatricial<br />
pemphigoid : immunoblotting <strong>de</strong>tection<br />
of involved autoantigens. Autoimmuniry 1989 ;<br />
2 : 145-53.<br />
16. Bernard P, Didierjean L, Denis F, Saurat<br />
JH, Bonnetb<strong>la</strong>nc JM. Heterogeneous<br />
bullous pempbigoid antibodies : <strong>de</strong>tection<br />
and caracterization by immunoblotting when<br />
absent by indirect immunofluorescence.<br />
J lnvest Dermatol 1989 ; 92 : 1 71-4.<br />
17. Machado P, Micha<strong>la</strong>ki H, Roche P,<br />
Gaucherand M, Thivolet J, Nico<strong>la</strong>s JF.<br />
Comparison of the sensitivity of indirect IF<br />
on salt-split skin to immunoblotting fo r the<br />
<strong>de</strong>tection of circu<strong>la</strong>ting autoantibodies. Br J<br />
Dermatol 1992 ; 126 : 236-41.<br />
18. Bernard P, Prost C, Du repaire N,<br />
Basset-Seguin N, Didierjean L, Saurat JH.<br />
The major cicatricial pemphigoid antigen is<br />
a 180-kD protein that shows immunologie<br />
cross-reactivities with the bullous pemphigoid<br />
antigen. J lnvest Dermatol 1992 ; 99 : 174-79.<br />
19. Sawamura D, Li K, Chu ML, Uitto J.<br />
Human bullous pe mphigoid antigen<br />
(BPAG I). J Biol Chem 1991 ; 266 :<br />
17784-90.<br />
20. Tanaka T, Korman J, Shimizu H,<br />
Eady RAJ, K<strong>la</strong>us-Kovtun V, Cehrs K,<br />
Stanley JR. Production of rabbit antibodies<br />
against carboxytermi.nal epitopes enco<strong>de</strong>d by<br />
bullous pemphigoid eDNA. J lnvest Dermatol<br />
1990 ; 94 : 617-23.<br />
21. Stanley JR, Tanaka T, Mueller S,<br />
K<strong>la</strong>us-Kovtun V, Roop D. Iso<strong>la</strong>tion of<br />
eDNA for bullous pemphigoid antigen by<br />
use of patients' autoantibodies. J Clin lnvest<br />
1988 ; 82 : 1864-70.<br />
22. Diaz LA, Ratrie III H, Saun<strong>de</strong>rs WS,<br />
Futamura S, Squiquera HL, Anhalt CH,<br />
Guidicc GJ . Iso<strong>la</strong>tion of a hu man cpidcrmal<br />
eDNA corresponding to the 180 kD<br />
autoantigen rccognized by bullous pemphigoid<br />
and herpes gestationis sera. J Clin lnvest<br />
1990 ; 86 : 1088-94.<br />
23. Sawamura D, Li K, Uitto J. 230-kD<br />
and 180-kD bullous pemphigoid antigens are<br />
distinct gene products. J fnvest Dermatol<br />
1992 ; 98 : 942-3.<br />
24. Amagai M, Elgart GW, K<strong>la</strong>us<br />
Kovtun V, Stanley JR. Southern analysis of<br />
the 230 kDa bullous pemphigoid antigen<br />
gene in normal humans, animals, and<br />
patients with junctional epi<strong>de</strong>rmolysis bu!-<br />
- losa. J lnvest Dermatol 1991 ; 97 : 249-53.<br />
380<br />
actuellement connues, seul un nombre<br />
restreint est immunogène, sur <strong>la</strong><br />
base <strong>de</strong> l'existence <strong>de</strong> ma<strong>la</strong>dies autoimmunes<br />
spontanées, associées à <strong>la</strong><br />
présence dans le sérum <strong>de</strong>s patients<br />
d'auto-anticorps spécifiques <strong>de</strong> ces<br />
molécules. Deux <strong>de</strong> ces molécules, les<br />
antigènes <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong> bulleuse<br />
(BP Ag 1 et 2) et le col<strong>la</strong>gène <strong>de</strong><br />
type VII, ont un intérêt particulier.<br />
En effet, les patients présentant une<br />
pemphigoï<strong>de</strong> bulleuse et une épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong> possè<strong>de</strong>nt<br />
respectivement <strong>de</strong>s anticorps dirigés<br />
contre les BP Ag et le col<strong>la</strong>gène <strong>de</strong><br />
type VII. La nicéine/épiligrine est<br />
actuellement l'objet <strong>de</strong> recherches<br />
importantes en raison du rôle majeur<br />
qu'elle semble jouer dans l'adhérence<br />
<strong>de</strong> l'épi<strong>de</strong>rme au <strong>de</strong>rme, comme semble<br />
le prouver son absence dans certaines<br />
ma<strong>la</strong>dies bulleuses héréditaires<br />
[1] et l'existence d'auto-anticorps<br />
anti-épiligrine dans un sous-groupe <strong>de</strong><br />
ma<strong>la</strong>dies auto-immunes bulleuses [8].<br />
1 Pemphigoï<strong>de</strong>s<br />
bulleuses<br />
Nous regroupons dans cc chapitre<br />
trois ma<strong>la</strong>dies distinctes en raison <strong>de</strong><br />
leurs similitu<strong>de</strong>s immunopathologiques<br />
: ( 1) elles peuvent être définies<br />
comme une auto-immunisation vis-àvis<br />
<strong>de</strong>s antigènes <strong>de</strong>s hémi<strong>de</strong>smosomes<br />
[7] ; (2) elles sont caractérisées<br />
par <strong>la</strong> présence d'auto-anticorps fixés<br />
au niveau <strong>de</strong> <strong>la</strong> peau lésionnelle et/ou<br />
circu<strong>la</strong>nts dirigés contre <strong>de</strong>ux antigènes<br />
<strong>de</strong>s hémi<strong>de</strong>smosomes : BP<br />
Ag 1 et BP Ag 2.<br />
Trois ma<strong>la</strong>dies composent ce groupe :<br />
( 1) <strong>la</strong> pemphigoï<strong>de</strong> bulleuse qui, dans<br />
ses formes généralisée et localisée<br />
atteint <strong>de</strong>s sujets âgés et se présente<br />
sous forme <strong>de</strong> lésions urticariennes<br />
sur lesquelles surviennent <strong>de</strong>s bulles<br />
tendues et hémorragiques ; les faces<br />
internes <strong>de</strong>s membres et les faces <strong>la</strong>térales<br />
du tronc sont les sites <strong>de</strong> prédilection<br />
<strong>de</strong> l'affection [9] ; (2) <strong>la</strong> pemphigoï<strong>de</strong><br />
cicatricielle touche <strong>de</strong>s sujets<br />
plus jeunes et donne surtout <strong>de</strong>s<br />
lésions muqueuses (ocu<strong>la</strong>ires, buccales)<br />
évoluant vers <strong>de</strong>s cicatrices<br />
rétractiles ; le pôle céphalique et le<br />
tronc peuvent être atteints et sont<br />
aussi le siège d'une évolution cicatricielle<br />
; (3) <strong>la</strong> pemphigoï<strong>de</strong> gestationis,<br />
qui atteint les femmes enceintes au<br />
cours du <strong>de</strong>rnier trimestre <strong>de</strong> <strong>la</strong> gros-<br />
sesse, et donne une éruption urticarienne<br />
et bulleuse débutant sur<br />
l'abdomen et se résolvant spontanément<br />
dans les jours ou semaines qui<br />
suivent l'accouchement [10].<br />
La pemphigoï<strong>de</strong> bulleuse est <strong>la</strong> plus<br />
fréquente <strong>de</strong>s <strong>de</strong>rmatoses bulleuses<br />
<strong>acquise</strong>s <strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique,<br />
ce qui explique les progrès<br />
récents dans <strong>la</strong> compréhension<br />
<strong>de</strong> cette affection. Les paragraphes<br />
suivants se rapportent principalement<br />
à cette ma<strong>la</strong>die.<br />
• Le diagnostic <strong>de</strong> pemphigoï<strong>de</strong> bulleuse,<br />
suspecté d'après le tableau clinique<br />
et l'image histologique (figures<br />
5a et 5b ), qui montre une bulle<br />
sous-épi<strong>de</strong>rmique, est confirmé par<br />
l'immunopathologie [7, 9]. L'immunofluorescence<br />
directe met en évi<strong>de</strong>nce<br />
in situ, dans <strong>la</strong> peau périlésionnelle,<br />
un dépôt d'IgG et <strong>de</strong> fractions<br />
du complément (C3 notamment)<br />
(figure 5c). Ce critère est indispensable<br />
au diagnostic. L'immunofluorescence<br />
indirecte permet <strong>de</strong> détecter,<br />
dans un nombre variable <strong>de</strong> cas<br />
(30-90 % ), <strong>la</strong> présence d'anticorps<br />
circu<strong>la</strong>nts (IgG) anti-<strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique.<br />
L'immunomicroscopie<br />
électronique directe et indirecte montre<br />
que les antigènes cibles <strong>de</strong>s autoanticorps<br />
sont <strong>de</strong>s constituants <strong>de</strong>s<br />
hémi<strong>de</strong>smosomes et <strong>de</strong> <strong>la</strong> <strong>la</strong>mina<br />
lucida [ 11].<br />
• Les progrès dans le domaine diagnostique<br />
<strong>de</strong> <strong>la</strong> ma<strong>la</strong>die ont reposé<br />
sur le développement <strong>de</strong> <strong>la</strong> technique<br />
d'immunofluorescence sur peau clivée<br />
par le Na Cl et sur le développement<br />
<strong>de</strong>s techniques d'immunotransfert. Le<br />
NaCl à <strong>la</strong> concentration <strong>de</strong> 1 M est<br />
responsable du clivage <strong>de</strong> <strong>la</strong> peau au<br />
niveau <strong>de</strong> <strong>la</strong> <strong>la</strong>mina lucida, ce qui crée<br />
une bulle dont le toit correspond à<br />
l'épi<strong>de</strong>rme et dont le p<strong>la</strong>ncher est<br />
constitué par <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa et le<br />
<strong>de</strong>rme. L'immunofluorescence indirecte<br />
sur peau dissociée au Na Cl permet<br />
ainsi <strong>de</strong> confirmer le diagnostic<br />
<strong>de</strong> pemphigoï<strong>de</strong> bulleuse si <strong>la</strong> ftxation<br />
<strong>de</strong>s auto-anticorps circu<strong>la</strong>nts se fait<br />
du côté épi<strong>de</strong>rmique [12,13]<br />
(figure 5d).<br />
L'analyse par immunoprécipitation <strong>de</strong><br />
<strong>la</strong> réactivité <strong>de</strong>s auto-anticorps sur<br />
<strong>de</strong>s extraits protéiques radiomarqués<br />
d'épi<strong>de</strong>rme en culture a permis <strong>de</strong><br />
définir les antigènes cibles <strong>de</strong> <strong>la</strong><br />
réponse immunitaire comme étant<br />
<strong>de</strong>s polypepti<strong>de</strong>s d'un poids molécu-<br />
mis n ° 4 vol. 9, avril 93
<strong>la</strong>ire <strong>de</strong> 230 et 180 kDa (14).<br />
L'immunotransfert remp<strong>la</strong>ce<br />
l'immunoprécipitation pour le diagnostic<br />
sérologique <strong>de</strong> <strong>la</strong> ma<strong>la</strong>die<br />
[ 15-18) (figure 5e) .<br />
• L'antigène <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong> bulleuse<br />
(BP Ag) est l'antigène <strong>de</strong>s<br />
hémi<strong>de</strong>smosomes le plus anciennement<br />
connu. Il est défini grâce à <strong>la</strong><br />
réactivité <strong>de</strong>s sérums <strong>de</strong> patients présentant<br />
une pemphigoï<strong>de</strong> bulleuse.<br />
L'antigène apparaît dès le troisième<br />
mois <strong>de</strong> vie intra-utérine, et les étu<strong>de</strong>s<br />
phylogéniques ont montré sa présence<br />
dans <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
cutanée d'espèces aussi<br />
éloignées <strong>de</strong> l'homme que les batraciens.<br />
L'antigène BP est présent dans<br />
les épithéliums malpighiens stratifiés<br />
(peau, lèvres, <strong>la</strong>ngue, œsophage ;<br />
muqueuses buccale, ocu<strong>la</strong>ire, vaginale<br />
et anale). Il est produit par les kératinocytes<br />
<strong>de</strong> <strong>la</strong> couche basale épi<strong>de</strong>rmique<br />
et est po<strong>la</strong>risé à <strong>la</strong> face basale<br />
<strong>de</strong> ces cellules en culture. Les étu<strong>de</strong>s<br />
immunochimiques et <strong>la</strong> caractérisation<br />
molécu<strong>la</strong>ire <strong>de</strong> <strong>la</strong> cible <strong>de</strong>s autoanticorps<br />
<strong>de</strong>s patients souffrant <strong>de</strong><br />
pemphigoï<strong>de</strong> bulleuse ont montré<br />
qu 'il existait <strong>de</strong>ux antigènes <strong>de</strong> <strong>la</strong><br />
pemphigoï<strong>de</strong> bulleuse : BP Ag 1<br />
(230 kDa) et BP Ag 2<br />
(180 kDa) (19-22). BP Ag 1 et 2 sont<br />
codés par <strong>de</strong>ux gènes différents non<br />
homologues, présents chez l'homme,<br />
respectivement sur le bras court du<br />
chromosome 6 (BP Ag 1, locus<br />
6p 11-12) et sur le bras long du chromosome<br />
10 (BP Ag 2, locus 1 Oq<br />
24.3) (23). L'ARNm codant pour BP<br />
Ag 1 est <strong>de</strong> 9 kb, celui codant pour<br />
BP Ag 2, <strong>de</strong> 6 kb. Le gène codant<br />
pour BP Ag 1 est en copie unique<br />
chez l'homme (24), même s'il existe<br />
un certain polymorphisme. La<br />
séquence en aci<strong>de</strong>s aminés <strong>de</strong> <strong>la</strong><br />
molécule BP Ag 1, déduite <strong>de</strong> <strong>la</strong><br />
séquence en nucléoti<strong>de</strong>s <strong>de</strong> l'ADNe,<br />
présente, dans certaines régions, <strong>de</strong>s<br />
homologies avec <strong>la</strong> <strong>de</strong>smop<strong>la</strong>kine 1 ;<br />
ces régions correspondraient à <strong>de</strong>s<br />
sites d'interaction <strong>de</strong> BP Ag 1 avec<br />
les fi<strong>la</strong>ments intermédiaires <strong>de</strong> kératine<br />
(25). La structure <strong>de</strong> <strong>la</strong> molécule<br />
serait celle d'une hélice a (simi<strong>la</strong>ire<br />
à celJe <strong>de</strong>s fi<strong>la</strong>ments intermédiaires)<br />
dans <strong>la</strong> partie centrale <strong>de</strong> <strong>la</strong> molécule,<br />
f<strong>la</strong>nquée <strong>de</strong> <strong>de</strong>ux domaines globu<strong>la</strong>ires<br />
aux extrémités <strong>de</strong> <strong>la</strong> molécule<br />
(19) . L'homologie entre les BP<br />
Ag 1 humain et murin est supérieure<br />
mis n ° 4 vol. 9, avril 93<br />
à 80 % et atteint 100 % dans les<br />
régions hydrophiles. L'existence <strong>de</strong><br />
ces régions très conservées entre les<br />
<strong>de</strong>ux espèces suggère un rôle fonctionnel<br />
important <strong>de</strong> ces segments qui<br />
ont dû subir <strong>de</strong>s contraintes sélectives<br />
plus importantes que le reste <strong>de</strong><br />
<strong>la</strong> molécule, probablement pour assurer<br />
leur présentation correcte à <strong>la</strong> sur-<br />
face cellu<strong>la</strong>ire . Ces régions très conservées<br />
contiennent certainement <strong>de</strong>s<br />
déterminants antigéniques <strong>de</strong> <strong>la</strong> molécule<br />
BP.<br />
Le clonage du gène codant pour BP<br />
Ag 2 <strong>de</strong> 180 kDa a permis <strong>de</strong> montrer<br />
qu'aucune homologie n'existait<br />
avec <strong>la</strong> molécule BP Ag 1 <strong>de</strong><br />
230 kDa. BP Ag 2 présente plusieurs<br />
Figure 5. Pemphigoï<strong>de</strong> bulleuse : aspects anatomo-clinique et immunopathologique.<br />
A : aspect clinique : bulles tendues hémorragiques et croûtes.<br />
B : histologie : bulle sous-épi<strong>de</strong>rmique. C : immunofluorescence directe sur peau<br />
inf<strong>la</strong>mmatoire péribulleuse : dépôt d'lgG. D : immunofluorescence indirecte sur<br />
peau humaine normale dissociée au NaCI 1 M. Les anticorps du patient se<br />
fixent sur <strong>la</strong> partie épi<strong>de</strong>rmique <strong>de</strong> <strong>la</strong> membrane basale. E : analyse <strong>de</strong> <strong>la</strong> réactivité<br />
<strong>de</strong>s sérums <strong>de</strong> patients sur un extrait <strong>de</strong> kératinocyte en culture par<br />
immuno-empreinte. Les sérums reconnaissent <strong>de</strong>ux antigènes épi<strong>de</strong>rmiques <strong>de</strong><br />
230 kDa (sérum 3) et 180 kDa (sérums 1 et 2). e ou E: épi<strong>de</strong>rme ; 0: <strong>de</strong>rme ;<br />
8: bulle. -<br />
381
RÉFÉRENCES<br />
25. Tanaka T, Parry DAD, K<strong>la</strong>us<br />
Kovtun V, Steinert PM, Stanley JR. Comparison<br />
of molecu<strong>la</strong>rly cloned bullous pemphigoid<br />
antigen to <strong>de</strong>smop<strong>la</strong>kin I confirms<br />
that they <strong>de</strong>fine a new family of cell adhesion<br />
junction p<strong>la</strong>que proteins. J Biol Chem<br />
1991 ; 266 : 12555-9.<br />
26. Guidice GJ , Squiquera HL, Elias PM,<br />
Diaz LA. I<strong>de</strong>ntification of two col<strong>la</strong>gen<br />
domains within the bullous pemphigoid<br />
autoantigen, BP 180. J Clin lnvesl 1991 ;<br />
87 : 734-8.<br />
27. Guidice GJ , Emery DJ , Diaz LA. Cloning<br />
and primary structural analysis of the<br />
bullous pemphigoid autoantigen BP 180.<br />
J lnvest Dermatol 1992 ; 99 : 243-50.<br />
28. Hopkinson SB, Rid<strong>de</strong>lle KS,<br />
Jones JCR. Cytop<strong>la</strong>smic domain of the<br />
180 kD bullous pemphigoid antigen, a hemi<strong>de</strong>smosomal<br />
component : molecu<strong>la</strong>r and cell<br />
biologie characterization. J lnvest Dermatol<br />
1992 ; 99 : 264-70.<br />
29. Rico MJ , Korman NJ , Stanley JR,<br />
Tanaka T, Hall RP. IgG antibodies from<br />
patients with bullous pemphigoid bind to<br />
localized epitopes on synthetic pepti<strong>de</strong>s enco<strong>de</strong>d<br />
by bullous pemphigoid antigen eDNA.<br />
J lmmunol 1990 ; 145 : 3728-33.<br />
30. Sugi T, Hashimoto T, Hibi T, Nishikawa<br />
T. Production of human monoclonal<br />
anti-basement membrane zone (BMZ) antibodies<br />
from a patient with bullous pemphigoid<br />
(BP) by Epstein-Barr virus transformation.<br />
J Clin lnvest 1989 ; 84 : 1050-5.<br />
31. Peyron E, Rousset F, Roche P, Frances<br />
V, Banchereau J, Schmitt D, Thivolet J,<br />
Nico<strong>la</strong>s JF. Generation of B cell lines producing<br />
human antibodies against skin antigens.<br />
J lnvesl Dermatol 1992 ; 98 : 509A.<br />
32. Micha<strong>la</strong>ki H, Staquet M-J, Cerri A,<br />
Berti E, Roche P, Machado P, Nico<strong>la</strong>s JF.<br />
Expression of a6/34 integrin in lesional skin<br />
differentiates bullous pemphigoid (BP) from<br />
epi<strong>de</strong>rmolysis bullosa acquisita. J lnvest Dermato!<br />
1992 ; 98 : 204-8.<br />
33. Dubertret L, Bertaux B, Fosse M, Touraine<br />
R. Cellu<strong>la</strong>r events leading to blister<br />
formation in bullous pemphigoid. Br J Dermato!<br />
1980 ; 104 : 615-24.<br />
34. Micha<strong>la</strong>ki H, Nico<strong>la</strong>s JF, Kanitakis J,<br />
Machado P, Roche P, Thivolet J. T cells<br />
in bullous pemphigoid. Presence of activated<br />
CD4 + T cells at the basement membrane<br />
zone in pre- and peribullous skin.<br />
Regional lmmunol 1991 ; 3 : 151-5.<br />
35. Micha<strong>la</strong>ki H, Nico<strong>la</strong>s JF, Gaucherand,<br />
Thivolet J, Hercend T, Ferradini L. ln situ<br />
preferential usage of V aB T cell receptor<br />
gene segments in a patient with bullous<br />
pemphigoid. J lnvest Dermatol 1992 ; 98 :<br />
839A.<br />
36. Nico<strong>la</strong>s JF, Micha<strong>la</strong>ki H, Dcmi<strong>de</strong>m A.<br />
Récepteurs à l'antigène <strong>de</strong>s lymphocytes T.<br />
In : Thivolet J, Faure M, Schmitt D, eds.<br />
Implication dans les <strong>de</strong>rmatoses inf<strong>la</strong>mmatoires et<br />
auto-immunes. Biologie <strong>de</strong> lil, peau. Colloque<br />
<strong>Inserm</strong>, vol. 104. Paris : Editions <strong>Inserm</strong>,<br />
- 1991 : 35-50.<br />
382<br />
caractéristiques, parmi lesquelles <strong>la</strong><br />
position intracytop<strong>la</strong>smique <strong>de</strong> son<br />
extrémité N-terminale, propriété partagée<br />
par seulement 5 % <strong>de</strong>s protéines<br />
transmembranaires [22]. Une<br />
autre caractéristique <strong>de</strong> BP Ag 2 est<br />
<strong>de</strong> présenter <strong>de</strong>s homologies <strong>de</strong><br />
séquence avec le col<strong>la</strong>gène, d'où<br />
l'hypothèse selon <strong>la</strong>quelle BP Ag 2<br />
serait un nouveau col<strong>la</strong>gène <strong>de</strong>s épithéliums<br />
<strong>de</strong> revêtement [26]. L'extrémité<br />
carboxy-terminale <strong>de</strong> <strong>la</strong> molécule<br />
porte cette région d'homologie, et sa<br />
situation dans le domaine extracellu<strong>la</strong>ire<br />
permettrait l'interaction <strong>de</strong> BP<br />
Ag 2 avec les molécules <strong>de</strong> <strong>la</strong> matrice<br />
extracellu<strong>la</strong>ire [27, 28].<br />
Les antigènes BP sont <strong>de</strong>s constituants<br />
<strong>de</strong>s hémi<strong>de</strong>smosomes <strong>de</strong>s kératinocytes<br />
<strong>de</strong> <strong>la</strong> couche basale <strong>de</strong> l'épi<strong>de</strong>rme.<br />
Leur localisation précise au<br />
sein <strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique<br />
reste controversée. Les<br />
résultats <strong>de</strong>s étu<strong>de</strong>s molécu<strong>la</strong>ires et<br />
ceux <strong>de</strong> l'immunolocalisation électronique<br />
concor<strong>de</strong>nt pour l'antigène Bp<br />
Ag 2 <strong>de</strong> 180 kDa, qui apparaît<br />
comme une molécule transmembranaire<br />
avec une région intracytop<strong>la</strong>smique<br />
associée aux hémi<strong>de</strong>smosomes,<br />
une région transmembranaire et une<br />
région extracellu<strong>la</strong>ire s'étendant dans<br />
<strong>la</strong> <strong>la</strong>mina lucida [28]. A l'inverse, les<br />
résultats sont discordants pour 1' antigène<br />
Bp Ag 1 <strong>de</strong> 230 kDa, qui serait<br />
uniquement intracellu<strong>la</strong>ire selon les<br />
résultats obtenus en immunomicroscopie<br />
électronique directe [20], alors<br />
que les résultats <strong>de</strong> 1' analyse <strong>de</strong> <strong>la</strong><br />
séquence nucléotidique <strong>de</strong>s ADNe<br />
sont en faveur <strong>de</strong> l'existence d'une<br />
regwn intracytop<strong>la</strong>smique, d'une<br />
région transmembranaire et d'une<br />
région extracellu<strong>la</strong>ire [ 19].<br />
Les recherches actuelles s'orientent<br />
vers <strong>la</strong> mise en évi<strong>de</strong>nce <strong>de</strong>s épitopes<br />
<strong>de</strong>s <strong>de</strong>ux molécules BP Ag. La majorité<br />
(75 %) <strong>de</strong>s sérums <strong>de</strong>s patients<br />
contiennent <strong>de</strong>s anticorps anti-BP<br />
Ag 1 (230 kDa) d'où son nom d'antigène<br />
à propos <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong> cicatricielle,<br />
il est important <strong>de</strong> signaler <strong>la</strong><br />
mise en évi<strong>de</strong>nce récente, dans trois<br />
cas <strong>de</strong> ma<strong>la</strong>die bulleuse <strong>de</strong> type pemphigoï<strong>de</strong><br />
cicatricielle, d'anticorps circu<strong>la</strong>nts<br />
dirigés contre l'épiligrine, le<br />
ligand situé dans <strong>la</strong> <strong>la</strong>mina lucida <strong>de</strong>s<br />
molécules d'adhérence a31 et a6<br />
<strong>de</strong> <strong>la</strong> membrane <strong>de</strong>s kératinocytes [8].<br />
Des étu<strong>de</strong>s complémentaires préciseront<br />
<strong>la</strong> prévalence <strong>de</strong> ce type d'autoanticorps<br />
dans les ma<strong>la</strong>dies bulleuses<br />
auto-immunes sous-épi<strong>de</strong>rmiques.<br />
D'ores et déjà, l'épiligrine apparaît<br />
comme une molécule immunogène<br />
intervenant dans <strong>la</strong> pathogénie <strong>de</strong><br />
certaines <strong>de</strong> ces affections.<br />
• Les mécanismes physiopathologiques<br />
à l'origine <strong>de</strong>s lésions <strong>de</strong> pemphigoï<strong>de</strong><br />
bulleuse sont encore inconnus,<br />
tant au niveau initial <strong>de</strong><br />
l'inf<strong>la</strong>mmation qu'au niveau tardif <strong>de</strong><br />
formation <strong>de</strong> <strong>la</strong> bulle (figure 6) . La<br />
bulle résulte <strong>de</strong> <strong>la</strong> perte <strong>de</strong> cohésion<br />
entre l'épi<strong>de</strong>rme et le <strong>de</strong>rme, ellemême<br />
liée à <strong>la</strong> <strong>de</strong>struction <strong>de</strong> molé-<br />
A<br />
Protéases<br />
Eo Ma<br />
cules amarrant le pôle basal <strong>de</strong>s kératinocytes<br />
à <strong>la</strong> <strong>la</strong>me <strong>de</strong>nse. Mais <strong>la</strong><br />
(les) structure( s) responsable( s) <strong>de</strong><br />
l'adhérence n'est (ne sont) pas connue(s).<br />
Les BP Ag peuvent être en<br />
cause, <strong>de</strong> même que <strong>la</strong> molécule<br />
a64 qui leur est associée, ou les<br />
complexes a6M/épiligrine-nicéine et<br />
a31/épiligrine-nicéine [8, 32]. Les<br />
polynucléaires éosinophiles qui constituent<br />
le type cellu<strong>la</strong>ire prédominant<br />
dans l'infiltrat inf<strong>la</strong>mmatoire lésionnel<br />
semblent jouer un rôle, et on<br />
peut admettre que les enzymes protéolytiques<br />
produites par les polynucléaires<br />
éosinophiles activés pourraient<br />
être responsables <strong>de</strong> <strong>la</strong> dégradation<br />
du complexe d'adhérence <strong>de</strong> l'épi<strong>de</strong>rme<br />
à <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa [33]. Les étapes<br />
initiales <strong>de</strong> <strong>la</strong> réponse inf<strong>la</strong>mmatoire<br />
sont mal connues. Les autoanticorps<br />
an ti-BP Ag jouent probablement<br />
un rôle dans l'initiation <strong>de</strong><br />
l'inf<strong>la</strong>mmation, peut-être par activation<br />
du complément et par recrutement<br />
et activation secondaire <strong>de</strong>s<br />
BULLE<br />
B<br />
IL-5<br />
IL-4<br />
'<br />
1<br />
1<br />
1 ,._<br />
<br />
- - - - - - -<br />
- - <br />
Ma@-<br />
éosinophiles et <strong>de</strong>s mastocytes. Mais<br />
leur rôle exclusif est peu probable,<br />
surtout en raison <strong>de</strong> l'incapacité <strong>de</strong>s<br />
anticorps à transférer <strong>la</strong> ma<strong>la</strong>die à <strong>la</strong><br />
souris. Les recherches récentes se sont<br />
attachées à apprécier <strong>la</strong> p<strong>la</strong>ce <strong>de</strong><br />
l'immunité cellu<strong>la</strong>ire dans <strong>la</strong> pathogénie<br />
<strong>de</strong> <strong>la</strong> ma<strong>la</strong>die. Les lymphocytes<br />
T CD4 + <strong>de</strong> phénotype mémoire<br />
activés (CD25 • , CD45RO • , HLA<br />
DR • ) représentent un contingent<br />
notable <strong>de</strong>s cellules <strong>de</strong> l'infiltrat<br />
inf<strong>la</strong>mmatoire et sont retrouvés précocement<br />
dans les lésions prébulleuses<br />
en contact avec <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique [34]. L'étu<strong>de</strong> du<br />
répertoire du récepteur T in situ au<br />
niveau <strong>de</strong> <strong>la</strong> peau lésionnelle chez un<br />
patient a permis <strong>de</strong> montrer l'utilisation<br />
préférentielle <strong>de</strong> certains segments<br />
codant pour les régions variables<br />
du récepteur T [35, 36]. Ces<br />
résultats, s'ils suggèrent un rôle<br />
potentiel <strong>de</strong>s lymphocytes T dans le<br />
processus <strong>de</strong> l'inf<strong>la</strong>mmation pathogène,<br />
méritent d'être confirmés par <strong>la</strong><br />
basaux<br />
Figure 6. Hypothèses pathogéniques dans <strong>la</strong> pemphigoï<strong>de</strong> bulleuse. La théorie anticorps (à gauche) suppose <strong>la</strong><br />
fixation <strong>de</strong>s auto-anticorps sur les antigènes BP <strong>de</strong>s hémi<strong>de</strong>smosomes, entraînant une activation du complément, suivie<br />
du recrutement <strong>de</strong> cellules in f<strong>la</strong>mmatoires dont <strong>de</strong>s polynucléaires éosinophiles et <strong>de</strong>s mastocytes. La théorie cellu<strong>la</strong>ire<br />
(à droite) suppose l'activation <strong>de</strong> cellules T spécifiques d'antigènes BP, avec production <strong>de</strong> cytokines inf<strong>la</strong>mmatoires<br />
aboutissant à l'accumu<strong>la</strong>tion <strong>de</strong> cellules inf<strong>la</strong>mmatoires, en particulier polynucléaires éosinophiles. Les <strong>de</strong>ux théories<br />
ne sont pas mutuellement exclusives. L T : lymphocyte T; Eo : polynucléaire éosinophile ; Ma : mastocyte ; BPA : antigène(s)<br />
<strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong> bulleuse ; C3b C5a : fragments du complément ; Ac : anticorps anti-PB. Pour les autres<br />
abréviations, voir légen<strong>de</strong> <strong>de</strong> <strong>la</strong> figure 2.<br />
mis n ° 4 vol. 9, avril 93<br />
LD<br />
-<br />
383
384<br />
RÉFÉRENCES<br />
37. Rico MJ , Hall RP. Characterization of<br />
T cell epitopes enco<strong>de</strong>d by the 230 kD huilous<br />
pemphigoid antigen eDNA. J lnvest Dermato/<br />
1991 ; 96 : 555A.<br />
38. Rico MJ , White LDS, Bartow S,<br />
Hall RP. Detection of cross-reactive idiotypes<br />
in the serum of patients with bullous<br />
pemphigoid. J Invest Dermatol 1991 ; 96 :<br />
809-14.<br />
39. Woodley DT, Briggaman RA,<br />
O'Keefe EJ , Inman AO, Queen LL, Garnmon<br />
WR. I<strong>de</strong>ntification of the skin<br />
basement-membrane autoantigen in epi<strong>de</strong>rmolysis<br />
bullosa acquisita. N Engl J Med<br />
1984 ; 310 : 1007-13.<br />
40. Gammon WR. Epi<strong>de</strong>rmolysis bullosa<br />
acquisita : a disease of autoimmunity to type<br />
VII col<strong>la</strong>gen. J Autoimmuniry 1991 ; 4 :<br />
59-71.<br />
41. Camisa C, Sharma HM. Vesiculobullous<br />
systemic lupus erythematosus. Report<br />
of two cases and a review of the literature.<br />
j Am Acad Dermatol 1983 ; 9 : 924-32.<br />
42. Uitto J, Chung-Honet L, Christiano<br />
AM. Molecu<strong>la</strong>r biology and pathology<br />
of type VII col<strong>la</strong>gen. Exp Dermatol 1992 ; 1 :<br />
2-1 1.<br />
43. Mars<strong>de</strong>n RA. Linear IgA disease of<br />
childhood. In : Wojnarowska F, Briggaman<br />
RA, eds. Management of Blistering Diseases.<br />
Chapmann and Hall medical, 1990 :<br />
119-26.<br />
44. Wojnarowska F, Mars<strong>de</strong>n RA, Bhogal<br />
BS, B<strong>la</strong>ck MM. Chronic bullous disease<br />
of childhood, childhood cicatricial pemphigoid<br />
and linear IgA disease of adults. J Am<br />
Acad Dermatol 1988 ; 19 : 792-802.<br />
45. Prost C, Colonna De Leca A, Combemale<br />
P, Labeille B, Martin N, Cosnes A,<br />
Guil<strong>la</strong>ume JC, Venecie PY, Verret JL,<br />
Dubertret L, Touraine R. Diagnosis of<br />
adult linear IgA <strong>de</strong>rmatosis by immunoelectronmicroscopy<br />
in 16 patients with Iinear<br />
IgA <strong>de</strong>posits. J lnvest Dermatol 1989 ; 92 :<br />
39-45.<br />
46. Willsteed E, Bhogal BS, B<strong>la</strong>ck MM,<br />
McKee P, Wojnarowska F. Use of lM Nad<br />
split skin in the indirect immunofluorescence<br />
of the linear IgA bullous <strong>de</strong>rmatoses. J Cut<br />
Pathol 1990 ; 17 : 144-8.<br />
47. Zone JJ , Taylor TB, Kadunce DP,<br />
Meter LJ . I<strong>de</strong>ntification of the cutaneous<br />
basement membrane zone antigen and iso<strong>la</strong>tion<br />
of antibody in linear immunoglobulin<br />
A bullous <strong>de</strong>rmatosis. J Clin lnvest 1990 ;<br />
85 : 812-20.<br />
48. Thivolet J. A propos <strong>de</strong> <strong>la</strong> nosologie <strong>de</strong>s<br />
<strong>de</strong>rmatoses bulleuses auto-immunes. Ann<br />
Dermatol Venereol 1992 ; 119 : 391.<br />
démonstration <strong>de</strong> 1 'existence <strong>de</strong><br />
lymphocytes T spécifiques <strong>de</strong>s BP Ag<br />
chez les patients. Un premier travail<br />
a rapporté <strong>la</strong> réponse proliférative <strong>de</strong>s<br />
lymphocytes du sang périphérique <strong>de</strong><br />
trois patients sur six à <strong>de</strong>s pepti<strong>de</strong>s<br />
<strong>de</strong> synthèse 230 kDa correspondant à<br />
<strong>la</strong> région carboxy-terminale [37]. Si<br />
ce résultat se confirmait, le rôle<br />
pathogène <strong>de</strong>s lymphocytes T dans <strong>la</strong><br />
formation <strong>de</strong>s lésions cutanées serait<br />
fortement consolidé.<br />
• Les recherches actuelles dans le<br />
domaine <strong>de</strong>s pemphigoï<strong>de</strong>s bulleuses<br />
s'orientent aussi vers l'étu<strong>de</strong> <strong>de</strong> <strong>la</strong><br />
réponse anti-idiotypique [38) chez les<br />
patients, qui expliquerait <strong>la</strong> rémission<br />
spontanée <strong>de</strong>s poussées bulleuses<br />
après quelques semaines d'évolution,<br />
et qui pourrait déboucher sur une<br />
thérapeutique immunologique. Par<br />
ailleurs, <strong>de</strong>s tests sérologiques diagnostiques<br />
utilisant <strong>de</strong>s protéines BP<br />
Ag recombinantes et une technique<br />
ELISA sont en voie <strong>de</strong> développement.<br />
1 Épi<strong>de</strong>rmolyse bulleuse<br />
1 <strong>acquise</strong>-lupus<br />
érythémateux bulleux<br />
Le col<strong>la</strong>gène <strong>de</strong> type VII, constituant<br />
principal <strong>de</strong>s fibrilles d'ancrage est<br />
l'auto-antigène <strong>de</strong> l'épi<strong>de</strong>rmolyse bulleuse<br />
<strong>acquise</strong> [39). L'épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong> est une ma<strong>la</strong>die<br />
caractérisée par une séparation<br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique sous <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa et par l'existence d'anticorps<br />
anti-<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique spécifiques<br />
du col<strong>la</strong>gène <strong>de</strong> type VII<br />
[ 40]. L' épi<strong>de</strong>rmolyse bulleuse <strong>acquise</strong><br />
est hétérogène sur le p<strong>la</strong>n clinique et<br />
comprend schématiquement trois formes<br />
cliniques : ( 1) une forme chronique,<br />
proche <strong>de</strong>s épi<strong>de</strong>rmolyses bulleuses<br />
héréditaires et <strong>de</strong> <strong>la</strong> porphyrie<br />
cutanée tardive, associant une fragilité<br />
cutanée, <strong>de</strong>s bulles posttraumatiques<br />
avec <strong>de</strong>s érosions <strong>de</strong>s<br />
faces d'extension <strong>de</strong>s membres<br />
(genoux, cou<strong>de</strong>s, dos <strong>de</strong>s mains et<br />
dos <strong>de</strong>s pieds), et un aspect cicatriciel<br />
<strong>de</strong>s lésions avec grains <strong>de</strong><br />
milium ; cette forme est <strong>la</strong> forme<br />
« c<strong>la</strong>ssique ,, <strong>la</strong> première reconnue ;<br />
(2) une forme inf<strong>la</strong>mmatoire, qui<br />
peut mimer <strong>la</strong> présentation clinique<br />
<strong>de</strong>s pemphigoï<strong>de</strong>s bulleuses avec survenue<br />
<strong>de</strong> bulles spontanées sur base<br />
érythémateuse urticarienne pouvant<br />
toucher tout le tégument ; (3) une<br />
forme proche cliniquement <strong>de</strong> <strong>la</strong><br />
pemphigoï<strong>de</strong> cicatricielle et touchant<br />
surtout les muqueuses mais aussi le<br />
pôle céphalique.<br />
L'image histologique montre une<br />
bulle sous-épi<strong>de</strong>rmique. L'immunofluorescence<br />
directe met en évi<strong>de</strong>nce<br />
un dépôt d'immunoglobulines et <strong>de</strong><br />
composants du complément le long<br />
<strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique.<br />
Le diagnostic d'épi<strong>de</strong>rmolyse bulleuse<br />
<strong>acquise</strong> repose sur une <strong>de</strong>s techniques<br />
permettant d'affirmer l'autoimmunisation<br />
anti-col<strong>la</strong>gène VII et<br />
comportant : (a) <strong>la</strong> mise en évi<strong>de</strong>nce<br />
d'anticorps circu<strong>la</strong>nts se fixant sur le<br />
p<strong>la</strong>ncher <strong>de</strong> peau humaine dissociée<br />
par le NaCl lM ; (b) l'analyse <strong>de</strong> <strong>la</strong><br />
réactivité <strong>de</strong>s sérums <strong>de</strong> patients sur<br />
un extrait protéique <strong>de</strong> <strong>jonction</strong><br />
<strong>de</strong>rmo-épi<strong>de</strong>rmique permettant<br />
d'i<strong>de</strong>ntifier comme cible <strong>de</strong>s autoanticorps<br />
une molécule <strong>de</strong> 290 kDa<br />
qui correspond à <strong>la</strong> molécule intacte<br />
<strong>de</strong> col<strong>la</strong>gène <strong>de</strong> type VII (figure 7) ;<br />
(c) l'immunomicroscopie électronique<br />
directe qui montre que le dépôt<br />
d'anticorps se localise au niveau <strong>de</strong>s<br />
fibrilles d'ancrage. Les auto-anticorps<br />
lgG anti-col<strong>la</strong>gène <strong>de</strong> type VII ne<br />
sont pas spécifiques <strong>de</strong> l'épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong>. Ils ont été décrits<br />
dans le lupus érythémateux systémique<br />
avec ou sans éruption bulleuse.<br />
• Le lupus érythémateux bulleux est<br />
une forme clinique du lupus érythémateux<br />
systémique [ 41] dans <strong>la</strong>quelle<br />
les patients, en plus <strong>de</strong> l'existence <strong>de</strong>s<br />
signes cliniques du lupus érythémateux<br />
systémique et d'anticorps antinucléaires,<br />
présentent <strong>de</strong>s lésions bulleuses<br />
et <strong>de</strong>s auto-anticorps anticol<strong>la</strong>gène<br />
<strong>de</strong> type VII. L'immunopathologie<br />
du lupus bulleux est en<br />
tout point simi<strong>la</strong>ire à celle <strong>de</strong> l'épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong>. Des<br />
résultats récents suggèrent que l'autoimmunité<br />
vis-à-vis du col<strong>la</strong>gène <strong>de</strong><br />
type VII dans 1 'épi<strong>de</strong>rmolyse bulleuse<br />
<strong>acquise</strong> et le lupus érythémateux bulleux<br />
est contrôlée par les mêmes<br />
gènes au sein du complexe majeur<br />
d'histocompatibilité [40). Ces simi<strong>la</strong>rités<br />
entre les <strong>de</strong>ux affections expliquent<br />
les difficultés <strong>de</strong> c<strong>la</strong>ssement<br />
nosologique <strong>de</strong> l'épi<strong>de</strong>rmolyse bulleuse<br />
<strong>acquise</strong> et du lupus bulleux au<br />
sein <strong>de</strong>s lupus érythémateux.<br />
• Le col<strong>la</strong>gène <strong>de</strong> type VII (<strong>de</strong> poids<br />
molécu<strong>la</strong>ire le plus élevé <strong>de</strong>s col<strong>la</strong>gè-<br />
mis n ° 4 vol. 9, avril 93
nes connus : 1 million <strong>de</strong> daltons), est<br />
synthétisé par les kératinocytes et les<br />
fibrob<strong>la</strong>stes <strong>de</strong>rmiques. Il est constitué<br />
<strong>de</strong> trois chaînes i<strong>de</strong>ntiques al<br />
(VII), qui s'assemblent pour former<br />
une triple hélice f<strong>la</strong>nquée <strong>de</strong> part et<br />
d'autre par <strong>de</strong>s domaines globu<strong>la</strong>ires<br />
carboxy- et amino-terminaux (revues<br />
dans (3) et (42]). Le domaine globu<strong>la</strong>ire<br />
amino-terminal est <strong>la</strong> région <strong>la</strong><br />
plus antigénique <strong>de</strong> <strong>la</strong> molécule,<br />
puisqu'il est <strong>la</strong> cible <strong>de</strong>s autoanticorps<br />
circu<strong>la</strong>nts anti-col<strong>la</strong>gène VII<br />
dans l'épi<strong>de</strong>rmolyse bulleuse <strong>acquise</strong><br />
et que pratiquement tous les anticorps<br />
monoclonaux anti-col<strong>la</strong>gène VII<br />
actuellement disponibles sont dirigés<br />
contre ce domaine et ne reconnaissent<br />
pas <strong>la</strong> triple hélice. Deux monomères<br />
<strong>de</strong> col<strong>la</strong>gène VII s'agrègent entre eux<br />
<strong>de</strong> façon antiparallèle, pour former<br />
une structure d'environ 1 micromètre<br />
<strong>de</strong> longueur. Plusieurs dimères<br />
s'assemblent <strong>la</strong>téralement pour former<br />
les fibrilles d'ancrage, qui sont donc<br />
pratiquement constituées <strong>de</strong> col<strong>la</strong>gène<br />
<strong>de</strong> type VII pur. Les fibrilles<br />
d'ancrage sont amarrées à une extrémité<br />
à <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa et à l'autre<br />
extrémité aux p<strong>la</strong>ques d'ancrage, qui<br />
sont <strong>de</strong>s structures du <strong>de</strong>rme papil<strong>la</strong>ire<br />
contenant du col<strong>la</strong>gène <strong>de</strong><br />
type IV. Elles forment ainsi un<br />
réseau très serré qui arrime <strong>la</strong> <strong>la</strong>mina<br />
<strong>de</strong>nsa au <strong>de</strong>rme superficiel. Ce rôle<br />
fondamental dans l'intégrité <strong>de</strong> <strong>la</strong><br />
peau est démontré indirectement par<br />
l'absence ou <strong>la</strong> diminution du nombre<br />
<strong>de</strong>s fibrilles d'ancrage dans certaines<br />
épi<strong>de</strong>rmolyses bulleuses héréditaires,<br />
caractérisées par une fragilité<br />
cutanée avec décollement bulleux<br />
sous-épi<strong>de</strong>rmique. Dans l'épi<strong>de</strong>rmolyse<br />
bulleuse <strong>acquise</strong>, les autoanticorps<br />
anti-col<strong>la</strong>gène <strong>de</strong> type VII<br />
induiraient une réaction inf<strong>la</strong>mmatoire<br />
secondaire à <strong>la</strong> production <strong>de</strong><br />
dérivés du complément chimiotactiques,<br />
en particulier le C5. Si le rôle<br />
<strong>de</strong>s anticorps dans <strong>la</strong> pathogénie <strong>de</strong><br />
1 'épi<strong>de</strong>rmolyse bulleuse <strong>acquise</strong><br />
inf<strong>la</strong>mmatoire avec présence d'anticorps<br />
fixés au niveau <strong>de</strong> <strong>la</strong> peau<br />
lésionnelle et capables d'activer le<br />
complément paraît probable, il reste<br />
hypothétique dans les formes chroniques<br />
c<strong>la</strong>ssiques qui évoluent sur <strong>de</strong>s<br />
années et dans les cas où les anticorps<br />
ne fixent pas le complément.<br />
Dans ces cas, l'immunité à médiation<br />
cellu<strong>la</strong>ire ou <strong>de</strong>s propriétés fonctionnelles<br />
<strong>de</strong>s auto-anticorps autres que<br />
l'activation du complément pourraient<br />
intervenir.<br />
Le clonage du gène codant pour le<br />
col<strong>la</strong>gène <strong>de</strong> type VII et l'analyse <strong>de</strong><br />
<strong>la</strong> séquence nucléotidique <strong>de</strong> <strong>la</strong><br />
chaîne pro(al) VII ont montré<br />
d'intéressantes caractéristiques [ 42).<br />
Le grand domaine globu<strong>la</strong>ire Nterminal<br />
adopterait une conformation<br />
{3 plissée. Trois séquences tripeptidiques<br />
RGD et <strong>de</strong>ux séquences DGR<br />
ont été i<strong>de</strong>ntifiées. Celles-ci représenteraient<br />
autant <strong>de</strong> sites <strong>de</strong> liaison cellu<strong>la</strong>ire<br />
<strong>de</strong> <strong>la</strong> molécule <strong>de</strong> col<strong>la</strong>gène.<br />
Le segment 5' contient aussi <strong>de</strong>s<br />
régions présentant <strong>de</strong>s homologies <strong>de</strong><br />
séquence avec <strong>la</strong> fibronectine.<br />
1 Dermatoses<br />
à /gA linéaire (DA LJ<br />
Le terme « <strong>de</strong>rmatoses à lgA<br />
linéaire '' désigne un groupe d'affections<br />
hétérogènes sur le p<strong>la</strong>n clinique<br />
et immunopathologique, dont <strong>la</strong><br />
nosologie précise au sein <strong>de</strong>s <strong>de</strong>rmatoses<br />
bulleuses auto-immunes reste à<br />
preciser. Les <strong>de</strong>rmatoses à IgA<br />
linéaire sont <strong>de</strong>s ma<strong>la</strong>dies bulleuses<br />
sous-épi<strong>de</strong>rmiques <strong>de</strong> l'enfant et <strong>de</strong><br />
l'adulte, dans lesquelles on retrouve<br />
en immunofluorescence directe un<br />
dépôt d'lgA à <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmoépi<strong>de</strong>rmique.<br />
Figure 7. Épi<strong>de</strong>rmolyse bulleuse <strong>acquise</strong> : immunopathologie. (A}. immunofluorescence indirecte sur peau humaine<br />
normale dissociée au NaCI 1 M. Les anticorps circu<strong>la</strong>nts du patient se fixent sur le côté <strong>de</strong>rmique <strong>de</strong> <strong>la</strong> membrane basale.<br />
(8}. Analyse par <strong>la</strong> technique d'immuno-empreinte <strong>de</strong> <strong>la</strong> réactivité du sérum du patient sur un extrait <strong>de</strong>rmique (0) ;<br />
le sérum reconnaÎt le col<strong>la</strong>gène <strong>de</strong> type VI/ <strong>de</strong> 290 kDa. En comparaison, l'antigène BP <strong>de</strong> 230 kDa reconnu par le<br />
sérum d'un patient porteur <strong>de</strong> pemphigoi<strong>de</strong> bulleuse sur un extrait <strong>de</strong> cellules épi<strong>de</strong>rmiques en culture (E). --mis<br />
n ° 4 vol. 9, avril 93 385<br />
230<br />
E D
386<br />
Chez l'enfant, c'est <strong>la</strong> plus fréquente<br />
<strong>de</strong>s ma<strong>la</strong>dies auto-immunes bulleuses<br />
sous-épi<strong>de</strong>rmiques [ 43]. Elle débute<br />
avant l'âge <strong>de</strong> 5 ans <strong>de</strong> façon brutale<br />
par 1' apparition <strong>de</strong> bulles tendues disposées<br />
en rosettes dans les régions<br />
péri-buccale et génitale. La forme<br />
observée chez l'adulte peut survenir<br />
à tout âge [44].<br />
L'aspect clinique est variable. Certains<br />
tableaux sont proches d'une<br />
<strong>de</strong>rmatite herpétiforme avec survenue<br />
<strong>de</strong> vésiculo-bulles sur les fesses et<br />
dans les zones d'extension <strong>de</strong>s membres.<br />
Le plus souvent, <strong>la</strong> présentation<br />
clinique est celle d'une pemphigoï<strong>de</strong><br />
bulleuse avec atteinte <strong>de</strong>s faces <strong>de</strong><br />
flexion <strong>de</strong>s membres et du tronc.<br />
Enfin, l'atteinte muqueuse buccale et<br />
ocu<strong>la</strong>ire fréquente peut être au premier<br />
p<strong>la</strong>n et suggérer un diagnostic<br />
initial <strong>de</strong> pemphigoï<strong>de</strong> cicatricielle.<br />
Le traitement repose sur <strong>la</strong> dapsone<br />
(Disulone ® ). Chez l'enfant, comme<br />
chez l'adulte, le diagnostic repose sur<br />
l'immunopathologie, qui retrouve un<br />
dépôt d'IgA exclusif ou prédominant.<br />
A l'hétérogénéité <strong>de</strong>s tableaux cliniques<br />
correspond une variabilité du<br />
niveau <strong>de</strong> clivage <strong>de</strong> <strong>la</strong> <strong>jonction</strong><br />
<strong>de</strong>rme-épi<strong>de</strong>rmique et <strong>de</strong> l'antigènecible<br />
<strong>de</strong>s auto-anticorps. Les anticorps<br />
<strong>de</strong> type lgA peuvent être retrouvés<br />
dans <strong>la</strong> <strong>la</strong>mina lucida (site du dépôt<br />
<strong>de</strong>s anticorps IgG dans <strong>la</strong> pemphigoï<strong>de</strong><br />
bulleuse), sous <strong>la</strong> <strong>la</strong>mina <strong>de</strong>nsa<br />
(site du dépôt <strong>de</strong>s anticorps IgG dans<br />
l'épi<strong>de</strong>rmolyse bulleuse <strong>acquise</strong>) ou<br />
donner un marquage combiné <strong>de</strong>s<br />
<strong>de</strong>ux zones [ 45]. Les antigènes cibles<br />
<strong>de</strong>s auto-anticorps ne sont pas connus,<br />
en particulier à cause du taux<br />
faible voire nul, dans cette affection,<br />
d'anticorps circu<strong>la</strong>nts an ti-<strong>jonction</strong><br />
<strong>de</strong>rme-épi<strong>de</strong>rmique susceptibles d'être<br />
utilisés pour <strong>la</strong> caractérisation biochimique<br />
<strong>de</strong> l'antigène par immunoprécipitation.<br />
Pour certains il s'agit d'un<br />
antigène épi<strong>de</strong>rmique (ou encore <strong>de</strong>rmique)<br />
spécifique <strong>de</strong> <strong>la</strong> ma<strong>la</strong>die [ 46,<br />
47]. D'autres considèrent que les <strong>de</strong>rmatoses<br />
à IgA linéaire ne sont en fait<br />
que <strong>de</strong>s variants isotypiques <strong>de</strong> <strong>de</strong>rmatoses<br />
à IgG plus c<strong>la</strong>ssiques. Ainsi,<br />
il y aurait <strong>de</strong>s pemphigoï<strong>de</strong>s bulleuses<br />
à IgA (dépôt d'anticorps dans <strong>la</strong><br />
<strong>la</strong>mina lucida) et <strong>de</strong>s épi<strong>de</strong>rmolyses<br />
bulleuses <strong>acquise</strong>s à IgA (dépôt<br />
d'anticorps au niveau <strong>de</strong> <strong>la</strong> sub<strong>la</strong>mina<br />
<strong>de</strong>nsa). Le fait qu'un patient produise<br />
<strong>de</strong>s lgA, et non pas <strong>de</strong>s IgG spécifi-<br />
ques d'un même antigène, dépendrait<br />
<strong>de</strong> facteurs immunitaires propres, et<br />
en particulier <strong>de</strong> <strong>la</strong> production <strong>de</strong><br />
cytokines capables d'induire <strong>la</strong> commutation<br />
isotypique IgG (IL-10) ou<br />
IgA (IL-5). Les étu<strong>de</strong>s en cours<br />
<strong>de</strong>vraient permettre d'atteindre un<br />
consensus au cours <strong>de</strong>s prochaines<br />
années.<br />
1 Conclusion<br />
Les progrès réalisés ces dix <strong>de</strong>rnières<br />
années ont permis <strong>de</strong> connaître les<br />
antigènes cibles <strong>de</strong> <strong>la</strong> réponse inf<strong>la</strong>mmatoire<br />
dans les <strong>de</strong>rmatoses bulleuses<br />
auto-immunes, <strong>de</strong> cloner les gènes<br />
correspondants et <strong>de</strong> commencer<br />
à appréhen<strong>de</strong>r l'organisation supramolécu<strong>la</strong>ire<br />
<strong>de</strong> <strong>la</strong> <strong>jonction</strong> <strong>de</strong>rmeépi<strong>de</strong>rmique.<br />
Le diagnostic sérologique<br />
<strong>de</strong> ces affections ainsi que leur<br />
nosologie se précisent [ 48].<br />
Les étu<strong>de</strong>s en cours visent à apprécier<br />
les mécanismes immunologiques<br />
aboutissant à <strong>la</strong> formation <strong>de</strong>s lésions.<br />
La meilleure compréhension <strong>de</strong> <strong>la</strong><br />
pathogénie <strong>de</strong> <strong>la</strong> pemphigoï<strong>de</strong> bulleuse,<br />
<strong>de</strong> l'épi<strong>de</strong>rmolyse bulleuse<br />
<strong>acquise</strong> et <strong>de</strong>s <strong>de</strong>rmatoses à IgA<br />
linéaire est en effet indispensable au<br />
développement <strong>de</strong> nouveaux traitements<br />
immunologiques. L'avenir<br />
<strong>de</strong>vrait permettre le développement<br />
d'une immune-intervention spécifique<br />
d'antigène •<br />
Remerciements<br />
Nous remercions, pour leur ai<strong>de</strong> dans <strong>la</strong><br />
réalisation <strong>de</strong> ce travail, nos collègues <strong>de</strong><br />
l'<strong>Inserm</strong> U. 34-6 et <strong>de</strong> <strong>la</strong> clinique <strong>de</strong>rma<br />
tologique : Martine Gaucherand, Pascale<br />
Roche, Jean Kanitakis (crédit pour <strong>la</strong><br />
figure 1), Marie-Jeanne Staquet et Yves<br />
Sarret.<br />
Nos remerciements vont aussi - pour<br />
leur ai<strong>de</strong> dans notre recherche sur les<br />
ma<strong>la</strong>dies auto-immunes bulleuses <strong>de</strong> <strong>la</strong><br />
<strong>jonction</strong> <strong>de</strong>rmo-épi<strong>de</strong>rmique - à Jacques<br />
Banchereau, Françoise Rousset et Domi<br />
nique B<strong>la</strong>nchard (<strong>la</strong>boratoires Schering<br />
Plough, Dardilly) ; Jean-Pierre Magaud<br />
et Jean-Pierre Rouault (<strong>la</strong>boratoire <strong>de</strong><br />
biologie molécu<strong>la</strong>ire, hématologie , pavil<br />
lons E bis, hôpital E.-Herriot, Lyon) ;<br />
Michel Jolivet et G<strong>la</strong>ucia Bacca<strong>la</strong> (<strong>la</strong>boratoires<br />
BioMérieux, Lyon) et Marek<br />
Haftek (<strong>Inserm</strong> U. 34-6, Lyon).<br />
Summary<br />
Recent advances in acquired<br />
diseases affecting the <strong>de</strong>rmoepi<strong>de</strong>rmal<br />
junction<br />
The <strong>de</strong>rmoepi<strong>de</strong>rmal junction<br />
(DEJ) is a supramolecu<strong>la</strong>r structure<br />
between the epi<strong>de</strong>rmis and<br />
the <strong>de</strong>rmis. Its importance in the<br />
integrity of the skin is evi<strong>de</strong>nced<br />
by the numerous inherited and<br />
acquired diseases which affect the<br />
DEJ and lead to subepi<strong>de</strong>rmal<br />
bullous disor<strong>de</strong>rs. Consi<strong>de</strong>rable<br />
progress has recenùy been ma<strong>de</strong><br />
in the characterization of the<br />
molecules which constitute the<br />
basement membrane zone and of<br />
receptor/ligand interactions at the<br />
DEJ. Sorne molecules appear critical<br />
for the adhesion of the epi<strong>de</strong>rmis<br />
to the <strong>de</strong>rmis since a genetic<br />
alteration in their structure or<br />
an autoimmune reaction directed<br />
to these molecules ultimately lead<br />
to <strong>de</strong>rmal epi<strong>de</strong>rmal split and bul<strong>la</strong>e<br />
formation. In respect to acquired<br />
bullous disor<strong>de</strong>rs, three molecules<br />
of the DEJ (bullous pemphigoid<br />
antigens (BP Ag 1 and<br />
BP Ag 2), col<strong>la</strong>gen type VII and<br />
epiligrin/niceine) have been shown<br />
to be antigenic and are the targets<br />
of patients autoantibodies in three<br />
distinct diseases affecting the DEJ,<br />
namely bullous pemphigoid, epi<strong>de</strong>rmolysis<br />
bullosa acquisita and<br />
cicatricial pemphigoid. The better<br />
un<strong>de</strong>rstanding in the molecu<strong>la</strong>r<br />
basis of acquired blistering skin<br />
diseases has already allowed the<br />
improvement of the diagnostic<br />
procedures and new insights in the<br />
nosology of this group of <strong>de</strong>rmatoses.<br />
TIRÉS A PART<br />
J.-F. Nico<strong>la</strong>s.<br />
mis n ° 4 vol. 9, avril 93