TP2 - Dosage Potentiométrique
TP2 - Dosage Potentiométrique
TP2 - Dosage Potentiométrique
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
TSI1 Série 8 CM – <strong>TP2</strong> : Redox 2 – <strong>Dosage</strong> potentiométrique<br />
Série 8 CM – <strong>TP2</strong> : Redox 2 – <strong>Dosage</strong> Potentiométrique<br />
Objectifs :<br />
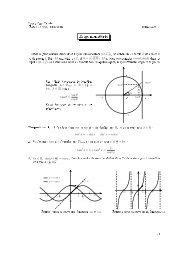
Partie I : Principe<br />
→ Réaliser un dosage – suivi par potentiométrie (potentiel redox)<br />
→ Découverte des électrodes utilisées en électrochimie<br />
Rappel : Qu’est qu’un dosage ?<br />
Objectif :<br />
<strong>Dosage</strong> acido-basique ?<br />
Autre dosage ?<br />
Elément titrant<br />
Bases<br />
HO −<br />
On cherche à mesurer la concentration C0 d’une solution<br />
2 + 2 −<br />
aqueuse contenant du Fer (II) : FeSO = Fe + SO<br />
4 4<br />
Le fer (II) n’appartient à aucun couple acidobasique,<br />
ni fort, ni faible. Est-il possible de procéder<br />
à un dosage pH-métrique ?<br />
Par contre, le fer (II) appartient à un couple oxydantréducteur<br />
: F e F e +<br />
3 + 2<br />
, de potentiel standard<br />
0<br />
E<br />
2<br />
= 0, 77V<br />
. Si on réfléchit de manière analogue aux<br />
acides/bases, avec quoi pourrait-on doser le Fe 2+ ?<br />
Comparons les échelles pKA / Potentiel :<br />
pKA<br />
H O<br />
AH<br />
A − 2<br />
Acides<br />
Acide à doser<br />
MnO −<br />
4<br />
E<br />
MnO<br />
2( s )<br />
2( s )<br />
3<br />
Fe + 2<br />
Fe +<br />
Alors ? Avec quelle espèce doseriez-vous le Fe 2+ ?<br />
Ecrivez la réaction correspondante.<br />
Ox<br />
1,69V<br />
MnO − 2<br />
4<br />
Mn + 1,51V<br />
2<br />
MnO Mn + 1,23V<br />
2<br />
CrO −<br />
4<br />
2<br />
Fe +<br />
Cr ( OH ) 3<br />
Fe<br />
( s )<br />
0,77V<br />
-0,11V<br />
-0,44V<br />
Equivalence ? Qu’est l’équivalence, et quelle relation peut-on y écrire ?<br />
Red<br />
Réducteur<br />
à doser<br />
Réaction totale ?<br />
Et le Fer solide ?<br />
Partie II : Les électrodes<br />
Problématique :<br />
Cette relation reste-t-elle valable quel que soit le couple<br />
choisi ? Ou y a-t-il une condition particulière ?<br />
2<br />
Que penser du couple Fe<br />
Comment suivre l’évolution d’un tel dosage ?<br />
+<br />
Fe , va-t-il se former du Fer(s)<br />
Quelle grandeur peut refléter les concentrations en oxydant / réducteur ?<br />
Expliquons les différentes électrodes disponibles au laboratoire : (voir annexe)<br />
Electrode de<br />
ère espèce de Fer<br />
= ½ Pile<br />
1 ère<br />
Fe<br />
2<br />
Fe +<br />
Première manipulation<br />
:<br />
On dispose d’une pile au Cuivre dont on connait le potentiel standard<br />
E<br />
0<br />
Cu<br />
2+ =<br />
Cu<br />
0,345V<br />
Mesurer le potentiel de l’électrode de référence que vous avez sur vos tables<br />
Vérifier cette valeur avec l’ESH disponible sur le bureau<br />
Préparation du dosage :<br />
Quelles électrodes va-t-on utiliser pour suivre le dosage ?<br />
Proposer un schéma du montage.<br />
Electrode de<br />
nde espèce : ESF<br />
2 nde<br />
Fil élec<br />
Hg(l)<br />
Hg2SO4<br />
Electrolyte<br />
Paroi<br />
poreuse<br />
Electrode de<br />
3 ème espèce<br />
(Fil de Platine)<br />
Pt<br />
3+ 2+<br />
Fe Fe<br />
HECKEL - 1/2
TSI1 Série 8 CM – <strong>TP2</strong> : Redox 2 – <strong>Dosage</strong> potentiométrique<br />
Partie III : Réalisation du dosage<br />
On va donc doser la solution de<br />
FeSO = Fe + SO , de<br />
2+ 2−<br />
4 4<br />
concentration C0 inconnue, à l’aide d’une solution de permanganate de potassium<br />
+ −<br />
−2 −1<br />
KMnO<br />
4<br />
= K + MnO , de concentration connue<br />
4<br />
C = 2.10 mol . L . Le<br />
1<br />
pH sera maintenu constamment proche de 0 (ajout d’acide), pour éviter que<br />
n’interviennent d’autres types de réactions parasites.<br />
Réflexion préliminaire :<br />
Effectuer l’inventaire des espèces présentes en<br />
début de dosage dans le bécher et dans la<br />
burette graduée.<br />
D’après l’échelle de pKA tracée au recto, prévoir<br />
la réaction du dosage (attention aux<br />
coefficients stœchiométriques).<br />
Manipulation :<br />
Réaliser le dosage en notant :<br />
Le volume de solution ajoutée<br />
Le potentiel à chaque instant<br />
La couleur de la solution<br />
Remarque : les ions MnO − 2<br />
sont violets, Mn + presque transparents,<br />
4<br />
3<br />
légèrement rosés, Fe + 2<br />
couleur rouille et Fe + de couleur verte.<br />
Tracer l’évolution du potentiel en fonction du volume ajouté<br />
Trouver l’équivalence, et en déduire la concentration de fer initial<br />
(attention aux coefficients stœchiométriques)<br />
E solution<br />
?<br />
V ajouté<br />
?<br />
?<br />
Justification Théorique :<br />
Construire un tableau d’avancement de la réaction, tracer alors l’évolution<br />
des concentrations de chacun des ions au cours du dosage<br />
n 2<br />
Fe +<br />
V<br />
n −<br />
MnO 4<br />
n 3<br />
Fe +<br />
n 2+<br />
Mn<br />
En déduire le potentiel de la solution à l’équivalence (exprimer les<br />
potentiels des deux couples, et simplifier en additionnant)<br />
Quel est le potentiel de la solution à la demi équivalence : V = VE / 2 ?<br />
Quel est le potentiel de la solution à la double équivalence : V = 2 VE ?<br />
Pour V < VE, les ions Fe 2+ sont en excès. Exprimer le potentiel du couple<br />
Fe<br />
Fe<br />
3+ 2+<br />
en fonction des volumes ajouté, initial et des<br />
concentrations des ions en solution<br />
En faire de même lorsque V > VE, mais en exprimant le potentiel de l’autre<br />
− 2<br />
couple : MnO Mn<br />
+ .<br />
Résumé des données :<br />
2<br />
Couples mis en jeu - Fe<br />
Simplification<br />
0 V<br />
1<br />
V<br />
EQ<br />
EQ<br />
2<br />
4<br />
Fe<br />
+ , 0<br />
3 2<br />
- + + , 0<br />
Fe<br />
Fe<br />
E<br />
1<br />
= − 0, 44V<br />
E<br />
2<br />
= 0, 77V<br />
− 2<br />
- MnO<br />
4<br />
Mn + 0<br />
, E<br />
RT ln 10<br />
F<br />
3<br />
= 1, 51V<br />
V<br />
2EQ<br />
( )<br />
= 0,06V<br />
pour T = 298K ( 25°<br />
C )<br />
V<br />
V<br />
V<br />
HECKEL - 2/2