You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
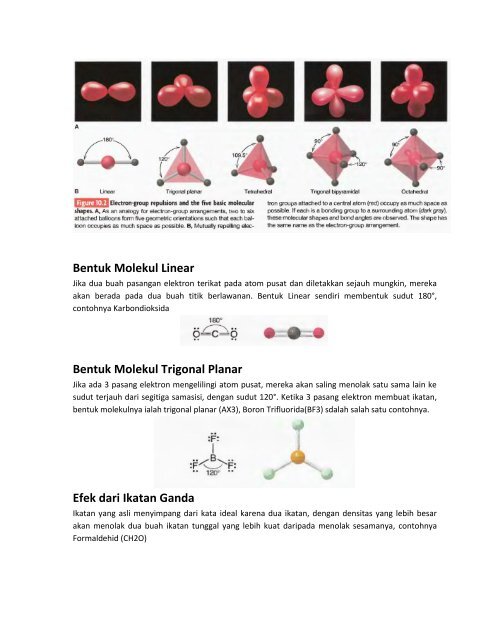
<strong>Bentuk</strong> <strong>Molekul</strong> Linear<br />
Jika dua buah pasangan elektron terikat pada atom pusat <strong>dan</strong> diletakkan sejauh mungkin, mereka<br />
akan berada pada dua buah titik berlawanan. <strong>Bentuk</strong> Linear sendiri membentuk sudut 180°,<br />
contohnya Karbondioksida<br />
<strong>Bentuk</strong> <strong>Molekul</strong> Trigonal Planar<br />
Jika ada 3 pasang elektron mengelilingi atom pusat, mereka akan saling menolak satu sama lain ke<br />
sudut terjauh dari segitiga samasisi, dengan sudut 120°. Ketika 3 pasang elektron membuat ikatan,<br />
bentuk molekulnya ialah trigonal planar (AX3), Boron Trifluorida(BF3) sdalah salah satu contohnya.<br />
Efek dari Ikatan Ganda<br />
Ikatan yang asli menyimpang dari kata ideal karena dua ikatan, dengan densitas yang lebih besar<br />
akan menolak dua buah ikatan tunggal yang lebih kuat daripada menolak sesamanya, contohnya<br />
Formaldehid (CH2O)