Hoofdstuk 2 DE BRANDSTOFFEN Technologie II- 1 - 1)INLEIDING a ...
Hoofdstuk 2 DE BRANDSTOFFEN Technologie II- 1 - 1)INLEIDING a ...
Hoofdstuk 2 DE BRANDSTOFFEN Technologie II- 1 - 1)INLEIDING a ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
1)<strong>INLEIDING</strong><br />
a)Het brandbare gasmengsel<br />
0 %<br />
Te weinig<br />
brandstof<br />
brandstof<br />
LEL<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
warmte<br />
Brandbaar mengsel<br />
brandstof<br />
zuurstof<br />
<strong>Technologie</strong> <strong>II</strong>- 1 -<br />
UEL<br />
Te weinig<br />
zuurstof<br />
100 %<br />
100 % zuurstof<br />
0 %<br />
De branddriehoek<br />
stelt dat er naast<br />
energie (warmte)<br />
ook zuurstof nodig<br />
is voordat de<br />
brandstof kan<br />
branden.<br />
Het brandstof –<br />
lucht mengsel is<br />
slechts brandbaar<br />
tussen twee uiterste<br />
grenzen. Buiten<br />
deze grenzen is er<br />
ofwel te weinig<br />
zuurstof ofwel te<br />
weinig brandstof.<br />
UEL: Upper Explosion Limit<br />
LEL: Lower Explosion Limit<br />
De dampspanning is dus een belangrijk gegeven voor de brandveiligheid of studie van<br />
ontbranding.<br />
De dampspanning en de partiële druk:<br />
In een gasballon wordt de druk geleverd door de gasmoleculen die tegen de wand botsen. Elk<br />
gas levert zijn bijdrage, de druk veroorzaakt door een afzonderlijk gas is de partiële druk pi<br />
van dit gas. De partiële druk is dus een maat voor de hoeveelheid moleculen aanwezig in de<br />
gasfase van deze stof. De dampspanning is de partiële druk gemeten in een aangepast apparaat<br />
en onder genormaliseerde omstandigheden.<br />
De wet van Dalton voor ideale gassen: p = ∑ pi<br />
De totale druk is dus de som van de partiële druk van de lucht plus de partiële druk van de<br />
brandstof.<br />
Bijgevolg moet de dampspanning van de brandstof hoog genoeg zijn om tot een brandbaar<br />
mengsel te komen.<br />
Opmerking: Tegenwoordig spreekt men ook van de brandvijfhoek waarbij men dan rekening<br />
houdt met twee extra factoren die een verbranding beïnvloeden namelijk aanwezigheid van<br />
katalysator en vorm van de brandstof.
)De chemisch reactie<br />
De exotherme reacties<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Bij chemische reacties wordt er energie uitgewisseld. De energie-inhoud van de moleculen<br />
voor en na de reacties is verschillend. Bij de exotherme reacties wordt er energie afgestaan bij<br />
de endotherme reacties wordt er energie opgenomen door de reagerende moleculen.<br />
Som energie-inhoud<br />
van de moleculen<br />
Voor de reactie<br />
Na de reactie<br />
Afgestane<br />
energie<br />
Exotherme reactie<br />
De verbranding is een exotherme reactie:<br />
CH4 + 2 O2 → CO2 + 2 H2O ∆H = -890 kJ/mol (H2 – H1 < 0)<br />
tijd<br />
De activeringsenergie: (evenredig met exp(-Ea/RT)<br />
Bij een chemische reactie moeten er verbindingen gebroken worden om er nieuwe te vormen.<br />
Hiervoor is energie nodig, de activeringsenergie. Eenmaal de reactie opgang gebracht, komt<br />
er energie vrij (bij de exotherme reactie). Bij de verbranding is deze vrijgekomen energie<br />
voldoende om de activeringsenergie te leveren voor de volgende moleculen. De reactie houdt<br />
zich zelf in stand.<br />
Bij de benzinemotor wordt de activeringsenergie geleverd door de vonk.<br />
Invloed van de druk en de temperatuur op de activeringsenergie:<br />
Opdat twee moleculen met elkaar zouden reageren, moeten ze eerst botsen. Hoe meer kans op<br />
botsingen hoe sneller de reactie verloopt. De reactie zal dus sneller verlopen en de<br />
activeringsenergie zal dalen als de temperatuur stijgt (meer kans op botsingen omdat de<br />
kinetische energie van de moleculen stijgt) en / of als de druk stijgt (moleculen dichter bij<br />
elkaar).<br />
<strong>Technologie</strong> <strong>II</strong>- 2 -<br />
Som energie-inhoud<br />
van de moleculen<br />
na<br />
voor<br />
Endotherme reactie<br />
Opgenomen<br />
energie<br />
tijd
c)Zelfontsteking versus verbranding<br />
De zelfontsteking<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Bij hoge druk zal de temperatuur voldoende zijn om de reactie op gang te brengen<br />
(activeringsenergie daalt bij drukverhoging). Dit is de zelfontsteking. Alle moleculen reageren<br />
zo goed als tegelijkertijd. Deze reactie is dus explosief en gaat gepaard met een plotse<br />
drukopbouw in de motor. De motor is ondervindt gecontroleerde drukstoten.<br />
Bij de dieselmotor wordt de activeringsenergie geleverd door de zelfontsteking van de eerste<br />
ingespoten brandstof.<br />
De verbranding<br />
Bij de verbranding is er externe activeringsenergie nodig. Bij de benzine motor wordt deze<br />
externe activeringsenergie geleverd door de vonk. De vrijgekomen energie van de verbrande<br />
brandstof dient op zijn beurt om de overige brandstof te doen branden. De verbranding is een<br />
véél trager verlopende reactie dan de zelfontsteking.<br />
vlamfront<br />
Bij de motoren, zowel de benzine als de dieselmotoren, wensen we steeds een verbranding te<br />
bekomen. De piston wordt dan gelijkmatig teruggeduwd gedurende de expansieslag.<br />
Drukstoten (kloppen, detoneren, pingelen een lichte vorm van kloppen) als gevolg van de<br />
ongewenste zelfontsteking moeten worden vermeden. De piston wordt dan teruggeslingerd<br />
(weggeslagen i.p.v. weggeduwd) en wordt beschadigd.<br />
<strong>Technologie</strong> <strong>II</strong>- 3 -<br />
Snelheid vlamfront:<br />
- verbranding: 1 tot 10 m/sec<br />
- zelfontsteking: 1000 m/sec<br />
( snelheid van het geluid)
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
2)HET VERBRAN<strong>DE</strong>N BIJ VERBRANDINGSMOTOREN<br />
a)De verbranding bij de benzinemotor:<br />
• Principe<br />
Bij de benzinemotor wordt het mengsel extern ontstoken om tot ontbranding te komen. De<br />
vonk leidt de verbranding in. Bij de benzine motor gebeurt deze verbranding snel, er is een<br />
snel vlamfront. De benzinemotor wordt een explosiemotor genoemd.<br />
De temperatuur en druk kunnen echter zo hoog oplopen dat de brandstof tussen het vlamfront<br />
en de piston tot zelfontsteking komt (explosie). De daardoor plotseling vrijgekomen energie<br />
veroorzaakt een hoge drukstoot.Als dit gebeurt gebeurt de verbranding ongecontroleerd en zal<br />
de piston tegen het vlamfront geduwd worden wat tot schede van de motor kan leiden. De<br />
motor wordt hierdoor mechanisch en thermisch zwaar belast. De zuiger wordt als het ware<br />
weggeslagen in plaats van weggeduwd.<br />
vlamfront Zelfontsteking<br />
Opmerkingen:<br />
- Door het toevoegen van anti-klop “dopes” of organische loodverbindingen wordt de<br />
klopvastheid verbeterd.<br />
verbranding<br />
• De verbranding in de benzinemotor gebeurt na volledige injectie. Na deze injectie wordt<br />
het mengsel ontstoken.<br />
<strong>Technologie</strong> <strong>II</strong>- 4 -
Het octaangetal<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
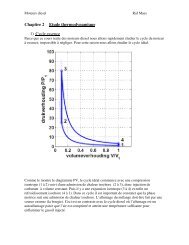
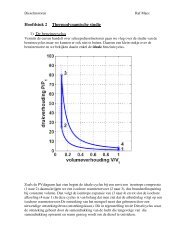
Bij de bepaling van het octaan getal van een benzine is een specifieke compressieverhouding<br />
belangrijk: deze waarbij zelfontsteking plaats grijpt bij het bovenste dode punt van de zuigerslag.<br />
Een bepaalde koolwaterstof nl. Iso-octaan (C8H18) in zuivere toestand gebruikt zal de motor bij<br />
de gebruikelijke compressies zeker niet doen kloppen. Men noemt bij definitie deze brandstof<br />
"100 octaan benzine". Normaal heptaan (C7 H16) daarentegen klopt bij een veel lagere compressie.<br />
Men noemt dit "nul octaan benzine". Men kan dus een mengsel maken van deze twee<br />
koolwaterstoffen dat dezelfde klopkarakteristieken zal hebben als een te onderzoeken willekeurige<br />
benzine.<br />
Het octaan gehalte in de benzine aan de pomp is het percentage iso-octaan in het<br />
vergelijkingsmengsel dat net klopt bij het bereiken van het bovenste dode punt bij dezelfde<br />
compressieverhouding.<br />
Het bepalen van het octaangetal<br />
Men gebruikt een testmotor waarvan de compressie regelbaar is. De benzine waarvan het<br />
octaangetal moet bepaald worden wordt in de motor gelaten. De compressie wordt geleidelijk<br />
verhoogd. Op zeker ogenblik zal de motor op het bovenste dode punt kloppen. Men noteert deze<br />
compressie. Vervolgens bereidt men twee verschillende mengsels iso-octaan en normaal<br />
heptaan, bijvoorbeeld één met 88% iso-octaan en één met 96% iso-octaan.<br />
Men laat de motor achtereenvolgens met die mengsels lopen en men registreert wanneer de<br />
motor respectievelijk juist klopt.<br />
Men zet de waarden uit in grafiek en men verbindt de twee punten. Vanaf deze rechte kan men<br />
het octaangetal van de te onderzoeken benzine bepalen vermits men de "klop" kompressie kent.<br />
<strong>Technologie</strong> <strong>II</strong>- 5 -
• Antiklopmiddelen<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Product dat, in zeer kleine hoeveelheden aan de brandstoffen voor motoren met vonkontsteking<br />
toegevoegd,er de klopvastheid van verbetert. In de praktijk worden organische<br />
metaalverbindingen als antiklopmiddel gebruikt, voornamelijk tetraëthyllood of tetramethyllood,<br />
samen met halogeenderivaten die na verbranding het verwijderen van lood vergemakkelijken.<br />
Omwille van de giftigheid wil men geleidelijk van lood afstappen. Daarom worden er andere<br />
octaanverhogers gebruikt “dopes” zoals: methanol (CH3OH), ethanol (C2H5OH), TBA<br />
(Tertiary butyl alcohol), MTBE (Methyl tertiary butyl ether).<br />
Opmerking:De RON (research octane number) is het octaangetal voor een testmotor met een lager toerental. De<br />
MON (motor octane number) is het octaangetal voor een testmotor met hoger toerental. De Anti knock index AKI is<br />
Amerikaans en is het gemiddelde van de RON en de MON. AKI wordt soms ook het Road Octane number (RdON)<br />
genoemd.<br />
• De dampspanning (RVP)<br />
Naast het octaangetal is de RVP ook belangrijk voor de verbranding van benzine.<br />
De dampspanning moet hoog genoeg zijn om een koude start mogelijk te maken: immers het gas<br />
moet voor +- 10% verdampt zijn om een ontsteekbaar mengsel te vormen. Eens dat die damp<br />
ontstoken is zal de rest mee ontbranden. Langs de andere kant mag de dampspanning niet te<br />
hoog zijn want dit zou verhinderen dat er lucht mee aangezogen wordt.<br />
De maat voor de dampspanning is de zgn. "RVP" (Reid Vapor Pressure).<br />
De ideale RVP varieert uiteraard met het seizoen .In de koudste streken bedraagt die 13 psi in de<br />
warmste 8.5 psi. (1 psi = 0.07 bar)<br />
De RVP wordt gemeten bij 15.6° (60°F)<br />
De "vapor lock":<br />
Bij een hoge temperatuur op grote hoogte kan er verdamping ontstaan in de benzineleidingen<br />
zodat de brandstofpomp afslaat. De motor kan maar gestart worden nadat hij gekoeld is.<br />
Butaanmenging:<br />
De RVP van de meeste onbehandelde benzines is veel te laag zijn. Het zal nodig zijn een<br />
bepaalde koolwaterstof te mengen om de RVP omhoog te brengen. Men kan isobutaan<br />
gebruiken dat een RVP heeft van 71 psi.<br />
Isobutaan komt echter in onvoldoende hoeveelheden uit de raffinageprocessen. Men gebruikt<br />
daarom normaal butaan dat veel meer voorkomt en dus goedkoper is, alhoewel de RVP van<br />
butaan 52 psi bedraagt.<br />
<strong>Technologie</strong> <strong>II</strong>- 6 -
)De verbranding bij de dieselmotor:<br />
• Het principe<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Bij de dieselmotor wordt alleen in het begin van de brandstofinspuiting zelfontsteking<br />
toegestaan, nadien moet de brandstof verbranden. De verbranding bij de dieselmotor gebeurt<br />
traag, er is een traag vlamfront (zie figuur). De dieselmotor is een verbrandingsmotor.<br />
Het grote rendement en vermogen van de dieselmotor wordt gerealiseerd door de hoge<br />
drukopbouw in de motor. Bij hoge druk kunnen er veel brandstofmoleculen verbranden in één<br />
slag.<br />
Belangrijk: de brandgewilligheid (ontsteking door zelfontbranding) van dieselbrandstof moet<br />
hoog zijn, deze is hoger dan bij de benzine (zie tabel). Eenmaal ontstoken moet de volgende<br />
ingespoten brandstof verbranden en niet zelfontsteken.<br />
Bij de verbranding kan men twee fasen onderscheiden:<br />
1) zelfontsteking<br />
2) de verbrandingsfase (gecontroleerde verbranding)<br />
Inspuiting Begin verbranding Einde inspuiting<br />
ontstekingsuitstel verbrandingsfase<br />
Zodra er brandstof als een fijne nevel in de verbrandingskamer komt, zal deze brandstof eerst<br />
moeten verdampen en in temperatuur stijgen voor ze tot zelfontbranding komt. Op het<br />
moment dat de zelfontbranding begint zal er zich een drukstoot voordoen. De mate van de<br />
drukverhoging hangt af van de hoeveelheid brandstof die op dat moment inmiddels is<br />
ingespoten. Dit uitstel wordt bepaald door het cetaangetal. De injectie van de diesel gebeurt<br />
deels in het begin en de resterende hoeveelheid wordt dan verder geinjecteerd na de<br />
zelfontsteking.<br />
•<br />
Verbranding<br />
<strong>Technologie</strong> <strong>II</strong>- 7 -<br />
brandstof kooktemperatuur ontstekingstemperatuur<br />
benzine 25°C …210°C 300 à 400°C<br />
diesel 150°C…360°C 250 °C<br />
propaan - 43°C 470°C
Het cetaangetal<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
De belangrijkste karakteristiek van dieselolie is de ontstekingskwaliteit weergegeven door het<br />
cetaan getal. Dit is het volumeprocent cetaan (C16H34) in een referentiemengsel dat dezelfde<br />
ontbrandingsvertraging heeft als de te onderzoeken brandstof. Hoe hoger het cetaangetal, hoe<br />
korter de ontbrandingsvertraging. De ontstekingsvertraging is namelijk het kleinst voor cetaan.<br />
Wanneer dieselolie dezelfde ontstekingskarakteristiek heeft als een bepaald testmengsel met<br />
cetaan, dan heeft de dieselolie een cetaangetal gelijk aan dat percentage in het testmengsel. Men<br />
laat een testmotor met regelbare compressie draaien met verschillende mengsels van n-cetaan en<br />
heptamethylnonane totdat men dezelfde ontstekingscondities heeft gevonden als deze met het<br />
monster.<br />
Zoals bij benzine zijn er verschillende graden van dieselolie.<br />
Het cetaangetal van rechtstreeks geraffineerde gasoil: 50 – 55<br />
Gekraakte gasoil: 32 - 35<br />
Kerosene: 55<br />
Met deze componenten kan men mengsels bekomen met een cetaangetal naar keuze.<br />
Aanbevolen cetaangetallen:<br />
Snelle motoren: 1500 t/min < n : 55<br />
Halfsnelle motoren: 600 t/min < n < 1500 t/min: 40<br />
Langzame motoren: n < 600 t/min: 25<br />
• Invloed van het cetaangetal<br />
Het ontstekingsuitstel of ook ontbrandingsvertraging heeft een grote invloed op het klopgedrag<br />
van de motor. Want de hoeveelheid brandstof ontbrandt bij het einde van de klopfase praktisch<br />
onmiddellijk, dus bij constant volume en dus met drukopbouw.<br />
Een verlaging van het cetaangetal verlengt het ontstekingsuitstel. Dit geeft aanleiding tot een<br />
verhoging van de verbrandingsdruk (zie figuur) wat mechanische spanningen veroorzaakt in de<br />
cilinder en de koppelingen.<br />
Bovendien brengt een verlenging van het ontstekingsuitstel in extreme gevallen een onvolledige<br />
verbranding met zich mee. Daardoor verhoogt de hoeveelheid onverbrande brandstof en<br />
veroorzaakt aldus versnelde bevuiling van de verbrandingskamers, van de turboblazers, de<br />
uitlaatpijpen en het oliereservoir.<br />
Dus een verlenging van het ontstekingsuitstel geeft aanleiding tot kloppen en vandaar meer<br />
mechanische vermoeidheid en minder geleverde arbeid.<br />
<strong>Technologie</strong> <strong>II</strong>- 8 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Invloed van het cetaangetal op verbrandingsdruk en ontstekingsuitstel.<br />
<strong>Technologie</strong> <strong>II</strong>- 9 -
• Het dieselgetal<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Jammer genoeg is de motor voor de bepaling van het cetaangetal niet geschikt voor het testen<br />
van zware brandstoffen.<br />
Het dieselgetal is een variante op het cetaangetal, met dit verschil dat het mits een eenvoudige<br />
test kan bepaald worden. Men maakt gebruik van de volgende vergelijking:<br />
Het dieselgetal = °API x anilinepunt / 100<br />
De achtergrond van deze, en van de volgende methodes is dat aromaten in de brandstof minder goede<br />
ontstekingseigenschappen heeft dan de andere componenten. Men tracht nu het gehalte aan aromaten te bepalen en<br />
hieruit een index te bepalen.<br />
Het anilinepunt (ASTM D 611) is de laagste temperatuur bij dewelke gelijke volumes van<br />
zuivere aniline en de olie nog juist volledig mengbaar zijn.<br />
De betrekking tussen het cetaangetal en het dieselgetal:<br />
Het cetaangetal = 13 + 0,65 x het dieselgetal.<br />
• Het aromatisch koolstof getal<br />
Sinds begin '80 bestaat er een nieuwe index: CCAI (Calculated Carbon Aromaticity Index) dat<br />
steunt op het feit dat de aromaten een hogere densiteit en viscositeit hebben. (De aromaten zijn<br />
niet gewenst in de brandstof).<br />
800 is het getal voor een goede fuel, 950 voor een slechte.<br />
CCAI = d - 81 - 141.log log(v + 0.85)<br />
waarin: d = de densiteit in kg/m3 bij 15°C<br />
v = de kinematische viscositeit in mm²/s bij 50°C<br />
Er bestaat ook “ het berekende cetaangetal”. Dit cijfer wordt berekend met de densiteit uitgedrukt<br />
in API en met de temperatuur in F waarbij 50% destilleert is. Deze methode is niet altijd<br />
toepasbaar.<br />
<strong>Technologie</strong> <strong>II</strong>- 10 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
3)<strong>DE</strong> EIGENSCHAPPEN VAN <strong>BRANDSTOFFEN</strong><br />
a)Mogelijke problemen bij de opslag van stookolie<br />
• Inleiding<br />
De zware stookoliën bestaan uit vaste en vloeibare bestanddelen. De asfaltenen zijn de vaste<br />
zwarte bestanddelen die onder normale omstandigheden neerslaan (maltenen zijn de vloeibare<br />
bestanddelen van het product). De stookolie kan niet beschouwd worden als een zuivere<br />
oplossing, maar als een zeer fijne verdeling (dispersie) van de vaste en de vloeibare bestanddelen<br />
dus een suspensie. Fuel oil wordt daarom beschouwd als een “colloidaal systeem” (een gelei),<br />
waarin de asfaltenen in evenwicht zijn met de maltenen.<br />
Asfaltenen hebben de eigenschap uit te zakken (uitvlokken) en daardoor sludge te vormen. Deze<br />
neerslag kan zich vormen in de opslagtanks of in de pijperijen. De weerstand tegen de vorming<br />
van sludge heet STABILITEIT. In een fuel oil moet minder dan 0,15 gew.% sludge aanwezig<br />
zijn.<br />
Asfaltenen zijn dus vaste deeltjes, zwevend in de brandstof. Om de vorming van sludge te<br />
vermijden moeten deze deeltjes in suspensie worden gehouden. Zoals u kunt constateren hebben<br />
de harsen analoge structuurdelen met zowel de asfaltenen als met de paraffines (belangrijke<br />
componenten in de ruwe aardolie). De harsen kunnen dus de asfaltenen in suspensie houden<br />
(verklaar). Tevens kunnen er additieven worden toegevoegd om de werking van de harsen te<br />
bevorderen.<br />
<strong>Technologie</strong> <strong>II</strong>- 11 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
1)Incompatibiliteit (compatibiliteit of mengbaarheid)<br />
Bij menging van twee residuale brandstoffen of een residuale brandstof met een destillaat kan er<br />
zich quasi onmiddellijk een neerslag vormen. Dit fenomeen gaat samen met de aanwezigheid<br />
van asfaltenen. De neerslag ontstaat omdat de hoeveelheid harsen onvoldoende zijn om alle<br />
asfaltenen in suspensie te houden.<br />
De compatibiliteit van twee brandstoffen hangt natuurlijk samen met de natuur van de aardolie,<br />
de graad van kraken, de gebruikte verdunningsmiddelen (destillaten) en de concentratie van de<br />
verschillende componenten (asfaltenen, paraffines, harsen …)<br />
Er bestaat een test om de mengstabiliteit te meten, dit is een vlekkentest. Deze test kan<br />
gemakkelijk aan boord uitgevoerd worden alvorens twee petroleumproducten te mengen.Men<br />
gaat een staal oplossen in een product (testkoffer) en men laat een druppel vallen op een<br />
gecalibreerd papiertje. Men kijkt naar de vlek en men vergelijkt deze met een stel gegeven foto’s.<br />
Blijkt de gevormde vlek quasi van dezelfde vorm als deze op de foto’s mag men mengen anders<br />
zijn deze brandstoffen niet compatibel.<br />
Het is duidelijk dat twee zware oliën, of een distillaat en een residuele brandstof beiden van zeer<br />
goede kwaliteit kunnen zijn, maar dat niet meer zijn bij menging. Menging van brandstoffen is<br />
dus te vermijden, ook is het preventieve gebruik van additieven aan te bevelen. Verhoging van<br />
de temperatuur vermindert het incompatibiliteitsgevaar.<br />
2)Instabiliteit<br />
Dit fenomeen hangt af van de tijd en niet van een menging. Het is het gevolg van chemische<br />
reacties van de verschillende componenten, polymerisatie en flocculatie (uitvlokking) treedt op.<br />
De instabiliteit hangt af van de natuur van de mengsels en van de productiemethode (kraken).<br />
In geval van instabiliteit verandert de viscositeit samen met de vlokvorming na verloop van tijd.<br />
Om het risico op instabiliteit te verminderen kan men de temperatuur verminderen, preventief<br />
roeren en additieven toevoegen.<br />
3)Neerslag<br />
Soms vormen er zich ook een brandstof lagen die meer of minder dik zijn als gevolg van een<br />
natuurlijke ontmenging van de mengsels. Dit fenomeen heeft geen verband met neerslagvorming<br />
als gevolg van incompatibiliteit of instabiliteit. Het is het neerslaan van de zwaarste delen, de<br />
asfaltenen.<br />
4)Decantatie<br />
Waterachtige onzuiverheden hebben de natuurlijke neiging om zich af te scheiden. Men<br />
constateert dat de ontmenging versnelt als de viscositeit vermindert.<br />
De stookolie wordt reeds in de bunkerstanks verwarmd om de olie verpompbaar te houden. In de<br />
settlingtanks wordt deze brandstof verder verwarmd tot b.v. 40°C . Door verhoging van de<br />
temperatuur wordt een verdere verlaging van de viscositeit verkregen, waardoor de afscheiding<br />
van water (en sediment) versneld wordt. Het afgescheiden water en sediment zakken uit en<br />
zullen zich op de bodem van de tank verzamelen.<br />
<strong>Technologie</strong> <strong>II</strong>- 12 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Om de afscheiding van dit water te verzekeren moeten de opslagbakken voorzien zijn van laag<br />
geplaatste aftapkraan, meteen kan er best ook een aftap mogelijk voorzien worden bovenaan<br />
voor het geval dat de densiteit van de brandstof meer is dan 1.<br />
De eigenschappen van stookoliën<br />
Inleiding<br />
Zware stookolie:<br />
Het gebruik impliceert investeringen in verwarmingsinstallaties om de olie te verpompen.<br />
De belangrijkste specificatie is de viscositeit. Om de viscositeit te verbeteren is men soms<br />
verplicht een lichtere component te mengen.<br />
Een andere eigenschap is het zwavelgehalte: 0.5 tot zelfs 5 % . De eliminatie van zwavel is een<br />
zeer dure investering; vandaar het prijsverschil tussen zwavelarme - en andere stookolie.<br />
Samenstelling:<br />
De meeste stookoliën zijn een mengsel van koolwaterstoffen, voorgesteld door de formules C nH 2n+2 (alkanen of<br />
paraffinen) en C nH 2n (naftenen). Een zeker percentage asfaltenen – dit zijn hoog moleculaire aromatische<br />
verbindingen C nH n – komt voor. Deze laatste zijn ongewenst wegens o.a. hun verhoogde roetvorming.<br />
Opmerking: De densiteit (uitgedrukt in API) en het cetaangetal werden reeds behandeld, de stookwaarde wordt<br />
besproken tijdens het hoofdstuk verbranding<br />
1)Het "Flash point".<br />
Het vlampunt is de laagste temperatuur waarbij voldoende gas ontstaat om met de lucht<br />
een brandbaar mengsel te vormen.<br />
Het vlampunt is dus de laagste temperatuur waartoe men een product moet verwarmen om de<br />
ontwikkelde dampen in aanwezigheid van een vlam even te doen ontvlammen onder<br />
genormaliseerde omstandigheden.<br />
Dit punt is belangrijk omwille van de veiligheid. Bij een open opslag mag het vlampunt niet<br />
lager zijn dan 60°C. Bovendien moet men er rekening mee houden dat tijdens de opslag het<br />
vlampunt kan verlagen door chemische reacties die voortgaan zelfs na de raffinage. Ook voor<br />
zware stookoliën is het vlampunt belangrijk daar deze brandstof moet opgewarmd worden<br />
vooraleer ze getransporteerd of ingespoten wordt. Het kan een begrenzende factor zijn voor<br />
allerlei componenten die men in deze olie wenst onder te brengen. Bespreek “N2 blanketting”<br />
<strong>Technologie</strong> <strong>II</strong>- 13 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
2)Het "pourpoint" (vloeibaarheidspunt of schenkpunt).<br />
Het vloeibaarheidspunt is de temperatuur waarbij de brandstof nog juist vloeibaar is. Bij<br />
bepaling ligt dit punt 5°C boven de temperatuur bij de welke de olie niet meer vloeit.<br />
Het is nodig dit punt te kennen als men wil verpompen.<br />
Bepaling:<br />
In een proefbuis koelt men langzaam een monster en bij elke daling van 3°C houdt men de buis<br />
horizontaal. Indien binnen de 5 seconden de olie niet vloeit heeft men na bijtelling van 5°C het<br />
stollingspunt.<br />
Enkele waarden:<br />
Marine dieselolie: maximum -6°<br />
Zware oliën: tot maximum 30°.<br />
Noot: Men kent ook het "cloudpoint" of troebelpunt voor de heldere brandstoffen.<br />
3)Het Conradson getal of het Ramsbottom getal.<br />
Het roetgetal is wat er overblijft na een onvolledige verbranding. Een gedeelte van de olie<br />
verbrandt niet maar blijft achter onder de vorm van roet. Het spreekt vanzelf dat roet het<br />
rendement nadelig beïnvloedt.<br />
Onvolledige verbranding van methaan met roetvorming: CH4 + O2 → C + 2H2O<br />
Bepaling:<br />
Een monster wordt verbrand in een gedeeltelijk afgesloten recipiënt, derwijze dat er een<br />
minimaal luchtverbruik is. Men zorgt er voor dat de verbrandingsgassen kunnen ontsnappen. Het<br />
Conradson of het Ramsbottom getal is het massa quotiënt tussen de hoeveelheid roet en de<br />
hoeveelheid initiële brandstof.<br />
Enkele gebruikelijke waarden:<br />
Lichte stookoliën: 0.2 tot 2.5 %<br />
Residuale stookoliën: 10 tot 22 %<br />
<strong>Technologie</strong> <strong>II</strong>- 14 -
4)Het asgehalte.<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Dit is het massapercentage van wat overblijft na een zo volledig mogelijke verbranding.<br />
Zij bevat metaalelementen zoals Va, Na, Ni, Fe, Si en verhoogt de slijtage, de deeltjes zijn<br />
abrasief, evenals de bevuiling. Samen met de zwavel en de koolstof in de brandstof vormen deze<br />
metalen sulfaten en carbonaten. Deze producten vormen afzettingen op de motorkleppen die<br />
aanleiding kunnen geven tot ongewenste ontstekingsbronnen.<br />
Volledige verbranding van methaan: CH4 +2 O2 → CO2 + 2H2O<br />
Bepaling:<br />
Het monster wordt langzaam en zo volledig mogelijk met een overmaat aan lucht verbrand. Wat<br />
overblijft wordt in een oven op 775°C gebracht om de laatste resten aan koolstof te verbranden.<br />
Enkele gebruikelijke waarden:<br />
Lichte stookolie: tot 0.05 %<br />
Zware stookolie: tot 0.2 %<br />
5)Het zwavelgehalte<br />
Zwavel is een niet-metaal aanwezig in de zware stookoliën voornamelijk in de vorm van<br />
organische verbindingen, soms ook in de vorm van oxides. Het zwavelgehalte in de huidige<br />
zware stookolie ligt in de orde tussen 3,5 à 5%.<br />
De zwavelverbindingen gevormd in de dieselmotor en in de ketels bestaan voornamelijk uit SO2.<br />
Deze SO2 is verantwoordelijk voor de vorming van uiterst corrosieve zuren bij lage temperaturen<br />
dus bij condensatie.<br />
Dus een verhoogd gehalte aan zwavel bevordert de corrosie van de cilinders, het is te zeggen op<br />
de koudere plaatsen, en bevordert de corrosie in de schouw van de ketel (de koude<br />
temperatuurscorrosie).<br />
Het zwavelgehalte is belangrijk in verband met het milieu, de koude temperatuurscorrosie en het<br />
calorische vermogen. De bepaling van het zwavelgehalte is zeer omslachtig. De hoeveelheid<br />
zwavel in de brandstof wordt uitgedrukt in percentage van de totale massa.<br />
<strong>Technologie</strong> <strong>II</strong>- 15 -
6)Het gehalte aan metalen.<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Men wil vooral het gehalte kennen aan vanadium, natrium, nikkel… gezien deze metalen<br />
de corrosie bevorderen. Het gehalte aan metalen is sterk afhankelijk van de herkomst van de<br />
ruwe aardolie en van de bewerkingen hiervan. Het gehalte aan metaal wordt uitgedrukt in ppm<br />
(partikels per miljoen; 1mg/kg komt overéén met 1 ppm)<br />
De aanwezigheid van natrium is meestal te wijten aan contaminatie met zeewater.<br />
Uit natrium en vanadium ontstaan bij verbranding zouten, die heel corrosief zijn bij hun<br />
smeltpunt (350°C en 680°C). De geproduceerde zouten lost het ijzeroxide Fe2O3 op en bevordert<br />
de oxidatie - corrosie van het ijzer.<br />
Bepaling:<br />
Men maakt gebruik van de spectrograaf. Het monster wordt verstoven en doorheen een vlam<br />
gejaagd. De hitte is zodanig dat de atomen "geëxciteerd" worden, d.w.z. dat enkele elektronen<br />
een baan volgen op een schil van hogere orde. De atomen zijn dus energetisch geladen. Eens de<br />
vlam verlaten keren de elektronen terug naar hun oorspronkelijke schil en geven daarbij energie<br />
terug onder de vorm van licht. De golflengte van dit licht is karakteristiek voor elk element. Deze<br />
golflengten van het uitgestraalde licht worden elektronisch vergeleken waardoor men het metaal<br />
kan bepalen. De intensiteit van het licht geeft een aanduiding van de concentratie.<br />
7)Het watergehalte.<br />
Het watergehalte drukt de stookwaarde, dit water moet namelijk verdampt worden. Door<br />
spectroscopisch het natriumgehalte na te gaan kan zien of het hier gaat om zeewater of om zoet<br />
water.<br />
Daar de oplosbaarheid van water beperkt is kan het aanwezige water enkel van buitenaf komen. Het kan condensaat<br />
zijn van ingespoten stoom, ergens in een proces gebruikt, of het condensaat kan duiden op een lek in de<br />
verwarmingspijpen of het kan condensaat zijn gecondenseerd in de opslagtanks.<br />
8)De sedimenten.<br />
Het gaat hier om deeltjes vreemd aan de brandstof zoals verfresten, roest, zand, stukjes<br />
van dichtingsringen enz. Het is duidelijk dat deze tot verstoppingen kunnen leiden en meer<br />
slijtage veroorzaken.<br />
9)Katalysator resten(catalityc fines)<br />
Deze bestaan in de vorm van aluminium silicaten (zeolieten, een soort klei) in de brandstof,<br />
gemaakt met het residu van de katalytische kraakeenheid. Deze deeltjes zijn heel abrasief.<br />
<strong>Technologie</strong> <strong>II</strong>- 16 -
10)De asfaltenen<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
De asfaltenen kunnen zowel goed als slecht verbranden naargelang de samenstelling van de<br />
moleculen.<br />
Het zijn koolwaterstofmoleculen met een hoog moleculair gewicht (1000 gr), die zich verzameld<br />
hebben in het residu van de destillatietorens. Ze zijn in de brandstof fijn verdeeld in colloïdale<br />
vorm (in suspensie gehouden dank zij de harsen).<br />
Indien deze asphaltenen neerslaan hebben we een stabiliteitsprobleem.<br />
Het is duidelijk dat zulks filters, afscheiders en pompen kan blokkeren. Bovendien is de kwaliteit<br />
van uitgezakte olie niet constant.<br />
Bepaling.<br />
Ofwel door het filteren van een monster.<br />
Ofwel door de vlekproef.<br />
Men bereidt een mengsel van 50 % van de te onderzoeken brandstof en 50 % van een bepaald<br />
distillaat. Men laat en druppel vallen op een gekalibreerd papier. Men vergelijkt de vorm met een<br />
reeks referentiefoto's.<br />
Niveau 1: zeer stabiel: geen centrale ring.<br />
Niveau 2: een nauwelijks te onderscheiden ring.<br />
Niveau 3: een fijne maar duidelijk zichtbare ring.<br />
Niveau 4: Een zeer dikke en donker gekleurde ring.<br />
Niveau 5: Een centrale zone waarin de vaste particules zelfs te onderscheiden zijn.<br />
Opm.: In het geval van zware olie gebruikt men als "distillaat" white spirit.<br />
11)De viscositeit (viscositeit wordt ook behandeld in het hoofdstuk smeermiddelen)<br />
De viscositeit is een maat voor de inwendige wrijving in de vloeistof (bepaling zie<br />
smeermiddelen).<br />
De viscositeit neemt af als de temperatuur toeneemt (opmerking ook de densiteit vermindert bij<br />
toename van de temperatuur).<br />
Het verband tussen de temperatuur en de viscositeit kan grafisch voorgesteld worden. Door<br />
gebruik te maken van de gepaste (logaritmische) schalen kan dit verband gegeven worden door<br />
een rechte. Bij brandstoffen zijn deze rechten nagenoeg evenwijdig (zie figuur). Kent men de<br />
viscositeit van de brandstof bij een enkele temperatuur, dan kan men de rechte trekken en de<br />
viscositeit bepalen bij elke temperatuur. Hieruit volgt dat men de viscositeit van de brandstof kan<br />
beschrijven enkel door de viscositeit bij een standaardtemperatuur te geven, bijvoorbeeld de<br />
viscositeit in centistokes cSt bij 40°C.<br />
De meeste brandstoffen zijn mengsels van residuen en destillaten uit het raffinageproces.<br />
Met het “blending” diagram bekomt men de viscositeit van een mengsel van twee brandstoffen<br />
indien de viscositeit van de afzonderlijke oliën gekend is.<br />
Hoe kunt u een brandstof maken met een viscositeit van 30 cSt?<br />
<strong>Technologie</strong> <strong>II</strong>- 17 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
<strong>Technologie</strong> <strong>II</strong>- 18 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
<strong>Technologie</strong> <strong>II</strong>- 19 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
Bestudeer het analyse verslag “marine diesel oil”<br />
Nog enkele verbrandingswaarden: (in MJ/kg)<br />
Steenkool: 27 - 32<br />
Benzine: 43 - 47<br />
Diesel: 42<br />
Petroleum: 41 - 43<br />
Stookolie: 40 - 41<br />
Aardgas: 30<br />
Acetyleen: 57<br />
<strong>Technologie</strong> <strong>II</strong>- 20 -
c)Specificaties van brandstoffen.<br />
Benamingen<br />
Gasoil: straight-run produkten<br />
Marine destillate oil: straight-run produkten<br />
Marine diesel oil: geblend met 1500”R I stookolie<br />
1500”R I stookolie: Residuale stookoliën<br />
3500”R I stookolie: Residuale stookoliën<br />
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
De aanduiding in “Redwood I seconden” is een aanduiding voor viscositeit. Er is een rechtstreeks verband tussen de<br />
verschillende viscositeiteenheden.<br />
• De verschillende standaards<br />
Het is duidelijk dat deze benamingen onvoldoende zijn om de verschillende brandstoffen te<br />
specificeren. Verschillende instanties hebben vanaf 1970 gepoogd om een internationale<br />
standaard op te stellen. Er zijn dus meerdere standaards in omloop, tussen deze standaards is er<br />
uiteraard een verband. In 1990 zijn de aanbevelingen van CIMAC internationaal van kracht<br />
geworden. Deze standaard moet dus gebruikt worden bij bestelling en levering van de<br />
scheepsbrandstof.<br />
De “Britisch Standard Specifacation” werd in 1970 van kracht. Deze geeft een indeling volgens:<br />
A1, A2, B1, B2, E ,F ,G , H<br />
In 1977 werden de viscositeiten uitgedrukt in centistokes bij 40°C en 50°C, de brandstoffen<br />
werden IF grades genoemd (IF grades betekend interfuels en duidt op “blended”)<br />
In 1982 werd een andere standaard ingevoerd met een classificering van M1 tot M12<br />
In 1989 werd de “Britisch Standard Specification BS MA 100 :1989 ” van kracht die ook de<br />
viscositeit laat bepalen bij hogere temperaturen. Dit is de ISO 8217 norm.<br />
Vanaf 1990 is dus de CIMAC standaard geldig<br />
<strong>Technologie</strong> <strong>II</strong>- 21 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
• Het verband tussen de verschillende standaards<br />
Volgende tabel geeft het verband tussen de standaard voor 1990 namelijk “ISO 8217” en de<br />
huidige standaard CIMAC.<br />
CIMAC DX DA DB DC<br />
ISO DMX DMA DMB DMC<br />
DMX, DMA, DMB zijn straight-run produkten. De brandstof DMC is hoofdzakelijk een destillaat maar reeds een<br />
weinig gemengd met residuele brandstof.<br />
CIMAC A10 B10 C10 D15 E25 F25 G35 H35 K35 H45 K45 H55 K55<br />
ISO RMA10 RMB10 RMC10 RMD15 RME25 RMF25 RMG35 RMH35 RMK35 RMH45 RMK45 RMH55 -<br />
Bij de ISO standaard staat:<br />
M staat voor marine kwaliteit<br />
D staat voor destillaat<br />
R staat voor residuale brandstof en is in meer of minder mate gemengd met destillaat.<br />
Het cijfer duidt op de viscositeit<br />
De letter geeft een andere kwaliteit aan.<br />
<strong>Technologie</strong> <strong>II</strong>- 22 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
D staat voor destillaat, M voor marine, X, A, B, C, zijn kwaliteiten<br />
<strong>Technologie</strong> <strong>II</strong>- 23 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
R staat voor residu, M voor marine, A, B, C …. voor kwaliteiten<br />
10, 15, 25 …. voor de viscositeit.<br />
<strong>Technologie</strong> <strong>II</strong>- 24 -
<strong>Hoofdstuk</strong> 2 <strong>DE</strong> <strong>BRANDSTOFFEN</strong><br />
<strong>Technologie</strong> <strong>II</strong>- 25 -