Galvaniska element - Wordpress Wordpress
Galvaniska element - Wordpress Wordpress
Galvaniska element - Wordpress Wordpress
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Galvaniska</strong> <strong>element</strong><br />
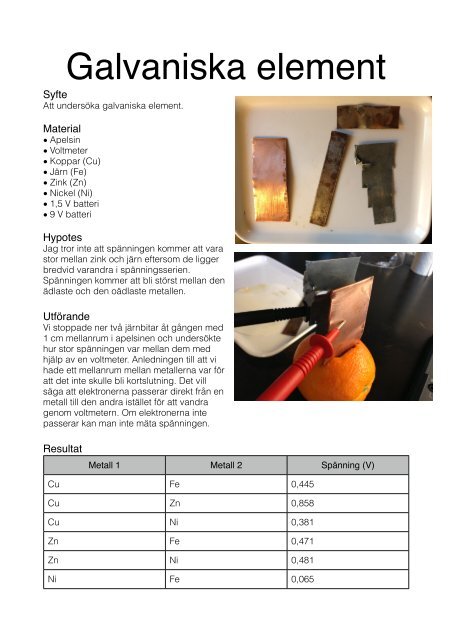
Syfte<br />
Att undersöka galvaniska <strong>element</strong>.<br />
Material<br />
• Apelsin<br />
• Voltmeter<br />
• Koppar (Cu)<br />
• Järn (Fe)<br />
• Zink (Zn)<br />
• Nickel (Ni)<br />
• 1,5 V batteri<br />
• 9 V batteri<br />
Hypotes<br />
Jag tror inte att spänningen kommer att vara<br />
stor mellan zink och järn eftersom de ligger<br />
bredvid varandra i spänningsserien.<br />
Spänningen kommer att bli störst mellan den<br />
ädlaste och den oädlaste metallen.<br />
Utförande<br />
Vi stoppade ner två järnbitar åt gången med<br />
1 cm mellanrum i apelsinen och undersökte<br />
hur stor spänningen var mellan dem med<br />
hjälp av en voltmeter. Anledningen till att vi<br />
hade ett mellanrum mellan metallerna var för<br />
att det inte skulle bli kortslutning. Det vill<br />
säga att elektronerna passerar direkt från en<br />
metall till den andra istället för att vandra<br />
genom voltmetern. Om elektronerna inte<br />
passerar kan man inte mäta spänningen.<br />
Resultat<br />
Metall 1 Metall 2 Spänning (V)<br />
Cu Fe 0,445<br />
Cu Zn 0,858<br />
Cu Ni 0,381<br />
Zn Fe 0,471<br />
Zn Ni 0,481<br />
Ni Fe 0,065
Slutsats<br />
Metaller av olika ädelhet som sänks ner i en elektrolyt får en elektrisk spänning mellan sig.<br />
Metallerna bildar alltså elektroderna i ett galvaniskt <strong>element</strong>. En elektrolyt är en jonlösning<br />
och vi använde oss av en apelsin när vi gjorde vårt experiment. En apelsin innehåller<br />
citronsyra och syror är kemiska föreningar som kan avge vätejoner. Alla syror består av en<br />
eller flera karboxylgrupper.<br />
När man kopplar ihop elektroderna med en metalltråd omvandlas den kemiska energin till<br />
elektrisk energi. Den oädlare metallen oxideras i jonlösningen och omvandlas till joner. De<br />
överblivna elektronerna vandrar genom metalltråden till den ädlare metallen. Den oädlare<br />
metallen blir anod och den ädlare blir katod. De positiva vätejonerna i citronsyran dras till<br />
elektronerna som vandrat till katoden. Vätejonerna och elektronerna bildar tillsammans<br />
vätgas.<br />
Det här händer med zink och koppar som elektroder<br />
Anod: Zn → Zn 2+ + e -<br />
Katod: 2 H + + 2 e - → H2<br />
Beroende på hur långt ifrån varandra de olika metallerna ligger i spänningsserien blir<br />
spänningen olika stor. Ju längre ifrån varandra<br />
desto större spänning och närmre desto mindre<br />
spänning. Av de metaller vi undersökte låg<br />
koppar och zink längst ifrån varandra.<br />
Detta är ett galvaniskt <strong>element</strong>. Ett galvaniskt<br />
<strong>element</strong> ger energi och är en så kallad exoterm.<br />
Batterier är galvaniska <strong>element</strong> som består av<br />
starka syror med många joner och ju större<br />
skillnad det är på ädelheten i elektroderna desto<br />
mer volt ger batterierna. Batterier fungerar som<br />
experimentet med apelsinen men de ser<br />
annorlunda ut.<br />
Ett alkaliskt batteri har ytterst ett hölje av stål.<br />
Innanför det finns ett lager av brunsten som är<br />
indränkt i kaliumhydroxid. Mellan zinkpulvret och<br />
brunstenen finns ett lager av porös plast som<br />
släpper igenom jonerna men hindrar brunstenen<br />
och zinken från att blanda sig med varandra.<br />
Även zinkpulvret är indränkt i kaliumhydroxid. Det<br />
finns en strömledare av mässing som är kopplad<br />
till zinken och en annan metall som är kopplad till<br />
brunstenen.<br />
Brunsten<br />
Brunsten (mangandioxid) är en kemisk förening<br />
av manganjoner och oxidjoner. När man får en<br />
sluten strömkrets vandrar elektronerna från zink<br />
till manganjonerna. Manganjonerna tar upp en<br />
elektron var. Detta gör att zink blir minuspol (anod) och brunsten pluspol (katod).<br />
Strömledare av mässing<br />
Zinkpulver
Det här händer i ett alkaliskt batteri<br />
Anod: Zn → Zn 2+ + e -<br />
Katod: Mn 4+ + e - → Mn 3+<br />
Ett brunstensbatteri fungerar ungefär som ett<br />
alkaliskt batteri men zink och brunsten har bytt<br />
plats. Inuti ett 9 V batteri finns 6 st alkaliska<br />
batterier som vardera är 1,5 V.<br />
9 V batteri<br />
Felkällor<br />
Det är inte säkert att vi hade metallerna på exakt<br />
samma avstånd från varandra och på så sätt kan spänningen mellan dem blivit olika.