1 - Acervo Digital da Unesp
1 - Acervo Digital da Unesp
1 - Acervo Digital da Unesp
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
tema1<br />
TEMAS<br />
ficha<br />
No.<br />
H 1<br />
Li 2<br />
No.<br />
F 8<br />
Na 9<br />
sumário bibliografia<br />
No. No. No. No. No. No.<br />
1<br />
Cl 15 Co e Ni 22 Br 29 Pd 36 I 42 Pt & Ir 50<br />
2<br />
K 16 Cu 23 Rb 30 Ag 37 Cs 44 Os 51<br />
G 3 Mg10 Ca 17 Zn 24 Sr 31 Cd 38 Ba e V 45 Hg 52<br />
3<br />
Bo 4<br />
C 5<br />
Al 11<br />
Si 12<br />
Cr 19<br />
Ti 18<br />
Y 25<br />
In 26<br />
Ce e La 33<br />
Zr 32<br />
U 40<br />
Sn 39<br />
Ta 46<br />
W 47<br />
Tl 53<br />
Pb 54<br />
4<br />
N 6 P 13 Mn 20 As 27 Di e Mo 34 Sb 41 Nb 48 Bi 55<br />
O 7 S 14 Fe 21 Se 28 Ro e Ru 35 Te 43 Au 49 Th 56<br />
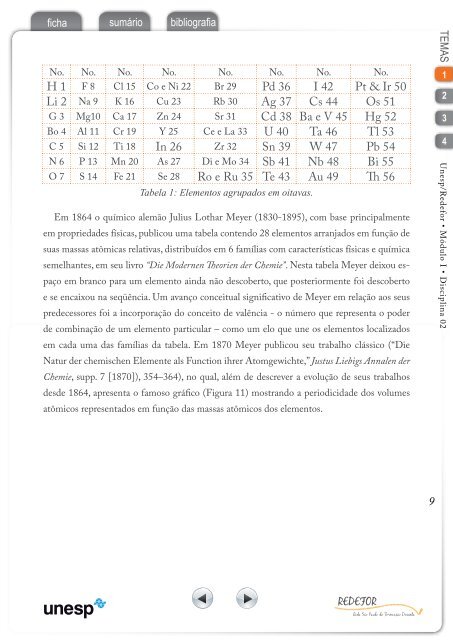
Tabela 1: Elementos agrupados em oitavas.<br />
Em 1864 o químico alemão Julius Lothar Meyer (1830-1895), com base principalmente<br />
em proprie<strong>da</strong>des físicas, publicou uma tabela contendo 28 elementos arranjados em função de<br />
suas massas atômicas relativas, distribuídos em 6 famílias com características físicas e química<br />
semelhantes, em seu livro “Die Modernen Theorien der Chemie”. Nesta tabela Meyer deixou espaço<br />
em branco para um elemento ain<strong>da</strong> não descoberto, que posteriormente foi descoberto<br />
e se encaixou na seqüência. Um avanço conceitual significativo de Meyer em relação aos seus<br />
predecessores foi a incorporação do conceito de valência - o número que representa o poder<br />
de combinação de um elemento particular – como um elo que une os elementos localizados<br />
em ca<strong>da</strong> uma <strong>da</strong>s famílias <strong>da</strong> tabela. Em 1870 Meyer publicou seu trabalho clássico (“Die<br />
Natur der chemischen Elemente als Function ihrer Atomgewichte,” Justus Liebigs Annalen der<br />
Chemie, supp. 7 [1870]), 354–364), no qual, além de descrever a evolução de seus trabalhos<br />
desde 1864, apresenta o famoso gráfico (Figura 11) mostrando a periodici<strong>da</strong>de dos volumes<br />
atômicos representados em função <strong>da</strong>s massas atômicos dos elementos.<br />
9<br />
<strong>Unesp</strong>/Redefor • Módulo I • Disciplina 02