Dendritische Zellen in der Krebsimmuntherapie - ACTIVARTIS ...
Dendritische Zellen in der Krebsimmuntherapie - ACTIVARTIS ...
Dendritische Zellen in der Krebsimmuntherapie - ACTIVARTIS ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Umgebung von dendritischen<br />
<strong>Zellen</strong> signalisiert. Die Aktivierung<br />
<strong>der</strong> DC führt e<strong>in</strong>erseits dazu,<br />
dass diese ihren Wachtposten im<br />
Gewebe verlassen und <strong>in</strong> die regionalen<br />
Lymphknoten e<strong>in</strong>wan<strong>der</strong>n,<br />
an<strong>der</strong>erseits werden die zuletzt<br />
aufgenommenen Prote<strong>in</strong>e,<br />
unter denen sich auch die Prote<strong>in</strong>e<br />
<strong>der</strong> Mikroorganismen bef<strong>in</strong>den,<br />
an die T-<strong>Zellen</strong> im Lymphknoten<br />
<strong>in</strong> e<strong>in</strong>er immunstimulierenden<br />
Form präsentiert.<br />
<strong>Dendritische</strong> <strong>Zellen</strong><br />
im Tumorgewebe<br />
Genauso wie <strong>in</strong> an<strong>der</strong>en Geweben<br />
f<strong>in</strong>den sich unreife DC auch<br />
im Tumorgewebe. Dort machen<br />
sie genau das, was ihre wichtigste<br />
Aufgabe ist: Sie schalten die<br />
T-<strong>Zellen</strong> <strong>in</strong> ihrer Umgebung ab,<br />
um zu verh<strong>in</strong><strong>der</strong>n, dass diese gegen<br />
Autoantigene aktiv werden.<br />
Im Tumor ist das natürlich kontraproduktiv,<br />
weil unter den als<br />
Autoantigene präsentierten Prote<strong>in</strong>en<br />
auch Tumorantigene enthalten<br />
s<strong>in</strong>d. Die im Pr<strong>in</strong>zip gegen Tumorantigene<br />
gerichteten T-<strong>Zellen</strong> werden also von<br />
den DC aktiv abgeschaltet, was e<strong>in</strong> wichtiger<br />
Beitrag zum Schutz des Tumors vor<br />
dem Immunsystem ist. Das Problem dabei<br />
liegt dar<strong>in</strong>, dass Tumorzellen über<br />
ke<strong>in</strong>e mikrobiellen Gefahrensignale verfügen.<br />
Die DC werden daher nicht aktiviert,<br />
und es wird unter normalen Umständen<br />
auch ke<strong>in</strong>e Antitumorimmunität<br />
ausgelöst.<br />
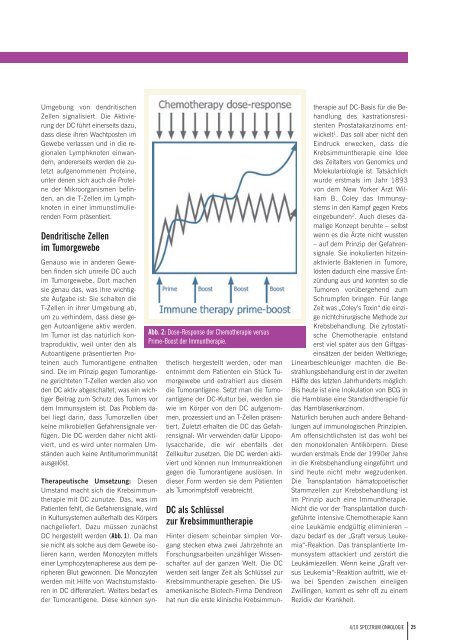
Abb. 2: Dose-Response <strong>der</strong> Chemotherapie versus<br />
Prime-Boost <strong>der</strong> Immuntherapie.<br />
Therapeutische Umsetzung: Diesen<br />
Umstand macht sich die <strong>Krebsimmuntherapie</strong><br />
mit DC zunutze. Das, was im<br />
Patienten fehlt, die Gefahrensignale, wird<br />
<strong>in</strong> Kultursystemen außerhalb des Körpers<br />
nachgeliefert. Dazu müssen zunächst<br />
DC hergestellt werden (Abb. 1). Da man<br />
sie nicht als solche aus dem Gewebe isolieren<br />
kann, werden Monozyten mittels<br />
e<strong>in</strong>er Lymphozytenapherese aus dem peripheren<br />
Blut gewonnen. Die Monozyten<br />
werden mit Hilfe von Wachstumsfaktoren<br />
<strong>in</strong> DC differenziert. Weiters bedarf es<br />
<strong>der</strong> Tumorantigene. Diese können synthetisch<br />
hergestellt werden, o<strong>der</strong> man<br />
entnimmt dem Patienten e<strong>in</strong> Stück Tumorgewebe<br />
und extrahiert aus diesem<br />
die Tumorantigene. Setzt man die Tumorantigene<br />
<strong>der</strong> DC-Kultur bei, werden sie<br />
wie im Körper von den DC aufgenommen,<br />
prozessiert und an T-<strong>Zellen</strong> präsentiert.<br />
Zuletzt erhalten die DC das Gefahrensignal:<br />
Wir verwenden dafür Lipopolysaccharide,<br />
die wir ebenfalls <strong>der</strong><br />
Zellkultur zusetzen. Die DC werden aktiviert<br />
und können nun Immunreaktionen<br />
gegen die Tumorantigene auslösen. In<br />
dieser Form werden sie dem Patienten<br />
als Tumorimpfstoff verabreicht.<br />
DC als Schlüssel<br />
zur <strong>Krebsimmuntherapie</strong><br />
H<strong>in</strong>ter diesem sche<strong>in</strong>bar simplen Vorgang<br />
stecken etwa zwei Jahrzehnte an<br />
Forschungsarbeiten unzähliger Wissenschafter<br />
auf <strong>der</strong> ganzen Welt. Die DC<br />
werden seit langer Zeit als Schlüssel zur<br />
<strong>Krebsimmuntherapie</strong> gesehen. Die USamerikanische<br />
Biotech-Firma Dendreon<br />
hat nun die erste kl<strong>in</strong>ische <strong>Krebsimmuntherapie</strong><br />
auf DC-Basis für die Behandlung<br />
des kastrationsresistenten<br />
Prostatakarz<strong>in</strong>oms entwickelt<br />
1 . Das soll aber nicht den<br />
E<strong>in</strong>druck erwecken, dass die<br />
<strong>Krebsimmuntherapie</strong> e<strong>in</strong>e Idee<br />
des Zeitalters von Genomics und<br />
Molekularbiologie ist. Tatsächlich<br />
wurde erstmals im Jahr 1893<br />
von dem New Yorker Arzt William<br />
B. Coley das Immunsystems<br />
<strong>in</strong> den Kampf gegen Krebs<br />
e<strong>in</strong>gebunden 2 . Auch dieses damalige<br />
Konzept beruhte – selbst<br />
wenn es die Ärzte nicht wussten<br />
– auf dem Pr<strong>in</strong>zip <strong>der</strong> Gefahrensignale.<br />
Sie <strong>in</strong>okulierten hitze<strong>in</strong>aktivierte<br />
Bakterien <strong>in</strong> Tumore,<br />
lösten dadurch e<strong>in</strong>e massive Entzündung<br />
aus und konnten so die<br />
Tumoren vorübergehend zum<br />
Schrumpfen br<strong>in</strong>gen. Für lange<br />
Zeit was „Coley’s Tox<strong>in</strong>“ die e<strong>in</strong>zige<br />
nichtchirurgische Methode zur<br />
Krebsbehandlung. Die zytostatische<br />
Chemotherapie entstand<br />
erst viel später aus den Giftgase<strong>in</strong>sätzen<br />
<strong>der</strong> beiden Weltkriege;<br />
L<strong>in</strong>earbeschleuniger machten die Bestrahlungsbehandlung<br />
erst <strong>in</strong> <strong>der</strong> zweiten<br />
Hälfte des letzten Jahrhun<strong>der</strong>ts möglich.<br />
Bis heute ist e<strong>in</strong>e Inokulation von BCG <strong>in</strong><br />
die Harnblase e<strong>in</strong>e Standardtherapie für<br />
das Harnblasenkarz<strong>in</strong>om.<br />
Natürlich beruhen auch an<strong>der</strong>e Behandlungen<br />
auf immunologischen Pr<strong>in</strong>zipien.<br />
Am offensichtlichsten ist das wohl bei<br />
den monoklonalen Antikörpern. Diese<br />
wurden erstmals Ende <strong>der</strong> 1990er Jahre<br />
<strong>in</strong> die Krebsbehandlung e<strong>in</strong>geführt und<br />
s<strong>in</strong>d heute nicht mehr wegzudenken.<br />
Die Transplantation hämatopoetischer<br />
Stamm zellen zur Krebsbehandlung ist<br />
im Pr<strong>in</strong>zip auch e<strong>in</strong>e Immuntherapie.<br />
Nicht die vor <strong>der</strong> Transplantation durchgeführte<br />
<strong>in</strong>tensive Chemotherapie kann<br />
e<strong>in</strong>e Leukämie endgültig elim<strong>in</strong>ieren –<br />
dazu bedarf es <strong>der</strong> „Graft versus Leukemia“-Reaktion.<br />
Das transplantierte Immunsystem<br />
attackiert und zerstört die<br />
Leukämiezellen. Wenn ke<strong>in</strong>e „Graft versus<br />
Leukemia“-Reaktion auftritt, wie etwa<br />
bei Spenden zwischen e<strong>in</strong>eiigen<br />
Zwill<strong>in</strong>gen, kommt es sehr oft zu e<strong>in</strong>em<br />
Rezidiv <strong>der</strong> Krankheit.<br />
4/10 SPECTRUM ONKOLOGIE<br />
25