Elektronischer Sonderdruck für p53 unterdrückt die Bildung von Typ-II
Elektronischer Sonderdruck für p53 unterdrückt die Bildung von Typ-II
Elektronischer Sonderdruck für p53 unterdrückt die Bildung von Typ-II
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
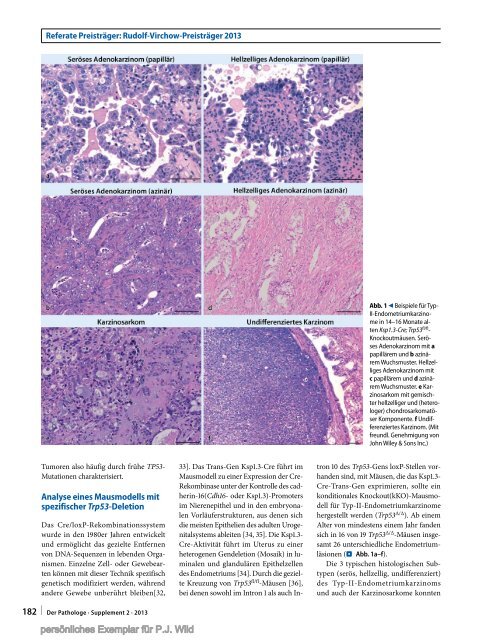
Referate Preisträger: Rudolf-Virchow-Preisträger 2013Abb. 1 9 Beispiele <strong>für</strong> <strong>Typ</strong>-<strong>II</strong>-Endometriumkarzinomein 14–16 Monate altenKsp1.3-Cre; Tr<strong>p53</strong> fl/fl -Knockoutmäusen. SerösesAdenokarzinom mit apapillärem und b azinäremWuchsmuster. HellzelligesAdenokarzinom mitc papillärem und d azinäremWuchsmuster. e Karzinosarkommit gemischterhellzelliger und (heterologer)chondrosarkomatöserKomponente. f UndifferenziertesKarzinom. (Mitfreundl. Genehmigung <strong>von</strong>John Wiley & Sons Inc.)Tumoren also häufig durch frühe TP53-Mutationen charakterisiert.Analyse eines Mausmodells mitspezifischer Tr<strong>p53</strong>-DeletionDas Cre/loxP-Rekombinationssystemwurde in den 1980er Jahren entwickeltund ermöglicht das gezielte Entfernen<strong>von</strong> DNA-Sequenzen in lebenden Organismen.Einzelne Zell- oder Gewebeartenkönnen mit <strong>die</strong>ser Technik spezifischgenetisch modifiziert werden, währendandere Gewebe unberührt bleiben[32,33]. Das Trans-Gen Ksp1.3-Cre führt imMausmodell zu einer Expression der Cre-Rekombinase unter der Kontrolle des cadherin-16(Cdh16-oder Ksp1.3)-Promotersim Nierenepithel und in den embryonalenVorläuferstrukturen, aus denen sich<strong>die</strong> meisten Epithelien des adulten Urogenitalsystemsableiten [34, 35]. Die Ksp1.3-Cre-Aktivität führt im Uterus zu einerheterogenen Gendeletion (Mosaik) in luminalenund glandulären Epithelzellendes Endometriums [34]. Durch <strong>die</strong> gezielteKreuzung <strong>von</strong> Tr<strong>p53</strong> fl/fl -Mäusen [36],bei denen sowohl im Intron 1 als auch Intron10 des Tr<strong>p53</strong>-Gens loxP-Stellen vorhandensind, mit Mäusen, <strong>die</strong> das Ksp1.3-Cre-Trans-Gen exprimieren, sollte einkonditionales Knockout(kKO)-Mausmodell<strong>für</strong> <strong>Typ</strong>-<strong>II</strong>-Endometriumkarzinomehergestellt werden (Tr<strong>p53</strong> Δ/Δ ). Ab einemAlter <strong>von</strong> mindestens einem Jahr fandensich in 16 <strong>von</strong> 19 Tr<strong>p53</strong> Δ/Δ -Mäusen insgesamt26 unterschiedliche Endometriumläsionen(. Abb. 1a–f).Die 3 typischen histologischen Subtypen(serös, hellzellig, undifferenziert)des <strong>Typ</strong>-<strong>II</strong>-Endometriumkarzinomsund auch der Karzinosarkome konnten182 | Der Pathologe · Supplement 2 · 2013