PHYSIQUE-CHIMIE
Sujet de Physique-Chimie MP 2009 - Concours Centrale-Supélec
Sujet de Physique-Chimie MP 2009 - Concours Centrale-Supélec
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>PHYSIQUE</strong>-<strong>CHIMIE</strong><br />
Filière MP<br />
Pour ce faire, calculer le volume<br />
Ten o C<br />
minimum V d’ammoniac à 100<br />
S<br />
mettre au contact d’un litre 90<br />
d’eau liquide, l’ensemble étant<br />
80<br />
maintenu à 0°C. Calculer la<br />
masse du mélange liquide ainsi<br />
70<br />
obtenu. Commenter la valeur de 60<br />
V S et proposer un argument<br />
50<br />
microscopique pour expliquer<br />
40<br />
cette hydrosolubilité de NH 3 .<br />
Pour cette question, on prendra 30<br />
la masse volumique de l’eau<br />
20<br />
liquide égale à 1000 kg ⋅ m – 3 .<br />
10<br />
d) Pour simuler des conditions<br />
0<br />
plus anciennes dans l’histoire de<br />
Titan, on porte la phase liquide −10<br />
de l’échantillon précédent à<br />
−20<br />
40°C. Déterminer la masse de<br />
−30<br />
liquide et de vapeur obtenues,<br />
ainsi que leur composition en<br />
−40<br />
x<br />
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0 H 2O<br />
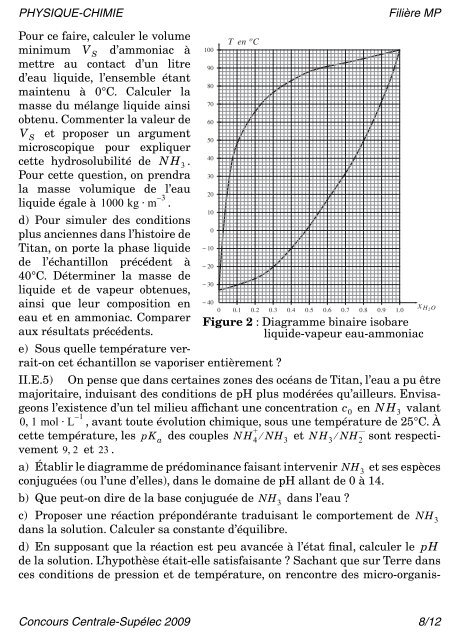
eau et en ammoniac. Comparer Figure 2 : Diagramme binaire isobare<br />
aux résultats précédents.<br />
liquide-vapeur eau-ammoniac<br />
e) Sous quelle température verrait-on<br />
cet échantillon se vaporiser entièrement ?<br />
II.E.5) On pense que dans certaines zones des océans de Titan, l’eau a pu être<br />
majoritaire, induisant des conditions de pH plus modérées qu’ailleurs. Envisageons<br />
l’existence d’un tel milieu affichant une concentration c 0 en NH 3 valant<br />
0,<br />
1 mol ⋅ L – 1 , avant toute évolution chimique, sous une température de 25°C. À<br />
+ —<br />
cette température, les pK a<br />
des couples NH 4 ⁄ NH3 et NH 3 ⁄ NH 2<br />
sont respectivement<br />
92 , et 23 .<br />
a) Établir le diagramme de prédominance faisant intervenir NH 3<br />
et ses espèces<br />
conjuguées (ou l’une d’elles), dans le domaine de pH allant de 0 à 14.<br />
b) Que peut-on dire de la base conjuguée de NH 3<br />
dans l’eau ?<br />
c) Proposer une réaction prépondérante traduisant le comportement de NH 3<br />
dans la solution. Calculer sa constante d’équilibre.<br />
d) En supposant que la réaction est peu avancée à l’état final, calculer le pH<br />
de la solution. L’hypothèse était-elle satisfaisante ? Sachant que sur Terre dans<br />
ces conditions de pression et de température, on rencontre des micro-organis-<br />
Concours Centrale-Supélec 2009 8/12