Nuance Communications, Inc.
Nuance Communications, Inc.
Nuance Communications, Inc.
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Para alcanzar el exito en el diagnostico micologico<br />
es fundamental realizar adecuadamente la<br />
recogida de la muestra, su transporte y procesamien-<br />
to, la siembra de la misma en los medios idoneos y a<br />
la temperatura adecuada, asf como la identificacion<br />
e interpretacion correcta de los aislamientos.<br />
A la hora de valorar un crecimiento fungico,<br />
hay que tener siempre presente la necesidad de dife-<br />
renciar un “aislamiento significativo” de otros debi-<br />
dos a hongos contaminantes, ya que no es lo mismo<br />
identificar una especie fungica que diagnosticar una<br />
micosis.<br />
En este Capftulo se detallan los fundamentos<br />
y recomendaciones basicas del diagnostico micologico<br />
y en los siguientes, las caracterfsticas especffi-<br />
cas del procesam iento de cada m uestra segun el<br />
origen anatomico de la misma.<br />
3.1. Recogida de muestras<br />
El diagnostico de las micosis comienza con<br />
su sospecha clmica por lo que una adecuada obten-<br />
cion de la muestra, a partir de la lesion, y su correcta<br />
manipulacion, para mantener la viabilidad del<br />
agente etiologico y evitar posibles contaminaciones,<br />
son aspectos fundam entales que siem pre deben<br />
tenerse en cuenta para la obtencion de un correcto<br />
diagnostico micologico.<br />
No debe olvidarse la importancia de etiquetar<br />
y rellenar adecuadamente el volante de petition, de<br />
forma que refleje claramente la sospecha clmica y<br />
los factores predisponentes del paciente; destacan-<br />
do, si los hubiera, la existencia de tratamientos que<br />
pudieran interferir en el aislamiento del miceto.<br />
3.1.2, Consejos generales para optimizar<br />
la recogida de muestras<br />
1. Debe disponerse de un protocolo de recogida de<br />
muestras actualizado periodicamente.<br />
2. Es necesario recoger las muestras asepticamente,<br />
utilizando contenedores esteriles, remitirlas al<br />
laboratorio antes de 2 h y sembrarlas lo antes<br />
posible.<br />
Antonio Rezusta Lopez<br />
Aurora Sanchez Sousa<br />
Joaquina Gil Tomas<br />
Asociacion Espanola de M icologia<br />
3. La muestra debe recogerse antes de instaurar el<br />
tratamiento y siempre de la parte activa de la<br />
lesion (cuando se sospecha una micosis pulmo-<br />
nar es preferible una muestra respiratoria antes<br />
que un hemocultivo).<br />
4. Los hisopos deben ser evitados, siempre que el<br />
tipo de lesion lo perm ita. Pero hay muestras<br />
(conducto auditivo, faringe, vagina o cervix) que<br />
no pueden ser recogidas de otra manera.<br />
5. En el caso de heridas abiertas, drenajes o lesio-<br />
nes superficiales, debe limpiarse la zona previa-<br />
mente para evitar contaminaciones.<br />
6. Las muestras de lesiones cerradas y abscesos<br />
suelen ser de gran rendimiento. Deben ser aspi-<br />
radas con jeringa y transferidas a un contenedor<br />
esteril, prestando atencion a la recogida de gra-<br />
nulos, si los hubiese.<br />
7. El raspado de lesiones de piel y faneras puede<br />
realizarse con distintos materiales; los mas utili-<br />
zados son bistun, moqueta o cepillo.<br />
8. En situaciones que requieran un estudio epide-<br />
miologico, debe establecerse la necesidad de una<br />
recogida de muestras ambientales, familiares o<br />
de animales.<br />
3.2. Transporte de las muestras<br />
Las muestras deben ser transportadas en un<br />
recipiente esteril, humidificado y a prueba de verti-<br />
dos; sin embargo, las muestras dermatologicas pueden<br />
transportarse en un recipiente seco (placa de<br />
Petri, papel de fotografi'a negro, entre dos portas,<br />
etc.) o, de forma ideal, sembrada directamente sobre<br />
el medio de cultivo.<br />
No deben introducirse en medios de transporte,<br />
a no ser que sea facil retirar la muestra del<br />
medio.<br />
Los raspados corn eales y h em ocultivos<br />
deben sembrarse directamente en el medio de cultivo<br />
adecuado.<br />
Las muestras, una vez obtenidas, deben sembrarse<br />
lo antes posible despues de la recogida.<br />
Aunque hay pocos estudios sobre el descenso de la
Fundamentos basicos para el diagnostico micologico<br />
viabilidad de los hongos a temperatura ambiente o<br />
por la accion del hielo seco, es conocida la dificul-<br />
tad de recuperar Rhizopus arrhizus en m uestras<br />
demoradas y, tambien, la perdida de viabilidad de<br />
algunos hongos por la desecacion, temperatura ele-<br />
vada (>37 °C) o baja (
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Tabla 3.1. Medios de cultivo basicos recomendados.<br />
Micosis superficiales « Agar glucosado de Sabouraud (SDA) + cloranfenicol (SDAC)<br />
Agar glucosado de Sabouraud + cloranfenicol + cicloheximida (Mycobiotic®,<br />
Mycosel®)<br />
Dermatophyte test medium (DTM), opcional<br />
Ante la sospecha de Malassezia utilizar medio de Leeming (LNA) o de Dixon<br />
modificado (mDixon), en el caso de pitiriasis no es necesario el cultivo para el<br />
diagnostico<br />
Para la deteccion de Candida en las muestras mucocutaneas, la utilizacion de<br />
medios cromogenicos facilita la deteccion de cultivos mixtos, y la identificacion<br />
rapida<br />
Micosis subcutaneas * SDA, SDAC, Mycobiotic o Mycosel (MYC), Agar infusion cerebro-corazon (BHIA)<br />
Micosis sistemicas * SDAC<br />
* BHIA (Dimorficos)<br />
* Agar de Staib (Cryptococcus)<br />
- BHIA con antibacterianos e, incluso, con cicloheximida en muestras muy contami-<br />
nadas (Dimorficos)<br />
* LNA o mDixon (Malassezia)<br />
Miscelanea « SDAC<br />
(aspergilosis, mucormicosis, otomicosis)<br />
detallan las caracterfsticas de las tecnicas de exa-<br />
men microscopico mas utilizadas en Micologfa.<br />
Las limitaciones y los problemas del examen<br />
microscopico tambien deben ser tenidos en cuenta:<br />
i) un examen negativo no excluye la infection;<br />
ii) el examen microscopico puede originar falsos<br />
positivos al confundirse ciertas estructuras con<br />
elem entos fungicos (lin fo cito s lisados por<br />
Cryptococcus neoformans en la tincion con tinta<br />
china, fibras de colageno o del hisopo pueden<br />
confundirse con elementos fungicos, gotas de<br />
grasa con levaduras gemantes, etc);<br />
iii) si la muestra es escasa, el cultivo debe ser priori-<br />
tario.<br />
El examen microscopico debe realizarse, al<br />
menos, en todas las muestras con alta sospecha de<br />
micosis; aunque lo ideal serfa realizarlo siempre que<br />
fuese posible.<br />
Las muestras para estudio micologico deben<br />
ser examinadas tanto macroscopica como microsco-<br />
picamente:<br />
Observacion macroscopica<br />
Antes de inocular los medios de cultivo y<br />
realizar el examen microscopico, la muestra debe<br />
ser examinada en busca de granulos, material caseo-<br />
so, purulento, hemorragico o necrotico.<br />
Asociacion Espanola de M icologia<br />
Examen microscopico<br />
La observacion microscopica se realiza con<br />
bajo aumento, seguida de alto aumento en seco y, si<br />
es necesario, con objetivo de inmersion. Las dos<br />
formas observadas habitualmente son levaduras y/o<br />
elementos miceliares.<br />
Es aconsejable utilizar periodicamente con-<br />
troles positivos y negativos y, si una tincion se<br />
emplea ocasionalmente, deben emplearse siempre<br />
controles que aseguren su correcta utilizacion.<br />
Aunque es muy dificil identificar una especie<br />
fungica por la morfologfa observada en el examen<br />
microscopico directo de la muestra, algunas estructuras<br />
pueden asociarse a ciertos generos o especies:<br />
Levaduras<br />
a. Celulas, con o sin gemas, de varios tamanos y<br />
formas, posiblemente sean Candida spp. u hon-<br />
gos dimorficos.<br />
b. Celulas de pared gruesa, generalmente con una<br />
gema de base amplia, podrfan corresponder a<br />
Blastomyces dermatitidis.<br />
c. Celulas de pared delgada con gemacion multiple<br />
rodeando a la celula madre, posiblemente sean<br />
Paracoccidioides brasiliensis.<br />
d. Celulas rodeadas de una capsula grande, proba-<br />
blemente corresponden a C. neoformans.<br />
e. Celulas pequenas, de gemacion simple observadas<br />
en tinciones especiales, posiblemente son<br />
Histoplasma capsulatum.
Fundamentos basicos para el diagnostico micologico<br />
f. C elu las con p seudohifas: C andida spp.,<br />
Geotrichum spp., o Trichosporon spp. Las dos<br />
ultimas pueden mostrar artrosporas.<br />
g. C elulas redondas de pared gruesa de varios<br />
tamanos, algunas de las cuales (las mas grandes)<br />
pueden contener esporas podrfan tratarse de<br />
esferulas de Coccidioides immitis. Sin embargo.<br />
Rhinosporidium seeberi tambien puede mostrar<br />
esferulas grandes y endosporas.<br />
Elementos miceliales<br />
(con o sin otras estructuras asociadas)<br />
a. Hifas no septadas, de pared gruesa, algunas de<br />
las cuales pueden mostrar ramificaciones en 90°:<br />
Rhizopus spp., Mucor spp., Absidia spp.<br />
b. Hifas septadas, ramificadas, algunas en V, con o<br />
sin cabezas de Aspergillus, posiblemente corres-<br />
pondan a Aspergillus spp.<br />
c. Hifas septadas, pigmentadas (marrones oscuras)<br />
con o sin cuerpos esfericos, probablemente sean<br />
de hongos dematiaceos.<br />
d. Racimos de pared gruesa y oscura, con aparien-<br />
cia de gemas, posiblemente pertenezcan a un<br />
agente de cromomicosis.<br />
e. Fragmentos de hifas con o sin esporas, con o sin<br />
levaduras probablemente correspondan a derma-<br />
tofitos o a M. furfur complex.<br />
Las tecnicas mas habitualm ente utilizadas<br />
para la observacion microscopica de las muestras se<br />
resumen en la Tabla 3.2 y se comentan detallada-<br />
mente en el Capftulo 14.<br />
Tabla 3,2. T ecnicas de o b se rva cio n m icro sco p ica .<br />
En fresco Tinciones<br />
3.4. Medios de cultivo<br />
El objetivo fundamental de la utilization de<br />
los medios de cultivo es optimizar el crecimiento de<br />
los microorganismos. El primer medio de cultivo<br />
que perm itio el aislam iento de los germ enes en<br />
medios artificiales fue el propuesto por Koch, en<br />
1876, basado en el uso de gelatina. Posteriormente,<br />
Frost en 1909 utilizo medios deshidratados y, en<br />
1919, anadio agar, lo que proporciono un gran avan-<br />
ce en el estudio de la microbiologfa.<br />
La composicion basica de un medio incluye<br />
nutrientes, agente solidificante (en los medios soli-<br />
dos o semisolidos), pH adecuado y componentes<br />
especfficos. En los medios de cultivo para el aislamiento<br />
de hongos, los antimicrobianos se utilizan<br />
con frecuencia, tanto para inhibir el crecimiento<br />
bacteriano como el de otros hongos ambientales.<br />
Atendiendo a su composicion, los medios de cultivo<br />
puede ser generales, enriquecidos, selectivos, dife-<br />
renciales y especializados:<br />
A. Generales: El mas caracterfstico y clasico es el<br />
agar glucosado de Sabouraud (SDA) y su equi-<br />
valente en EEUU, el medio para mohos. Ambos<br />
se utilizan frecuentemente para el aislamiento a<br />
partir de la muestra y para la description de las<br />
caracterfsticas de la mayorfa de los hongos.<br />
B. Enriquecidos: Se utilizan especialm ente en<br />
micosis sistemicas endemicas (histoplasmosis,<br />
coccidioidomicosis, etc.), un ejemplo es la infusion<br />
cerebro-corazon (BHI).<br />
• KOH<br />
KOH + tinta Parker, KOH + bianco calcofluor:<br />
Uso general<br />
* KOH + tinta Parker<br />
• Giemsa: micetoma, histoplasmosis, coccidioidomicosis,<br />
KOH + bianco calcofluor Pneumocystis, otras micosis cutaneas con exudado o pus<br />
• Tinta china (Cryptococcus) • PAS: micetoma, coccidioidomicosis, onicomicosis<br />
• Grocott: Pneumocystis<br />
• Fontana Masson: Pneumocystis<br />
• Inmunofluorescencia: Pneumocystis<br />
©2004 Revista Iberoamericana de Micologfa - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
C. Selectivos: Son medios que favorecen el aisla-<br />
miento de los microorganismos deseados impi-<br />
diendo el de o tro s. L os com p o n entes mas<br />
utilizados como agentes selectivos son antibac-<br />
terianos (cloranfenicol, gentamicina, penicilina,<br />
estreptomicina) y tambien inhibidores de hon-<br />
gos, como la cicloheximida que es especialmen-<br />
te util en las muestras cutaneas y respiratorias de<br />
micosis sistemicas endemicas.<br />
E. Diferenciales: Se utilizan para ayudar a la identification<br />
del hongo basada en la apariencia de<br />
este en dicho medio, merced a la adicion de<br />
determinados componentes como por ejemplo<br />
sustancias crom ogenas, o indicadores de pH<br />
como en el DTM (que tambien es selectivo).<br />
F. Especializados: Son aquellos medios que con-<br />
tienen algun componente (Guizotia abyssinica)<br />
d estin ad o a a isla r un agente co n creto<br />
(Cryptococcus neoform ans) o a favorecer la<br />
identification de ciertas especies (m edio de<br />
Czapeck).<br />
3.4.1. Preparacion de los medios de cuitivo<br />
La buena calidad de los medios es indispensable<br />
para conseguir el aislamiento y la identificacion<br />
en Micologfa; por lo tanto, cuando se utilicen<br />
medios comerciales es necesario tener en cuenta la<br />
garantfa que aporta el proveedor y la calidad de la<br />
distribution.<br />
Cuando se prepara un medio deshidratado<br />
deben seguirse rigurosamente las instrucciones del<br />
fabricante, evitando errores en la forma de disolver-<br />
lo o suspenderlo, en la temperatura y/o duration de<br />
la esterilizacion, para preservar la calidad del pro-<br />
ducto final. La esterilizacion en autoclave es mas<br />
eficaz si se utilizan frascos de volumenes inferiores<br />
a 500 ml; si se han utilizado imanes para la disolu-<br />
cion, deben retirarse antes de introducir los medios<br />
en el autoclave. Tambien hay que tener presente que<br />
algunos antibioticos deben anadirse al medio una<br />
vez esterilizado y a la temperatura adecuada, para<br />
no ser desactivados por las altas temperaturas de la<br />
esterilizacion.<br />
3.4.2. Control de calidad<br />
Para asegurar la correcta utilization de los<br />
medios, debe controlarse periodicamente sus carac-<br />
terfsticas mas importantes: apariencia, esterilidad,<br />
pH y funcionamiento. El funcionamiento se puede<br />
evaluar utilizando las cepas de control adecuadas<br />
para cada medio. En este proceso se recomienda<br />
Asociacion Espanola de M icologia<br />
seguir las especificaciones del documento M22-A<br />
del NCCLS en aquellos casos en los que esta esta-<br />
blecido [3],<br />
Los controles de calidad deben realizarse<br />
tanto, a los medios elaborados en el laboratorio,<br />
como a los medios comerciales ya preparados; en<br />
este caso, es conveniente solicitar al fabricante los<br />
controles a utilizar y los resultados para el lote<br />
sum inistrado. En el Capftulo 18 de esta Gufa se<br />
detallan todos los aspectos del control de calidad de<br />
los medios de cuitivo.<br />
3.4.3. Soporte de los medios de cuitivo<br />
El soporte habitual para los medios de cuitivo<br />
en Micologfa suele ser tubos de cristal o placas<br />
de Petri (90 mm). La election depende del usuario;<br />
autores como De Hoog y Guarro proponen el uso<br />
habitual de placas excepto, por razones de seguri-<br />
dad, en los casos de sospecha de histoplasmosis,<br />
coccidioidomicosis, blastomicosis, paracoccidioido-<br />
micosis e infecciones por Penicillium marneffei [4],<br />
Si se utilizan tubos, deben incubarse en position<br />
horizontal las primeras 24 h para que el inoculo<br />
no se concentre en el fondo. Los tubos no deben ser<br />
los habituales de Microbiologfa porque, en ellos, las<br />
colonias no son faciles de aislar. Si los tubos utilizados<br />
son de tapon de rosea, el cierre debe mantenerse<br />
parcialm ente abierto para garantizar las mejores<br />
condiciones atmosfericas.<br />
Cuando se eligen placas, es conveniente que<br />
contengan 40 ml de medio para evitar que se sequen<br />
y deben sellarse con cinta adhesiva para que no se<br />
abran involuntariamente. El precintado debe ser permeable<br />
al aire, ya que cuando el aire circula libre-<br />
mente se favorece la production de pigmento y la<br />
superficie del agar se seca, permitiendo el desarrollo<br />
de micelio aereo y esporas.<br />
3.4.4. Almacenamiento<br />
Los medios se deben guardar refrigerados a<br />
2-8 °C. Para mejorar su conservation y prevenir la<br />
desecacion, es aconsejable invertir las placas e<br />
introducirlas en bolsas de plastico.<br />
Las placas de Petri suelen conservarse en<br />
buen estado unos tres m eses, m ientras que los<br />
medios semisolidos o lfquidos en tubo de rosea se<br />
conservan bien hasta seis meses. Sin embargo, cier-<br />
tos medios, al contener sustancias inestables (antibioticos,<br />
vitaminas, sangre, etc.), no se conservan en<br />
buen estado tanto tiempo. Tambien hay que tener
Fundamentos basicos para el diagnostico micologico<br />
presente que algunos com ponentes de cierto s<br />
medios pueden verse afectados por la luz, por lo que<br />
estos medios deben almacenarse en contenedores<br />
opacos.<br />
Com o norm a g eneral, todos los m edios<br />
deben utilizarse antes de la fecha de caducidad indi-<br />
cada por el fabricante y, antes de su utilizacion,<br />
deben atemperarse, durante unos minutos, a tempe-<br />
ratura ambiente.<br />
3.4.5. Eleccion de los medios de cultivo<br />
Los medios mas utilizados en el cultivo de<br />
hongos son: agar glucosado de Sabouraud, habitual-<br />
mente con la modificacion de Emmons (SDA); agar<br />
infusion cerebro-corazon (BHIA) con o sin sangre<br />
de cordero al 5%, con o sin antibacterianos; agar<br />
in h ib id o r p ara m ohos (M IA ); agar<br />
M ycosel/M ycobiotic y agar glucosado de patata<br />
(PDA). Sin embargo, los hongos tambien pueden<br />
crecer en medios no selectivos, incluidos la mayorfa<br />
de los medios bacteriologicos, si se incuban el tiem-<br />
po suficiente.<br />
La eleccion y el numero de medios a utilizar<br />
estan condicionados por el coste, la disponibilidad y<br />
las preferencias personales, pero siempre se deben<br />
incluir medios con antibacterianos y sin ellos.<br />
La incorporacion de cicloheximida, inhibidor<br />
de muchos hongos considerados contam inantes,<br />
ayuda especialmente en las micosis de la piel, aun-<br />
que pueda inhib ir algunos patogenos fungicos<br />
importantes; por ello, debe utilizarse siempre en<br />
combination con otro medio sin cicloheximida.<br />
El aislamiento de algun hongo puede verse<br />
dificultado por otros factores como la acidification<br />
del medio utilizado (para impedir el crecimiento de<br />
bacterias) o, en el caso de Malassezia spp., la utilizacion<br />
de gentamicina. [5]<br />
Los medios mas em pleados en M icologfa<br />
pueden agruparse en dos categories en funcion de su<br />
utilidad: aislamiento e identificacion. Para el aislamiento,<br />
la utilizacion de 3-4 medios practicamente<br />
cubre todas las necesidades: SDA con/sin antimicro-<br />
bianos (el mas utilizado en Europa y sustituido con<br />
frecuencia en EE.UU. por M IA); un medio con<br />
cicloheximida y agar infusion cerebro corazon, para<br />
las micosis sistemicas endemicas.<br />
Sin embargo, en ciertas situaciones es reco-<br />
mendable la utilizacion de otros medios:<br />
i) LNA, Dixon, o SDAC con aceite de oliva para el<br />
aislamiento de Malassezia',<br />
ii) medio cromogenico en las muestras de mucosas,<br />
para facilitar el diagnostico de infecciones mixtas,<br />
iii) medio para Cryptococcus, para facilitar su detec-<br />
cion en muestras donde es frecuente el aisla-<br />
miento de otras levaduras (muestras respiratorias).<br />
Para la identificacion, puede ser necesario un<br />
numero mayor de medios que dependera del numero<br />
de muestras, las etiologfas mas probables en la zona<br />
geografica, las posibilidades del laboratorio y el<br />
nivel diagnostico esperable segun el tipo de centra.<br />
3.4.6. Medios de cultivo mas utilizados<br />
A continuation se detallan las principales<br />
indicaciones, composition, forma de preparation y<br />
los controles de calidad de los medios de cultivo<br />
mas utilizados en el laboratorio de Micologfa clfni-<br />
ca. Los m edios com erciales pueden p resentar<br />
pequenas variaciones respecto a lo expuesto en los<br />
cuadros.<br />
3.4.7. <strong>Inc</strong>ubacion<br />
La temperatura optima de crecimiento de la<br />
m ayorfa de los hongos p ato g en o s es 30 °C.<br />
Sin embargo, Sporothrix schenckii es una exception,<br />
crece mas rapido a 27-28 °C.<br />
Hay laboratories que utilizan la temperatura<br />
ambiente en lugar de 30 °C, pero no es recomenda-<br />
ble, ya que en los cambios de temperatura son notables<br />
entre el dfa y de la noche en la mayorfa de los<br />
laboratorios. La temperatura de 37 °C no se reco-<br />
m ienda por dos razones principales: 1) m uchas<br />
muestras contienen abundantes bacterias que crecen<br />
muy bien a esta temperatura y 2) algunos hongos<br />
crecen mal a esta temperatura o no crecen, especialmente<br />
los hongos que infectan la piel [9],<br />
No hay ventaja en incubar simultaneamente a<br />
30 °C y a 37 °C. La tem peratura de 37 °C debe<br />
reservarse para hongos dimorficos o algun hongo<br />
que se desarrolle mejor a esta tem peratura [10].<br />
Una estufa a 37 °C es tambien necesaria para verifi-<br />
car la tolerancia a esta temperatura. Sin embargo,<br />
utilizar 37 °C para el aislamiento del estadio levadu-<br />
riforme de Histoplasma o Blastomyces no aporta<br />
ventajas y, ademas, son morfologicamente indistin-<br />
guibles de otras levaduras [9].<br />
Si la estufa no esta humedecida, es conve-<br />
niente poner un recipiente con agua cerca de las pla-<br />
cas de cultivo. [10]. Los cultivos de hongos deben<br />
incubarse durante 3-4 semanas antes de ser desecha-<br />
dos. Los cultivos no deben desecharse cuando se<br />
afsla un hongo, debe com pletarse el periodo de<br />
incubacion [11]. Sin embargo, hay muestras que se<br />
pueden elim inar a los 7 dfas de form a habitual<br />
(orina y exudados de mucosas).<br />
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Agar agua<br />
Estimula la formacion de conidios. Recomendable para hifomicetes de pigmentacion oscura (dematiaceos) e incluso<br />
para dermatofitos poco o nada esporulados. Favorece la esporulacion de hongos saprofitos.<br />
Composicion<br />
Agar 20 g<br />
Agua destilada 1.000 ml<br />
Preparacion<br />
a) Calentar hasta disolver todos los componentes.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en placas de Petri.<br />
d) De forma opcional, se pueden depositar fragmentos de papel esteril en la superficie del medio solidificado.<br />
C o n tro l de calidad<br />
Aspecto: solido transparente.<br />
Microsporum canis: abundante produccion de macroconidios principalmente en la zona de contacto entre el agar agua y<br />
los bordes del fragmento de colonia poco o nada esporulada.<br />
Agar Czapek Dox*<br />
Se utiliza en el cultivo de hongos saprofitos, especialmente Aspergillus spp. y Penicillium spp. Es el medio de referencia<br />
para la identificacion de Aspergillus spp.<br />
C o m posicion<br />
Nitrato sodico (NOsNa) 3 g<br />
Fosfato dipotasico (PO4K2H) 1 9<br />
Sulfato magnesico (SOtMgJHUO) 0,5 g<br />
Cloruro potasico (CIK) 0,5 g<br />
Sulfato ferroso (SOiFe./hbO) 0,01 g<br />
Sacarosa 30 g<br />
Agar 15 g<br />
Agua desionizada 1.000 ml<br />
P reparacion<br />
a) Calentar hasta disolver todos los componentes.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en placas de Petri.<br />
C o n tro l de calidad<br />
Apariencia: Ambar palido, solido trasparente.<br />
pH final a 25 °C: 7,3 ± 0,2.<br />
Aspergillus flavus: crece, colonia amarilla-verde.<br />
(*) Disponible comercialmente (Becton Dickinson, Difco, Merck, Remel)<br />
Asociacion Espahola de M icologia
Fundamentos basicos para el diagnostico micologico<br />
Agar Dixon modificado (mDixon)<br />
Utilizado en el cultivo de Malassezia spp. Puede modificarse anadiendo cloranfenicol o bien cloranfenicol y cicloheximida.<br />
C om posicion<br />
Extracto de malta 36 g<br />
Peptona 6 g<br />
Ox bile, desecada 20 g<br />
Tween 40 10 ml<br />
Glicerol 2 ml<br />
Acido oleico 2 ml<br />
Agar 12 g<br />
Agua desionizada 1.000 ml<br />
P reparacion<br />
a) Calentar hasta disolver todos los componentes.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en placas de Petri.<br />
C ontrol de calidad<br />
Aspecto: Blanco amarillento, no muy solido.<br />
pH final: 6,0<br />
Malassezia restricts: Crece.<br />
En el medio inhibidor:<br />
M. restricts. Crece.<br />
Aspergillus flavus: Inhibicion parcial o completa.<br />
Staphylococcus epidermidis: Inhibicion parcial o completa.<br />
Comprobar el crecimiento de las 7 especies.<br />
Agar extracto de malta (MEA)*<br />
Medio para el aislamiento y recuento de levaduras y hongos miceliares. Adecuado para la identificacion de zigomice-<br />
tes, y especies de Aspergillus, Penicillium, Paecilomyces, etc. Se han descrito varias formulaciones que incluyen el<br />
extracto de malta y agar suplementados con peptonas, maltosa y/o dextrina y/o glicerol.<br />
C o m posicion<br />
Extracto de malta<br />
Peptona<br />
Glucosa<br />
Agar<br />
Agua destilada<br />
P reparacion<br />
a) Calentar hasta disolver todos los componentes.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Enfriar a 45 QC.<br />
d) Dispensar en placas de Petri.<br />
Importante: no recalentar.<br />
C ontrol de calidad<br />
Aspecto: ambar, transparente.<br />
pH final: 5,6 ±0,1.<br />
Aspergillus niger ATCC 9642: micelio bianco, conidias negras.<br />
Candida albicans ATCC10231: buen crecimiento, colonias crema.<br />
Si se desea ajustar el pH a 3,5, enfriar a 55gC anadir 2-3 ml de acido lactico al 10% a 100 ml de agar extracto de malta.<br />
Una vez acidificado no se debe volver a calentar.<br />
(*) Disponible comercialmente (Merck; Oxoid)<br />
20 g<br />
1 g<br />
20 g<br />
15 g<br />
1.000 ml<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para ei diagnostico micologico<br />
Agar glucosado de patata* (PDA)<br />
Es un medio utilizado para la estimulacion de la form ation de conidias, en la preparation de inoculos de hongos mice-<br />
lia le s y en la e s tim u la c io n de p ro d u c c io n de p ig m e n to s : ro jo en T ric h o p h y to n ru b ru m , ro s a s a lm o n en<br />
M icrosporum audouinii y amarillo en Microsporum canis. Se utiliza con frecuencia en microcultivos para observar las<br />
caracteristicas morfologicas.<br />
Composicion<br />
Patata<br />
Glucosa<br />
Agar<br />
Agua desionizada<br />
Preparacion<br />
a) Pelar las patatas, cortarlas en cubos y hervir en agua durante 1 h.<br />
b) Filtrar con papel Whatman nQ 2, anadir la glucosa y el agar y hervir hasta disolver el agar completamente.<br />
c) Ajustar el volumen a un litro.<br />
d) Esterilizar a 121 °C durante 15 min.<br />
C o n tro l de calidad<br />
20 0 g<br />
10 g<br />
18 g<br />
1.000 ml<br />
Aspecto: incoloro o amarillo suave, medio solido, transparente o translucido.<br />
pH final a 25 °C: 5,6 ± 0,2.<br />
M. audouinii-. pigmento salmon en el reverso de la colonia.<br />
T. rubrum: rojo intenso en el reverso de la colonia.<br />
T. mentagrophytes: pigmento marron en el reverso.<br />
(*) Disponible comercialmente (Becton Dickinson, bioMerieux, Merck, Oxoid, Remel)<br />
A g a r g lu c o s a d o d e S a b o u ra u d *<br />
Medio poco utilizado ya que normalmente se usa la m odification de Emmons.<br />
Puede no crecer Blastomyces dermatitidis.<br />
C o m posicion<br />
Peptona 10 g<br />
Glucosa 40 g<br />
Agar 15 g<br />
Agua desionizada 1.000 ml<br />
P reparacion<br />
a) Mezclar los ingredientes y hacerlos hervir hasta su disolucion completa.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en tubos o placas (si se utilizan tubos de cristal, tambien se puede dispensar antes de esterilizar).<br />
d) Solidificar en position inclinada.<br />
M o d ific a tio n<br />
Anadir cloranfenicol (50 mg/l).<br />
C o n tro l de calidad<br />
Aspecto: medio solido, ambar, transparente.<br />
pH final a 25 °C: 5,6 ± 0,2.<br />
Trichophyton mentagrophytes: crece.<br />
Staphylococcus epidermidis: inhibition partial o total en el medio con cloranfenicol.<br />
(*) Disponible comercialmente (Becton Dickinson, Fluka, Oxoid, Remel, Sigma)<br />
Asociacion Espahola de M icologia
Fundamentos basicos para el diagnostico micologico<br />
Agar glucosado de Sabouraud m odificado por Emmons* (SDA)<br />
Es el medio estandar para el aislamiento, esporulacion y conservacion de muchos hongos. El cambio en el pH y la<br />
concentration de glucosa favorece la esporulacion.<br />
C om posicion<br />
Peptona<br />
Glucosa<br />
Agar<br />
Agua desionizada<br />
P reparacion<br />
a) Mezclar los ingredientes y hacerlos hervir hasta su disolucion completa.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en tubos o placas (si se utilizan tubos de cristal, tambien se puede dispensar antes de esterilizar).<br />
d) Solidificar en posicion inclinada.<br />
M o d ifica cio n (SOAC)<br />
Anadir cloranfenicol (50 mg/l).<br />
C ontrol de calidad<br />
Aspecto: medio solido, ambar, transparente.<br />
pH final a 25 °C: 7,0 ±0,2.<br />
10 g<br />
20 g<br />
15 g<br />
1.000 ml<br />
Trichophyton mentagrophytes: crece.<br />
Staphylococcus epidermidis: inhibicion parcial o total en el medio con cloranfenicol.<br />
(*) Disponible comercialmente (Becton Dickinson, bioMerieux, Fluka, Oxoid, Remel)<br />
Agar harina de avena (OA)<br />
Favorece la esporulacion. Recomendable para la identification de especies de Acremonium, Cladosporium, Fusarium,<br />
Paecilomyces, Phialophora, Scopuiariopsis, etc. y para la obtencion de las formas teleomorficas asociadas.<br />
C o m posicion<br />
Harina de avena 30 g<br />
S04Mg.7H20 1 g<br />
PO4H2K 1,5 g<br />
Agar 15 g<br />
Agua destilada 1.000 ml<br />
P reparacion<br />
a) Hervir lentamente los 30 g de harina de avena en 1 I de agua durante 1 h.<br />
b) Filtrar y ajustar el volumen del caldo a 1 I.<br />
c) Anadir las sales y calentar hasta su disolucion.<br />
d) Esterilizar a 121 °C durante 15 min.<br />
e) Dispensar en placas de Petri.<br />
C o n tro l de calidad<br />
Aspecto: medio solido, blanquecino, opaco.<br />
Fusarium solani: crecimiento rapido, colonia bianco amarillenta, mucosa en el centra.<br />
Cladophialophora carrioni: crecimiento lento, colonia gris verdosa, pulverulenta.<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Agar harina de mai'z con Tween 80* (Corn Meal Agar, CMA)<br />
Se utiliza en el cultivo y diferenciacion de especies de Candida basandose en las caracteri'sticas miceliales. El Tween<br />
80 se incorpora para demostrar la formacion de clamidosporas. Si se le anaden 10 g de glucosa puede utilizarse en la<br />
diferenciacion de Trichophyton rubrum y Trichophyton mentagrophytes basandose en la produccion de pigmento.<br />
C o m posicion<br />
Harina de maiz 40 g<br />
Agar 20 g<br />
Tween 80 3 ml<br />
Agua desionizada 1.000 ml<br />
P reparacion<br />
a) Mezclar la harina de mai'z en agua.<br />
b) Hervir a fuego lento durante 1 h.<br />
c) Filtrar con gasa.<br />
d) Medir y completar hasta 1.000 ml..<br />
e) Esterilizara 121 "C durante 10 min. Filtrar.<br />
f) Anadir el agar y el Tween 80 y calentar hasta disolver.<br />
g) Esterilizar a 121 °C durante 15 min.<br />
h) Dipensar en placas de Petri.<br />
C o n tro l de calidad<br />
Candida albicans produce clamidosporas.<br />
(*) Disponible comercialmente (Becton Dickinson, Difco, Remel)<br />
Agar infusion de cerebro corazon* (BHIA)<br />
Puede utilizarse como medio enriquecido para aumentar los aislam ientos de Cryptococcus neoform ans a partir de<br />
muestras esteriles como el LCR. Mantenimiento de la fase levaduriforme de algunas micosis sistemicas, ya sea con<br />
sangre o sin ella. En general esta indicado para el aislamiento de una gran variedad de patogenos, incluyendo levaduras,<br />
mohos y bacterias como Nocardia. Adicionado de sangre de camera al 10%, se utiliza para el aislamiento de todos<br />
los hongos incluidos los dimorficos. Pueden anadirse antibacterianos (cloranfenicol y/o gentamicina) para convertirlo en<br />
selectivo. En algunas ocasiones tambien puede adicionarse cicloheximida (facilita el aislamiento de Histoplasma capsu-<br />
latum y Blastomyces dermatitidis).<br />
P reparacion<br />
a) Preparar de acuerdo con el fabricante.<br />
b) Hervir los componentes hasta su completa disolucion.<br />
c) Dispensar en matraces o tubos.<br />
d) Esterilizar a 121 °C durante 15 min.<br />
e) Enfriar en posicion inclinada, si se utilizan tubos.<br />
C o n tro l de calidad<br />
Aspecto: Ambar claro a semitransparente, sin precipitado (cuando no esta adicionado de sangre).<br />
pH final: 7,4 ±0,2.<br />
Neisseria meningitidis ATCC 13090: crecimiento aceptable a bueno.<br />
Candida albicans: crece bien.<br />
Sporothrix schenckii: conversion a levadura a 37 °C.<br />
(*) Disponible comercialmente. Tambien puede utilizarse en forma de caldo (Becton Dickinson, Biomedic, Difco, Fluka.Oxoid)<br />
Asociacion Espanola de M icologia
Fundamentos basicos para el diagnostico micologico<br />
Agar inhibidor para mohos* (MIA)<br />
Es un medio enriquecido con sales inorganicas, cloranfenicol y gentamicina. Se utiliza en el aislamiento de hongos sen-<br />
sibles a la cicloheximida (Cryptococcus, zigomicetos, etc.) de muestras contaminadas. Permite el desarrollo de la mayo-<br />
ria de los mohos y de las levaduras.<br />
C om posicion<br />
Triptona 3 g<br />
Extracto de came 2 g<br />
Dextrosa 5 g<br />
Extracto de levadura 5 g<br />
Almidon soluble 2 g<br />
Dextrina 1 g<br />
Cloranfenicol 0,125 g<br />
Gentamicina 5 mg<br />
Sal A 10 ml<br />
Sal C 20 ml<br />
Agar 17 g<br />
Agua desionizada 970 ml<br />
P re p a ra tio n<br />
a) Calentar hasta disolver todos los componentes. Enfriar y ajustar el pH a 6,7.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en placas de Petri.<br />
C o n tro l de calidad<br />
Trichophyton mentagrophytes: Crece.<br />
Staphylococcus epidermidis: Inhibicion parcial o completa.<br />
(*) Disponible comercialmente (Becton Dickinson)<br />
Sal A:<br />
PO.HzNa 25 g<br />
POtHNaz 25 g<br />
H2O 250 ml<br />
SO.1Mg.7 H2O 10 g<br />
S04Fe.7H20 0,5 g<br />
CINa 0,5 g<br />
S04Mn.7H20 2 g<br />
Agua desionizada 250 ml<br />
Agar con leche, glucosa y purpura de bromocresol*<br />
Puede utilizarse para la diferenciacion de Trichophyton rubrum y Trichophyton mentagrophytes. Trichophyton rubrum<br />
melanoide secreta un pigmento que puede parecer alcalinizacion. El pigmento ti'pico de T. rubrum puede verse a traves<br />
de la colonia, pero no a traves del medio. T. mentagrophytes granular puede necesitar 10 dias para originar un positivo<br />
claro. Microsporum persicolor crece profusamente pero no alcaliniza.<br />
C o m posicion<br />
• Solucion A:<br />
Leche desnatada en polvo<br />
Purpura de bromocresol 1,6%<br />
Agua desionizada<br />
• Solucion B:<br />
Glucosa<br />
Agua desionizada<br />
• Solucion C:<br />
Agar<br />
Agua desionizada<br />
P reparacion<br />
a) Preparar las soluciones A y B y esterilizar por separado a 115 °C durante 8 min.<br />
b) Hervir la solucion C hasta disolver el agar completamente y esterilizar a 121 °C durante 15 min.<br />
c) Anadir las soluciones A y B a la C, mezclar, enfriar a 50 °C y ajustar el pH a 6,6 con acido clorhfdrico 1N.<br />
d) Dispensar asepticamente en tubos y dejar enfriar en posicion inclinada.<br />
C o n tro l de calidad<br />
Aspecto: medio solido, azul cielo, opaco.<br />
pH final a 25 °C: 6,6 ±0,1.<br />
80 g<br />
2 ml (diluido en etanol)<br />
1.000 ml<br />
40 g<br />
200 ml<br />
30 g<br />
800 ml<br />
T. rubrum: Crecimiento restringido y sin cambio de pH a los 7 dias a 25 °C.<br />
T. mentagrophytes-. Crecimiento profuso y alcalinizacion a los 5 dfas a 25 °C.<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Agar Leeming & Notman (ALN)<br />
Utilizado en el cuitivo de Malassezia spp. Puede modificarse anadiendo cloranfenicol o bien cloranfenicol y cicloheximida.<br />
C om posicion<br />
Peptona 10 g<br />
Glucosa 5 g<br />
Extracto de levadura 100 mg<br />
Ox bile desecada 8 g<br />
Glicerol 1 ml<br />
Monoestearato de glicerol 500 mg<br />
Tween 60 0,5 ml<br />
Leche de vaca entera 10 ml<br />
Agar 12 g<br />
Agua desionizada 1.000 ml<br />
P reparacion<br />
a) Calentar todos los componentes (excepto la leche) hasta disolver correctamente.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Anadir la leche.<br />
d) Dispensar en placas.<br />
C o n tro l de calidad<br />
Aspecto: Blanco amarillento, no muy solido.<br />
Malassezia restricta: Crece.<br />
En el medio inhibidor:<br />
M. restricta: crece.<br />
Aspergillus flavus: inhibicion parcial o completa.<br />
Staphylococcus epidermidis: inhibicion parcial o completa.<br />
Agar de Leonian modificado<br />
Indicado para estimular la esporulacion en cepas que no esporulan o que presentan estructuras aberrantes.<br />
C o m posicion<br />
Maltosa 6,25 g<br />
Extracto de malta 6,25 g<br />
Extracto de levadura 1 g<br />
KH2PO4 1,25 g<br />
MgS04-7 H?0 0,625 g<br />
Peptona 0,625 g<br />
Agar 20 g<br />
Agua destilada 1.000 ml<br />
P reparacion<br />
a) Calentar hasta disolver todos los componentes.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
c) Dispensar en placas de Petri.<br />
C o n tro l de calidad<br />
Aspecto: medio solido, transparente.<br />
Aspergillus fum igatusa 37 °C: esporulacion caracteristica.<br />
Asociacion Espanola de M icologia
Fundamentos basicos para el diagnostico micologico<br />
Agar patata zanahoria (PCA)<br />
Idoneo para estimular la esporulacion de hongos miceliares; muy indicado para la identificacion de hongos dematiaceos.<br />
C o m posicion<br />
Patata rallada<br />
Zanahoria rallada<br />
Agar<br />
Agua<br />
P re p a ra tio n<br />
a) Lavar, pelar y rallar o trocear los vegetales y hervirlos lentamente en 11 de agua durante 1 h.<br />
b) Filtrar y anadir al caldo el agar correspondiente.<br />
c) Esterlizar a 121 °C durante 15 min.<br />
d) Dispensar en placas de Petri o tubos.<br />
C o n tro l de calidad<br />
20 g<br />
20 g<br />
18 g<br />
1.000 ml<br />
Aspecto: medio solido, transparente o translucido.<br />
Alternaria alternata: poco micelio y abundante produccion de conidios en cadenas.<br />
Agar Sabouraud con ciclohexim ida y cloranfenicol* (MYC)<br />
Es un medio selectivo utilizado para el aislamiento de hongos patogenos a partir de muestras muy contaminadas con<br />
hongos saprofitos y bacterias. Se utiliza fundam entalmente en el aislamiento de dermatofitos y hongos dimorficos.<br />
Inhibe algunas especies de hongos de interes medico (Candida no albicans, Aspergillus, Zygomycetes, Cryptococcus<br />
neoformans, etc.).<br />
C o m posicion<br />
Se utilizan fundamentalmente Mycosel y Mycobiotic, ambos comercializados.<br />
P reparacion<br />
De acuerdo con las instrucciones, evitar manipular la cicloheximida.<br />
C ontrol de calidad<br />
Aspecto: Agar firme, amarillento, transparente.<br />
Trichophyton mentagrophytes: Crece.<br />
Aspergillus flavus: Inhibicion parcial o completa.<br />
Staphylococcus epidermidis: Inhibicion parcial o completa.<br />
(*) Disponible comercialmente (Becton Dickinson, Biomedics, Bio-Rad, Difco, Oxoid, Remel, Sigma)<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Agar de Staib (Guizotia abyssinica). Agar semillas de alpiste<br />
Utilizado para aislar Cryptococcus spp. y Cryptococcus neoformans. C. neorformans es el unico que al metabolizar la<br />
Guizotia abyssinica (alpiste), produce melanina originando un color marron oscuro. El cloranfenicol lo convierte en<br />
medio selectivo. Tambien puede ser util en la diferenciacion de Candida dubiiniensis [6].<br />
Composicion<br />
Glucosa 10 g<br />
Creatinina 0,78 g<br />
Cloranfenicol 0,05 g<br />
Difenilo (disuelto en 10 ml de etanol 95%) 100 mg<br />
Guizotia abyssinica 70 g<br />
Agar 20 g<br />
Agua desionizada 1.000 ml<br />
P reparacion<br />
a) Moler las semillas y anadir 350 ml de agua.<br />
b) Esterilizar en autoclave y filtrar.<br />
c) Anadir agua hasta 1.000 ml.<br />
d) Anadir el resto de los componentes excepto el difenilo.<br />
e) Esterilizar a 121 °C 15 min. Enfriar a 45 °C.<br />
f) Anadir el difenilo antes de dispensar el medio en las placas.<br />
C ontro le s<br />
C. neoformans y Cryptococcus spp.<br />
A g a r T r ic h o p h y to n (1 a 7 )*<br />
Son siete medios que se utilizan en la identificacion de especies de Trichophyton basandose en sus requerimientos<br />
nutricionales. El crecimiento se valora desde el 1 al 4 (0 = no-crecimiento; 1 = crecimiento ligero; 2 = parcialmente esti-<br />
mulado, pero inferior al control; 4 = crecimiento comparable con el control).<br />
C o m posicion<br />
Trichophyton agar #1:<br />
• Trichophyton agar #5 = #1<br />
Acidos casaminicos (libres de vitaminas) 2,5 g<br />
+ acido nicotfnico (niacina) 2,0 mg<br />
Glucosa<br />
Fosfato monopotasico (PO4KH2)<br />
Sulfato magnesico (S0
Fundamentos basicos para el diagnostico micologico<br />
Agar urea de Christensen*<br />
Se utiliza en la identification de algunos dermatofitos, especialmente Trichophyton rubrum de Trichophyton m entagrophytes,<br />
y de aigunas levaduras (Cryptococcus neoformans).<br />
C o m posicion<br />
Peptona 1 g<br />
Glucosa 1 g<br />
CINa 5 g<br />
PO-KHz 2 g<br />
Rojo de fenol 12 mg<br />
Agar 20 g<br />
Agua desionizada 900 ml<br />
Preparacion<br />
a) Esterilizar los 900 ml de agar a 121 °C durante 15 min.<br />
b) Anadir 100 ml de solution de urea (20% en agua, esterilizar por filtration) a 900 del medio enfriado a 50 °C.<br />
c) Dispensar en tubos. Solidificar en position inclinada.<br />
d) Tambien puede prepararse a partir Urea agar base (Christensen), que se esteriliza por filtration y se afiade al<br />
agar esteril.<br />
C o n tro l de calidad<br />
Aspecto: Agar inclinado, naranja, trasparente.<br />
pH final: 6,8 ± 0,2<br />
T. mentagrophytes: ureasa positiva (rojo).<br />
T. rubrum: ureasa negativa (naranja).<br />
Cuando se usa para levaduras: C. neoformans (positiva) y Candida albicans (negativa).<br />
(*) Disponible comercialmente (Becton Dickinson, Biomedics, Difco, Fluka, Merck, Remel, Sigma)<br />
CHROMagar Candida*<br />
CHROMagar contiene diversos sustratos enzimaticos que estan unidos a compuestos cromogenicos. Cuando enzimas<br />
especificas descomponen el sustrato, se produce color. Las colonias deben evaluarse a las 48 h. La siembra de muestras<br />
directamente aumenta un 20% el numero de cultivos mixtos [7], Puede utilizarse para identificar levaduras aisladas<br />
en otros medios no cromogenicos. Es interesante tambien su utilization para comprobar la pureza de las cepas en las<br />
pruebas de sensibilidad. Permite la identification rapida de especies resistentes. Puede utilizarse en mucosas, heridas<br />
con flora mixta, hemocultivos y orinas, especialmente. Es necesario seguir con rigor las condiciones establecidas por el<br />
fabricante. <strong>Inc</strong>ubar a 35 °C, en camara humeda y en oscuridad, 48 a 72 h (no
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fundamentos basicos para el diagnostico micologico<br />
Dermatophyte test medium* (DTM)<br />
Medio utilizado para el aislamiento de dermatofitos en muestras muy contaminadas, proporcionando una identificacion<br />
presuntiva. Los dermatofitos producer) alcalinizacion, virando el medio de amarillo a rojo, algunas bacterias y hongos<br />
tambien pueden producir alcalinizacion. El pigmento caracteristico de algunos dermatofitos no se puede identificar. La<br />
cicloheximida inhibe muchos de los hongos saprofitos.<br />
Composicion<br />
Peptona 10 g<br />
Glucosa 10 g<br />
Agar 20 g<br />
Solucion de rojo fenol 40 ml<br />
CIH 0,8 M 6 ml<br />
Cicloheximida 0,5 g<br />
Sulfato de gentamicina 100 Mg/ml<br />
Clortetraciclina 100 pg/ml<br />
P reparacion<br />
a) Mezclar la peptona, glucosa y agar en 1.000 ml de agua desionizada y hervir hasta disolver el agar.<br />
b) Anadir 40 ml de la solucion de rojo fenol mientras se remueve (Solucion de rojo fenol: 0,5 g de Bacto-Phenol red<br />
disolver en 15 ml de NaOH 0,1 N; completar hasta 100 ml con agua desionizada).<br />
c) Ajustar el pH ahadiendo 6 ml de C!H 0,8 M mientras se remueve.<br />
d) Disolver 0,5 g de cicloheximida en 2 ml de acetona y anadir al medio caliente mientras se remueve.<br />
e) Disolver el sulfato de gentamicina en 2 ml de agua, anadir al medio mientras se remueve.<br />
f) Esterilizar a 121 °C. Enfriar hasta unos 47 °C.<br />
g) Disolver la clortetraciclina en 25 ml de agua desioinizada esteril. Anadir al medio mientras se agita.<br />
h) Dispensar en placas o en tubos.<br />
C o n tro l de calidad<br />
Aspecto: Agar amarillo naranja, trasparente.<br />
Trichophyton verrucosum: crece y alcaliniza.<br />
Aspergillus flavus: inhibicion parcial o completa.<br />
Staphylococcus epidermidis: inhibicion parcial o completa.<br />
(*) Disponible comercialmente (Becton Dickinson, Fluka, Merck, Remel)<br />
Medio de arroz<br />
Se utiliza para la diferenciacion de cepas atfpicas de Microsporum audouinii y M icrosporum canis.<br />
C o m posicion<br />
Arroz bianco no enriquecido 8 g<br />
Agua desionizada 25 ml<br />
P reparacion<br />
a) Mezclar los ingredientes en un matraz Erlenmeyer.<br />
b) Esterilizar a 121 °C durante 15 min.<br />
C o n tro l de calidad<br />
Aspecto: granos de arroz cocido.<br />
M. canis: presenta buen crecimiento, pigmento amarillo y esporulacion abundante.<br />
M. audouinii: no presenta crecimiento o es escaso, coloracion marronacea.<br />
Con asa micologica, transferir una pequena porcion del aislamiento al matraz con los granos esteriles.<br />
Asociacion Espanola de M icologia
Fundamentos basicos para el diagnostico micologico<br />
3.5. Informe de los resultados<br />
El diagnostico micologico no acaba con el<br />
aislamiento y la identificacion del agente causal.<br />
Finaliza cuando la information sobre el mismo llega<br />
al conocimiento del medico responsable del pacien-<br />
te. Esta ultima etapa del procedimiento diagnostico<br />
no es menos importante que las anteriores, por lo<br />
que debe cuidarse al maximo todos los detalles de la<br />
misma.<br />
3.5.1. Observacion microscopica<br />
Debe informarse en el dfa ya que aporta una<br />
importante ayuda al clfnico; sus pacientes pueden<br />
salir de la consulta de dermatologfa con un diagnostico<br />
presuntivo (dermatofitosis), que habra que con-<br />
firm ar con el cu ltiv o . o d e fin itiv o (p itiria sis<br />
versicolor). La tinta china en buenas manos (cripto-<br />
cocosis) y la inmunofluorescencia (peumocistosis)<br />
tambien son diagnosticas. Otras observaciones posi-<br />
tivas permiten una orientation terapeutica (mucor-<br />
m ico sis, asp erg ilo sis, etc.). Es recom endable<br />
observar los examenes en fresco negativos al dfa<br />
siguiente.<br />
Este informe es fundamental en toda muestra<br />
esteril y permite saber si la muestra posee suficiente<br />
calidad.<br />
El inform e oral es muy im portante para<br />
la correcta valoracion de la muestra y contrastar la<br />
eficiencia del laboratorio, ademas de adecuar la<br />
relation con el clfnico. Todo inform e oral debe<br />
seguirse de otro escrito, reflejando que existe un<br />
informe oral previo.<br />
3.5.2. Cultivo<br />
El cultivo negativo se descarta, generalmen-<br />
te, a las cuatro sem anas de incubacion, con las<br />
excepcio n es c itad as en el tiem po de lectu ra.<br />
La prolongation de la incubacion despues de tres<br />
sem anas aporta poca in fo rm atio n adicional y,<br />
dependiendo del sistema de lectura, puede suponer<br />
una sobrecarga de trabajo que hay que valorar ade-<br />
cuadamente en cada laboratorio [12].<br />
Los cultivos positivos se inform an, de la<br />
misma manera que la observacion microscopica, en<br />
el momento en el que se disponga del crecimiento.<br />
En los casos en los que hay que realizar aislamien-<br />
tos repetidos (unas), al cuestionarse el significado<br />
del hongo aislado, se informara de la misma manera.<br />
En ambos casos, hay que valorar el beneficio<br />
para el paciente y el esfuerzo en la localization del<br />
clfnico responsable, por lo que la utilizacion del<br />
correo electronico para este tipo de informes, ayuda<br />
sensiblemente al establecimiento de una rapida y<br />
fluida comunicacion entre el micologo y el clfnico.<br />
En todo informe escrito debe figurar si se<br />
trata de un informe provisional o definitivo. Para los<br />
aislamientos realizados en Bacteriologfa y remitidos<br />
a Micologi'a, debe establecerse un mecanismo que<br />
garantice la correcta llegada del resultado al medico:<br />
1. Si la numeration del laboratorio es unica, se rea-<br />
lizaran inform es provisionales en los que se<br />
refleje la trasferencia de la cepa.<br />
2. Si la numeration es diferente, en el registro de<br />
Micologia figurara que es una cepa recibida de<br />
Bacteriologfa y su numero original.<br />
En el informe debe figurar el resultado definitivo.<br />
En el caso de ser positivo, debe incluir la<br />
identificacion de la especia aislada y el estudio de<br />
sensibilidad, si procede.<br />
Cuando el significado es de dudosa interpretation<br />
debe hacerse constar.<br />
3.5.3. Informe telefonico<br />
Por sus especiales caracterfsticas, en este tipo<br />
de informes se deben seguir unas recomendaciones<br />
especiales:<br />
1. Cuando no sea posible contactar con el facultati-<br />
vo solicitante, se intentara hablar con el responsable<br />
o el jefe de servicio. No se dara nunca el<br />
informe a una persona no cualificada.<br />
2. Deben facilitarse siempre los datos que garanti-<br />
cen que el informe corresponde al paciente sobre<br />
el que se nos pregunta:<br />
• Nombre del paciente<br />
• Localization (habitation, centro de salud, etc.)<br />
• Tipo de cultivo<br />
• Fecha de recogida de la muestra<br />
• Resultados<br />
3 . En el registro del laboratorio debe anotarse:<br />
• Dfa y hora de la llamada<br />
• Nombre del medico que recibe la information<br />
• Persona que proporciona la information<br />
4. La persona que da el inform e debe seguir al<br />
menos los siguientes pasos:<br />
• Repetir el nombre del paciente<br />
• Repetir la localization del paciente<br />
• Informar el estado actual del estudio<br />
La gestion de la information hay que adap-<br />
tarla a las circunstancias de cada laboratorio y un<br />
modelo podrfa ser el reflejado en la Figura 3 . 1.<br />
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Referencias<br />
10.<br />
11.<br />
12.<br />
Fundamentos basicos para el diagnostico micologico<br />
Figura 3.1. Modelo de gestion de la informacion en un laboratorio de M icologia Clinica.<br />
Land CA, Stringfellow J, Flores M. Collection and transport<br />
ot specimens. En: Isenberg HD (Ed.) Clinical microbiology<br />
procedures handbook. W ashington DC, American Society<br />
tor Microbiology, 1992.<br />
Hazen KC. Mycology and aerobic Actinomycetes. En:<br />
Isenberg HD (Ed.) Essential procedures for clinical<br />
Microbiology. W ashington, American Society for<br />
Microbiology, 1998: 255-357.<br />
National Com mittee for Clinical Labotatory Standard. QC<br />
assurance for com m ercially prepared microbiological culture<br />
media. Approved Standard. M22-A. Villanove, Pa,<br />
National Com mittee for Clinical Laboratory Standard, 1990.<br />
De Hoog GS, Guarro J, Figueras MJ, Gene J. Atlas of clinical<br />
fungi (2“ ed.). Baarn / Reus, Centralbureau voor<br />
Schilm m elcultures / Universitat Rovira i Virgili, 2000.<br />
Aspiroz C, Rezusta A, Rubio MC, Gom ez-Lus R.<br />
Malassezia pachyderm atis failure to grow on a commercial<br />
Sabouraud medium with gentamycin. 14,h ISHAM World<br />
Congress, Buenos Aires, Argentina 2000.<br />
Staib F, Arasteh K. Chlam ydospore form ation on Staib<br />
agar. Observations made before Candida dubliniensis was<br />
described. Mycoses 2001: 44: 23-27<br />
Pfaller MA, Houston A, Coffmann S. Application of<br />
CHROMagar Candida for rapid screening of clinical specimens<br />
for Candida albicans, Candida tropicalis, Candida<br />
krusei and Candida ( Torulopsis) giabrata. J Clin Microbiol<br />
1995; 34: 59-61.<br />
Jabra-Rizk MA, Brenner TM, Romagnoli M, e ta l.<br />
Evaluation of a reformulated CHROMagar Candida.<br />
J Clin Microbiol 2001; 39: 2015-2016.<br />
Kwon-Chung KJ, Bennett JE. Medical Mycology.<br />
Philadelphia, Lea & Febiger, 1992.<br />
Larone D. Medically important fungi. A guide to identification.<br />
W ashington DC, American Society for Microbiology<br />
1995.<br />
Passarell L. 1999 Use and publishing guideline. URL:<br />
http://fungus.utmb.edu<br />
Labarca JA, W agar EA, Grasm ick AE, Kokkinos HM,<br />
Bruckner DA. Critical evaluation of 4-week incubation for<br />
fungal cultures: Is the fourth week useful? J Clin Microbiol<br />
1998; 36: 3683-3685.<br />
Asociacion Espaiiola de M icologia<br />
Bibliografia complementaria<br />
Al-Doory Y. Laboratory Medical Mycology. Piladelphia, Lea<br />
y Febiger, 1980.<br />
Smith E, Rogers AL. Medical m ycology and human m ycoses.<br />
Belmont California, Star Publishing Co., 1996.<br />
Goodman NL, Roberts GD. Laboratory diagnosis. In:<br />
Ajello L, Hay RJ (Volume 4 Eds.) Medical Micology. In:<br />
Collier L, Balows A, Sussman M (Eds.) Topley & W ilson’s.<br />
Microbiology and Microbial Infections. 9" ed. London,<br />
Arnold, 1998: 75-87.<br />
Merz WG, Roberts GD. Algorithm s for detection and identification<br />
of fungi. En Murray PR, Baron EJ, Pfaller MA,<br />
Tenover FC, Yolken RH (Eds.) Manual of Clinical<br />
Microbiology. W ashington DC, American Society for<br />
Microbiology, 1999: 1167-1183.<br />
Chapin KC, Murray PR. En Murray PR, Baron EJ,<br />
Pfaller MA, Tenover FC, Yolken RH (Eds.) Manual of<br />
Clinical Microbiology. W ashington DC, Am erican Society<br />
for M icrobiology 1999: 1701-1704.<br />
St-Germain G, Sum merbell R. Identifying filam entous<br />
fungi. A clinical handbook. Belmont, California, Star<br />
Publising Co., 1996.<br />
Kwon-Chung KJ, Bennett JE. Medical Mycology.<br />
Philadelphia, Lea & Febiger, 1992.<br />
Koneman EW, Roberts GD. M icologia practica de laboratorio.<br />
3a ed. Buenos Aires, Panamericana 1987.<br />
Kane J, Summerbell RC. Trichophyton, Microsporum,<br />
Epidermophyton, and agents of superficial mycoses. En:<br />
Murray PR, Baron EJ, Pfaller MA, Tenover FC, Yolken RH<br />
(Eds.) Manual of Clinical Microbiology. Washington,<br />
American Society for M icrobiology 1999: 1275-1294.<br />
McGinnis MR. Laboratory Handbook of Medical Mycology.<br />
New York, Academ ic Press, 1980.<br />
Sutton DA. Specimen collection, transport and processing.<br />
En: Murray PR, Baron EJ, Pfaller MA, Tenover FC,<br />
Yolken RH (Eds.). Manual of Clinical Microbiology (8,B ed).<br />
Washington DC, ASM Press, 2003: 1659-1667.
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6<br />
Identificacion de otros hongos miceliares<br />
Josepa Gene<br />
Josep Guarro<br />
13.1. Introduccion 13. 2. Zigomicetes<br />
El aumento de pacientes con alteraciones en<br />
su sistema inmunitario o la utilization de tecnicas<br />
agresivas en la medicina modema, entre otros facto-<br />
res, han propiciado en las ultimas decadas un considerable<br />
incremento de las infecciones producidas<br />
por microorganismos saprotrofos. Entre ellos cabe<br />
citar numerosos hongos miceliares habitualmente<br />
colonizadores de diferentes tipos de sustratos vege-<br />
tales y frecuentes en el ambiente que rodea al hom-<br />
bre (su elo , paredes h um edas, a ire ...). H ace<br />
relativamente poco tiempo, cuando dichos hongos<br />
eran aislados de muestras clmicas solfan ser consi-<br />
derados como meros contaminantes. Sin embargo,<br />
se ha demostrado reiteradam ente que muchos de<br />
estos hongos son capaces de infectar al hombre.<br />
Estos hechos deben ser considerados por los microbiologos<br />
clfnicos, los cuales segun las evidencias<br />
(historia clfnica del paciente, tipos de muestra, etc.),<br />
no deben desestimar a los hongos ambientales sino<br />
tenerlos en cuenta como posibles agentes responsa-<br />
bles de infecciones en el hombre, especialm ente<br />
aquellas especies cuyas cepas son capaces de crecer<br />
a 35-37 °C.<br />
Los hongos miceliares considerados patogenos<br />
oportunistas para el hombre pertenecen princi-<br />
palm ente al grupo de los zigom icetes y de los<br />
hifomicetes. Su identificacion es fundamental no<br />
solo para fines epidemiologicos o meramente cientf-<br />
ficos, sino tambien por la diferente sensibilidad a los<br />
antifungicos entre especies de un mismo genero.<br />
Tambien es importante que la cepa identificada se<br />
conserve en colecciones de cultivo de referenda,<br />
dando la posibilidad de realizar investigaciones pos-<br />
teriores o cualquier otra comprobacion necesaria. La<br />
identificacion se basa principalmente en el estudio<br />
de los caracteres morfologicos, macro y microscopi-<br />
cos, del hongo en cultivo.<br />
A continuation se describen los caracteres<br />
morfologicos mas im portantes de algunas de las<br />
especies mas comunes de hongos miceliares respon-<br />
sables de infecciones humanas.<br />
Asociacion Espanola de M icologia<br />
Los zigomicetes se diferencian del resto de<br />
hongos miceliares por presentar hifas anchas, rami-<br />
ficadas, generalmente no septadas, y esporas sexua-<br />
les denom inadas zigosporas (Figura 13.1). Las<br />
infecciones ocasionadas por estos hongos son referi-<br />
das como zigomicosis. Sin embargo, este termino es<br />
muy amplio ya que incluye a zigomicetes que pertenecen<br />
a dos grupos (ordenes) muy diferentes, los<br />
entomoftorales y los mucorales. Los primeros son<br />
hongos endemicos de pafses tropicales y subtropica-<br />
les que suelen ocasionar micosis subcutaneas [1-3]<br />
y que no vamos a tratar en este capftulo ya que es<br />
diffcil encontrarlos en nuestro pais. Los mucorales,<br />
en cambio, estan ampliamente distribuidos por las<br />
diferentes areas geograficas del globo, y algunos de<br />
ellos son capaces de ocasionar un amplio rango de<br />
infecciones en el hombre [1-3]. Las infecciones ocasionadas<br />
por estos hongos suelen denom inarse<br />
mucormicosis [3,4]. El diagnostico precoz de estas<br />
infecciones es esencial ya que evolucionan con rapi-<br />
dez y su pronostico suele ser fatal. La identificacion<br />
del genero o de la especie solo es posible con el cultivo<br />
de las cepas.<br />
13.2.1. Caracteres morfologicos basicos<br />
y condiciones de cultivo<br />
Las caracterfsticas morfologicas mas repre-<br />
sentativas de los mucorales son su rapido crecimien-<br />
to y su m icelio carente de septos, aunque estos<br />
pueden estar presentes en hifas fertiles y en el micelio<br />
vegetativo de cultivos viejos. Estos hongos generalm<br />
en te solo d e sa rro lla n esp o ras asexuales<br />
(esporangiosporas) a partir de hifas fertiles (espo-<br />
rangioforos), ramificadas o no, en el interior de una<br />
especie de vesfculas (esporangios), consistentes en<br />
un ensan ch am ien to apical del esp o ran g io fo ro<br />
(Figura 13.1). Otras estructuras con valor diagnostico<br />
son la columela (prolongation esteril, a menudo<br />
hinchada, del esporangioforo dentro del esporan-<br />
gio), la apofisis (ligero hinchamiento en la parte apical<br />
del esporangioforo, por debajo del esporangio),<br />
los rizoides (estructura semejante a una rafz) y los<br />
estolones (hifas aereas, no ramificadas, que conec-<br />
tan los rizoides). El estudio de dichas estructuras es<br />
util para diferenciar los generos mas frecuentes en<br />
clfnica, tales como Absidia, Rhizopus y Saksenaea.
Identificacion de otros hongos miceliares<br />
Figura 13.1. Dibujo esquematico de las estructuras fertiles de los zigomicetes.<br />
La identificacion de genero en los mucorales<br />
puede llevarse a cabo a partir de los cultivos prima-<br />
rios de las muestras clfnicas sobre SDA (Capftulo<br />
3). Sin embargo, para la identificacion de la especie<br />
se requiere el uso de medios de cultivo mas especf-<br />
ficos tales como agar glucosado de patata (PDA) o<br />
agar extracto de m alta (M EA), incubando en la<br />
oscuridad a 25 y a 35 °C, ya que hay especies que<br />
son termofilas. Ambos medios se hallan comerciali-<br />
zados y, tanto su composicion como elaboration, se<br />
detallan en el Capftulo 3.<br />
13.2.2. Description de las especies,<br />
diagnostico diferencial y comentarios<br />
Absidia corymbifera (Cohn) Sacc. & Trott<br />
(Figura 13.2)<br />
Colonias de crecimiento rapido a 37 °C, ocu-<br />
pando toda la placa a los 4 dfas, algodonosas, de<br />
color banco a pardo grisaceas. Estolones y rizoides<br />
presentes. Esporangioforos desarrollandose a partir<br />
de los estolones y entre los rizoides, solitarios o en<br />
grupos, de hasta 450 pm de longitud, generalmente<br />
ra m ific a d o s, con ap o fisis de form a conica.<br />
Esporangios terminales, subesfericos o piriformes,<br />
de 25-150 pm de diam etro, grisaceos; colum ela<br />
hemiesferica, generalmente con una pequena protu-<br />
berancia apical. Esporangiosporas lisas, esfericas u<br />
ovales, 3-5 x 2.5-4 pm. Zigosporas usualm ente<br />
ausentes.<br />
Diagnostico diferencial<br />
Se distingue de la otra especie descrita como<br />
oportunista (A. coerulea), aunque mucho menos fre-<br />
cuente, por crecer a 45-50 °C. A. coerula no crece a<br />
37 °C y sus colonias presentan coloraciones azula-<br />
das [5].<br />
Comentarios<br />
Es una especie de amplia distribution que se<br />
afsla de suelo y material vegetal en descomposicion<br />
[4,6]. Se ha considerado, despues de Rhizopus ory-<br />
zae y R. rhizopodiformis, el tercer agente de zigomi-<br />
cosis de mayor incidencia en clfnica [3], aunque<br />
existe cierta controversia al respecto puesto que<br />
Kwon-Chung & Bennett [2] o Larone [7], entre<br />
otros, lo consideran como infrecuente. Se ha descri-<br />
to como agente responsable de infecciones profun-<br />
das en cereb ro , pulm on y rin o n , asf com o de<br />
infecciones cutaneas [4, 5].<br />
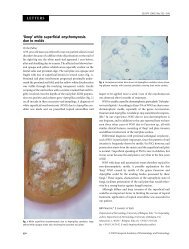
F igura 13.2. Absidia corymbifera. a: colonia sobre PDA a los 7 dfas<br />
de cultivo a 37 °C; b: esporangioforos.<br />
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Identificacion de otros hongos miceliares<br />
Rhizopus oryzae Went & Prins. Geerl<br />
(Figura 13.3)<br />
Colonias de crecimiento rapido a 37 °C que<br />
ocupan toda la placa de Petri a los 4 dfas, inicial-<br />
m ente b lan cas v o lv ien d o se gris p ard u scas.<br />
Estolones y rizoides presentes. Esporangioforos no<br />
ramificados, de hasta 2 mm de longitud, general-<br />
mente agrupados formando verticilos en cuya base<br />
se situan los rizoides; apofisis presente pero poco<br />
evidente. Esporangios esfericos de 50-300 pm de<br />
ancho, de color gris pardusco a negro; columela<br />
subesferica, ocupando el 50-70% del esporangio.<br />
Esporangiosporas grisaceas, estriadas longitudinal-<br />
mente, angulares, subesfericas o elipsoidales, 6-8 x<br />
4-5 pm.<br />
F ig ura 13.3. Rhizopus oryzae. a: colonia sobre PDA a los 7 dias de<br />
cultivo a 25 °C; b: esporangioforos con columela y rizoides en la<br />
base; c: esporangiosporas.<br />
Dicignostico diferencial<br />
R. oryzae y R. rhizopodiformis son las especies<br />
de mucorales mas frecuentes en clfnica. La pri-<br />
mera no crece a 45 °C y sus esporas son angulares y<br />
con estrfas longitudinales, mientras que R. rhizopodiform<br />
is crece a 50 °C y sus esporas son mas o<br />
menos esfericas y equinuladas. Otras especies de<br />
Rhizopus oportunistas, tales como R. azygosporus,<br />
R. microsporus, R. schipperae y R. stolonifer, son<br />
mucho menos frecuentes [3,5].<br />
Comentarios<br />
R. oryzae se afsla frecuentemente a partir de<br />
suelos, asf como de madera, de estiercol, plumas,<br />
etc., generalmente en regiones de clima tropical y<br />
subtropical, aunque tambien de regiones templadas<br />
[6]. Es la especie mas comun del genero y a ella se<br />
atribuyen la mayorfa de casos de mucormicosis des-<br />
critas hasta la fecha, siendo la infection rinocerebral<br />
la mas habitual [1,2,4,8],<br />
Asociacion Espanola de M icologia<br />
Saksenaea vasiformis Saksena<br />
(Figura 13.4)<br />
Colonias de crecimiento rapido a 37 °C, ocupando<br />
toda la placa de Petri a los 4 dfas, algodono-<br />
sas, b lancas. E sto lo n es y riz o id e s p resen tes.<br />
Esporangioforos no ramificados, de hasta 60 pm de<br />
longitud, solitarios. Esporangios en forma de bote-<br />
11a, de pared equinulada, de hasta 50 pm de longitud,<br />
de color gris pardusco; columela hemiesferica.<br />
Esporangiosporas grises, lisas, elipsoidales o cilfn-<br />
dricas, 3-4 x 2-2.5 pm.<br />
F igura 13.4. Saksenaea vasiformis. Esporangioforos con rizoides.<br />
Diagnostico diferencial<br />
El mayor problema para la identificacion de<br />
esta especie es que no suele esporular en los medios<br />
de cultivo habituales. Para su fructification se reco-<br />
m ienda realizar el procedim iento descrito por<br />
Padhye & Ajello [9] y que, brevemente, consiste en<br />
cortar asepticamente un fragmento de la colonia no<br />
esporulada, de aproximadamente 1 cm2, y transferirlo<br />
a una placa con 20 ml de agua destilada esteril<br />
con 0,2 ml de una solution al 10 % de extracto de<br />
levadura. Se sella la placa para evitar que sobresalga<br />
el micelio y se incuba a 35-37 °C. El hongo suele<br />
desarrollar los esporangioforos a partir de 5-7 dfas.<br />
Comentarios<br />
Se ha descrito como agente responsable de<br />
infecciones principalmente cutaneas, aunque tambien<br />
de osteomielitis, infecciones rinocerebrales e<br />
infecciones diseminadas de pronostico fatal [3-5],<br />
A continuation se incluye una clave dicoto-<br />
mica para la identificacion de los generos de zigo-<br />
micetes descritos como oportunistas para el hombre<br />
y/o animales.
Identificacion de otros hongos miceliares<br />
Clave de los generos de zigomicetes patogenos oportunistas<br />
1 Micelio abundante. Las esporangiosporas son liberadas pasivamente (M ucorales)................................................................. 2<br />
Micelio muy reducido o ausente. Las esporangiosporas son liberadas con fuerza (Entom oftorales)..................................9<br />
2 Esporangios pequenos, con una sola espora o con pocas, formandose en zonas hinchadas del apice del esporangioforo<br />
o de sus ra m a s ...................................................................................................................................................................................3<br />
Esporangios grandes, con muchas esporas, formandose en el apice del esporangioforo o de sus ra m a s ...................... 4<br />
3 Esporangios mas o menos esfericos, uniesporados........................................................................................ C unningham ella<br />
Esporangios cih'ndricos o mazudos, con varias esporas dispuestas en hileras..................................... S yncephalastrum<br />
4 Esporangioforos con a pofisis....................................................................................................................................................................5<br />
Esporangioforos sin a p o fis is .................................................................................................................................................................. 7<br />
5 Esporangios con la parte superior muy alargada. Esporangioforos solitarios.......................................................... Saksenaea<br />
Esporangios esfericos, subesfericos o piriformes. Esporangioforos dispuestos en ve rticilo s................................................6<br />
6 Esporangios esfericos. Esporas con estrias, usualmente muy o s c u ra s ...................................................................... R hizopus<br />
Esporangios piriformes. Esporas lisas, palidas......................................................................................................................A b sid ia<br />
7 Presencia de colum ela............................................................................................................................................................................... 8<br />
Ausencia de colum ela......................................................................................................................................................... M ortierella<br />
8 Rizoides presentes; term ofilos........................................................................................................................................ R hizom ucor<br />
Rizoides ausentes; mesofilos o term otolerantes.................................................................................................................. M ucor<br />
9 Colonias pulverulentas, con hifas septadas al envejecer. Esporangioforos alargados.<br />
Zigosporas esfericas......................................................................................................................................................... C o n id io b olus<br />
Colonias membranosas. Esporangioforos cortos, generalmente hinchados hacia el apice.<br />
Zigosporas c o n ic a s ........................................................................................................................................................... B a sid io b o lu s<br />
13.3. Hifomicetes<br />
Los hifomicetes constituyen el grupo mas<br />
numeroso de hongos microscopicos. Presentan una<br />
gran diversidad y una amplia distribution. Ademas<br />
de los derm atofitos (Capftulo 12) o patogenos<br />
primarios para el hombre como son Blastomyces<br />
dermatitidis, Histoplasma capsulatum, Coccidioides<br />
immitis, Sporothrix schenckii o Penicillium marnef-<br />
fei, entre otros, este grupo incluye el mayor numero<br />
de especies oportunistas y las de mayor incidencia<br />
en clmica (Capftulo 2). Muchos de estos hongos son<br />
ascomicetes que en cuitivo solamente muestran su<br />
fase asexual, reproduciendose a traves de la formation<br />
de una gran cantidad de conidios.<br />
13.3.1. Caracteres morfologicos basicos<br />
y condiciones de cuitivo<br />
La caracterfstica comun a todos ellos es la<br />
presencia de hifas septadas. Las esporas o conidios<br />
se desarrollan a partir de celulas conidiogenas que<br />
suelen form arse en hifas soporte o conidioforos<br />
(Figura 13.5), aunque tambien pueden desarrollarse<br />
directamente sobre las hifas vegetativas (no diferen-<br />
ciadas) del micelio. Los conidioforos pueden crecer<br />
F igura 13.5. Dibujo esquematico de las estructuras fertiles de los<br />
hifomicetes.<br />
solitarios o agrupados. Si los conidioforos son cortos<br />
y se agrupan formando estructuras similares a<br />
cojines nos referimos a ellos como esporodoquios.<br />
Por el contrario, si son largos y se agrupan formando<br />
estructuras similares a arboles reciben el nombre<br />
se sinemas. Las celulas conidiogenas pueden ser de<br />
diferentes tipos. Se llaman fialides cuando tienen<br />
forma de botella con un cuello largo y cilmdrico o<br />
en forma de copa (collarete) y los conidios emergen<br />
de su interior. Las anelides, a diferencia de las fialides,<br />
presentan en su apice una serie de cicatrices<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Identificacion de otros hongos miceliares<br />
anulares que son el resultado de la formacion suce-<br />
siva de conidios. El cuello de las anelides aumenta<br />
de longitud a medida que se forman los conidios, el<br />
de las fialides no. Una celula conidiogena puede<br />
tener, a su vez, mas de un punto (locus) de formacion<br />
de conidios (polifialies o celulas conidiogenas<br />
poliblasticas). Los conidios pueden formar masas<br />
mucosas o disponerse en cadenas. Nos referimos a<br />
cadenas acropetas cuando el conidio mas joven se<br />
encuentra en el extremo libre -apical- de la cadena,<br />
y a cadenas basfpetas cuando el conidio mas joven<br />
se encuentra en la base de la cadena, en contacto<br />
con la celula conidiogena. Para la observation de la<br />
disposition de los conidios es util el examen de la<br />
colonia mediante la lupa u observarla directamente<br />
mediante el microscopio optico con los objetivos de<br />
lOx o 20x. D eterm inadas especies desarrollan<br />
estructuras de resistencia tales como esclerocios<br />
(masa compacta de hifas de consistencia variable,<br />
que suele desarrollarse en la superficie de un sustra-<br />
to y que puede ser observada a simple vista) o clamidosporas<br />
(espora asexual que suele originarse de<br />
un segmento de hifa intercalar o terminal, suelen ser<br />
pigmentadas, de pared gruesa y con la superficie<br />
lisa u omamentada). La formacion de estas dos ultimas<br />
estructuras se ve muy influenciada por las con-<br />
diciones de cultivo de la cepa. El examen de todos<br />
estos caracteres resulta imprescindible para la identification<br />
tanto a nivel generico como espetifico de<br />
estos hongos. Para tal finalidad, son de gran ayuda<br />
las claves dicotomicas o las tablas comparativas que<br />
se elaboran a partir de los caracteres mas relevantes<br />
que distinguen generos y especies.<br />
Aunque hoy en dfa algunas tecnicas de bio-<br />
logfa molecular pueden ser de gran ayuda para el<br />
diagnostico micologico, especialmente de patoge-<br />
nos primarios, el cultivo todavfa es imprescindible<br />
en muchos casos. En ch'nica es habitual utilizar<br />
medios de cultivo ricos en nutrientes como SDA<br />
(Capi'tulo 3) para el aislamiento de los hongos. Sin<br />
embargo, el empleo de dichos medios no es reco-<br />
mendable para la identificacion de la mayorfa de los<br />
oportunistas ya que estimula la production de mice-<br />
lio en detrimento de las estructuras esporulantes<br />
im prescindibles para el reconocim iento de estos<br />
hongos. Para favorecer la esporulacion, es util el<br />
empleo de medios como PDA, el agar harina de<br />
mafz (CMA) o agar harina de avena (OA) que apor-<br />
tan fuentes de carbono distintas a la glucosa, o<br />
incluso m edios de cultivo pobres en nutrientes<br />
como agar patata-zanahoria (PCA) o agar agua con<br />
fragmentos de papel de filtro esteril en la superficie<br />
(Capftulo 3). Estos dos ultimos medios son princi-<br />
palmente recomendables para estimular la esporulacion<br />
de hifo m icetes con p ig m e n ta tio n oscura<br />
(dematiaceos). Asf mismo, es obligado el uso de<br />
MEA y/o agar Czapek Dox para la identificacion de<br />
especies de generos como Aspergillus o Penicillium<br />
(Capi'tulo 3). A pesar de que muchos de estos hongos<br />
son capaces de crecer entre 30 y 37 °C, las con-<br />
diciones mas adecuadas de incubation son a 25 °C<br />
y en la oscuridad.<br />
Asociacion Espanola de M icologia<br />
13.3.2. Descripcion de las especies,<br />
diagnostico diferencial y comentarios<br />
Acremonium strictum W. Gams<br />
(Figura 13.6)<br />
C olonias de crecim iento m oderado (16-<br />
23 mm PDA, 25 °C, 7 dfas), de color bianco a rosa<br />
palido, inicialm ente aterciopeladas volviendose<br />
algodonosas y con abundantes hifas formando fascf-<br />
culos de donde emergen perpendiculares las celulas<br />
conidiogenas (fialides). Los conidioforos a menudo<br />
se reducen a una simple fialide larga y delgada que<br />
se estrecha hacia el apice (subulada), de hasta 50 x<br />
1,5-2 |im. Conidios formando masas mucosas en el<br />
apice de las fialides, hialinos, lisos, elipsoidales o<br />
cilmdricos, 3,5-6 x 1-2 |am. Clamidosporas ausen-<br />
tes.<br />
F ig ura 13.6. Acrem onium strictum. a: colonias sobre PDA a los<br />
14 dias de cultivo a 25 °C; b: fialides y conidios.<br />
Diagndstico diferencial<br />
De entre las especies de Acremonium descri-<br />
tas como oportunistas [5,10], A. strictum es muy<br />
similar a A. kiliense. Esta ultima se diferencia prin-<br />
cipalmente por la presencia de clamidosporas en el<br />
micelio sumergido en el agar.<br />
Comentarios<br />
Es un hongo cosmopolita que suele encon-<br />
trarse como colonizador de material vegetal en des-<br />
composicion y en el suelo [6]. Se ha descrito como<br />
agente responsable de infecciones diseminadas en<br />
pacientes severam ente inm unocom prom etidos e,<br />
incluso, causando infecciones cerebrales de pronos-<br />
tico fatal en todos los casos [5,10], probablemente<br />
debido a su elevada resistencia a los diferentes anti-<br />
fungicos [11]. En la revision de alguna de las cepas<br />
cli'nicas de casos ya publicados se ha comprobado<br />
que las identificaciones eran incorrectas, lo que dis-<br />
minuye el numero real de casos atribuidos a dicha<br />
especie [10]. Ademas, la dificultad en su identification<br />
queda patente en el reciente estudio molecular<br />
de Novicki et al. [12], en el que, a traves del analisis<br />
de diferentes fragmentos del ADN ribosomico de
Identificacion de otros hongos miceliares<br />
varias cepas de A. strictum aisladas de infecciones<br />
diseminadas, se demostro que practicamente todas<br />
ellas podi'an pertenecer a especies diferentes.<br />
Alternaria alternata (Fr.) Keissl.<br />
(Figura 13.7)<br />
Colonias de crecimiento rapido (50-70 mm,<br />
OA, 25 °C, 7 dfas), verde olivaceas, algodonosas,<br />
p u lv e ru le n ta s si estan m uy e sp o ru lad as.<br />
Conidioforos cilmdricos, ocasionalmente ramifica-<br />
dos, con 1-3 septos, de hasta 50 pm de longitud.<br />
Conidios formando largas cadenas acropetas escasa-<br />
mente ramificadas, pardos, septados longitudinal y<br />
transversalm ente, paredes intensam ente rugosas,<br />
ovoides o ampuliformes, 20-60 x 8-18 pm.<br />
F igura 13.7. Alternaria alternata. a: colonia sobre OA a los 10 di'as<br />
de cultivo a 25 °C; b: cadena acropeta de conidios.<br />
Diagnostico diferencial<br />
Se diferencia de A. infectoria, la otra especie<br />
del genero de importancia clfnica, porque esporula<br />
con mayor facilidad, sus conidios son de mayor<br />
tamano, presentan septos tanto transversales como<br />
longitudinales, suelen tener la pared rugosa y las<br />
cadenas raramente se ramifican.<br />
Comentarios<br />
Es la especie mas comun del genero, coloni-<br />
zadora de una amplia gama de sustratos, aislandose<br />
con mucha frecuencia del suelo y cualquier sustrato<br />
vegetal [6]. Es un contaminante comun del laboratorio.<br />
Se ha descrito como agente causal de feohifomi-<br />
cosis cutaneas y subcutaneas [5,8],<br />
Alternaria infectoria Simmons<br />
(Figura 13.8)<br />
Colonias de crecimiento rapido (50-60 mm,<br />
OA, 25 °C, 7 dfas), bianco grisaceas y algodonosas<br />
debido a su escasa esporulacion. Conidioforos raramente<br />
ram ificados, de hasta 85 pm de longitud.<br />
Conidios en cadenas acropetas ramificadas, pardus-<br />
cos. de pared lisa o ligeramente verrugosa, ovoides,<br />
aunque tienden a deformarse y volverse tubulifor-<br />
mes con una predominancia de septos transversales,<br />
12-30 x 7-9 pm.<br />
Figura 13.8. Alternaria infectoria. a: colonia sobre OA a los 10 dias<br />
de cultivo a 25 °C; b: conidioforos no ramificados y una cadena<br />
ramificada de conidios.<br />
Diagnostico diferencial<br />
Los conidios de A. infectoria se diferencian<br />
de los de A. alternata por ser de menor tamano, su<br />
pared es lisa o ligeramente verrugosa y predominan<br />
los septos transversales. Ademas, suelen form ar<br />
cadenas muy ramificadas. Para conseguir una buena<br />
esporulacion se recomienda transferir uno o varios<br />
fragmentos de la colonia creciendo en SDA o PDA<br />
a placas con agar agua en las que previamente se<br />
deposito en la superficie papel de filtro esteril de<br />
aproximadamente 1 cm2. La esporulacion suele apa-<br />
recer a partir de los 10-14 dfas de incubacion.<br />
Comentarios<br />
Es tambien un hongo ubicuo y, actualmente,<br />
se cree que es la especie de Alternaria de mayor<br />
incidencia en clfnica [5].<br />
Aspergillus flavus Link<br />
(Figura 13.9)<br />
Colonias de crecimiento rapido (40-60 mm,<br />
MEA, 25 °C, 7 dfas), verde amarillentas, pulverulentas<br />
o granulosas, ocasionalmente algodonosas en<br />
el centro o margen de la colonia. Conidioforos no<br />
ramificados, generalmente de 400-800 pm de longitud,<br />
terminados en una vesfcula mas o menos esferi-<br />
ca a partir de la cual las fialides se diferencian<br />
directamente (uniseriadas) o a partir de una celula<br />
soporte denominada metula (biseriadas). Metulas y<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Figura 13.9. Aspergillus flavus. a: colonias sobre MEA a los 7 di'as<br />
de cultivo a 25 °C; b: parte apical de un conidioforo con fialides<br />
biseriadas y cadenas de conidios.<br />
Identificacion de otros hongos miceliares<br />
fialides dispuestas radialmente cubriendo toda la<br />
vesi'cula. Conidios en cadenas basfpetas, verde ama-<br />
rillentos, lisos o finam ente rugosos, esfericos o<br />
subesfericos, de 3,5-4,5 pm . Puede desarrollar<br />
esclerocios, aunque raramente a partir de aislados<br />
clinicos.<br />
Diagnostico diferencial<br />
Para diferenciarla de las otras especies de<br />
Aspergillus incluidas en el capftulo, ver Tabla 13.1.<br />
Comentarios<br />
Crece rapidam ente a 37 °C. Es un hongo<br />
cosmopolita que se afsla con frecuencia del suelo,<br />
asf com o de diferentes sustratos vegetales [6],<br />
Frecuente contaminante de los cultivos en el labora-<br />
torio. Junto con A. fumigatus constituyen las especies<br />
de Aspergillus de mayor incidencia en clfnica.<br />
Ambas son importantes agentes de infecciones pul-<br />
monares principalmente en pacientes inmunocom-<br />
prom etidos, especialm ente n eutropenicos. No<br />
obstante, a diferencia de A. fumigatus, suele ser res-<br />
ponsable de muchos mas casos de sinusitis y otitis<br />
que de aspergilosis pulmonares [5,8,10].<br />
Aspergillus fumigatus Fresen.<br />
(Figura 13.10)<br />
Colonias de crecimiento rapido (50-60 mm,<br />
MEA, 25 °C, 7 di'as), verde azuladas, aterciopeladas<br />
o pulv eru len tas, m argen blanquecino o beige.<br />
Conidioforos de hasta 300 pm de longitud, uniseria-<br />
dos, vesfculas hemisfericas. Las fialides ocupan las<br />
2/3 partes de la parte superior de la vesfcula.<br />
C onidios en cadenas, form ando una com pacta<br />
columna sobre la vesfcula, verde grisaceos, finamente<br />
rugosos, subesfericos, de 2,5-3 pm.<br />
F ig ura 13.10. Aspergillus fumigatus. a: colonias sobre MEA a los<br />
7 dias de cultivo a 25 °C; b: conidioforos con fialides uniseriadas y<br />
cadenas de conidios.<br />
Diagnostico diferencial<br />
Para diferenciarla de las otras especies de<br />
Aspergillus incluidas en el capitulo, ver Tabla 13.1.<br />
La mayorfa de aislados crecen y esporulan bien a<br />
45 °C. En ocasiones, pueden aislarse cepas que no<br />
esporulan o presentan estructuras aberrantes que<br />
confunden la identificacion. Para la confirm ation<br />
Tabla 13.1. Diferencias morfologicas entre las especies de Aspergillus mas frecuentes en clinlca.<br />
Especie Colonias Conidioforos Fialides Conidios<br />
A. flavus verde amarillentas,<br />
pulverulentas<br />
o granulosas<br />
A. fumigatus verde azuladas,<br />
aterciopeladas<br />
o pulverulentas<br />
A. niger bianco amarillentas<br />
volviendose negras,<br />
granulosas<br />
de longitud variable,<br />
equinulados<br />
uni- y biseriadas,<br />
ocupando toda<br />
la vesicula<br />
Identificacion de otros hongos miceliares<br />
del cultivo se puede inducir la esporulacion transfi-<br />
riendo una portion de la colonia esteril a una placa<br />
que contien e agar de L eo n ian m o d ificado<br />
(Capftulo 3) incubando a 37 °C [13]. En el caso de<br />
no tener exito, los aislados esteriles se pueden iden-<br />
tificar a traves de exoantfgenos (Capftulo 14) o tec-<br />
nicas moleculares especfficas [10].<br />
Comentarios<br />
Es una especie termofila, de amplia distribu-<br />
cion en la naturaleza y se ai'sla de una gran diversi-<br />
dad sustratos [6]. Tam bien es un contam inante<br />
frecuente de los cultivos en el laboratorio. Es, de<br />
entre los hongos miceliares, la especie de mayor<br />
incidencia en clfnica y, por tanto, la que m ejor<br />
conocemos en cuanto a su patologfa y patron epide-<br />
miologico [5,8,10].<br />
Aspergillus niger Tiegh.<br />
(Figura 13.11)<br />
Colonias de crecimiento rapido (55-70 mm,<br />
MEA, 25 °C, 7 dfas), inicialmente de blancas a amarille<br />
n ta s, v o lv ien d o se n eg ras, g ran u lo sas.<br />
Conidioforos generalmente de unos 500 jam, pero<br />
pueden alcanzar los 3 mm de longitud, biseriados,<br />
vesfcula esferica. M etulas y fialides dispuestas<br />
radialmente cubriendo toda la vesfcula. Conidios en<br />
cadenas, pardo oscuros, densamente rugosos, esfericos<br />
o subesfericos, de 3,5-5 ^im.<br />
F igura 13.11. Aspergillus niger. a: colonias sobre MEA a los 7 dias<br />
de cultivo a 25 °C; b: detalle del apice de un conidioforo con fialides<br />
biseriadas y conidios.<br />
Diagnostico diferencial<br />
Para diferenciarla de las otras especies de<br />
Aspergillus incluidas en el capftulo, ver Tabla 13.1.<br />
Comentarios<br />
Crece abundantemente a 37 °C. Esta especie<br />
ubicua se afsla de una gran variedad de sustratos [6].<br />
Es el hongo mas comun causante de otomicosis y,<br />
mas raramente, agente de infecciones pulmonares y<br />
aspergilosis alergicas [5,8,10],<br />
Aspergillus terreus Thom<br />
(Figura 13.12)<br />
Colonias de crecimiento rapido (40-50 mm,<br />
MEA, 25 °C, 7 dfas), inicialmente amarillentas, vol-<br />
viendose de color pardo claro, de aterciopeladas a<br />
pulverulentas. Conidioforos de hasta 250 |am de<br />
longitud, biseriados, vesfcula subesferica. Metulas y<br />
fialides ocupando 1/2 o las 2/3 partes de la parte<br />
superior de la vesfcula. Conidios en cadenas, for-<br />
mando una compacta columna sobre la vesfcula,<br />
hialinos o amarillentos, lisos, esfericos o elipsoida-<br />
les, de 2-3 |am. En las hifas sumergidas se suelen<br />
desarrollar conidios solitarios, esfericos u ovoides y<br />
de 4-6 |am de longitud, que nacen laterales sobre<br />
cortas protuberancias.<br />
F igura 13.12. Aspergillus terreus. a: colonias sobre MEA a los<br />
7 dias de cultivo a 25 °C; b: parte apical de dos conidioforos con<br />
fialides biseriadas y conidios.<br />
Diagnostico diferencial<br />
Para diferenciarla de las otras especies de<br />
Aspergillus incluidas en el capftulo, ver Tabla 13.1.<br />
Algunos aislados clfnicos, como consecuencia de un<br />
estado de adaptation al huesped, presentan estructu-<br />
ras aberrantes y practicamente no esporulan, y si lo<br />
hacen solo producen conidios solitarios que nacen<br />
directamente de las hifas del micelio. Dicha esporulacion,<br />
asf como la apariencia de la colonia recuer-<br />
dan a un im p o rtan te p ato g en o , B la sto m yces<br />
dermatitidis [10]. Sin embargo, este ultimo al ser un<br />
tfpico hongo dimorfico se diferencia claramente por<br />
su crecimiento levaduriforme a 37 °C.<br />
Comentarios<br />
Crece abundantemente a 37 °C. Es una especie<br />
de amplia distribution, pero es mas comun en<br />
regiones tropicales y subtropicales que en las de<br />
clima templado [6]. De las especies de Aspergillus<br />
incluidas en este capftulo, A. terreus es la de menor<br />
incidencia en clfnica, a pesar de ello se ha descrito<br />
como agente productor de un amplio espectro de<br />
infecciones [5,8,10],<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Identificacion de otros hongos miceliares<br />
Cladophialophora bantiana (Sacc.) de Hoog<br />
(Figura 13.13)<br />
Colonias de crecimiento moderado a lento<br />
(15-20 mm, OA, 25 °C, 7 dias), aterciopeladas, pul-<br />
verulentas en el caso de presentar buena esporulacion,<br />
de colo r gris o liv aceo . No p resen ta<br />
conidioforos manifiestos. Conidios naciendo direc-<br />
tamente de las hifas del micelio, dispuestos en lar-<br />
gas cadenas acropetas escasamente ramificadas, de<br />
color oliva palido, lisos, elipsoidales o fusiformes,<br />
4-10 x 2,5-5 jam.<br />
Figura 13.13. Cladophialophora bantiana. a: colonia sobre OA a<br />
las 3 semanas de cultivo a 25 °C; b: micelio de donde emergen<br />
cadenas acropetas de conidios.<br />
Diagnostico diferencial<br />
Se diferencia claramente de C. carrioni por<br />
la ausencia de conidioforos y por crecer a 40 °C.<br />
Comentarios<br />
Es una especie que presenta un claro tropis-<br />
mo por el sistema nervioso central, siendo el principal<br />
agente de in feccio n es cereb rales en areas<br />
geograficas de clima templado [14], ocasionalmente<br />
produce infecciones cutaneas y subcutaneas [5,8].<br />
Cladophialophora carrionii (Trejos) de Hoog,<br />
Kwon-Chung & McGinnis<br />
(Figura 13.14)<br />
Colonias de crecimiento lento (10-15 mm,<br />
OA, 25 °C, 7 dias), aterciopeladas volviendose pul-<br />
verulentas, de color gris olivaceo. Conidioforos<br />
diferenciados, en cuyo apice se desarrollan cadenas<br />
de conidios ram ificadas que se desarticulan con<br />
cierta facilidad al ser m anipuladas. Conidios de<br />
color oliva palido, lisos o ligeramente verrugosos,<br />
fusiformes o limoniformes, 4-7 x 2-3 pm, general-<br />
mente con cicatrices evidentes en los extremos.<br />
C uando crece en m edios de cultivo pobres en<br />
nutrientes suele desarrollar ademas celulas conidio-<br />
genas similares a las que caracterizan los miembros<br />
del genero Phialophora.<br />
a<br />
Asociacion Espanola de M icoiogia<br />
Figura 13.14. Cladophialophora carrioni. a: colonia sobre OA a las<br />
3 sem anas de cultivo a 25 °C; b: conidioforo con conidios.<br />
Diagnostico diferencial<br />
Se diferencia principalmente de C. bantiana<br />
por no presentar crecimiento a 40 °C y por sus conidioforos<br />
bien diferenciados.<br />
Comentarios<br />
Crece a 37 °C. Es uno de los agentes tfpicos<br />
productores de cromoblastomicosis [1,2,10].<br />
Cladosporium herbarum (Pers.) Link ex S.F. Gray<br />
(Figura 13.15)<br />
C olonias de crecim iento m oderadam ente<br />
rapido (25-35 mm, OA, 25 °C, 7 dfas), aterciopeladas<br />
volviendose pulverulentas, de color verde oliva<br />
a verde oscuro. Conidioforos de hasta 250 pm de<br />
longitud, ramificados especialmente hacia el apice,<br />
con nodulos a lo largo del conidioforo que coinci-<br />
den con los locus formadores de conidios. Conidios<br />
en cadenas acropetas y ramificadas, pardos, general-<br />
mente verrugosos, unicelulares, elipsoidales o sub-<br />
cilfn d rico s, de 5-11 x 4-5 pm , con c icatrices<br />
prominentes y mas oscuras que el resto del conidio,<br />
pueden nacer de celulas soporte (ramoconidos) de<br />
mayor tamano con uno o mas septos transversales,<br />
de hasta 14x6 pm, que se separan del conidioforo<br />
con mucha facilidad.<br />
F igura 13.15. Cladosporium herbarum. a: colonia sobre OA a las<br />
4 semanas de cultivo a 25 °C; b: parte apical de un conidioforo con<br />
ram oconidios y cadenas acropetas de conidios.
Identificacion de otros hongos miceliares<br />
Diagnostico diferencial<br />
Se diferencia de las otras dos especies mas<br />
frecuentes del genero y tam bien descritas como<br />
oportunistas, C. cladosporioides y C. sphaerosper-<br />
mum, por el color, ornamentation e incluso forma<br />
de los conidios. C. cladosporioides posee los coni-<br />
dios de color verde palido y lisos, mientras que los<br />
de C. sphaerosperm um son predom inantem ente<br />
esfericos.<br />
Comentarios<br />
No crece a 37 °C. Cosm opolita. Se suele<br />
encontrar colonizando material vegetal en descom-<br />
posicion [6]. Es uno de los hongos tfpicos contami-<br />
nantes de laboratorio. Su implication en clfnica es<br />
cuestionable, aunque se ha descrito como agente<br />
responsable de infecciones cutaneas y queratitis<br />
[5,15],<br />
Curvularia lunata (Waskker) Boedijn<br />
(Figura 13.16)<br />
Colonias de crecimiento rapido (45-50 mm,<br />
OA, 25 °C, 7 dfas), algodonosas, grises o pardo<br />
negruzcas. Conidioforos no ramificados, a menudo<br />
marcadam ente sinuosos hacia el apice. Conidios<br />
pardo olivaceos, septados transversalmente (3 sep-<br />
tos), obovoides o anchamente mazudos, 20-30 x 8-<br />
12 pm, curvados.<br />
F igura 13.16. Curvularia lunata. a: colonia sobre OA a los 14 dias<br />
de cultivo a 25 °C; b: parte apical de un conidioforo con conidios.<br />
Diagnostico diferencial<br />
C. g e n ic u la ta , la seg u n d a e sp ecie de<br />
Curvularia de importancia clfnica, se diferencia por<br />
tener los conidios de mayor tamano (18-37 x 8-14)<br />
y predominantemente con 4 septos.<br />
Comentarios<br />
Colonizador comun de material vegetal en<br />
descom posicion. Es la especie de Curvularia de<br />
mayor incidencia en clfnica. Se ha descrito como<br />
agente responsable de casos de sinusitis y queratitis,<br />
aunque tambien ocasionando infecciones cutaneas,<br />
subcutaneas y sistemicas [5,8].<br />
Exophiala dermatitidis (Kano) de Hoog<br />
(Figura 13.17)<br />
C olonias de crecim iento restringido (14-<br />
18 mm, PDA, 25 °C, 14 dfas), levaduriformes, lisas<br />
y de color pardo a negro pardusco, aunque pueden<br />
volverse ligeramente filamentosas con el tiempo;<br />
con un pigmento pardo oscuro que difunde por el<br />
agar. Celulas levaduriformes abundantes, subesfericas<br />
u ovales. Celulas conidiogenas anelfdicas, inter-<br />
calares, laterales o terminales con uno o varios locus<br />
conidiogenicos relativam ente anchos. C onidios<br />
m ucosos, subhialinos o de color pardo palido,<br />
subesfericos o elipsoidales, 2,5-4 x 2-3 pm. Pueden<br />
observarse tam bien fialides sim ilares a las de<br />
Phialophora spp., de donde nacen conidios, elipsoidales<br />
o cilfndricos, que suelen ser mas pequenos que<br />
los anteriormente descritos.<br />
F igura 13.17. Exophiala dermatitidis. a: colonia sobre PDA a las<br />
4 semanas de cultivo; b: celulas levaduriform es y celulas conidiogenas<br />
produciendo conidios.<br />
Diagnostico diferencial<br />
La diferenciacion microscopica de las especies<br />
de Exophiala es diffcil por su gran parecido<br />
morfologico, aunque E. dermatitidis se puede reco-<br />
nocer por la production de pigmento difusible, por<br />
presentar locus conidiogenicos mas anchos que el<br />
resto de especies y por ser, de las especies descritas<br />
como oportunistas, la unica que crece a 40 °C; solo<br />
algunas cepas de E. lecani-corni crecen debilmente<br />
a dicha temperatura. No obstante, para confirmar la<br />
identificacion se deberfa recurrir a las pruebas bio-<br />
qufmicas; E. dermatitidis no asimila nitrato, nitrito,<br />
creatina ni creatinina como fuentes de nitrogeno<br />
[16]. Cabe destacar que el perfil del genero en cuan-<br />
to a especies ha variado considerablemente en estos<br />
ultimos anos a rafz de los diversos estudios sobre<br />
biologfa m olecular que se han llevado a termino<br />
principalmente a partir de cepas clfnicas [17-20].<br />
Comentarios<br />
C rece b ien a 40 °C. Es la esp ecie de<br />
Exophiala que se afsla con mayor frecuencia en clfnica.<br />
Presenta predilection por el sistema nervioso<br />
central, siendo el principal agente de infecciones<br />
cere b rale s en el E x trem o O rien te [14].<br />
Ocasionalmente se ha descrito como agente causan-<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
te de queratitis e infeceiones subcutaneas despues<br />
de traumatismos [5,7,8].<br />
Identificacion de otros hongos miceliares<br />
Fonsecaea pedrosoi (Brumpt) Negroni<br />
(Figura 13.18)<br />
Colonias de crecimiento lento (18-25 mm,<br />
PDA, 25 °C, 14 dfas), verde o gris oscuras a negruz-<br />
cas, aterciopeladas, pulverulentas cuando esporulan<br />
a los, aproximadamente, 14 dfas. Conidioforos erec-<br />
tos, ramificados, con zonas terminales o intercala-<br />
res, ligeram ente hinchadas, de donde em ergen<br />
cortas proyecciones (dentfculos) que dan lugar a los<br />
conidios. Los conidios a su vez pueden formar cortas<br />
cadenas acropetas que, en conjunto, recuerdan la<br />
conidiacion de Cladosporium. El hecho de presentar<br />
un maximo de 3 o 4 conidios por cadena y la presencia<br />
de dentfculos prom inentes a lo largo del<br />
conidioforo, la diferencian de cualquier miembro de<br />
Cladosporium. Los conidios que derivan de estas<br />
estructuras son lisos, subhialinos o pardo claro,<br />
ovoides, 2-6 x 1,5-3 pm . A dicionalm ente, este<br />
hongo puede tambien desarrollar conidios a partir<br />
de fia lid e s sim ilares a las de P h ia lo p h o ra<br />
verrucosa.<br />
a<br />
F ig ura 13.18. Fonsecaea pedrosoi. a: colonia sobre OA a los<br />
14 dias de cuitivo a 25 °C; b: parte apical de un conidioforo con<br />
denticulos produciendo conidios; c: detalle del collarete de una<br />
fialide con un conidio en su interior.<br />
Diagndstico diferencial<br />
F. compacta, la otra especie del genero des-<br />
crita como oportunista aunque con mucha menos<br />
frecuencia, se diferencia de F. pedrosoi por crecer y<br />
esporular mas lentamente (un mfnimo de 4 sema-<br />
nas), sus conidios son subesfericos y sus cadenas se<br />
desarticulan con dificultad [7,15].<br />
Comentarios<br />
Crece a 37 °C. Se afsla con relativa frecuencia<br />
de material vegetal y del suelo de regiones con<br />
clima tropical. Constituye uno de los principales<br />
agentes de crom oblastom icosis en los pafses de<br />
Latinoamerica. Tambien se ha descrito produciendo<br />
queratitis, feohifomicosis subcutaneas y en un caso<br />
de absceso cerebral [5,15].<br />
Asociacion Espanola de M icologia<br />
Fusarium oxysporum Schltdl.<br />
(Figura 13.19)<br />
Colonias de crecimiento rapido (65-70 mm,<br />
PDA, 25 °C, 7 dfas), algodonosas, con areas de<br />
color bianco mezcladas con zonas de color purpura,<br />
pudiendo aparecer en la superficie del agar masas<br />
mucosas de color anaranjado formadas por conidios<br />
largos y septados (m acroconidios) que nacen de<br />
esporodoquios. Conidioforos cortos, ramificados o<br />
no, naciendo de hifas aereas o de esporodoquios.<br />
Fialides cortas, de 8-14 pm de longitud, naciendo de<br />
conidioforos del sustrato que producen macroconidios,<br />
o de hifas aereas produciendo predominante-<br />
m ente co n id io s p equenos y u n icelu ares<br />
(microconidios), en forma de botella o mas o menos<br />
cilfndricas. Macroconidios en masas mucosas, de 4-<br />
5 septos, ligeramente curvados, fusiformes, 20-45 x<br />
3-4,5 pm. Microconidios en masas mucosas, gene-<br />
ralmente unicelulares, pueden ser ligeramente curv<br />
ados, e lip so id a le s o cilfn d ric o s, de 5-12 x<br />
2,5-4 pm. Clamidosporas terminales e intercalares,<br />
lisas o verrugosas de hasta 12 pm de ancho.<br />
F ig ura 13.19. Fusarium oxysporum. a: colonias sobre PDA a los<br />
7 dias de cuitivo a 25 °C; b: fialides del micelio aereo produciendo<br />
microconidios.<br />
Diagndstico diferencial<br />
Para diferenciarla de las otras especies de<br />
Fusarium incluidas en este capftulo, ver Tabla 13.2.<br />
Comentarios<br />
Puede crecer a 37 °C. Es una especie de<br />
amplia distribution, comunmente aislada de suelo y<br />
se ha descrito tambien como patogena de plantas<br />
[6]. Es la especie de Fusarium mas frecuentemente<br />
descrita como agente de onicomicosis en humanos,<br />
aunque tambien se ha descrito en casos de queratitis<br />
pero su incid en cia es m ucho m enor que la de<br />
F. solani. Raramente se ha asociado a infecciones<br />
cutaneas y diseminadas [5,10],
Tabla 13.2. Diferencias morfologicas entre las especies de Fusarium mas frecuentes en clfnica.<br />
Especie Colonias Fialides de<br />
hifas aereas<br />
F. oxysporum algodonosas,<br />
blanquecinas con<br />
zonas de color<br />
purpura palido<br />
F. solani lanosas,<br />
blanquecinas con<br />
zonas pupura palido,<br />
volviendose pardo<br />
claro o rojizo<br />
F. verticlllioldes algodonosas<br />
o pulverulentas,<br />
micelio aereo<br />
blanquecino,<br />
micelio sumergido<br />
de color violaceo<br />
Fusarium solani (C. Mart.) Sacc.<br />
(Figura 13.20)<br />
Colonias de crecimiento rapido (65-70 mm,<br />
PDA, 25 °C, 7 dfas), generalmente lanosas, de color<br />
bianco o crema, tambien de color pardo claro, pardo<br />
rojizo m ezcladas con zonas de color purpura e,<br />
incluso, pueden presentar (aunque raram ente en<br />
cepas clfnicas) masas mucosas verde azuladas for-<br />
madas por macroconidios que nacen de esporodo-<br />
quios. C onidioforos de esporodoquios cortos,<br />
ramificados; conidioforos de hifas aereas generalmente<br />
no ramificados, muy largos, reducidos a una<br />
simple fialide mas o menos cilfndrica, de hasta 40 x<br />
2-3 |im, en cuyo apice se suele encontrar un conidio<br />
no desprendido. Macroconidios en masas mucosas,<br />
hialinos, mayormente con 3 septos, ligeramente cur-<br />
vados, fusiformes pero con extremos mas o menos<br />
redondeados, 28-50 x 4-6 |im. M icroconidios en<br />
masas mucosas, hialinos, lisos, generalmente unice-<br />
lulares, pueden ser ligeramente curvados, elipsoida-<br />
les o su b cilfn d rico s, de 7-16 x 2 ,5 -4 ,5 pm .<br />
Clam idosporas term inales e intercalares, lisas o<br />
verrugosas, parduscas, de hasta 10 pm de ancho.<br />
Diagnostico diferencial<br />
Para diferenciarlo de las otras especies de<br />
Fusarium incluidas en este capftulo, ver Tabla 13.2.<br />
Cabe destacar que a partir de los recientes estudios<br />
moleculares realizados principalmente con cepas no<br />
clfnicas queda patente que se trata de una especie<br />
muy heterogenea y que bajo esta denomination se<br />
cortas (< 14 pm long.),<br />
laterales,<br />
cilfndricas o en<br />
forma de botella<br />
muy largas (< 40 pm long.),<br />
cilfndricas,<br />
a menudo con un<br />
conidio adherido<br />
en el apice<br />
Conidios Clamidosporas<br />
macroconidios<br />
usualmente de<br />
4-5 septos,<br />
con extremos picudos;<br />
microconidios en<br />
masas mucosas<br />
macroconidios<br />
usualmente de<br />
3 septos, con<br />
extremos romos;<br />
microconidios en<br />
masas mucosas<br />
subuladas (< 32 pm long.) macroconidios<br />
usualmente de<br />
3-5 septos,<br />
con extremos picudos;<br />
microconidios en<br />
largas cadenas<br />
presentes<br />
presentes<br />
ausentes<br />
Figura 13.20. Fusarium solani. a: colonias sobre PDA a los 7 dias<br />
de cultivo a 25 °C; b: fialides del micelio aereo produciendo microconidios.<br />
incluyen mas de 25 entidades que muy bien pueden<br />
considerarse especies diferentes [21,22],<br />
Comentarios<br />
Puede crecer a 37 °C. Cosmopolita. Se afsla<br />
a partir de una amplia gama de sustratos y, al igual<br />
que F. oxysporum, es un fitopatogeno importante<br />
[6], En humanos es la especie de Fusarium que se<br />
afsla con mayor frecuencia, siendo el agente mas<br />
comun de queratitis, asf como de infecciones cuta-<br />
neas y diseminadas en individuos inmunocompro-<br />
m etidos, especialm ente pacientes neutropenicos<br />
[5,8,10],<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Fusarium verticillioides (Sacc.) Nirenberg<br />
(Figura 13.21)<br />
Colonias de crecim iento muy rapido (80-<br />
90 mm, PDA, 25 °C, 7 dfas), algodonosas o pulve-<br />
rulentas, m icelio aereo de color bianco, m icelio<br />
inmerso en el medio de cultivo de color violaceo.<br />
Conidioforos que nacen de hifas aereas generalmen-<br />
te consistentes en simples fialides subuladas, de<br />
hasta 32 fim de longitud, productoras de microconi-<br />
dios; conidioforos del sustrato ramificados, agrupa-<br />
dos fo rm an d o esp o ro d o q u io s en donde se<br />
diferencian los macroconidios (raros en cepas clfni-<br />
cas). Macroconidios en masas mucosas, hialinos,<br />
con 3-5 septos, rectos o falciformes, 20-55 x 2,5-<br />
4 |jm. M icroconidios en cadenas (pueden formar<br />
m asas m ucosas si crecen en m edios rico s en<br />
nutrientes o por un exceso de humedad), unicelula-<br />
res, hialinos, lisos, mazudos y generalmente con la<br />
base plana, de 7-12 x 2,5-3,5 |am. Clamidosporas<br />
ausentes.<br />
F ig ura 13.21. Fusarium verticillioides. a: colonias sobre PDA a<br />
los 7 dias de cultivo a 25 °C; b: fialide con conidio; c: cadena de<br />
conidios desarticulada.<br />
Diagndstico diferencial<br />
Para diferenciarla de las otras especies de<br />
Fusarium incluidas en este capftulo, ver Tabla 13.2.<br />
Comentarios<br />
Puede crecer a 37 °C. F. verticillioides junto<br />
a F. oxysporum son, despues de F. solani. las especies<br />
del genero mas comunmente descritas como<br />
agentes de infecciones cutaneas y diseminadas en<br />
pacientes severam ente inm unocom prom etidos.<br />
Tambien se ha aislado, aunque raramente, en infecciones<br />
subcutaneas de pacientes inmunocompeten-<br />
tes y en queratitis [5,10],<br />
Paecilomyces lilacinus (Thom) Samson<br />
(Figura 13.22)<br />
C olonias de crecim iento m oderadam ente<br />
rapido (40-50 mm, PDA, 25 °C, 14 dfas), de color<br />
rosa palido a vinaceo, de flocosas a pulverulentas.<br />
Conidioforos de hasta 500 urn de longitud, rugosos,<br />
portadores de un compacto grupo de ramas hacia el<br />
apice, en cuyos extremos se desarrollan grupos (ver-<br />
Identificacion de otros hongos miceliares<br />
Asociacion Espahola de M icologia<br />
ticilos) de fialides. Fialides de base mas o menos<br />
hinchada y cuello largo (lageniformes), 7-10 x 2,5-<br />
3,5 |am. Conidios en largas cadenas divergentes,<br />
subhialinos, unicelulares, elipsoidales o fusiformes,<br />
2-3 x 2-2,5 |jm, lisos o ligeramente equinulados.<br />
Clamidosporas ausentes.<br />
F ig ura 13.22. Paecilom yces lilacinus. a: colonias sobre PDA a<br />
los 7 dias de cultivo a 25 °C; b: parte apical de un conidioforo con<br />
fialides y conidios.<br />
Diagndstico diferencial<br />
Podrfa confundirse con P. marquandii des-<br />
crita tam bien com o oportunista, aunque m ucho<br />
menos frecuente. No obstante, los conidioforos de<br />
esta ultima especie son lisos, desarrolla clamidosporas<br />
y el reverso de las colonias es amarillento.<br />
Comentarios<br />
Es una especie ampliamente distribuida y se<br />
afsla comunmente del suelo, insectos y de material<br />
vegetal [6]. Hasta la fecha, se han descrito un total<br />
de ocho especies de Paecilomyces como oportunistas<br />
para el hombre [5], pero las dos mas frecuentes<br />
son P. lilacinus y P. variotii. El espectro de infecciones<br />
es similar en ambas especies. P. lilacinus es<br />
un agente comun de sinusitis, aunque tambien se ha<br />
descrito como agente de queratitis, bursitis, endocarditis,<br />
micosis cutaneas y subcutaneas; los casos<br />
de infection diseminada o neumonfa siempre se dan<br />
en individuos severamente inmunocomprometidos<br />
[5,8],<br />
Paecilomyces variotii Bainier<br />
(Figura 13.23)<br />
Colonias de crecim iento muy rapido (70-<br />
80 mm, PDA, 25 °C, 7 dfas), inicialmente blancas y<br />
flocosas, volviendose de color amarillo verdoso o<br />
amarillo pardusco y pulverulentas. Conidioforos de<br />
hasta 200 (am de longitud, lisos, repetidam ente<br />
ramificados, con ramas dispuestas en verticilos o<br />
irregularmente distribuidas, portadoras de 2-7 fialides.<br />
Fialides lageniform es, de base elipsoidal o<br />
cilfndrica, 9-18 x 2,5-4 |im . Conidios en largas<br />
cadenas divergentes, amarillentos, uniceluares, elip-<br />
soidades o mazudos, 3-6,5 x 1,5-3,5 |jm, a menudo
Identificacion de otros hongos miceliares<br />
con extremos truncados, lisos. Clamidosporas abun-<br />
dantes en cultivos viejos, esfericas o subesfericas, 4-<br />
8 pm de ancho, color pardo, lisas o ligeramente<br />
verrugosas.<br />
F igura 13.23. Paecilomyces variotii. a: colonias sobre PDA a los<br />
7 dias de cultivo a 25 °C; b: parte apical de un conidioforo con<br />
fialides y conidios.<br />
Diagnostico diferencial<br />
Es una especie similar a la fase conidial del<br />
ascomicete Thermoascus crustaceus. La diferencia<br />
entre ambos hongos radica principalmente en que<br />
este ultimo siempre se desarrolla junto a la forma<br />
sexual y nunca presenta clamidosporas. A diferencia<br />
de P. lilacinus, las cepas de P. variotii son capaces<br />
de crecer a 45-50 °C, por eso se define como un<br />
hongo termofilo [5,10].<br />
Comentarios<br />
Es de amplia distribution y se afsla del aire y<br />
de una gran variedad de sustratos tales como suelo,<br />
aguas polucionadas, madera, papel, etc. [6], Se ha<br />
descrito como agente responsable de infecciones<br />
muy diversas, tanto en animales como en el hombre<br />
[5,8],<br />
Phaeoacremonium parasiticum (Ajello, Georg &<br />
Chin C Wang) W. Gams, Crous & Wingfield<br />
(Figura 13.24)<br />
C olonias de crecim iento m oderado (25-<br />
30 mm, PDA, 25 °C, 14 dfas), inicialmente blanque-<br />
cinas y con escaso micelio aereo, volviendose de<br />
color pardo grisaceo y aterciopeladas, excepto el<br />
m argen que sigue siendo de color blanquecino.<br />
Conidioforos escasamente ramificados, a menudo<br />
son muy simples y estan formados por una sola<br />
celula conidiogena (fialide). Fialides de longitud<br />
variable, mas o menos cilmdricas o subuladas, 15-<br />
45 x 2-3 pm, con un collarete tubular en el extremo,<br />
la base de la fialide suele tener la pared mas gruesa<br />
y presenta incrustaciones. Conidios acumulandose<br />
en masas mucosas, unicelulares, lisos, hialinos, elip-<br />
soidales o cilfndricos, 2,5-6 x 1-2 pm, a menudo<br />
curvados.<br />
F igura 13.24. Phaeoacremonium parasiticum. a: colonias sobre<br />
PDA a los 14 dias de cultivo a 25 °C; b: fialides produciendo<br />
conidios.<br />
Diagndstico diferencial<br />
P. aleophilum, P. inflatipes, P. parasiticum y<br />
P. ru b rigenum son las cuatro esp ecies de<br />
Phaeoacremonium descritas hasta la fecha como<br />
oportunistas [23], siendo las dos ultimas morfolo-<br />
gicam ente m uy sim ilares. Podem os d istin g u ir<br />
a P. rubrigenum por el color rojizo del reverso<br />
de sus colonias y porque es una especie que crece<br />
escasamente a 37 °C. P. parasiticum crece bien a<br />
dicha temperatura y sus colonias no producen ese<br />
pigmento.<br />
Comentarios<br />
Anteriormente conocida como Phialophora<br />
parasitica. Se describe como hongo fitopatogeno<br />
importante, aunque tambien es agente responsable<br />
de numerosos casos de infecciones en el hombre,<br />
principalmente subcutaneas [5,7]. De hecho, es la<br />
especie de Phaeoacremonium que se afsla mas fre-<br />
cuentemente en clfnica.<br />
Phialophora verrucosa Medlar<br />
(Figura 13.25)<br />
C olonias de crecim iento m oderadam ente<br />
lento (18-20 mm, PDA, 25 °C, 14 dfas), gris oliva-<br />
ceas y flocosas, volviendose negruzcas y lanosas<br />
con el tiempo. Fialides generalmente solitarias, cre-<br />
ciendo perpendiculares sobre las hifas vegetativas,<br />
lisas, de color pardo, en forma de botella, raramente<br />
cilmdricas, 8-24 x 3-4 pm, con un collarete promi-<br />
nente mas ancho (3-4,5 pm) que largo (2,5-3,5 pm)<br />
y mas oscuro que el resto de la fialide. Conidios en<br />
masas mucosas sobre las fialides, lisos, subhialinos,<br />
ovoides o elipsoidales, 2,5-5 x 1,5-3 pm.<br />
Diagnostico diferencial<br />
P. verrucosa es morfologicamente muy similar<br />
a P. americana. La principal diferencia entre<br />
ambas estriba en la forma del collarete de la fialide,<br />
que es mas largo que ancho (3,5-5 x 2-3 pm) en la<br />
ultima especie.<br />
©2004 Revista Iberoamericana de Micologi'a - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
a<br />
F igura 13.25. Phialophora verrucosa, a: colonia sobre PDA a los<br />
14 dias de cultivo a 25 °C; b: fialides con collarete manifiesto.<br />
Comentarios<br />
La m ayorfa de las cepas crecen a 37 °C.<br />
Es uno de los principales agentes productores de<br />
cromoblastomicosis y ocasionalmente se ha descrito<br />
en casos de feohifomicosis y micetomas [2,5,8].<br />
Identificacion de otros hongos miceliares<br />
Scedosporium apiospermum (Sacc.) Sacc.<br />
(Figura 13.26)<br />
C olonias de crecim iento m oderadam ente<br />
rapido (35-40 mm, PDA, 25 °C, 7 dfas), blancas y<br />
algodonosas, pero a medida que aumenta la esporulacion<br />
se vuelven de color gris o gris pardusco.<br />
Celulas conidiogenas (anelides) mas o menos cilfn-<br />
dricas, desarrollandose directam ente sobre hifas<br />
indiferenciadas o a partir de conidoforos escasa-<br />
m ente ram ificados. Conidios acum ulandose en<br />
masas mucosas sobre las anelides o solitarios y sesi-<br />
les desarrollandose de las hifas del micelio, lisos, de<br />
color pardo amarillento, ovales o elipsoidales, 5-12<br />
x 4-6,5 pm, con la base anchamente truncada.<br />
F ig ura 13.26. Scedosporium apiosperm um . a: colonia sobre PDA<br />
a los 14 dias de cultivo a 25 °C; b: anelides produciendo conidios.<br />
Diagnostico diferencial<br />
Se distingue de la otra especie del genero,<br />
S. prolificans, porque los conidios de esta ultima<br />
son ovoides y sus anelides presentan una base mas o<br />
m enos hinchada. Cabe destacar que en algunas<br />
cepas esta form a conidial se desarrolla junto a<br />
la fase sexual del hongo, Pseudallescheria boydii.<br />
Asociacion Espanola de M icologia<br />
Esta se caracteriza por desarrollar cuerpos fructffe-<br />
ros (ascomas) a los 7-10 dfas de incubation, esfericos<br />
(50-250 pm ), negruzcos, que al rom perse<br />
emergen esporas pardo amarillentas, lisas y elipsoidales,<br />
6-8,5 x 3,5-5,5 pm. En otras cepas, tambien<br />
ocasionalmente, S. apiospermum se desarrolla junto a<br />
otra forma conidial, Graphium. Esta se caracteriza<br />
por el desarrollo de conidioforos largos, erectos, de<br />
color marron y ramificados hacia el apice, los cuales<br />
se van agrupando formando sinemas en cuyo apice se<br />
acumulan los conidios mucosos. Los conidios de esta<br />
estructura suelen ser mas o menos cilfndricos o mazu-<br />
dos y suelen ser mas delgados (4-12 x 2-4 pm).<br />
Comentarios<br />
Todas las cepas crecen bien a 37 °C y la<br />
mayorfa tambien a 40 °C. Es un hongo telurico, de<br />
amplia distribution. Las cepas clfnicas raramente<br />
desarrollan la fase sexual. Su epidemiologfa es similar<br />
a la de Aspergillus fumigatus, afectando princi-<br />
palmente a pacientes neutropenicos o tratados con<br />
corticosteroides. El hongo tiene una marcada predilection<br />
por el sistema nervioso central, aunque pre-<br />
senta un amplio espectro de infecciones que pueden<br />
afectar tejido subcutaneo, huesos, pulmones, etc.<br />
[2,5,8,24],<br />
Scedosporium prolificans (Hennebert & B.G.<br />
Desai) E. Gueho & de Hoog<br />
(Figura 13.27)<br />
C olonias de crecim iento m oderado (18-<br />
23 mm, PDA, 25 °C, 7 dfas), de color verde grisa-<br />
ceo, generalmente mucosas, a menudo con micelio<br />
aereo algodonoso y blanquecino en el centro.<br />
Conidioforos cortos, generalmente ramificados, con<br />
mas de una celula conidiogena (anelide) por rama.<br />
A nelides creciendo solitarias de las hifas o en<br />
pequenos grupos de las ramas de los conidioforos,<br />
en forma de botella, a menudo con un largo cuello<br />
con cicatrices anulares poco evidentes, 10-30 x 2,5-<br />
5 pm. Conidios en masas mucosas, lisos, subhiali-<br />
nos o de color pardo olivaceo, ovoides, 4,5-8 x<br />
3-6 pm. Pueden desarrollarse tambien conidios sesi-<br />
les sobre las hifas indiferenciadas que suelen ser<br />
mas oscuros y mas hinchados.<br />
Figura 13.27. Scedosporium prolificans. a: colonias sobre PDA a<br />
los 14 dias de cultivo a 25 °C; b: conidioforos con anelides produciendo<br />
conidios.
Identificacion de otros hongos miceliares<br />
Diagnostico diferencial<br />
Se diferencia de S. apiospermum por la mor-<br />
fologfa de las celulas conidiogenas y de los conidios<br />
(ver diagnostico diferencial de S. apiospermum).<br />
Comentarios<br />
Todas las cepas crecen bien a 37 °C y la<br />
mayorfa tambien a 40 °C. Es un hongo emergente<br />
cuyo reservorio todavfa es incierto. Se ha aislado de<br />
suelos de maceta, de invernaderos [5] y en nuestro<br />
laboratorio hemos aislado cepas de S. prolificans a<br />
partir de muestras de suelo procedentes de jardines<br />
publicos (datos no publicados). Por lo que podemos<br />
suponer que, al igual que su congenere, es un hongo<br />
colonizador de suelos principalmente ricos en materia<br />
organica. El espectro de infecciones es similar al<br />
de S. apiosperm um ; sin embargo, se asocia mas<br />
comunmente a osteomielitis y artritis en humanos y<br />
animales [24]. En nuestro pais y en Australia se han<br />
descrito numerosos casos de infecciones disemina-<br />
das, principalmente en pacientes inmunocomprome-<br />
tid o s. La m ayoria de casos de in feccio n es<br />
localizadas se han descrito en los EE UU [25].<br />
Scopulariopsis brevicaulis (Sacc.) Bainier<br />
(Figura 13.28)<br />
C olonias de crecim iento m oderado (42-<br />
46 mm, PDA, 25 °C, 14 dfas), de color beige con<br />
margen blanquecino, de aspecto pulverulento si la<br />
esporulacion es abundante. Conidioforos general -<br />
mente cortos pero ram ificados, con mas de una<br />
celula conidiogena (anelide) por rama. Anelides<br />
creciendo solitarias de las hifas o en pequenos<br />
grupos de las ramas de los conidioforos, cilmdricas<br />
o en forma de botella, 10-25 x 3-5 |am, con un cue-<br />
llo con cicatrices anulares manifiestas. Conidios for-<br />
m ado larg as caden as b asfp etas, su b h ialin o s,<br />
inicialmente lisos volviendose marcadamente verrugosos,<br />
subesfericos, con la base anchamente trunca-<br />
da, 5-8 x 5-7 pm.<br />
F igura 13.28. Scopulariopsis brevicaulis. a: colonia sobre PDA<br />
a los 14 dfas de cultivo a 25 °C; b: conidioforos con anelides<br />
produciendo conidios en cadena.<br />
Diagnostico diferencial<br />
Las dos especies del genero que mas comunm<br />
ente se afslan en clinica son S. brevicaulis y<br />
S. brumptii, aunque esta ultima con mucha menos<br />
frecuencia. Las colonias de S. brumptii se caracteri-<br />
zan por ser de color gris oscuro y crecer lentamente.<br />
S. brumptii podrfa confundirse con S. prolificans.<br />
Sin embargo, los conidos dispuestos en cadenas y el<br />
aspecto pulverulento de las colonias son los caracte-<br />
res principales que diferencian S. brum ptii de<br />
S. prolificans.<br />
Comentarios<br />
Crece a 37 °C. Es una especie de amplia distribution,<br />
la mas comun del genero. Se afsla de una<br />
gran variedad de sustratos (suelo, madera y material<br />
vegetal en general, insectos m uertos, estiercol,<br />
papel, etc.) [6], Es uno de los principales agentes de<br />
onicomicosis no dermatofftica. A su vez, se ha descrito,<br />
aunque esporadicam ente, como agente de<br />
endocarditis, queratitis y de infecciones invasoras<br />
tanto en individuos inm unocom petentes com o<br />
inmunocomprometidos [5,24].<br />
A continuation se incluye una clave dicoto-<br />
mica para la identificacion de los generos de hifomi-<br />
cetes m as fre c u e n tem e n te aislad o s com o<br />
oportunistas para el hombre.<br />
©2004 Revista Iberoamericana de Micoiogia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Identificacion de otros hongos miceliares<br />
Clave dicotomica de los generos de hifomicetes oportunistas mas frecuentes en clrnica<br />
1 Colonias de colores oscuros (verde o pardo oscuro, n e g ru z c a s ).................................................................................................2<br />
Colonias de otros colores......................................................................................................................................................................13<br />
2 Colonias no m ucosas................................................................................................................................................................................ 3<br />
Colonias mucosas, al menos cuando son jovenes. Celulas conidiogenas anelidicas.<br />
Conidios unicelulares, hialinos o subhialinos................................................................................................................ E xophiala<br />
3 Conidios dispuestos en ca d e n a s ...........................................................................................................................................................4<br />
Conidos en otra disposicion...................................................................................................................................................................9<br />
4 Conidios unicelulares y/o con solo septos transversales................................................................................................................. 5<br />
Conidos con septos trasversales y longitudinales, grandes, parduscos, de base mas ancha que el apice . . A lte rn a ria<br />
5 Crecen a 37 °C o a temperaturas superiores......................................................................................................................................6<br />
No crecen a 37 °C. Conidioforos ramificados. Cicatrices conidiales muy marcadas y a menudo mas oscuras .. C la d o sp o riu m<br />
6 Conidioforos no ramificados, con un hinchamiento apical (vesi'cula). Conidios esfericos y<br />
muy ornamentados...............................................................................................................................................................A s p e rg illu s<br />
Conidioforos y conidios con otras c a ra cte ristica s........................................................................................................................... 7<br />
7 Conidos formando cadenas acropetas..................................................................................................................................................8<br />
Conidos formando cadenas basipetas, naciendo de anelides.........................................................S co p u la rio p sis<br />
8 Cadenas conidiales cortas (maximo 3-4 conidios), no ramificadas, junto a conidios solitarios y<br />
naciendo de denticulos agrupados en el apice de las ramas de un conidioforo o intercalares......................... Fonsecaea<br />
Cadenas de conidos largas, generalmente ramificadas; dentfculos a u s e n te s .....................C ladophialophora<br />
9 Conidos unicelulares y pequenos (< 15 pm long.).......................................................................................................................... 10<br />
Conidos septados transversalmente, de gran tamano (> 15 pm long.), muy curvados o solo ligeramente. . C urvularia<br />
10 Conidos solitarios naciendo sobre denticulos prominentes agrupados en el apice de las ramas del<br />
conidioforo o intercalares, tambien pueden formar cadenas c o rta s ........................................................................ Fonsecaea<br />
Conidos formando masas mucosas en el apice de las celulas conidiogenas.........................................................................11<br />
11 Celulas conidiogenas con collarete manifiesto (fialide). Conidos pequenos (< 6 pm lo n g .) ................................................12<br />
Celulas conidiogenas sin collarete, y con un largo y estrecho cuello (anelides),<br />
especialmente manifiesto al envejecer el hongo. Conidos mas grandes (> 6 pm lo n g .)............................S cedosporium<br />
12 Collarete abierto, en forma de copa y generalmente mas oscuro que el resto de la fialide.<br />
Fialide en forma de b o te lla .............................................................................................................................................. P hialophora<br />
Collarete cih'ndrico. Fialide larga, cilfndrica, subulada (estrechandose hacia el apice)<br />
o lageniforme (base ligeramente hinchada), con paredes engrosadas hacia la base........P haeoacrem onium<br />
13 Conidos de un solo tip o ......................................................................................................................................................................... 14<br />
Conidios de dos tipos (macro y microconidos). Macroconidios largos, septados transversalmente<br />
y ligeramente curvados; microconidios unicelulares o con pocos s e p to s ................................................................. Fusarium<br />
14 Conidios en ca d e n a ................................................................................................................................................................................ 15<br />
Conidos en masas m u c o s a s ...............................................................................................................................................................18<br />
15 Conidioforos no ramificados, terminados en una ve sicu la ......................................................................................... A s p e rg illu s<br />
Conidioforos ramificados, si no lo estan generalmente consisten en una celula conidiogena +/- c ilin d ric a ...................16<br />
16 Conidioforos ramificados, en forma de pincel. Colonias de color beige, lilaceas o blanquecinas.<br />
Cadenas de conidios bastante persistentes..................................................................................................................................... 17<br />
Conidioforos poco o nada ramificados. Colonias de blanquecinas a violaceas. Cadenas conidiales<br />
desarticulandose con mucha facilidad................................................................................................................................ F usarium<br />
17 Conidos esfericos o subesfericos, naciendo de anelides de cuello ancho y generalmente con<br />
cicatrices anulares evidentes................................................................................................................... S co p u la rio psis<br />
Conidos elipsoidales o cilmdricos, naciendo de fialides con cuello largo y estrecho,<br />
y base generalmente h in c h a d a ...................................................................................................................................P aecilom yces<br />
18 Conidos naciendo de fialides largas, cilfndricas o subuladas, que emergen perpendiculares<br />
de las hifas del micelio. Conidios pequenos (< 6 pm long.) .......................................................................................................19<br />
Conidos naciendo de anelides y de mayor tamano (> 6 pm long.)................................................. S cedosporium<br />
19 Colonias siempre de colores palidos (rosadas, amarillentas, blanquecinas, etc.)............................................. A crem onium<br />
(ver tambien Fusarium)<br />
Colonias que oscurecen al e n v e je c e r........................................................................................................... P haeoacrem onium<br />
Asociacion Espahola de M icologia
Referencias<br />
Identificacion de otros hongos miceliares<br />
1. Rippon JW. Medical mycology: the pathogenic fungi and<br />
the pathogenic actinom ycetes, 3 " ed, Philadelphia, Pa.,<br />
WB Saunders Co., 1988.<br />
2. Kwon-Chung KJ, Bennett JE. Medical mycology.<br />
Philadelphia, Pa., Lea & Febiger, 1992.<br />
3. Schipper MAA, Stalpers JA. Zygomycetes. The orden<br />
mucorales. En: Howard DH, Pathogenic fungi in humans<br />
and animals, 2nd ed, New York, Marcel Dekker, <strong>Inc</strong>., 2003.<br />
4. Ribes JA, Vanovers-Sam s CL, Baker DJ. Zygom ycetes in<br />
human disease. Clin Microbiol Rev 2000; 13: 236-301.<br />
5. De Hoog SG, Guarro J, Gene J, Figueras MJ. Atlas of clinical<br />
fungi. 2nd ed. Utrecht, The Netherlands, Centraalbureau<br />
voor Schimmelcultures, 2000.<br />
6. Domsch KH, Gams W, Anderson TH. Com pendium of soil<br />
fungi. London, Academ ic Press, 1980.<br />
7. Larone DH. Medical important fungi. A guide to identification.<br />
W ashington DC, ASM Press, 2002.<br />
8. Anaissie EJ, M cGinnis MR, Pfaller MA. Clinical mycology.<br />
New York, Churchill Livingstone, 2003.<br />
9. Padhye AA, Ajello L. Simple method of inducing s p o lia <br />
tion by Apophysom yces elegans and Saksenaea vasifor-<br />
mis. J Clin Microbiol 1988; 26: 1861-1863.<br />
10. Summerbell R. Aspergillus, Fusarium, Sporothrix, Piedraia,<br />
and their relatives, p. 237-498. En: Howard DH, Pathogenic<br />
fungi in humans and animals, 2 " ed, New York, Marcel<br />
Dekker, <strong>Inc</strong>., 2003.<br />
11. Guarro J, Gams W, Pujol I, Gene J. Acrem onium species:<br />
new emerging fungal opportunists-in vitro antifungal susceptibilities<br />
and review. Clin Infect Dis 1997; 25: 1222-<br />
1229.<br />
12. Novicki TJ, LaFe K, Bui L, Bui U, Geise R, Marr K,<br />
Cookson BT. Genetic diversity among clinical isolates of<br />
Acrem onium strictum determined during an investigation of<br />
a fatal mycosis. J Clin Microbiol 2003; 41: 2623-2628.<br />
13. Malloch D. Moulds. Their isolation, cultivation and identification.<br />
Toronto, Universiy of Toronto Press, 1981.<br />
14. Horre R, de Hoog GS. Primary cerebral infections by mela-<br />
nized fungi: a review. Stud Mycol 1999; 43: 176-193.<br />
15. Schell WA. Dematiaceous hyphomycetes. En: Howard DH,<br />
Pathogenic fungi in hum ans and animals, 2"d ed, New York,<br />
Marcel Dekker, <strong>Inc</strong>., 2003.<br />
16. De Hoog GS, Gerrits van den Ende AHG, Uijthof JMJ,<br />
Untereiner WA. Nutricional physiology of type isolates of<br />
currently accepted species of Exophiala and<br />
Phaeococcomyces. Antonie van Leeuwenhoek 1995; 68:<br />
43-49.<br />
17. Wang L, Yojoyam a K, Miyaji M, Nishimura K. Identification,<br />
classification, and phylogeny of the pathogenic species<br />
Exophiala jeanselm ei and related species by mitochondrial<br />
cytochrome b gene analysis. J Clin Microbiol 2001; 39:<br />
4462-4467.<br />
18. Vitale RG, de Hoog GS. M olecular diversity, new species<br />
and antifungal susceptibilities in the Exophiala spinifera<br />
clade. Med Mycol 2002, 40: 545-556.<br />
19. De Hoog GS, Vicente V, Caligiorne RB, Kantarcioglu S,<br />
Tintelnot K, Gerrits van den Ende AHG, Haase G.<br />
Species diversity and polym orphism in the Exophiala<br />
spinifera clade containing opportunistic black yeast-like<br />
fungi. J Clin Microbiol 2003, 41: 4767-4778.<br />
20. Bossier AD, Richter SS, Chavez AJ, Vogelgesang SA,<br />
Sutton DA, Grooters AM, Rinaldi MG, de Hoog GS,<br />
Pfaller MA. Exophiala oligosperm a causing olecranon<br />
bursitis. J Clin Microbiol 2003; 41: 4779-4782.<br />
21. O ’Donnell K. M olecular phylogeny of the Nectria haem ato-<br />
cocca-F. solani species complex. Mycologia 2000; 92:<br />
919-938.<br />
22. Aoki T, O ’Donnell K, Homma Y, Lattanzi AR. Sudden-<br />
death syndrom e of soybean is caused by two m orphologically<br />
and phylogenetically distinc species within the<br />
Fusarium solani species com ple x— F. virguliforme in<br />
North Am erica and F. tucum aniae in South America.<br />
Mycologia 2003; 95: 660-684.<br />
23. Guarro J, Hartz Alves S, Gene J, Aparecida Grazziotin N,<br />
Mazzuco R, Dalmagro C, Capilla J, Zaror L, Mayayo E.<br />
Two cases of subcutaneous infection due to<br />
Phaeoacrem onium spp. J Clin Microbiol 2003; 41: 1332-<br />
1336.<br />
24. Sigler L. M iscelaneous opportunistic fungi. Microascaceae<br />
and other ascomycetes, hyphomycetes, coelom icetes, and<br />
basidiomycetes. En: Howard DH, Pathogenic fungi in<br />
humans and animals, 2“ ed, New York, Marcel Dekker,<br />
<strong>Inc</strong>., 2003.<br />
25. Ortoneda M, Pastor FJ, Mayayo E, Guarro J. Comparison<br />
of the virulence of Scedosporium prolificans strains from<br />
different origins in a murine model. J Med Microbiol 2002;<br />
51: 924-928.<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
Absidia coerulea 13-2<br />
Absidia corymbifera 13-2<br />
Acremonium kiliense 13-5<br />
Acremonium strictum 13-5<br />
Acropeta, cadena 13-5<br />
Affirm VPIII® 14-20<br />
Agar agua<br />
Agar con leche, glucosa y purpura<br />
3-7<br />
de bromocresol 3-12<br />
Agar Czapek Dox 3-7<br />
Agar Staib 3-15<br />
Agar Dixon modificado 3-8<br />
Agar extracto de malta 3-8<br />
Agar glucosado de patata 3-9, 12-9<br />
Agar glucosado de Sabouraud<br />
Agar glucosado de Sabouraud modificado<br />
3-9<br />
por Emmons 3-10<br />
Agar harina de avena 3-10<br />
Agar harina de mafz 3-11, 11-4<br />
Agar infusion de cerebro corazon 3-11<br />
Agar inhibidor para mohos 3-12<br />
Agar Leeming & Notman<br />
Agar Sabouraud con cicloheximida<br />
3-13<br />
y cloranfenicol 3-14<br />
Agar Leonian modificado 3-13<br />
Agar SDA-MUAG® 11-7<br />
Agar patata zanahoria 3-14<br />
Agar semillas de alpiste 3-15<br />
Agar Trichophyton® 3-15<br />
Agar urea de Christensen 3-16<br />
Agentes biologicos 17-1<br />
Agua, agar 3-7<br />
Albicans ID2® 11-7<br />
Alpiste, agar semillas de 3-15<br />
Alternaria alternata 13-6<br />
Alternaria infectoria 13-6<br />
Anelide 13-4<br />
Anticuerpos antimicelio 14-14<br />
Antifungicos 15-1<br />
API 20 C AUX® 11-12<br />
API ID 32C® 18-7<br />
Apofisis 13-1<br />
Argentica, tincion 5-8, 14-5<br />
Arroz, medio de 3-17, 12-9<br />
Artritis fungica 6-6<br />
Artroconidias 11-4<br />
Ascoma 13-15<br />
Aspergillus flavus 8-3,13-6<br />
Aspergillusfumigatus 2-13, 8-3, 13-7<br />
Aspergillus niger 8-3,13-8<br />
Aspergillus terreus 13-8<br />
Aspergiloma pulmonar 14-13, 14-17<br />
Aspergilosis broncopulmonar alergica 14-13, 14-17<br />
Aspergilosis invasora 14-11<br />
Aspergilosis pulmonar 5-4, 5-6, 5-7<br />
Aspergilosis sistemica 2-13<br />
Aspirado traqueal 5-3<br />
Aspirado traqueal, cuitivo de 5-10<br />
Aspirados oculares 10-2<br />
ATB Fungus® 16-4<br />
ATCC 18-3, 18-4, 18-6, 18-7, 18-10<br />
Auxacolor® 11-11<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6 ■Indice alfabetico de materias<br />
Asociacion Espanola de M icologia<br />
Auxonograma 11-10<br />
Avena, agar harina de 3-10<br />
Azul Alamar 16-1<br />
BacT/Alert® 6-1<br />
BACTEC 9240® 6-1<br />
BactiCard Candida® 11-8, 18-7<br />
Balanitis 2-7, 7-1, 7-2, 7-5<br />
Basfpeta, cadena 13-5<br />
(1 -^3)-B-D-glucano 14-18<br />
Bichro-latex albicans® 11-16<br />
Biolog YT MicroPlate® 11-14<br />
Biologia molecular 14-18<br />
Biopsia 6-7<br />
Biopsia esofagica 9-1<br />
Biopsia gastrica 9-3<br />
Biopsia pleural 5-5<br />
Biopsia pulmonar 5-5<br />
Biopsia pulmonar, cuitivo de 5-10<br />
Biopsia transbronquial 5-4<br />
Bioseguridad ambiental 19-1<br />
Bioseguridad laboral 17-1<br />
Blanco de calcofluor 14-3<br />
Blastoconidias 11-4<br />
Blastomicosis 2-10<br />
Blastomicosis pulmonar 5-7<br />
Blastomyces dermatitidis 2-10, 5-7<br />
Blastoschizomyces 11-4<br />
Blefaritis 10-1<br />
Bolsa colectora 7-3<br />
Broncoaspirado, cuitivo de 5-10<br />
Brum-Buisson, tecnica de 10-5<br />
Cabinas de seguridad biologica 17-5<br />
Calcofluor, bianco de 14-3<br />
Candida albicans Screen® 11-9<br />
Candida albicans 8-1, 10-1, 10-5, 11-3, 11-4,<br />
11-5, 11-7, 11-8, 11-16, 14-14<br />
Candida dubliniensis 8-1, 11-5, 11-14<br />
Candida glabrata 11-5<br />
Candida ID® 11-7<br />
Candida krusei 11-5, 11-16<br />
Candida krusei ATCC 6258 15-7, 18-8<br />
Candida parapsilosis ATCC 22019 15-7, 18-8<br />
Candida tropicalis 11-5, 11-7<br />
Candidiasis cutanea 2-3<br />
Candidiasis del panal 2-3<br />
Candidiasis eritematosa aguda 8-1<br />
Candidiasis gastrointestinal 2-6<br />
Candidiasis hiperplasica 8-1<br />
Candidiasis mucocutanea cronica 2-7<br />
Candidiasis sistemica 2-13<br />
Candidiasis vaginal 7-5<br />
Candiduria 7-3, 7-5, 7-6, 7-7, 7-8<br />
CandiSelect® 11-7<br />
Cateter de Tenckhoff 10-6<br />
Cateter intravascular 10-5<br />
Cateter peritoneal 10-7<br />
Cateterismo vesical 7-3<br />
Cavidad oral 8-1<br />
CECT 18-10
Cepas de referencia 15-12, 18-10 Difusion en agar 16-4<br />
Cepillado bronquial 5-3 Difusion en discos 16-8<br />
Cepillado esofagico 9-1 Dilution en agar 16-7, 16-8<br />
Cepillado protegido 5-4 Dimetil sulfoxido (DMSO) 4-5<br />
Cerebro corazon, agar infusion de 3-11 Dixon (modificado), agar 2-1, 3-8<br />
CHROMagar Candida® 3-16, 11-5, 16-7<br />
Cistitis 7-1<br />
Cladophialophora bantiana 13-9 Ectotrix, infection tipo 12-8<br />
Cladophialophora carrionii 13-9 Emmons, agar glucosado de Sabouraud<br />
Cladosporium cladosporioides 13-10 modificado por 3-10<br />
Cladosporium herbarum 13-9 Endoftalmitis 10-1<br />
Cladosporium sphaerospermum 13-10 Endotrix, infection tipo 12-8<br />
Clamidosporas 11-4, 12-3, 13-5 Epidermophyton 12-1<br />
CMI (ver Concentracion minima inhibitoria) Epidermophyton floccosum 12-1, 12-5<br />
Coccidioides immitis 2-11,5-7 Eritrasma 4-6<br />
Coccidioidomicosis 2-11 Escamas, recogida de 4-2<br />
Colorante de Cohen 4-5 Esclerocio 13-5<br />
Colorante de Kane 4-5 Esofagitis 2-6<br />
Columela 13-1 Esofagitis candidiasica 9-1<br />
Collarete 13-4 Esporangio 13-1<br />
Comision de Infecciones 19-6 Esporangioforo 13-1<br />
Comision de Obras 19-6 Esporangiospora 13-1<br />
Concentracion minima inhibitoria 15-1, 15-6, 15-7, Esporodoquio 13-4<br />
15-9, 15-11, 15-12, Esporotricosis 2-7<br />
16-2, 16-5, 16-8, 18-8 Esputo 5-3<br />
Conductos lacrimales 10-2 Esputo inducido 5-3<br />
Conidio 13-4 Esputo, cultivo de 5-10<br />
Conidioforo 13-4 ESP® 6-1<br />
Conidiogena, celula 13-4 Estolon 13-1<br />
Conjuntivitis 10-1 Estomatitis 8-2<br />
Contention, niveles de 17-2 Etest® 16-5, 16-8<br />
Contrainmunoelectroforesis 14-17 Examen en fresco 5-6<br />
Control de calidad 18-1 Examen microscopico 3-3, 14-1<br />
Control de calidad, cepas de 15-7, 18-10 Exophiala dermatitidis 13-10<br />
Control de calidad extemo 18-9 Exophiala lecani-corni 13-10<br />
Controles microbiologicos 19-3 Extracto de malta, agar 3-8<br />
Controles microbiologicos ambientales 19-7 Exudado anal 7-2<br />
Coomassie, tincion de 14-16 Exudado balanoprepucial 7-2<br />
Criptococosis 2-11, 8-3 Exudado conjuntival 10-2, 10-3<br />
Criptococosis pulmonar 5-8, 5-9 Exudado uretral 7-2<br />
Cromogen Albicans® 11-7 Exudado vaginal 7-2<br />
Cromomicosis 2-8 Exudado vulvar 7-2<br />
Crypto-LA Test® 14-8<br />
Cryptococcus neoformans 2-11, 11-9, 14-8<br />
Cuerpos extranos 10-2 Favus 12-2, 12-8<br />
Curvularia geniculata 13-10 Fenol-oxidasa 11-10<br />
Curvularia lunata 13-10 Feohifomicosis cutanea 2-8<br />
Czapek Dox, agar 3-7 Fialide 13-4<br />
Filamentacion precoz 11-1<br />
Filtros HEPA 17-5, 17-6, 19-2,<br />
D-arabinitol 14-18 19-3, 19-5, 19-8<br />
Dacriocistitis 10-1, 10-3 Fluoroplate Candida® 11-7<br />
Dentfculos 13-11 Foliculitis 2-1,2-3<br />
Dermatitis seborreica 2-1 Fongiscreen 4H® 11-15<br />
Dermatofitos 12-1 Fonsecaea compacta 13-11<br />
Dermatofitos, conservation 12-10 Fonsecaea pedrosoi 13-11<br />
Dermatofitosis 2-2 Fungemia 2-1<br />
Dermatophyte test medium® 3-17 Fungitec G® 14-19<br />
Desinfectantes 17-8 Fungitest® 16-3<br />
Detection de anticuerpos 14-12 Fusarium oxysporum 13-11<br />
Detection de antfgeno 14-8, 14-10 Fusarium solani 13-12<br />
Dialisis peritoneal continua ambulatoria 10-6 Fusarium verticillioides 13-13<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Indice alfabetico<br />
Galactomanano 14-11 Lfquido pleural 5-5, 6-6<br />
Galena ID 32C® 11-12 Lfquido sinovial 6-6<br />
Geotrichum 11-3 Lisis-centrifugacion 6-2, 6-3, 6-7<br />
Gestion de residuos 17-9<br />
Giemsa, tincion de 5-8, 14-5<br />
Glositis 8-2 M27-A 15-1, 15-8<br />
Gomori-Grocott, tincion de 5-8 M38-P 15-10, 15-12<br />
Gomori-Grocott modificada, tincion de 14-5 Macroconidios 12-3, 13-11<br />
Graphium 13-15 Macrodilucion, hongos filamentosos 15-12<br />
Gram, tincion de 5-8, 14-4 Macrodilucion, levaduras 15-8<br />
Maki, tecnica de 10-5, 10-6<br />
Malassezia 2-1, 11-18<br />
Harina de avena, agar 3-10 Malassezia furfur 2-1, 11-18<br />
Harina de mai'z, agar 3-11, 11-4 Malassezia globosa 2-1, 11-18<br />
Heces, cultivo 9-3 Malassezia obtusa 2-1, 11-18<br />
Hemocultivo 6-1 Malassezia pachydennatis 11-18<br />
HEPA (ver Filtros) Malassezia restricta 2-1, 11-18<br />
Hidroxido potasico 14-2 Malassezia slooffiae 2-1, 11-18<br />
Hifas 11-3 Malassezia sympodialis 2-1, 11-18<br />
Hipopion 10-2 Malassezia spp., fungemia por 6-5<br />
Histoplasma capsulatum 2-9, 6-7 Malta, agar extracto de 3-8<br />
Histoplasmosis 2-9, 8-2 Manano 14-10<br />
Histoplasmosis pulmonar 5-6, 5-10 Material biologico, almacenamiento de 17-11<br />
Material biologico, transporte de 17-11<br />
Medios cromogenicos 11-5<br />
Identificacion de levaduras 11-1 Medios de cultivo 3-4<br />
<strong>Inc</strong>ubation 3-6 Medula osea 6-7<br />
Informe de los resultados 3-18 Meningitis 6-5<br />
Infusion de cerebro corazon, agar 3-11 Metula 13-6<br />
Inhibidor para mohos, agar 3-12 M iction espontanea 7-2<br />
Inmunoelectroforesis 14-17 Micetoma 2-9<br />
Inmunofluorescencia indirecta 14-6 Micosis orales 8-1<br />
Intertrigo 2-3 Micosis sistemicas 2-12<br />
Isolator® 6-2 Micosis subcutaneas 2-7<br />
Micosis superficiales 2-1, 4-1<br />
Microconidios 12-3, 13-11<br />
Jugo duodenal 9-2 Microdilucion, hongos filamentosos 15-10<br />
Jugo gastrico 9-2 Microdilucion, levaduras 15-1<br />
Microsporum 12-1<br />
Microsporum canis 12-1, 12-5<br />
KOH (ver Hidroxido potasico) Microsporum gypseum 12-1, 12-5<br />
Krusei-color® 11-16 Microsporum audouinii 12-5<br />
Monofluo Kit P. carinii® 14-7<br />
MOPS 15-1<br />
Lactofenol de Amman 4-5 Moqueta de Mariat 4-2<br />
Lageniforme, fialide 13-13 Mucormicosis 2-14, 8-3<br />
Lavado broncoalveolar 5-4 Mucormicosis pulmonar 5-6<br />
Lavado broncoalveolar, cultivo de 5-10 Muestras respiratorias 5-3<br />
Lavado bronquial o broncoaspirado 5-3 Muguet 2-5, 8-1<br />
Lavado nasofaringeo 5-3 Murex C. Albicans® 11-9<br />
Leche diluida 11-5 MYCO/F LYTIC® 6-2<br />
Leche, glucosa y purpura de bromocresol, Mycosis-IC/F® 6-2<br />
agar con 3-12<br />
Leeming & Notman, agar 2-1,3-13<br />
Lengua pilosa negra 2-6 Neumocistosis pulmonar 5-6, 5-8<br />
Lentes de contacto 10-2 Nitrato-reductasa 11-9<br />
Leonian modificado, agar de 3-13 Normas de seguridad 17-1, 17-12<br />
Levaduras lipofilas, identificacion 11-18<br />
Limpieza, procedimientos de 19-3<br />
Lfquido cefalorraqufdeo 6-5 Obras en el hospital 19-5<br />
Lfquido de dialisis 10-7 Observacion directa 14-2<br />
Lfquido pericardico 6-6 Onicomicosis 4-4<br />
Lfquido peritoneal 6-6 Onicomicosis candidiasica 2-3<br />
Asociacion Espanola de M icologia
Onicomicosis negra<br />
Orina<br />
Otomicosis<br />
Indice alfabetico<br />
2-4<br />
7-2<br />
8-1, 8-3<br />
Paecilomyces lilacinus 13-13<br />
Paecilomyces marquandii 13-13<br />
Paecilomyces variotii 13-13<br />
Paracoccidioides brasiliensis 2-11,5-7<br />
Paracoccidioidomicosis 2-11, 8-2<br />
Patata, agar glucosado de 3-9, 12-9<br />
Patata zanahoria, agar de 3-14<br />
Phaeoacremonium parasiticum 13-14<br />
Phialophora verrucosa 13-14<br />
PCR 14-19<br />
Pelo, perforation del 12-9<br />
Pelos, recogida de 4-3<br />
Pelos, vision directa 4-6<br />
Perionixis 2-3<br />
Peritonitis 10-6<br />
Peritonitis fungica 6-6<br />
Phaeoacremonium rubrigenum 13-14<br />
Phaeoannellomyces werneckii 2-2<br />
Phialophora americana 13-14<br />
Phialophora parasitica 13-14<br />
Pie de atleta 12-2<br />
Piedra blanca 2-2<br />
Piedra negra 2-2<br />
Piedraia hortae 2-2<br />
Pielonefritis 7-1<br />
Pitiriasis versicolor 2-1<br />
Platelia Aspergillus 14-11<br />
Platelia Candida Ab/Ac/Ak 14-13<br />
Platelia Candida Ag 14-10<br />
Pleomorfismo 12-11<br />
Pneumocystis carinii 14-7<br />
Polifialide 13-5<br />
Procesamiento de las muestras 3-2<br />
Protesis 10-8<br />
Protesis articular 10-8<br />
Protesis valvular 10-8<br />
Prototheca 11-5<br />
Pseudallescheria boydii 13-15<br />
Puncion pulmonar 5-5<br />
Puncion vesical 7-3<br />
Puncion-aspiracion transtraqueal 5-4<br />
Puntos de corte 15-7<br />
Queilitis angular 2-6, 8-1<br />
Queratitis 10-1<br />
Ramoconidos 13-9<br />
Rapid Yeast Identification® 11-14, 18-7<br />
RapID Yeast Plus System® 11-14, 18-7<br />
Raspado corneal 10-2, 10-3<br />
Recogida de muestras 3-1<br />
Residuos infecciosos 17-9<br />
Residuos quimicos 17-10<br />
Rhizopus arrhizus 8-3<br />
Rhizopus oryzae 13-3<br />
Rhizopus rhizopodiformis 13-3<br />
Riesgos biologicos 17-12<br />
Riesgos no biologicos 17-12<br />
Rinosinusitis fungica 8-1<br />
Rizoide 13-1<br />
RPMI 1640 15-1<br />
Sabouraud, agar glucosado de 3-9<br />
Sabouraud con cicloheximida y<br />
cloranfenicol, agar 3-14<br />
Sabouraud modificado por Emmons,<br />
agar glucosado de 3-10<br />
Saksenaea vasiformis 13-3<br />
Scedosporium apiospermum 13-15<br />
Scedosporium prolificans 13-15<br />
Scopulariopsis brevicaulis 13-16<br />
Scopulariopsis brumptii 13-16<br />
Scytalidium 2-3<br />
SDA-MUAG®, agar 11-7<br />
Seguridad, normas de 17-1, 17-12<br />
Seguridad biologica 17-1, 17-3<br />
Seguridad biologica, cabinas de 17-5<br />
Sensibilidad antifungica 15-1<br />
Sensititre YeastOne® 16-1, 16-8<br />
Sindrome de Gougerot-Carteaud 2-1<br />
Sinema 13-4<br />
Sinusitis 8-3<br />
Sistemas de ventilation 19-1<br />
Sonda de ADN 14-20<br />
Sonda vesical 7-3<br />
Sporothrix schenckii 2-7<br />
Staib, agar de 3-15<br />
Subulada, fialide 13-5<br />
Tecnica de Ouchterlony 14-16<br />
Tejidos 6-7<br />
Thennoascus crustaceus 13-14<br />
Tincion argentica 5-8, 14-5<br />
Tincion de Coomassie 14-16<br />
Tincion de Giemsa 5-8, 14-5<br />
Tincion de Gram 5-8, 14-4<br />
Tinea barbae 2-3, 12-2<br />
Tinea capitis 2-3, 12-2<br />
Tinea corporis 2-3, 12-2<br />
Tinea cruris 2-3, 12-2<br />
Tinea facei 12-2<br />
Tinea favosa (favus) 12-2<br />
Tinea imbricata 12-2<br />
Tinea manuum 2-3, 12-2<br />
Tinea pedis 2-3, 12-2<br />
Tinea unguium 2-3, 12-2<br />
Tinta china 5-8, 14-2<br />
Tina negra 2-2<br />
TOC, medio de 11-3, 11-5<br />
Tracto urinario, infection del 7-1, 7-2, 7-5<br />
Transporte de las muestras 3-1<br />
Trichophyton 12-1<br />
Trichophyton agar® 3-15, 12-10<br />
Trichophyton mentagrophytes 12-1, 12-5<br />
Trichophyton rub rum 12-1, 12-5<br />
Trichophyton schoenleinii 12-5<br />
Trichophyton tonsurans 12-1, 12-5<br />
©2004 Revista Iberoamericana de Micoiogia - ISBN: 84-607-3050-6
_<br />
©2004 Revista Iberoamericana de Micologia - ISBN: 84-607-3050-6<br />
Trichophyton verrucosum<br />
Trichophyton violaceum<br />
Trichosporon<br />
Trichosporon beigelii<br />
Tubo germinal<br />
Indice alfabetico<br />
12-5<br />
12-5<br />
11-4, 11-9<br />
2-2<br />
11-1<br />
Uni-Yeast-Tek® 11-11<br />
Unas, recogida de 4-4<br />
Unas, vision directa 4-7<br />
Urea de Christensen, agar 3-16<br />
Ureasa, prueba de la 11-9, 12-8<br />
Uretritis 7-2, 7-5, 7-7<br />
Verticilos<br />
Vital®<br />
Vitek®<br />
Vitek 2®<br />
Vulvovaginitis<br />
Asociacion Espanola de M icologia<br />
13-13<br />
6-1<br />
11-13, 18-7<br />
11-14<br />
2-6, 7-1, 7-2, 7-7<br />
Wood, lampara/luz de 4-1,12-8<br />
Zanahoria, agar de patata 3-14<br />
Zigomicosis 2-14<br />
Zigospora 13-1