UN rOSArINO EN BUENOS AIrES - Haze
UN rOSArINO EN BUENOS AIrES - Haze
UN rOSArINO EN BUENOS AIrES - Haze
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
sana<br />
Esto nos lleva a la hipótesis de la proteína de<br />
Tau. Podemos observar que cuando la misma<br />
proteína es hiperfosforilada, comienza a emparejarse<br />
con otras hebras de la proteína. El sistema<br />
de transporte en el interior de las neuronas,<br />
utiliza estructuras conocidas como microtúbulos,<br />
las cuales transportan nutrientes y químicos<br />
entre el cuerpo y el eje de las células.<br />
Las sub-unidades de estos microtubos se mantienen<br />
unidas por la proteína de Tau, y cuando<br />
ésta comienza a hiperfosforilarse y emparejarse<br />
con otras hebras de Tau para formar<br />
marañas neurofibrilares, se roba estas hebras<br />
de los microtubos. Esto lleva al desmoronamiento<br />
de los microtubos que resulta en interrupciones<br />
en la comunicación interneuronal<br />
y finalmente en la muerte de la célula (1).<br />
Aunque estas tres teorías compiten en la realidad<br />
científica, una teoría que incorpora las<br />
tres hipótesis parece ser lo más acertado debido<br />
a que los procesos descriptos en dichas<br />
teorías se interrelacionan.<br />
Las agencias regulatorias de todo el mundo<br />
solo han aprobado cuatro medicamentos hasta<br />
el momento para tratar la enfermedad, y la<br />
mayoría de opciones de tratamiento se enfocan<br />
en el cuidado paliativo.<br />
Las opciones farmacológicas disponibles proveen<br />
solo algunas leves mejorías en la progresión<br />
de la enfermedad, como mucho, alguna<br />
moderada mejoría en el daño cognoscitivo.<br />
Estas drogas consisten en un antagonista del<br />
receptor de ácido glutámico NMDA (me-<br />
Membrana<br />
celular<br />
Molécula APP<br />
Interior<br />
de la célula<br />
mantina) y 3 inhibidores de acetilcolinesterasa<br />
(donepezil, galantamine y rivastigmine), una<br />
enzima responsable de la degradación metabólica<br />
del neurotransmisor acetilcolina (1).<br />
En este nublado panorama existe un rayo<br />
de esperanza además de tomar medidas preventivas<br />
tales como evitar factores de riesgo<br />
ambientales, mantener una dieta apropiada<br />
y hacer ejercicio regularmente y continuar<br />
aprendiendo y desafiando al cerebro.<br />
El cannabis, y medicaciones a base de éste, ofrecen<br />
un gran halo de esperanza tanto a pacientes<br />
de Alzheimer como a quienes cuidan a los pacientes,<br />
que también soportan una ardua tarea.<br />
Los Cannabinoides combaten muchos de los<br />
mecanismos fundamentales del Alzheimer y,<br />
a diferencia de otros tratamientos disponibles<br />
en la actualidad, tiene la facultad de inhibir la<br />
progresión o el avance de la enfermedad.<br />
OMMa:<br />
CuidadO paliativO para paCientes COn<br />
alzheiMer ayudadO pOr el Cannabis<br />
Los cannabinoides fueron observados por<br />
primera vez como beneficiosos para el cuidado<br />
de pacientes con Alzheimer cuando Volicer,<br />
(2) (1997) administró THC en forma de<br />
Marinol a 15 pacientes con el mal de Alzheimer<br />
que rehusaban ingerir alimentos.<br />
Tal como se esperaba, los pacientes aumentaron<br />
más peso cuando fueron tratados con THC<br />
que cuando se les administraba un placebo.<br />
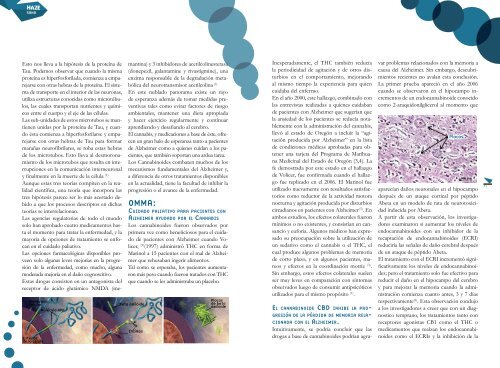
Beta amiloide<br />
Enzimas<br />
Placas<br />
de beta<br />
amiloide<br />
Inesperadamente, el THC también reducía<br />
la periodicidad de agitación y de otros disturbios<br />
en el comportamiento, mejorando<br />
al mismo tiempo la experiencia para quien<br />
cuidaba del enfermo.<br />
En el año 2000, este hallazgo, combinado con<br />
las entrevistas realizadas a quienes cuidaban<br />
de pacientes con Alzheimer que sugerían que<br />
la ansiedad de los pacientes se reducía notablemente<br />
con la administración del cannabis,<br />
llevó al estado de Oregón a incluir la “agitación<br />
producida por Alzheimer” en la lista<br />
de condiciones médicas aprobadas para obtener<br />
una tarjeta del Programa de Marihuana<br />
Medicinal del Estado de Oregón (3,4). La<br />
fe demostrada por este estado en el hallazgo<br />
de Volicer, fue confirmada cuando el hallazgo<br />
fue replicado en el 2006. El Marinol fue<br />
utilizado nuevamente con resultados satisfactorios<br />
como reductor de la actividad motora<br />
nocturna y agitación producida por disturbios<br />
circadianos en pacientes con Alzheimer (5) . En<br />
ambos estudios, los efectos colaterales fueron<br />
mínimos o no existentes, y consistían en cansancio<br />
y euforia. Algunos médicos han expresado<br />
su preocupación sobre la utilización de<br />
un sedativo como el cannabis o el THC, el<br />
cual produce algunos problemas de memoria<br />
de corto plazo, y en algunos pacientes, mareos<br />
y efectos en la coordinación motriz (3) .<br />
Sin embargo, estos efectos colaterales suelen<br />
ser muy leves en comparación con síntomas<br />
observados luego de consumir antipsicóticos<br />
utilizados para el mismo propósito (1) .<br />
el CannabinOide Cbd inhibe la prOgresión<br />
de la pérdida de M e M O r i a rela-<br />
CiOnada COn el alzheiMer.<br />
Intuitivamente, se podría concluir que las<br />
drogas a base de cannabinoides podrían agra-<br />
var problemas relacionados con la memoria a<br />
causa del Alzheimer. Sin embargo, descubrimientos<br />
recientes no avalan esta conclusión.<br />
La primer prueba apareció en el año 2006<br />
cuando se observaron en el hipocampo incrementos<br />
de un endocannabinoide conocido<br />
como 2-araquidonilglicerol al momento que<br />
Placas<br />
aparecían daños neuronales en el hipocampo<br />
después de un ataque cortical por péptido<br />
Abeta en un modelo de rata de neurotoxicidad<br />
inducida por Abeta.<br />
A partir de esta observación, los investigadores<br />
examinaron si aumentar los niveles de<br />
endocannabinoides con un inhibidor de la<br />
recaptación de endocannabinoides (ECRI)<br />
reduciría las señales de daño cerebral después<br />
de un ataque de péptido Abeta.<br />
El tratamiento con el ECRI incrementó significativamente<br />
los niveles de endocannabinoides;<br />
pero el tratamiento solo fue efectivo para<br />
reducir el daño en el hipocampo del cerebro<br />
y para mejorar la memoria cuando la administración<br />
comienza cuanto antes, 3 y 7 días<br />
respectivamente (6) . Esta observación condujo<br />
a los investigadores a creer que con un diagnostico<br />
temprano, los tratamientos tanto con<br />
receptores agonistas CB1 como el THC o<br />
medicamentos que realzan los endocannabinoides<br />
como el ECRIs y la inhibición de la<br />
67