REV03 - PARAFUSO ÂNCORA - Biomecanica
REV03 - PARAFUSO ÂNCORA - Biomecanica
REV03 - PARAFUSO ÂNCORA - Biomecanica
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>PARAFUSO</strong> <strong>ÂNCORA</strong> BIOMECANICA BIOMECANICA SUTURE ANCHOR<br />
PORTUGUÊS<br />
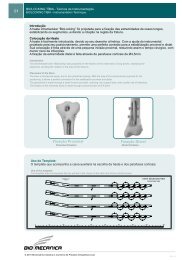
DESCRIÇÃO DO PRODUTO<br />
O Parafuso Âncora Biomecânica - Twister é destinado à fixação de tecidos moles ao osso em<br />
processos cirúrgicos realizados para o reparo de tendão-osso dos tendões flexores da mão e<br />
tendão-osso do manguito roteador (ombro). O conjunto consiste de Parafuso Âncora (liga de<br />
titânio - ASTM F136/ NBR ISO 5832-3), Fio de Sutura e Aplicador. O conjunto é fornecido<br />
montado, estéril e pronto para uso.<br />
COMPOSIÇÃO<br />
1. Parafuso Âncora: Liga de Titânio (Ti 6AL4V) / Normas aplicáveis: ASTM F136 / NBR ISO 5832-<br />
3<br />
Medidas: Ø2,0 (3125-20-000), Ø2,7 ( 3125-27-000), Ø3,5 ( 3125-35-000), Ø5,0 (3125-50-000).<br />
RESISTÊNCIA<br />
2. Fio de Sutura F.Fiber®: O Fio de Sutura F.Fiber® que acompanha o produto é não-absorvível,<br />
composta por uma fibra de polietileno e ultra-alto peso molecular, única no mercado, que garante<br />
uma excelente resistência a tensão e a ruptura, assim como maior lubrificação.<br />
Os Fios de Sutura F.Fiber® são trançados em branco/azul ou branco/preto, registradas no FDA<br />
(KO63778 / Ko70673) Normas aplicáveis: ABNT NBR 13904<br />
Carga (libras)<br />
N<br />
430<br />
230<br />
190<br />
90<br />
Média<br />
70<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
88,03<br />
2,0<br />
191,884<br />
2,7<br />
239,405<br />
3,5<br />
Comparação de Resistência<br />
80<br />
F. Fiber<br />
Resistência Tensão<br />
423,53<br />
5,0<br />
Tamanho<br />
Teste de Nó<br />
Ethibond #2<br />
FiberWire #2<br />
F. Fiber #2<br />
3. Aplicador para Parafuso Âncora: Eixo de Aço Inoxidável (AÇO AISI 304 de alta dureza) com<br />
cabo de Polipropileno. Normas aplicáveis: ASTM 276<br />
DESCRIÇÃO DO PRINCÍPIO FÍSICO E FUNDAMENTOS DA TECNOLOGIA APLICADOS<br />
PARA O SEU FUNCIONAMENTO E AÇÃO:<br />
O Conjunto Artroscópico Biomecânica é destinado à fixação do tecido mole ao osso. Este produto<br />
é recomendado para os seguintes procedimentos:<br />
INDICAÇÕES<br />
Mini Twister - 2,0mm e 2,7mm - Indicado para o reparo de tendão-osso dos tendões flexores da<br />
mão.<br />
Twister - 3,5mm e 5,0mm - Indicado para o reparo de tendão-osso do manguito roteador (ombro).<br />
SELEÇÃO E ESCOLHA CORRETA DO IMPLANTE<br />
A escolha correta do implante é extremamente importante: a possibilidade de êxito na fixação da<br />
fratura aumenta com a escolha apropriada do tamanho e desenho do implante.<br />
Nenhum dispositivo com a finalidade de suportar ou não algum peso poderá resistir às<br />
insuportáveis pressões geradas pelo peso total do corpo do paciente. Até que seja alcançada a<br />
recuperação da cirurgia o paciente deve utilizar algum suporte externo adequado e restringir as<br />
atividades físicas que possam colocar pressão adicional sobre o implante ou permitir qualquer<br />
movimento na área de fixação, que possa causar o retardamento do processo de consolidação.<br />
Ao decidir que um paciente deve usar um implante, os seguintes fatores podem ser de extrema<br />
importância para o sucesso do procedimento adequado:<br />
• O peso do paciente. Um paciente obeso ou com excesso de peso pode sobrecarregar o<br />
implante, o que conduzirá toda a operação bem como o dispositivo ao fracasso. • Se o paciente<br />
exerce ocupação ou atividade que exija dele grandes caminhadas ou até mesmo corridas,<br />
levantamentos de pesos ou força muscular, esses esforços podem também resultar em fracasso<br />
do dispositivo. • A senilidade, a doença mental ou alcoolismo entre outras, podem levar o paciente<br />
a ignorar certas limitações e precauções necessárias no uso do dispositivo, levando o implante à<br />
falha ou outras complicações. • Em certos casos as progressões de doenças degenerativas<br />
podem estar tão avançadas, que diminuem substancialmente a vida útil do implante. Para tais<br />
casos os implantes podem ser considerados como um expediente técnico para retardamento do<br />
avanço da doença ou apenas para um alívio temporário. • Quando há suspeita de que o paciente<br />
seja sensível a corpos estranhos ao seu organismo, ou que possa ter reações alérgicas, deve ser<br />
realizado testes apropriados antes da escolha e seleção do material a ser implantado. • Este<br />
implante poderá não ser adequado para pacientes com quantidade óssea insuficiente, e que não<br />
tenha crescimento ósseo concluído. O médico deve avaliar cuidadosamente a quantidade de<br />
osso antes de realizar cirurgia ortopédica em pacientes cujo crescimento ósseo é limitado. O uso<br />
de implante e a colocação de peças ou implantes no corpo não deve unir, perturbar ou prejudicar a<br />
placa de crescimento.<br />
O cuidado pós-operatório é importante. O paciente deve ser instruído sobre as limitações do seu<br />
implante e advertido para não carregar pesos ou provocar tensões no dispositivo até a total<br />
consolidação do osso e a completa cicatrização.<br />
MANUSEIO DO IMPLANTE<br />
O correto manejo do implante é extremamente importante. Deve-se evitar o quanto possível<br />
contorcer as peças. Em todo o caso, se a torção for absolutamente necessária, o dispositivo não<br />
deverá ser drasticamente vergado, ou torcido em contrário, tampouco deve ser chanfrado, nem<br />
arranhado ou esfolado. Todas estas operações podem lesar a superfície e o acabamento da<br />
peça, bem como iniciar pontos de danos internos, os quais poderão se tornar focos localizados de<br />
corrosão.<br />
Nenhum implante deve ser reaproveitado. Uma vez usados, os implantes deverão ser<br />
descartados, embalados em invólucro inviolável juntamente com o lixo hospitalar infectocontaminado,<br />
mesmo que pareçam novos e em boas condições. Eles poderão ter pequenas<br />
lesões imperceptíveis que certamente conduzirão a severas falhas pela fadiga de uso. De modo<br />
geral deve-se ter atenção redobrada na assepsia para evitar os riscos da contaminação ou<br />
infecção cirúrgica.<br />
RECOMENDAÇÕES NO CASO DE QUEDA DOS COMPONENTES:<br />
No caso de queda de um implante, durante o ato cirúrgico, mesmo que não haja danos, deverá ser<br />
descartada, embalada em invólucro inviolável juntamente com o lixo hospitalar infectocontaminado,<br />
uma vez que não é possível a sua re-esterilização.<br />
F. Fiber<br />
INSTRUÇÕES PÓS-OPERATÓRIAS AO PACIENTE<br />
O médico deve instruir e informar ao paciente sobre as limitações do implante para que tome<br />
precauções a respeito da atividade física e o suporte de peso e carga até a total consolidação do<br />
osso e a completa cicatrização das partes moles. Deve advertir-se que o não cumprimento das<br />
instruções pós-operatórias pode levar a uma ruptura do implante ou a uma possível migração,<br />
sendo necessária uma cirurgia de revisão para retirar o mesmo.<br />
MANUTENÇÃO DOS IMPLANTES PÓS-OPERAÇÃO / RASTREABILIDADE E EMBALAGEM<br />
A rastreabilidade é controlada através de um número de lote inserido no rótulo, que é concedido<br />
pelo fornecedor primário.<br />
Este número é usualmente 2 letras e 5 números e com ele pode-se constatar o ano de fabricação,<br />
a origem da matéria prima, data de esterilização e expedição.<br />
Dentro das embalagens são fornecidas cinco etiquetas: uma etiqueta é fixada no prontuário do<br />
PACIENTE, outra é fixada no documento de entrega da EMPRESA, a terceira fixada na NOTA<br />
FISCAL de venda e as outras devem ser entregues ao Paciente e ao Distribuidor.<br />
- O produto é fornecido na condição estéril, em duplo blister em embalagem rígida, devidamente<br />
identificados por etiquetas adesivas, garantindo rastreabilidade do produto.<br />
- A embalagem deve estar intacta.<br />
- Verifique sempre a data de validade do produto, não utilize em nenhuma circunstância, caso o<br />
prazo de esterilização esteja vencido.<br />
TÉCNICA CIRÚRGICA<br />
1. Estabeleça alinhamento axial. 2. Há 1 marca laser no instrumental, que delimita a extremidade<br />
do implante, a qual mostra a profundidade de inserção adequada. 3. Perfure ou insira o parafuso<br />
no sentido horário. Se estiver inserindo com aparelhos elétricos, insira o Parafuso Âncora num só<br />
movimento. Parar e reiniciar a perfuração pode resultar num excesso de força rotatória aplicada<br />
ao implante o qual pode resultar na falha do mesmo. As âncoras podem ser inseridas diretamente<br />
no tecido ósseo preparado ou inserido por meio do tecido quando for apropriado. 4. Puxe o<br />
instrumento de inserção em forma reta isto deixa a ancora ou implante em sua posição de sutura.<br />
5. Efetue a amarração do fio de sutura ForceF.® e corte as sobras do mesmo.<br />
CONTRA INDICAÇÕES:<br />
A. Infecções ativas; B. Pacientes esqueleticamente imaturos; C. Na presença de alterações<br />
quísticas, osteopenia grave, ou doença degenerativa, que pode comprometer a segurança da<br />
fixação da do Parafuso Ancora; D. Alterações patológicas dos tecidos moles que serão suturados,<br />
de modo a prejudicar a segurança da fixação pela sutura; E. Pacientes que não querem ou estão<br />
impossibilitados de cumprir as instruções pós-operatórias devido a condições físicas ou mentais<br />
que apresentam; F. Procedimentos que proporcionem contato prolongado com soluções salinas<br />
(tratos biliar e urinário), podendo resultar na formação de cálculos; G. Se houver um ambiente<br />
não-estéril, ou seja, cavidades abertas como seios; H. Sensibilidade a corpo estranho. Devem ser<br />
realizados testes de sensibilidade ao material nos casos de suspeita de rejeição; I. Cobertura<br />
inadequada com tecido saudável; J. Infecções e/ou limitações no fluxo sangüíneo que possam<br />
tornar a cicatrização lenta e aumentar a possibilidade de infecção e/ou rejeição do implante; K.<br />
Ocorrência de doença degenerativa que possa afetar adversamente a colocação apropriada dos<br />
implantes.<br />
EFEITOS ADVERSOS:<br />
A. Pode ocorrer rompimento da sutura; B. Ocasionalmente pode ocorrer eritema leve e dor no<br />
local da sutura devido ao trauma da ferida cirúrgica no tecido; C. As âncoras podem soltar-se ou<br />
perder a fixação; D. Alterações vasculares; E. É possível que a ressonância magnética cause um<br />
aquecimento dos implantes metálicos e dos tecidos vizinhos; F. Redução na densidade óssea<br />
e/ou necrose óssea devido à proteção contra a tensão; G. Reação alérgica ou sensibilidade ao<br />
metal do implante; H. Danos ao nervo devido a um trauma cirúrgico; I. Rompimento das âncoras<br />
devido ao retardamento da união ou desunião do tecido ósseo; J. Dobra ou fratura do Parafuso<br />
Ancora; K. Dor, desconforto e/ou sensação anormal devido à presença do Parafuso Ancora; L.<br />
Infecção superficial e/ou profunda; M. Restrição do crescimento; N. Transmigração passiva do<br />
Parafuso Ancora; O. Coloração do tecido.<br />
ADVERTÊNCIAS:<br />
A. A inserção incompleta do Parafuso Ancora Biomecânica não trará eficácia na fixação; B. O grau<br />
de mobilidade pós-operatória será determinado pelo médico e deve ser informado ao paciente; C.<br />
A literatura médica diz que a possibilidade de sucesso das cirurgias com ancora de sutura são<br />
maiores quando as mesmas são inseridas a 90º, pois a resistência à tração das mesmas são<br />
maiores do que quando inseridas em ângulos diferentes deste; D. Não implantar este dispositivo<br />
em placas de cartilagem epifisária de crescimento; E. Não é utilizado látex em nenhum dos<br />
dispositivos da âncora ou em sua embalagem; F. Os implantes cirúrgicos nunca devem ser<br />
reutilizados, e os implantes explantados nunca devem ser implantados novamente. Podem<br />
ocorrer pequenos defeitos e padrões de pressão interna, mesmo se o implante parecer intacto,<br />
causando falha e rompimento do implante; G. No caso de um dispositivo implantável, há um risco<br />
de introduzir materiais estranhos e particulados, incluindo talco de luvas, fiapos de materiais e<br />
agentes de limpeza e outros contaminantes da superfície. Todos os esforços devem ser feitos<br />
para limitar o manuseio dos dispositivos de fixação. Além disso, se algum dispositivo de fixação<br />
entrar em contato com fluidos corpóreos, ele não deve ser reutilizado devido à possível<br />
transmissão dos patogênicos sangüíneos; H. O médico é o responsável pela conclusão do<br />
treinamento adequado, seleção apropriada do paciente, escolha e colocação do implante, bem<br />
como pela decisão de deixar ou remover os implantes após o cumprimento de suas funções<br />
clínicas; I. Não utilizar este produto em locais em que os níveis de fixação sejam superiores aos<br />
limites pré-estabelecidos para este produto; J. O Parafuso Ancora Biomecânica não deve ser<br />
submetido à carga precoce, anteriormente à consolidação pós-cirúrgica. Para tanto, deve ser<br />
esclarecido ao paciente que o implante não substitui o tecido ósseo e nem as partes moles<br />
adjacentes, e que as recomendações médicas são importantes e deverão ser seguidas;<br />
INUTILIZAÇÃO E DESCARTE:<br />
Implantes explantados nunca devem ser implantados novamente. O estresse poderá provocar<br />
desenvolvimento de imperfeições microscópicas e, mesmo que o implante pareça intacto, pode<br />
ocasionar a falência do mesmo.<br />
Implantes que forem removidos da embalagem interna e inseridos dentro do ambiente cirúrgico,<br />
mesmo que não tenham sido implantados ou contaminados por outras fontes, devem ser tratados<br />
como material contaminado, o mesmo ocorrendo com dispositivos explantados. Estes<br />
dispositivos devem ser inutilizados para uso antes do descarte.<br />
Recomendamos que as peças sejam limadas, entortadas ou cortadas para sua inutilização.<br />
Dispositivos explantados são considerados lixo hospitalar (produtos potencialmente<br />
contaminantes), devendo ser tratados como tal, conforme normas da autoridade sanitária local.<br />
Conforme a Resolução RE nº 2605, de 11/08/06, dispositivos implantáveis de qualquer natureza<br />
enquadrados como de uso único são proibidos de serem reprocessados.<br />
ESTERILIZAÇÃO:<br />
O Conjunto Artroscópico Biomecânica é fornecido estéril através de Esterilização por óxido de<br />
etileno (E.T.O.) - parâmetros e procedimentos estabelecidos no protocolo de validação e na<br />
EN550:1994 Sterilization of Medical Devices – Validation and Routine Control of Ethylene Oxide<br />
Sterilization com validade de 5 anos.<br />
RESPONSÁVEL TÉCNICO<br />
Eng.º José Roberto Pengo - CREA-SP 06009567 65<br />
FABRICADO POR:<br />
BIOMECÂNICA IND. E COM. DE PRODUTOS ORTOPÉDICOS LTDA<br />
Rua Luiz Pengo, 145, 1º Distrito Industrial - CX Postal 1014 - CEP: 17203-970 - Fone: 55 (14)<br />
2104-7900 - FAX: 55 (14) 2104-7908 - CNPJ 58.526.047/0001-73 - INDÚSTRIA BRASILEIRA<br />
www.biomecanica.com.br - biovendas@biomecanica.com.br<br />
R.G. ANVISA: 80128580093<br />
EC REP<br />
CRUVAL sl<br />
Paseo de la Chopera, 15 - Madrid - Spain<br />
Phone: 0034 91 517 2492 Fax: 0034 91 842 9180<br />
MANUFACTURER’S AUTHORIZED EU REPRESENTATIVE<br />
CRUVAL sl<br />
Paseo de la Chopera, 15 - Madrid - Spain<br />
Phone: 0034 91 517 2492 Fax: 0034 91 842 9180<br />
MANUFACTURER’S AUTHORIZED EU REPRESENTATIVE<br />
ENGLISH<br />
DESCRIPTION OF THE PRODUCT<br />
<strong>Biomecanica</strong> Anchor Screw - Twister is used for the fixation of the soft tissue to bone in surgical<br />
procedures performed to repair the flexor tendons of the hand and rotator cuff (shoulder).<br />
COMPOSITION<br />
1. Anchor Screw: Titanium alloy (Ti 6AL4V)/Applicable Norms: ASTM F136/NBR ISO 5832-3<br />
Measures: Ø2,0 (3125-20-000), Ø2,7 ( 3125-27-000), Ø3,5 ( 3125-35-000), Ø5,0 (3125-50-000).<br />
RESISTENCE<br />
Média<br />
2,0 2,7 3,5 5,0 Tamanho<br />
2. F.Fiber® Suture Wire: The F.Fiber® Suture Wire that comes with the product is non-absorbed,<br />
composed by a fiber of polyethylene and extreme-high molecular weight, a single one in the market<br />
that guarantees an excellent tension and rupture resistance, as well as better lubrication. The F.Fiber®<br />
Suture Wires are tressed blank/blue or white/black, registered in the FDA (KO63778/Ko70673)<br />
applicable Norms: ABNT NBR 13904<br />
Resistance Comparison<br />
80<br />
Load (pounds)<br />
N<br />
430<br />
230<br />
190<br />
90<br />
70<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
88,03<br />
191,884<br />
239,405<br />
F. Fiber<br />
Resistance to Tension<br />
423,53<br />
Knot Test<br />
Ethibond #2<br />
FiberWire #2<br />
F. Fiber #2<br />
3. Anchor Screw Applicator: Stainless Steel axle (STEEL AISI 304 of high hardness) with<br />
Polypropylene wire.<br />
Applicable norms: ASTM 276<br />
DESCRIPTION OF THE PHYSICAL PRINCIPLE AND BEDDINGS OF THE TECHNOLOGY<br />
APPLIED FOR ITS FUNCTIONING AND ACTION:<br />
Biomecânica Arthroscopy Set is suitable for the setting of soft tissue to the bone. This product is<br />
recommended for the following procedures:<br />
INDICATIONS<br />
Mini Twister - 2.0 mm and 2.7 mm – used to repair the flexor tendons of the hand.<br />
Twister - 3.5 mm and 5.0 mm – used to repair the rotator cuff<br />
SELECTION AND CORRECT IMPLANT CHOICE<br />
The correct implant choice is extremely important: the possibility of success in the setting of the fracture<br />
increases with the appropriate choice of the size and drawing of the implantation.<br />
No device with the purpose to whether support or not some weight will be able to resist to the tough<br />
pressures caused by the patient's body weight. Until the recovery of the surgery is reached the patient<br />
must use some adequate external support and restrict the physical activities that can place additional<br />
pressure on the implant or allow any movement in the setting area, which can cause consolidation<br />
process retardation.<br />
When deciding that a patient must use an implant, the following factors can be of extreme importance<br />
for the success of the adequate procedure:<br />
• The patient's weight. Either a heavy or an overweight patient can overload the implantat, leading the<br />
whole operation as well as the device to failure. • If the patient is engaged in an occupation or any other<br />
activity that demands long walks or even running, lifting weights or muscular strength, these efforts can<br />
also result in failure of the device. • Senility, insanity or alcoholism among others, can take the patient to<br />
ignore certain limitations and necessary precautions in the use of the device, leading the implant to lack<br />
of efficiency in working or other complications. • In certain cases degenerative illnesses progressions<br />
can be so advanced, that they substantially diminish the useful life of the implant. For such cases the<br />
implant can be considered as a technical expedient for retardation of the advance of the illness or only<br />
for a temporary relief. • When in doubt regarding the patient's sensibility to strange bodies to his/her<br />
organism, or towards allergic reactions, the patient must be submitted to appropriate tests before the<br />
choice and selection of the material to be implanted. • This implantation could not be suitable for<br />
patients with bone insufficiency, and that haven't had concluded bone growth. The doctor must<br />
carefully evaluate the amount of bone before carrying through orthopedic surgery in patients whose<br />
bone growth is limited.<br />
The use of implant and the placement of parts or implant in the body must not join, disturb or harm the<br />
bone growth plate.<br />
Postoperative care is important. The patient must be instructed on the limitations of the implant and be<br />
warned not to carry weights or to provoke tensions in the device until the total consolidation of the bone<br />
and the complete healing.<br />
HANDLING OF THE IMPLANT<br />
The correct handling of the implant is extremely important. Twisting the parts has to be avoided as<br />
much as possible. Nonetheless, if the twist is absolutely necessary, the device cannot be drastically<br />
bent, or twisted in the opposite way, neither must be beveled, scratched nor flayed.<br />
All these operations can injure the surface and the part finishing, as well as initiating points of internal<br />
damages, which might become located corrosion focus.<br />
No implant must be reused. Once used, the implant must be discarded, packed in inviolable pack with<br />
the infectious-contaminated hospital garbage, even if they look being new and in good conditions of<br />
use. They may have small imperceptible injuries that will certainly lead to severe imperfections for the<br />
fatigue for use. In general, it demands extra attention to the asepsis in order to prevent risks of<br />
contamination or surgical infection.<br />
RECOMMENDATIONS IN CASE ONE OF THE COMPONENTS FALLS OFF IN SURGERY:<br />
In case of the falling off of an implant during the surgical act, even if it is not damaged, it has to be<br />
F. Fiber
S U T U R E A N C H O R<br />
discarded, packed in inviolable pack with the infectious-contaminated hospital garbage, since its<br />
re-sterilization is not possible.<br />
POSTOPERATIVE INSTRUCTIONS TO THE PATIENT<br />
The doctor must instruct and inform the patient the implant limitations so that he/she can take<br />
precautions regarding the physical activity and the load capacity and weight resistance until the<br />
total consolidation of the bone and the complete healing of the soft parts. It must be warned that the<br />
not observance of the postoperative instructions can lead the implant to a rupture or a possible<br />
migration, causing the need of removing the same.<br />
POSTOPERATIVE IMPLANTATIONS MAINTENANCE/TRACEABILITY AND PACKING<br />
Traceability is controlled through a batch number inserted in the label, which is granted by the<br />
primary supplier. This number usually consists of 2 letters and 5 numbers and it also provides year<br />
of its manufacture, the raw material origin, sterilization, and expedition date.<br />
Five labels are supplied inside the package: one is attached to the PATIENT'S medical record,<br />
another one is fixed to the COMPANY'S delivery document, and the third one fixed to the INVOICE<br />
and the other labels must be delivered to the Patient and to the Distributor.<br />
- The product is supplied in the sterilized condition, in double Blister in rigid packing, duly identified<br />
by adhesive labels, guaranteeing traceability of the product.<br />
- The packing must be unbroken.<br />
- Always assure the product is valid up to date, do not use it in any circumstance in case the<br />
sterilization stated period is no longer valid.<br />
SURGICAL TECHNIQUE<br />
1. Establish axial alignment. 2. There is 1 laser mark in the instrument delimiting the implantation<br />
extremity, which shows the adequate insertion depth. 3. Perforate or insert the screw clockwise. If<br />
inserting with electric devices, insert the Anchor Screw in one single movement. Stopping and<br />
restarting perforation can result in a rotatory force excess applied to the implant which can result in<br />
malfunction.<br />
The anchors can be inserted directly to the prepared bone tissue or inserted through the tissue<br />
when it is appropriate. 4. Pull the instrument of insertion straightforward in order to let the anchor or<br />
implant in its position of suture. 5. Proceed the ForceF.® suture wire knotting and cut the remnant<br />
part of it.<br />
CONTRAINDICATIONS:<br />
A. Active Infections; B. Patient with immature skeleton; C. In the presence of chemical alterations,<br />
severe osteopenia, or degenerative illness, that can interfere in the Anchor Screw setting security;<br />
D. Pathological Alterations of the soft tissue that will be sutured, in order to harm the security of the<br />
setting for the suture; E. Patients that do not want or are disabled to fulfill the postoperative<br />
instructions due the physical or mental conditions; F. Procedures that provide long term contact<br />
with saline solutions (biliary and urinary tracts), being able to result in the formation of calculations;<br />
G. In case of not-sterilized environment, that is, open sockets; H. Sensitivity to strange body. In<br />
case of rejection suspect, Tests of sensitivity to the material must be carried through; I. Inadequate<br />
covering with healthful tissue; J. Infections and/or limitations in the sanguine flow that can become<br />
healing slow and increase the possibility of infection and/or implant rejection; K. Degenerative<br />
illness occurrence that can adversely affect the appropriate settling of the implant.<br />
ADVERSE EFFECT:<br />
A. It can cause suture disruption; B. It can occasionally produce light erythema and pain in the<br />
suture place due tissue wound surgical trauma; C. The anchors can be freed or lose the setting; D.<br />
vascular Alterations; E. It is possible that the magnetic resonance causes metallic implant and<br />
surrounding tissues heating; F. Bone density reduction and/or bone necrosis due to protection<br />
against tension; G. Allergic reaction or sensitivity to the metal of the implant; H. Damages to the<br />
nerve due to a surgical trauma; I. Anchors disruption due bone tissue union delay or separation; J.<br />
Anchor Screw bend or breaking; K. Pain, discomfort and/or abnormal sensation due to presence of<br />
the Anchor Screw; L. superficial and/or deep Infection; M. Restriction to growth; N. Anchor Screw<br />
passive transmigration; O. Tissue coloration.<br />
WARNINGS:<br />
A. Biomecânica Anchor Screw incomplete insertion will not bring effectiveness in the setting; B.<br />
The degree of postoperative mobility will be determined by the doctor and must be informed to the<br />
patient; C. medical literature says that the possibility of success of surgeries with suture anchors is<br />
higher when the same ones are inserted 90º, since their tensile strength is higher than when they<br />
are inserted in different angles; D. Do not implant this device in epiphyseal cartilage growth plates;<br />
E. Latex has not been used in any of the devices of the anchor or in its packing; F. The surgical<br />
implants must never be reused, and the removed implants must never be implanted again. Small<br />
defects and chamber pressure standards can occur, even if the implantation seems flawless,<br />
causing implantation failure and disruption; G. In case of an implantable device, there is a risk to<br />
introduce strange materials and particles, including powder of gloves, lints of materials and agents<br />
of cleanness and other contaminated elements from the surface. All the efforts must be made to<br />
limit the handling of the setting devices. Moreover, if any device of setting is in contact with<br />
corporeal fluids, it must not be reused due to possible pathogenic blooded transmission; H. The<br />
doctor is the responsible one for the conclusion of the proper training, appropriate selection of the<br />
patient, choice and settling of the implant, as well as for the decision regarding keeping or removing<br />
the implants after fulfilling its clinical functions; I. Do not to use this product in places where the<br />
setting levels are superior to the limits presented for this product; J. Biomecânica Anchor Screws<br />
must not be submitted to precocious load, previously to after-surgical consolidation. To do so, it<br />
must be clarified to the patient that the implant does not substitute the bone tissue nor the adjacent<br />
soft parts, and that the medical recommendations are important and must be followed;<br />
DISABLE AND DISCARDING:<br />
Removed implants must never be implanted again. Their stress might provoke development of<br />
microscopical imperfections and, even if the implantation seems flawless, it can cause its own<br />
failure.<br />
Implants that were removed from their internal packing and inserted into the surgical environment -<br />
even if not implanted or contaminated for other sources yet - must be treated as contaminated<br />
material, the same procedure holds true when it comes to removed devices.<br />
These devices must be made unusable for use before the discarding. We recommend that the<br />
parts are rasped, warped or cut for its disable.<br />
Removed devices are considered hospital garbage (potentially contaminated products), having to<br />
be treated as so, according to norms of the local sanitary authority.<br />
According to the Resolution REVERSE SPEED nº 2605, of 11/08/06, implanted devices of any<br />
nature entitled one use only, are forbidden to be reused.<br />
STERILIZATION:<br />
Biomecânica Twister Anchor Screw is supplied sterilized through ethylene oxide (E.T.O.)<br />
Sterilization - parameters and procedures established in the protocol of validation and the EN550:<br />
1994 Sterilization of Medical Devices - Validation and Routine Control of Ethylene Oxide<br />
Sterilization with validity of 5 years.<br />
Responsible technician<br />
Eng.º José Roberto Pengo -CREA-SP 06009567 65<br />
MANUFACTURED BY:<br />
BIOMECÂNICA IND. E COM. DE PRODUTOS ORTOPÉDICOS LTDA<br />
Rua Luiz Pengo, 145, 1º Distrito Industrial - CX Postal 1014 - CEP: 17203-970 - Fone: 55 (14)<br />
2104-7900 - FAX: 55 (14) 2104-7908 - CNPJ 58.526.047/0001-73 - INDÚSTRIA BRASILEIRA<br />
www.biomecanica.com.br - biovendas@biomecanica.com.br R.G. ANVISA: 80128580093<br />
EC REP<br />
CRUVAL sl<br />
Paseo de la Chopera, 15 - Madrid - Spain<br />
Phone: 0034 91 517 2492 Fax: 0034 91 842 9180<br />
MANUFACTURER’S AUTHORIZED EU REPRESENTATIVE<br />
TORNILLO <strong>ÂNCORA</strong> BIOMECANICA<br />
ESPAÑOL<br />
DESCRIPCIÓN DEL PRODUCTO<br />
El Tornillo Áncora Biomecânica - Twister El tornillo Ancora Biomecânica – Twister es destinado a la<br />
fijación de tejidos mueles al hueso en procesos quirúrgicos realizados para el reparo del tendón –<br />
hueso de los tendones flexores de las manos y tendones – huesos del manguito rotador (hombro).<br />
COMPOSICIÓN<br />
1. Tornillo Áncora: Liga de Titanio (Ti 6AL4V) / Normas aplicables: ASTM F136 / NBR ISO 5832-3<br />
Medidas: Ø2,0 (3125-20-000), Ø2,7 ( 3125-27-000), Ø3,5 ( 3125-35-000), Ø5,0 (3125-50-000).<br />
RESISTENCIA<br />
N<br />
430<br />
2. Hilo de Sutura F.Fiber®: El hilo de Sutura F.Fiber® que acompaña el producto es no-absorbible,<br />
compuesto por una fibra de polietileno de ultra-alto peso molecular, única en el mercado, que<br />
garantiza una excelente resistencia a tensión y a ruptura, así como mayor lubricación.<br />
Los Hilos de Sutura F.Fiber® son trenzados en blanco/azul o blanco/negro, registrados en el FDA<br />
(KO63778 / Ko70673) Normas aplicables: ABNT NBR 13904<br />
Comparación de Resistencia<br />
80<br />
Ethibond #2<br />
70<br />
Carga (libras)<br />
230<br />
190<br />
90<br />
Média<br />
60<br />
50<br />
40<br />
30<br />
20<br />
10<br />
0<br />
88,03<br />
2,0<br />
191,884<br />
2,7<br />
239,405<br />
3,5<br />
F. Fiber<br />
Resistencia Tensión<br />
423,53<br />
5,0<br />
Tamanho<br />
Prueba de Nudo<br />
FiberWire #2<br />
F. Fiber #2<br />
3. Aplicador para Tornillo Áncora: Eje de Acero Inoxidable (ACERO AISI 304 de alta dureza) con<br />
cabo de Polipropileno.<br />
Normas aplicables: ASTM 276<br />
DESCRIPCIÓN DEL PRINCIPIO FÍSICO Y FUNDAMENTOS DE LA TECNOLOGÍA APLICADOS<br />
PARA SU FUNCIONAMIENTO Y ACCIÓN:<br />
El Conjunto Artroscópico Biomecânica es destinado a la fijación del tejido blando al hueso. Este<br />
producto es recomendado para los siguientes procedimientos:<br />
INDICACIONES:<br />
Mini Twister – 2,0 mm y 2,7 mm – indicado para el reparo del tendón-hueso de los tendones<br />
flexores de las manos.<br />
Twister – 3,5 mm y 5,0 mm – indicado para el reparo del tendón-hueso del manguito rotador<br />
(hombro).<br />
SELECCIÓN Y ELECCIÓN CORRECTA DEL IMPLANTE<br />
La elección correcta del implante es extremamente importante: la posibilidad de éxito en la fijación<br />
de la fractura aumenta con la elección apropiada del tamaño y diseño del implante.<br />
Ningún dispositivo, con la finalidad de soportar o no algún peso, podrá resistir a las insoportables<br />
presiones generadas por el peso total del cuerpo del paciente. Hasta que sea alcanzada la<br />
recuperación de la cirugía el paciente debe utilizar algún soporte externo adecuado y restringir las<br />
actividades físicas que puedan colocar presión adicional sobre el implante o permitir cualquier<br />
movimiento en el área de fijación, que pueda causar el atraso del proceso de consolidación.<br />
Al decidir que un paciente debe usar un implante, los siguientes factores pueden ser de extrema<br />
importancia para el éxito del procedimiento adecuado:<br />
• El peso del paciente. Un paciente obeso o con exceso de peso pode sobrecargar el implante, lo<br />
que conducirá toda la operación, incluyendo el dispositivo, al fracaso. • Si el paciente ejerce una<br />
ocupación o actividad que exija de él grandes caminatas o corridas, levantamiento de pesos o<br />
fuerza muscular, esos esfuerzos pueden también resultar en el fracaso del dispositivo. • A senilidad,<br />
las enfermedades mentales o alcoholismo entre otras, pueden llevar el paciente a ignorar ciertas<br />
limitaciones y precauciones necesarias en el uso del dispositivo, llevando el implante a fallar o a<br />
tener otras complicaciones. • En ciertos casos las progresiones de enfermedades degenerativas<br />
pueden estar tan avanzadas, que disminuyen sustancialmente la vida útil del implante. Para tales<br />
casos los implantes pueden ser considerados como un expediente técnico para retardo del avance<br />
de la enfermedad o apenas para un alivio temporal. • Cuando hay sospecha de que el paciente sea<br />
sensible a cuerpos extraños a su organismo, o que pueda tener reacciones alérgicas, debe ser<br />
realizado exámenes apropiados antes de la elección y selección del material a ser implantado. •<br />
Este implante podrá no ser adecuado para pacientes con cantidad ósea insuficiente, y que no<br />
tengan crecimiento óseo concluido. El médico debe evaluar cuidadosamente la cantidad de huesos<br />
antes de realizar la cirugía ortopédica en pacientes cuyo crecimiento óseo es limitado. El uso de<br />
implantes y la colocación de piezas o implantes en el cuerpo no debe unir, perturbar o perjudicar la<br />
placa de crecimiento.<br />
El cuidado pos -operatorio es importante. El paciente debe ser instruido sobre las limitaciones de su<br />
implante y advertido para no cargar pesos o provocar tensiones en el dispositivo hasta la total<br />
consolidación del hueso y la completa cicatrización.<br />
MANIPULACIÓN DEL IMPLANTE<br />
El correcto manejo del implante es extremamente importante. Se Debe evitar, cuanto sea posible,<br />
contorcer las piezas. En todo caso, si la torsión es absolutamente necesaria, el dispositivo no<br />
deberá ser drásticamente doblado, o torcido en sentido contrario, tampoco debe ser cortado, ni<br />
arañado o desollado. Todas estas operaciones pueden lesionar la superficie y el acabado de la<br />
pieza, así como iniciar puntos de daños internos, los cuales podrán tornarse focos localizados de<br />
corrosión.<br />
Ningún implante debe ser reaprovechado. Una vez usados, los implantes deberán ser descartados,<br />
embalados en envoltura inviolable juntamente con la basura hospitalaria infecto-contaminada,<br />
mismo que parezcan nuevos y en buenas condiciones. Ellos podrán tener pequeñas lesiones<br />
imperceptibles que ciertamente conducirán a severas fallas por la fatiga del uso. De modo general<br />
se debe tener atención redoblada en la asepsia para evitar los riesgos da contaminación o de<br />
infección quirúrgica.<br />
RECOMENDACIONES EN CASO DE CAÍDA DE LOS COMPONENTES:<br />
En caso de caída de un implante, durante el acto quirúrgico, mismo que no haya daños, deberá ser<br />
F. Fiber<br />
descartado, embalado en envoltura inviolable juntamente con la basura hospitalaria infectocontaminada,<br />
ya que no es posible su re-esterilización.<br />
INSTRUCCIONES POS-OPERATORIAS AL PACIENTE<br />
El médico debe instruir e informar al paciente sobre las limitaciones del implante para que tome<br />
precauciones respecto a la actividad física y al soporte de peso y carga hasta la total consolidación del<br />
hueso y la completa cicatrización de las partes blandas. Se debe advertir que el no cumplimiento de las<br />
instrucciones pos-operatorias pueden llevar a una ruptura del implante o a una posible migración,<br />
siendo necesaria una cirugía de revisión para retirar el mismo.<br />
MANTENIMIENTO DE LOS IMPLANTES POS-OPERACIÓN / RASTREABILIDADE E<br />
EMBALAGEM<br />
El rastreo es controlado a través de un número de lote inserido en el rótulo, que es concedido por el<br />
productor primario.<br />
Este número es usualmente formado por 2 letras y 5 números y con él se puede constatar el año de<br />
fabricación, el origen de la materia prima, la fecha de esterilización y expedición.<br />
Dentro de los embalajes son suministrados cinco etiquetas: una etiqueta es pegada en la historia del<br />
PACIENTE, otra en el documento de entrega de la EMPRESA, la tercera en la FACTURA de venta y las<br />
otras deben ser entregadas al Paciente y al Distribuidor.<br />
- El producto es suministrado en condición estéril, en doble blister en embalaje rígida, debidamente<br />
identificado por etiquetas adhesivas, garantizando el rastreo del producto.<br />
- El embalaje debe estar intacto.<br />
- Verifique siempre la fecha de validez del producto, no lo utilice en ninguna circunstancia, caso el plazo<br />
de esterilización este vencido.<br />
TÉCNICA QUIRÚRGICA<br />
1. Establezca alineamiento axial. 2. Hay 1 marca láser en el instrumental, que delimita la extremidad del<br />
implante, la cual muestra la profundidad de inserción adecuada. 3. Perfore o inserte el tornillo en el<br />
sentido horario. Si lo esta insertando con aparatos eléctricos, inserte el Tornillo Áncora en un solo<br />
movimiento. Parar y reiniciar la perforación puede resultar en un exceso de fuerza rotatoria aplicada al<br />
implante la cual puede resultar en la falla del mismo. Las Áncoras pueden ser insertadas directamente<br />
en el tejido óseo preparado o insertadas por medio del tejido cuando sea apropiado. 4. Hale el<br />
instrumento de inserción en forma recta esto deja el áncora o implante en su posición de sutura. 5.<br />
Efectúe el amarrado del hilo de sutura ForceF.® y corte las sobras del mismo.<br />
CONTRA INDICACIONES:<br />
A. Infecciones activas; B. Pacientes esqueléticamente inmaduros; C. En presencia de alteraciones<br />
quísticas, osteopenia grave, o enfermedad degenerativa, que puede comprometer la seguridad de la<br />
fijación del Tornillo Áncora; D. Alteraciones patológicas de los tejidos blandos que serán suturados, de<br />
forma que perjudiquen la seguridad de la fijación por la sutura; E. Pacientes que no quieren o están<br />
imposibilitados de cumplir las instrucciones pos-operatorias debido a condiciones físicas o mentales<br />
que presentan; F. Procedimientos que proporcionen contacto prolongado con soluciones salinas<br />
(tractos biliar y urinario), pudiendo resultar en la formación de cálculos; G. Se hay un ambiente noestéril,<br />
o sea, cavidades abiertas como senos; H. Sensibilidad al cuerpo extraño. Deben ser realizados<br />
pruebas de sensibilidad al material en los casos de sospecha de rechazo; I. Cobertura inadecuada con<br />
tejido saludable; J. Infecciones e/o limitaciones en el flujo sanguíneo que puedan tornar la cicatrización<br />
lenta y aumentar la posibilidad de infección e/o rechazo del implante; K. Ocurrencia de enfermedad<br />
degenerativa que pueda afectar adversamente la colocación apropiada de los implantes.<br />
EFECTOS ADVERSOS:<br />
A. Puede ocurrir rompimiento de la sutura; B. Ocasionalmente puede ocurrir eritema leve y dolor en el<br />
local de la sutura debido al trauma de la herida Quirúrgica en el tejido; C. Las Áncoras pueden soltarse o<br />
perder la fijación; D. Alteraciones vasculares; E. Es posible que la resonancia magnética cause un<br />
calentamiento de los implantes metálicos y de los tejidos vecinos; F. Reducción en la densidad ósea e/o<br />
necrosis ósea debido a la protección contra la tensión; G. Reacción alérgica o sensibilidad al metal del<br />
implante; H. Daños al nervio debido a un trauma quirúrgico; I. Ruptura de las áncoras debido al retraso<br />
de la unión o desunión del tejido óseo; J. Doblado o fractura del Tornillo Áncora; K. Dolor, incomodidad<br />
e/o sensación anormal debido a la presencia del Tornillo Áncora; L. Infección superficial e/o profunda;<br />
M. Restricción del crecimiento; N. Trasmigración pasiva del Tornillo Áncora; O. Coloración del tejido.<br />
ADVERTENCIAS:<br />
A. La inserción incompleta del Tornillo Áncora Biomecânica no traerá eficiencia en la fijación; B. El<br />
grado de movilidad pos-operatoria será determinado por el médico y debe ser informado al paciente; C.<br />
La literatura médica cita que la posibilidad de suceso de las cirugías con áncora de sutura son más<br />
grandes cuando las mismas son insertadas a 90º, pues la resistencia a la tracción de las mismas son<br />
más grandes que cuando son insertadas en ángulos diferentes a este; D. No implantar este dispositivo<br />
en placas de cartílago epifisárias de crecimiento; E. No es utilizado látex en ningún de los dispositivos<br />
del áncora o en su embalaje; F. Los implantes quirúrgicos nunca deben ser reutilizados, y los implantes<br />
explantados nunca deben ser implantados nuevamente. Pueden ocurrir pequeño defectos y padrones<br />
de presión interna, mismo si el implante parece intacto, causando falla y ruptura del implante; G. En el<br />
caso de un dispositivo implantable, hay un riesgo de introducir materiales extraños y partículas,<br />
incluyendo talco de guantes, hilachas de materiales y agentes de limpieza y otros contaminantes de la<br />
superficie. Todos los esfuerzos deben ser hechos para limitar el manoseo de los dispositivos de fijación.<br />
Además de eso, si algún dispositivo de fijación entra en contacto con fluidos corpóreos, él no debe ser<br />
reutilizado debido a la posible transmisión de los patogénicos sanguíneos; H. El médico es el<br />
responsable por la conclusión del entrenamiento adecuado, selección apropiada del paciente, elección<br />
y colocación del implante, así como por la decisión de dejar o remover los implantes después del<br />
cumplimiento de sus funciones clínicas; I. No utilizar este producto en locales en que los niveles de<br />
fijación sean superiores a los límites pre-establecidos para este producto; J. El Tornillo Áncora<br />
Biomecânica no debe ser sometido a carga precoz, anteriormente a la consolidación pos-quirúrgica.<br />
Por lo tanto, debe ser aclarado al paciente que el implante no substituye el tejido óseo y ni las partes<br />
blandas adyacentes, y que las recomendaciones médicas son importantes y deberán ser seguidas;<br />
INUTILIZACIÓN Y DESCARTE:<br />
Implantes explantados nunca deben ser implantados nuevamente. El estrés podrá provocar desarrollo<br />
de imperfecciones microscópicas y, mismo que el implante parezca intacto, puede ocasionar la falencia<br />
del mismo.<br />
Implantes que sean removidos del embalaje interno e inseridos dentro del ambiente quirúrgico, mismo<br />
que no hayan sido implantados o contaminados por otras fuentes, deben ser tratados como material<br />
contaminado, lo mismo ocurre con dispositivos explantados. Estos dispositivos deben ser inutilizados<br />
para uso antes del descarte.<br />
Recomendamos que las piezas sean limadas, torcidas o cortadas para su inutilización.<br />
Dispositivos explantados son considerados basura hospitalaria (productos potencialmente<br />
contaminantes), debiendo ser tratados como tal, conforme normas de la autoridad sanitaria local.<br />
Conforme la Resolución RE nº 2605, de 11/08/06, dispositivos implantables de cualquier naturaleza<br />
encuadrados como de uso único son prohibidos de ser reprocesados.<br />
ESTERILIZAÇÃO:<br />
El Tornillo Áncora Twister de Biomecânica es suministrado estéril a través de Esterilización por óxido de<br />
etileno (E.T.O.) - parámetros y procedimientos establecidos en el protocolo de validación y en la<br />
EN550:1994 Sterilization of Medical Devices – Validation and Routine Control of Ethylene Oxide<br />
Sterilization con validez de 5 años.<br />
RESPONSABLE TÉCNICO<br />
Ing.º José Roberto Pengo - CREA-SP 06009567 65<br />
FABRICADO POR:<br />
BIOMECÂNICA IND. E COM. DE PRODUTOS ORTOPÉDICOS LTDA<br />
Rua Luiz Pengo, 145, 1º Distrito Industrial - CX Postal 1014 - CEP: 17203-970 - Fone: 55 (14) 2104-<br />
7900 - FAX: 55 (14) 2104-7908 - CNPJ 58.526.047/0001-73 - INDÚSTRIA BRASILEIRA<br />
www.biomecanica.com.br - biovendas@biomecanica.com.br<br />
R.G. ANVISA: 80128580093<br />
EC REP<br />
CRUVAL sl<br />
Paseo de la Chopera, 15 - Madrid - Spain<br />
Phone: 0034 91 517 2492 Fax: 0034 91 842 9180<br />
MANUFACTURER’S AUTHORIZED<br />
EU REPRESENTATIVE<br />
<strong>REV03</strong>