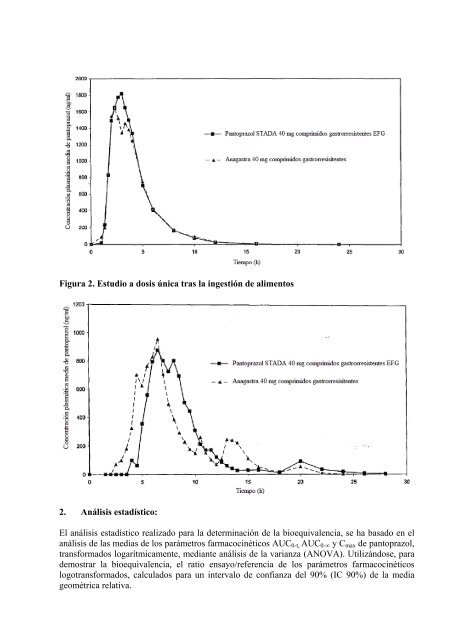
Estudio a dosis única tras la ingestión de alimentos: 28 horas. Nº de muestras por voluntario: Estudio a dosis única en ayunas: 18 muestras. Estudio a dosis única tras la ingestión de alimentos: 35 muestras. RESULTADOS 1. Análisis farmacocinético: El análisis farmacocinético para la determinación de la bioequivalencia consistió en el análisis de pantoprazol en plasma. La variable principal del estudio fue el cálculo de los parámetros farmacocinéticos que definen la bioequivalencia en magnitud y en velocidad (AUC 0-t , AUC 0-∞ y C max ). La determinación del principio activo en plasma y el análisis farmacocinético del pantoprazol se realizó en Algoritme Pharma Inc. (Canadá), utilizándose una metódica analítica validada de HPLC con detección por MS. Los resultados obtenidos se expresan en las Tablas 1 y 2 como medias ± coeficiente de variación, obtenidas a partir de los parámetros farmacocinéticos calculados para cada voluntario. Tabla 1. Estudio a dosis única en ayunas AUC 0-t AUC 0-∞ Fármaco (ng·h/ml) (ng·h/ml) C max (ng/ml) T max (h)* <strong>Pantoprazol</strong> <strong>STADA</strong> <strong>40</strong> <strong>mg</strong> <strong>comprimidos</strong> <strong>gastrorresistentes</strong> 6734,9 ± 58,0 6652,5 ± 55,9 2920,6 ± 37,7 2,33 ± 33,1 Anagastra ® <strong>40</strong> <strong>mg</strong> <strong>comprimidos</strong> <strong>gastrorresistentes</strong> 6100,0 ± 60,6 6373,4 ± 58,4 3118,6 ± 33,8 2,33 ± 38,2 * Datos expresados como mediana Tabla 2. Estudio a dosis única tras la ingestión de alimentos AUC 0-t AUC 0-∞ Fármaco (ng·h/ml) (ng·h/ml) C max (ng/ml) T max (h)* <strong>Pantoprazol</strong> <strong>STADA</strong> <strong>40</strong> <strong>mg</strong> <strong>comprimidos</strong> <strong>gastrorresistentes</strong> 4384,2 ± <strong>40</strong>,6 4632,0 ± 38,8 2480,9 ± 30,6 6,75 ± 50,3 Anagastra ® <strong>40</strong> <strong>mg</strong> <strong>comprimidos</strong> <strong>gastrorresistentes</strong> 4580,5 ± 48,8 4781,5 ± 48,1 2619,9 ± 26,9 6,00 ± 55,5 * Datos expresados como mediana En las Figuras 1 y 2 se muestran las medias de las curvas de los niveles plasmáticos obtenidos a partir de la concentración en cada tiempo de muestreo de pantoprazol para ambas formulaciones, la de referencia (Anagastra ® <strong>40</strong> <strong>mg</strong> <strong>comprimidos</strong> <strong>gastrorresistentes</strong>) y la de ensayo (<strong>Pantoprazol</strong> <strong>STADA</strong> <strong>40</strong> <strong>mg</strong> <strong>comprimidos</strong> <strong>gastrorresistentes</strong> <strong>EFG</strong>). Figura 1. Estudio a dosis única en ayunas
Figura 2. Estudio a dosis única tras la ingestión de alimentos 2. Análisis estadístico: El análisis estadístico realizado para la determinación de la bioequivalencia, se ha basado en el análisis de las medias de los parámetros farmacocinéticos AUC 0-t, AUC 0-∞ y C max de pantoprazol, transformados logarítmicamente, mediante análisis de la varianza (ANOVA). Utilizándose, para demostrar la bioequivalencia, el ratio ensayo/referencia de los parámetros farmacocinéticos logotransformados, calculados para un intervalo de confianza del 90% (IC 90%) de la media geométrica relativa.