Susana Castillo-Rojas - Instituto de Ciencias Nucleares ...
Susana Castillo-Rojas - Instituto de Ciencias Nucleares ...
Susana Castillo-Rojas - Instituto de Ciencias Nucleares ...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
D.O.<br />
D.O.<br />
INFORME TÉCNICO 01, 1-11, (2007) <strong>Castillo</strong>-<strong>Rojas</strong>, S.<br />
Departamento <strong>de</strong> Química <strong>de</strong> Radiaciones y<br />
Radioquímica. ICN-UNAM<br />
4<br />
III. Preparación <strong>de</strong> la disolución buffer (6) .<br />
Pesar 8.2 g <strong>de</strong> CH 3 -COONa · 3H 20. Por otro lado, agregar agua <strong>de</strong>stilada hasta la mitad <strong>de</strong> un<br />
matraz <strong>de</strong> aforo <strong>de</strong> 100 mL, añadir cuantitativamente 1 mL <strong>de</strong> H 2SO 4 concentrado, agitar la<br />
disolución y entonces disolver la sal previamente pesada, completar el aforo con agua. El buffer<br />
tiene un pH = 5.<br />
IV.<br />
Realización <strong>de</strong> la curva <strong>de</strong> calibración para <strong>de</strong>terminar el coeficiente <strong>de</strong> extinción molar <strong>de</strong>l Fe 2+ a<br />
510nm.<br />
Pesar 0.0139 g <strong>de</strong> FeSO 4 ·7H 2O (PM = 278.02 g/mol), para preparar 100 mL <strong>de</strong> disolución <strong>de</strong><br />
concentración 5x10 - 4 M. En matraces <strong>de</strong> aforo <strong>de</strong> 100 mL agregar a cada uno sucesivamente<br />
alícuotas <strong>de</strong> 5.0, 10.0, 20.0 y 50.0 mL <strong>de</strong> Fe 2+ , añadir a todos 5 mL <strong>de</strong> buffer y 3 mL <strong>de</strong> 1,10-<br />
fenantrolina al 2%, agitar bien cada matraz y leer inmediatamente la <strong>de</strong>nsidad óptica a 510 nm.<br />
No olvidar preparar una muestra blanco.<br />
Resultados:<br />
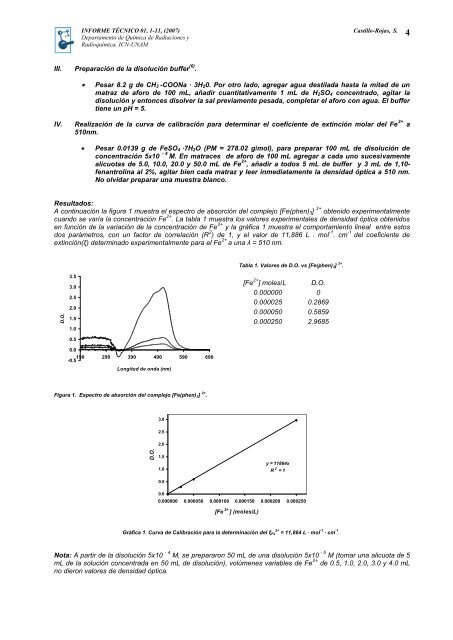
A continuación la figura 1 muestra el espectro <strong>de</strong> absorción <strong>de</strong>l complejo [Fe(phen) 3] 2+ obtenido experimentalmente<br />
cuando se varía la concentración Fe 2+ . La tabla 1 muestra los valores experimentales <strong>de</strong> <strong>de</strong>nsidad óptica obtenidos<br />
en función <strong>de</strong> la variación <strong>de</strong> la concentración <strong>de</strong> Fe 2+ y la gráfica 1 muestra el comportamiento lineal entre estos<br />
dos parámetros, con un factor <strong>de</strong> correlación (R 2 ) <strong>de</strong> 1, y el valor <strong>de</strong> 11,886 L . mol -1 . cm -1 <strong>de</strong>l coeficiente <strong>de</strong><br />
extinción(ξ) <strong>de</strong>terminado experimentalmente para el Fe 2+ a una λ = 510 nm.<br />
Tabla 1. Valores <strong>de</strong> D.O. vs [Fe(phen) 3] 2+ .<br />
3.5<br />
3.0<br />
2.5<br />
2.0<br />
1.5<br />
1.0<br />
0.5<br />
0.0<br />
190<br />
-0.5<br />
290 390 490 590 690<br />
Longitud <strong>de</strong> onda (nm)<br />
[Fe 2+ ] moles/L D.O.<br />
0.000000 0<br />
0.000025 0.2869<br />
0.000050 0.5859<br />
0.000250 2.9685<br />
Figura 1. Espectro <strong>de</strong> absorción <strong>de</strong>l complejo [Fe(phen) 3] 2+ .<br />
3.0<br />
2.5<br />
2.0<br />
1.5<br />
1.0<br />
y = 11864x<br />
R 2 = 1<br />
0.5<br />
0.0<br />
0.000000 0.000050 0.000100 0.000150 0.000200 0.000250<br />
[Fe 2+ ] (moles/L)<br />
Gráfica 1. Curva <strong>de</strong> Calibración para la <strong>de</strong>terminación <strong>de</strong>l ξ Fe 2+ = 11,864 L · mol -1 · cm -1 .<br />
Nota: A partir <strong>de</strong> la disolución 5x10 - 4 M, se prepararon 50 mL <strong>de</strong> una disolución 5x10 - 5 M (tomar una alicuota <strong>de</strong> 5<br />
mL <strong>de</strong> la solución concentrada en 50 mL <strong>de</strong> disolución), volúmenes variables <strong>de</strong> Fe 2+ <strong>de</strong> 0.5, 1.0, 2.0, 3.0 y 4.0 mL<br />
no dieron valores <strong>de</strong> <strong>de</strong>nsidad óptica.