CONSEJERIA DE MEDIO AMBIENTEJARDÍN BOTÁNICO CANARIO VIERA Y CLAVIJOVial co<strong>de</strong> Taxon Population [μg/ml]470 Limonium spectabile Morro <strong>de</strong> La Galera. T665 Convolvulus perraudieri 316/04 cultivado JBCVC, C 62,22337 Convolvulus perraudieri Arguineguín, C 459,4490 Convolvulus baruriculatus Aluce, Gomera 222,0474 Convolvulus subaruriculatus Cañada Cabrera-Agulo, La 24,9664 Convolvulus glandulosus 2163/B/02 cultivado JBCVC, C 238,01144 Convolvulus glandulosus Amurga, C 28,42506 Convolvulus canariensis Centro Visitantes Garajonay,G 380,082614 Convolvulus canariensis Ancón Negro, G 368,0717 Convolvulus lopez-socasi 56/04 cultivado JBCVC, C 92,23868 Convolvulus lopez-socasi .Famara, L 1024,21333 Dendriopoterium Guayedra, C 5.294,01626 Dendriopoterium menen<strong>de</strong>zi Al<strong>de</strong>a San Nicolás, C 49,71586 Dendriopoterium pulidoi Bco. <strong>de</strong> Tejeda, C 87,71584 Dendriopoterium pulidoi Bco. <strong>de</strong> Tejeda. C 540,22632 Bencomia exstipulata Tiro <strong>de</strong>l Guanche, T 374,52634 Bencomia exstipulata Tiro <strong>de</strong>l Guanche, T 1337,02023 Bencomia sphaerocarpa Fuente <strong>de</strong> Tincos, H 1223,32025 Bencomia sphaerocarpa Tabanos, H 1181,93867 Bencomia brachystachya Barranco <strong>de</strong> Tirajana, C 1377,63867.2 Bencomia brachystachya Barranco <strong>de</strong> Tirajana, C 976,9BCA16 Bencomia caudata Barranco Añavingo, T 58,7BSUP12 Bencomia caudata Barranco Seco, P 47,5Pb154 Poligonum maritimum Lobos, F 73,9Pb158 Poligonum maritimum Lobos, F 123,8Pb58 Poligonum balansae El Médano, T 60Pb59 Poligonum balansae El Médano, T 56,5- Optimización <strong>de</strong> los protocolos <strong>de</strong> amplificación y secuenciación.Según convenio, las amplificaciones se han <strong>de</strong>sarrollado para tres regiones codificantes <strong>de</strong>l ADNcloroplástico (rpoB, rpoC1 y matK) utilizando los cebadores universales para estas regiones aceptadospor el “Consortium for the Barcoding of Life” (CBOL <strong>de</strong> aquí en a<strong>de</strong>lante). El CBOL todavía no hallegado a un consenso en cuanto a las regiones <strong>de</strong>finitivas que van a utilizarse para plantas, aunqueen la reciente reunión <strong>de</strong> Nueva York, en la que el Departamento <strong>de</strong> Biodiversidad Molecular <strong>de</strong>lJBCVC estuvo representado, se estableció un plazo máximo <strong>de</strong> cuatro semanas (finales <strong>de</strong> mayoprincipios<strong>de</strong> junio <strong>de</strong> 2008) para consensuar las regiones <strong>de</strong>finitivas, entre las que probablemente seencuentren al menos dos <strong>de</strong> las que se han incluido en este estudio. La relación <strong>de</strong> nuestroDepartamento con la iniciativa <strong>de</strong>l código <strong>de</strong> barras <strong>de</strong> la vida y el hecho <strong>de</strong> que los ADN <strong>de</strong> estasmuestras se hallan <strong>de</strong>positados en el Banco <strong>de</strong> ADN <strong>de</strong> la Flora Canaria van a hacer posible secuenciarestas mismas muestras para cualquier otra región que se incluya en la propuesta final para plantas.Para aquellas muestras con una concentración y pureza a<strong>de</strong>cuadas se montaron reacciones <strong>de</strong>amplificación (PCR) para un volumen final <strong>de</strong> 25µl y con las condiciones (nº <strong>de</strong> ciclos y tiempos)recomendadas por el CBOL, en el termociclador “Mastercycler Gradient” <strong>de</strong> la casa comercialEppendorf. En todos los casos, se utilizó el kit REDDY MIX TM PCR MASTER MIX (Abgene) y se añadióBSA al 0.4% como componente adicional <strong>de</strong>l cóctel <strong>de</strong> reacción. El ADN <strong>de</strong> aquellos especimenes paralos que se obtuvo una amplificación exitosa, fue purificado con las columnas “GENELUTE PCR CLEAN-UP” (Sigma-Aldrich, C.O). Las muestras purificadas se secuenciaron con "BIG DYE V·3.1" (AppliedBiosystems, California, USA) en el secuenciador automático ABI 3100 <strong>de</strong>l laboratorio <strong>de</strong> GenéticaForense <strong>de</strong> la Universidad <strong>de</strong> Las Palmas <strong>de</strong> Gran Canaria.Tanto para las reacciones <strong>de</strong> PCR como para las <strong>de</strong> secuenciación fue necesario realizar algunasmodificaciones (Newmaster, et al. 2007) respecto a los protocolos propuestos y recomendados porCBOL (Kress, et al, 2005; Chase et al, 2007). Algunas <strong>de</strong> estas modificaciones supusieron variaciones<strong>de</strong> la temperatura <strong>de</strong> anillamiento (Ta), <strong>de</strong> la concentración final <strong>de</strong> magnesio, <strong>de</strong>l número <strong>de</strong> ciclosen el termociclador o la adición <strong>de</strong> DMSO en un 0.8%.Una vez optimizada la s condiciones <strong>de</strong> amplificación se cuantificó la concentración <strong>de</strong>l producto<strong>de</strong> PCR y según el tamaño <strong>de</strong> la región a secuenciar se estimó la concentración <strong>de</strong>l ADN necesario aañadir al cóctel <strong>de</strong> reacción.Camino <strong>de</strong>l Palmeral 1535017 Las Palmas <strong>de</strong> Gran CanariaTel.: 928 219580 Fax: 928 219581
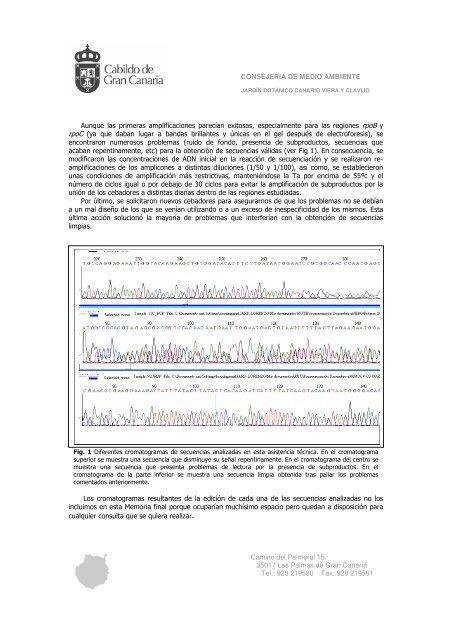
CONSEJERIA DE MEDIO AMBIENTEJARDÍN BOTÁNICO CANARIO VIERA Y CLAVIJOAunque las primeras amplificaciones parecían exitosas, especialmente para las regiones rpoB yrpoC (ya que daban lugar a bandas brillantes y únicas en el gel <strong>de</strong>spués <strong>de</strong> electroforesis), seencontraron numerosos problemas (ruido <strong>de</strong> fondo, presencia <strong>de</strong> subproductos, secuencias queacaban repentinamente, etc) para la obtención <strong>de</strong> secuencias válidas (ver Fig 1). En consecuencia, semodificaron las concentraciones <strong>de</strong> ADN inicial en la reacción <strong>de</strong> secuenciación y se realizaron reamplificaciones<strong>de</strong> los amplicones a distintas diluciones (1/50 y 1/100), así como, se establecieronunas condiciones <strong>de</strong> amplificación más restrictivas, manteniéndose la Ta por encima <strong>de</strong> 55ºc y elnúmero <strong>de</strong> ciclos igual o por <strong>de</strong>bajo <strong>de</strong> 30 ciclos para evitar la amplificación <strong>de</strong> subproductos por launión <strong>de</strong> los cebadores a distintas dianas <strong>de</strong>ntro <strong>de</strong> las regiones estudiadas.Por último, se solicitaron nuevos cebadores para asegurarnos <strong>de</strong> que los problemas no se <strong>de</strong>bíana un mal diseño <strong>de</strong> los que se venían utilizando o a un exceso <strong>de</strong> inespecificidad <strong>de</strong> los mismos. Estaúltima acción solucionó la mayoría <strong>de</strong> problemas que interferían con la obtención <strong>de</strong> secuenciaslimpias.Fig. 1 Diferentes cromatogramas <strong>de</strong> secuencias analizadas en esta asistencia técnica. En el cromatogramasuperior se muestra una secuencia que disminuye su señal repentinamente. En el cromatograma <strong>de</strong>l centro semuestra una secuencia que presenta problemas <strong>de</strong> lectura por la presencia <strong>de</strong> subproductos. En elcromatograma <strong>de</strong> la parte inferior se muestra una secuencia limpia obtenida tras paliar los problemascomentados anteriormente.Los cromatogramas resultantes <strong>de</strong> la edición <strong>de</strong> cada una <strong>de</strong> las secuencias analizadas no losincluimos en esta Memoria final porque ocuparían muchísimo espacio pero quedan a disposición paracualquier consulta que se quiera realizar.Camino <strong>de</strong>l Palmeral 1535017 Las Palmas <strong>de</strong> Gran CanariaTel.: 928 219580 Fax: 928 219581