Tulehduskipulääkkeiden turvallinen käyttö - Terveyskirjasto
Tulehduskipulääkkeiden turvallinen käyttö - Terveyskirjasto
Tulehduskipulääkkeiden turvallinen käyttö - Terveyskirjasto
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Käypä hoito -suositus<br />
<strong>Tulehduskipulääkkeiden</strong><br />
<strong>turvallinen</strong> <strong>käyttö</strong><br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys<br />
Tavoitteet<br />
Hoitosuosituksen tavoitteena on vähentää tulehduskipulääkeiden<br />
haittavaikutuksia ja etenkin<br />
niiden <strong>käyttö</strong>ön liittyvän maha- ja pohjukaissuolihaavan<br />
aiheuttamaa kuolleisuutta kiinnittämällä<br />
huomiota lääkehoidon aiheisiin, annoksiin<br />
ja laatuun, auttaa tunnistamaan alttius<br />
haittavaikutuksille, antaa suositus tulehduskipulääkeulkuksen<br />
ehkäisystä ja vähentää tulehduskipulääkkeiden<br />
tarpeetonta <strong>käyttö</strong>ä.<br />
Kohderyhmät<br />
Suosituksen kohderyhminä ovat tulehduskipulääkkeitä<br />
määräävät ja ulkuksen hoidosta vastaavat<br />
lääkärit, apteekkihenkilökunta sekä tulehduskipulääkkeitä<br />
käyttävät potilaat.<br />
Suosituksen keskeinen sisältö<br />
Tulehduskipulääke, myös reseptittä myytävä,<br />
voi aiheuttaa kuolemaan johtavan ulkuskomplikaation.<br />
Myös keuhkoihin tai maksaan kohdistuva<br />
haittavaikutus saattaa olla hengenvaarallinen.<br />
Ulkusriski on suurin iäkkäillä ja huonokuntoisilla<br />
potilailla, jotka ovat aikaisemmin<br />
sairastaneet ulkuksen tai ulkusvuodon. Tulehduskipulääkehoidon<br />
aihe, annos, kesto ja yhteisvaikutukset<br />
muiden lääkkeiden ja sairauksien<br />
kanssa tulee tarkoin punnita ennen hoidon<br />
aloittamista. Potilaalle pitää kertoa mahdollisista<br />
haitoista ja niihin viittaavista oireista sekä<br />
neuvoa ottamaan epäilyttävien oireiden ilmetessä<br />
yhteyttä hoitavaan lääkäriin. Suuren riskin<br />
potilaalle tulee antaa ensijaisesti parasetamolia.<br />
COX-2-selektiiviset ns. koksibit aiheuttavat vähemmän<br />
maha-suolikanavan haittoja kuin ei-selektiiviset<br />
tulehduskipulääkkeet, mutta valikoimattomista<br />
potilaista saatuja kokemuksia on<br />
toistaiseksi vielä vähän. Tarvittaessa on aloitettava<br />
ulkusprofylaksi.<br />
Käytön ja haittavaikutusten<br />
epidemiologia<br />
Käyttö. Tulehduskipulääkkeitä käytetään eniten<br />
tuki- ja liikuntaelinsairauksien (TULES) hoitoon.<br />
Erilaisten TULE-oireiden takia tehdään 10<br />
–20 % kaikista avohoidon vastaanottokäynneistä.<br />
Teollistuneiden maiden väestökehityksessä<br />
suurin lisäys lähivuosikymmeninä on yli 75-vuotiaiden<br />
määrässä eli ikäryhmässä, jossa nivelrikko-oireet<br />
ovat erittäin yleisiä [1]. Tulehduskipulääkkeet<br />
ovat antibioottien jälkeen toiseksi suurin<br />
suurin reseptilääkeryhmä teollistuneissa<br />
maissa [1]. Niitä koskevat lääkemääräykset ovat<br />
lisääntyneet viime vuosikymmeninä tasaisesti nimenomaan<br />
vanhemmissa ikäryhmissä. Joidenkin<br />
tutkimusten mukaan jopa puolet tulehduskipulääkeresepteistä<br />
kirjoitetaan yli 60-vuotiaille [1].<br />
Kansaneläkelaitoksen ja Stakesin vuosina 1995–<br />
96 tekemän väestötutkimuksen mukaan työikäisistä<br />
7 % ja 65 vuotta täyttäneistä 18 % käytti<br />
haastattelun aikaan jotakin reseptillä määrättyä<br />
tulehduskipulääkettä. Naiset käyttivät näitä<br />
lääkkeitä 1.5 kertaa useammin kuin miehet [2].<br />
Kansaneläkelaitoksen reseptitiedoston mukaan<br />
1914 Duodecim 2000; 116: 1914–31<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
Taulukko 1. <strong>Tulehduskipulääkkeiden</strong> haittavaikutukset.<br />
Haittavaikutus Esiintyvyys, %<br />
Vatsavaivat, maha-suolikanavan vauriot 10–45<br />
Keskushermosto-oireet 3–20<br />
Ihoreaktiot 2–5<br />
Ripuli 1–5<br />
Turvotukset 0–2<br />
Munuaisvaurio
COX-1 selektiivisyys<br />
COX-2 selektiivisyys<br />
Rofekoksibi<br />
Nimesulidi<br />
Selekoksibi<br />
Meloksikaami<br />
Diklofenaakki<br />
Ibuprofeeni<br />
Piroksikaami<br />
Naprokseeni<br />
6-NMA/nabumetoni<br />
Ketoprofeeni<br />
Indometasiini<br />
Asetyylisalisyylihappo<br />
1 000 100 10 1 0.1 0.01 0.001 0.0001<br />
COX-2/COX-1-estosuhde<br />
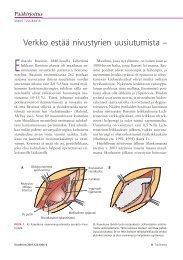
Kuva 1. <strong>Tulehduskipulääkkeiden</strong> COX-2/COX-1-estosuhde.<br />
noidien määrä kudoksissa lisääntyy huomattavasti<br />
tulehduksen yhteydessä. COX-2:n induktion<br />
tai aktiivisuuden esto rauhoittaa akuutin<br />
tulehdusreaktion [5,233,234,235].<br />
<strong>Tulehduskipulääkkeiden</strong> tulehdusta rauhoittavan<br />
vaikutuksen ajatellaan selittyvän pääosin<br />
COX-2-isoentsyymin estolla ja sivuvaikutusten<br />
johtuvan COX-1-isoentsyymin estosta [5,6,7,<br />
233,234,235]. Ilmeisesti näillä on myös muita,<br />
syklo-oksigenaasin estosta riippumattomia vaikutusmekanismeja,<br />
joissa eri tulehduskipulääkkeiden<br />
välillä voi olla merkittäviä eroja [233,<br />
234].<br />
COX-2-selektiivisyys<br />
Lähes kaikki nykyisin käytössä olevat tulehduskipulääkkeet<br />
vähentävät sekä COX-1- että<br />
COX-2-entsyymin aktiivisuutta. Niiden välillä<br />
on eroja siinä, kohdistuuko vaikutus pääosin<br />
COX-1- vai COX-2-entsyymiin vai tasaisesti<br />
molempiin. COX-1- ja COX-2-selektiivisyyttä<br />
kuvataan IC 50<br />
-luvulla, joka tarkoittaa 50-prosenttisesti<br />
entsyymin toimintaa estävää lääkepitoisuutta,<br />
ja COX-2/COX-1-estosuhteella,<br />
joka on lääkeaineen COX-2-entsyymin estolle<br />
laskettu IC 50<br />
-arvo jaettuna saman lääkeaineen<br />
COX-1-entsyymin estolle lasketulla IC 50<br />
-arvolla.<br />
Vaikka COX-2/COX-1-estosuhde ei olekaan<br />
ideaalinen selektiivisyyden mittari [10,11], se on<br />
vakiintunut tapa verrata eri tulehduskipulääkkeiden<br />
vaikutuksia eri COX-isoentsyymeihin.<br />
Eri tutkijoiden raportoimien IC 50<br />
-arvojen ja<br />
COX-2/COX-1-estosuhteiden erot selittynevät<br />
pääosin sillä, että tulokseen vaikuttavat koeasetelmassa<br />
mm. substraatin pitoisuus, inkubaatioaika,<br />
läsnä olevan proteiinin määrä ja se, miten<br />
lääkeaine vaikuttaa entsyymiin [10,12,233,234,<br />
235]. Koeasetelmaa sopivasti muuttamalla saattaa<br />
olla mahdollista jopa manipuloida tulosta<br />
tiettyjä lääkeaineita suosivaksi (D). Kuvaan 1<br />
on kerätty eri tutkimuksissa raportoituja tuloksia<br />
tulehduskipulääkkeiden COX-2/COX-1-estosuhteista<br />
[11–13,137–147](A). Tulosten perusteella<br />
on mahdotonta määrittää tarkasti yksittäisen<br />
lääkeaineen selektiivisyyden astetta, ja hyvin<br />
pienikään COX-2/COX-1-estosuhde ei välttämättä<br />
tarkoita täydellistä COX-2-selektiivisyyttä<br />
(eli COX-1-vaikutuksen täydellistä puuttumista).<br />
Kohtalaisen COX-2-selektiivisiä ovat meloksikaami,<br />
nabumetoni ja nimesulidi, joilla on kuitenkin<br />
kuvattu olevan ihmisen elimistössä estovaikutus<br />
myös COX-1-isoentsyymiin [70,71,<br />
1916<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
239,240,241,242](A). Hiljattain <strong>käyttö</strong>ön saadut<br />
ns. koksibit (rofekoksibi, selekoksibi) on kehitetty<br />
tavoitteena mahdollisimman hyvä estovaikutus<br />
COX-2-isoentsyymiin ja mahdollisimman<br />
vähäinen vaikutus COX-1-isoentsyymiin<br />
(COX-2-selektiivisyys) [11–13]. Lähinnä tavoitetta<br />
on rofekoksibi [236,237](D). Selekoksibi<br />
kyllä vähentää tehokkaasti COX-2-aktiivisuutta<br />
elimistössä, mutta pitoisuuden kasvaessa veressä<br />
lääkeaine vaikuttaa myös COX-1-isoentsyymiin<br />
[69](C).<br />
Selektiiviset COX-2-salpaajat rofekoksibi ja<br />
selekoksibi eivät ole muita tulehduskipulääkkeitä<br />
tehokkaampia tulehduskivun hoidossa [14–<br />
16]. Koska myös COX-1-salpauksella on ilmeisesti<br />
merkitystä tulehdusreaktiossa, selektiiviset<br />
COX-2-estäjät eivät välttämättä ole aivan parhaiden<br />
epäselektiivisten COX-estäjien veroisia teholtaan<br />
kaikissa <strong>käyttö</strong>aiheissa [51,238,243] (A).<br />
<strong>Tulehduskipulääkkeiden</strong><br />
aiheuttama gastropatia<br />
Esiintyminen. Tulehduskipulääkitystä käyttävistä<br />
70–90 %:lle kehittyy etenkin hoidon alkuvaiheessa<br />
akuutteja eroosioita ja muita pinnallisia<br />
limakalvovaurioita mahalaukkuun ja pohjukaissuoleen.<br />
Lääkityksen jatkuessa useamman viikon<br />
vauriot paranevat limakalvon adaptaation<br />
seurauksena osalla potilaista, ja niiden kliininen<br />
merkitys on ilmeisen vähäinen. Kroonistuneita<br />
pinnallisia limakalvoleesioita jää 30–50 %:lle<br />
tulehduskipulääkkeiden pitkäaikaiskäyttäjistä<br />
[17,18].<br />
Noin 25 %:lle tulehduskipulääkkeiden pitkäaikaiskäyttäjistä<br />
kehittyy krooninen maha- tai<br />
pohjukaissuolihaava. Mahahaava, joka useimmiten<br />
sijaitsee antrumissa, on noin kaksi kertaa<br />
yleisempi kuin duodenaaliulkus. Ikä- ja sukupuolivakioituun<br />
normaaliväestöön verrattuna tulehduskipulääkkeiden<br />
pitkäaikaiskäyttäjillä on noin<br />
nelinkertainen riski saada mahahaava ja 2.5-kertainen<br />
pohjukaissuolihaavan vaara [18]. Yli 60-<br />
vuotiailla ulkusriski on jopa kuusinkertainen.<br />
Kaikista ulkustaudin henkeä uhkaavista komplikaatiotapauksista<br />
noin 60 %:a ja ulkustautiin<br />
liittyvistä kuolemantapauksista jopa 80 %:a on<br />
edeltänyt tulehduskipulääkkeiden <strong>käyttö</strong>.<br />
COX-2-selektiivisyys näyttää vähentävän tulehduskipulääkkeen<br />
sivuvaikutuksia mahasuolikanavaan.<br />
Meloksikaamin on kuvattu aiheuttavan<br />
vähemmän näitä sivuvaikutuksia kuin diklofenaakin<br />
tai piroksikaamin [16,148–150](C).<br />
Verrattaessa nimesulidia diklofenaakkiin endoskooppisessa<br />
tutkimuksessa ei havaittu merkitsevää<br />
eroa maha-suolikanavan yläosaan kohdistuvien<br />
sivuvaikutuksien suhteen [19]. Rofekoksibin<br />
[90,93,94](B) ja selekoksibin [14,15,95](B)<br />
aiheuttamat haittavaikutukset maha-suolikanavan<br />
yläosaan ovat kliinisissä tutkimuksissa olleet<br />
vähäisemmät kuin epäselektiivisten COXestäjien<br />
ja ulkusten esiintyminen samanveroista<br />
kuin lumelääkityksen yhteydessä [20,21]. Toisaalta<br />
COX-2-isoentsyymin on raportoitu ekspressoituvan<br />
mahalaukun Helicobacter pylori<br />
-infektioiden yhteydessä, ja COX-2-esto saattaa<br />
hidastaa haavauman parantumista [22].<br />
COX-2-selektiivisyys tai -epäselektiivisyys ei<br />
ole ainoa tulehduskipulääkkeiden sivuvaikutuksia<br />
selittävä tekijä. Esimerkiksi nabumetonin sivuvaikutukset<br />
maha-suolikanavaan ovat vähäisemmät<br />
kuin useiden muiden tulehduskipulääkkeiden,<br />
vaikka nabumetoni ja sen aktiivinen metaboliitti<br />
6-metoksi-2-naftyylietikkahappo eivät<br />
olekaan osoittautuneet erityisen COX-2-selektiiviseksi<br />
[151,152](C).<br />
Patogeneesi. Mahan ja pohjukaissuolen limakalvo<br />
on sopeutunut kestämään hapanta mahanestettä<br />
monipuolisen suojausmekanismin ns.<br />
limakalvoesteen avulla [23]. Akuutti limakalvovaurio<br />
paranee nopeasti suojamekanismien toimiessa<br />
normaalisti [23]. Pysyvä limakalvovaurio<br />
syntyy, kun limakalvoeste pettää ja limakalvon<br />
paranemisprosessi samanaikaisesti estyy.<br />
Tällöin mahahappo ja muut mahanesteen toksiset<br />
komponentit (pepsiini, sappihapot, lysolesitiini,<br />
tulehduskipulääke ym.) pääsevät diffundoitumaan<br />
limakalvon sisään, missä ne aikaansaavat<br />
tulehdusprosessia muistuttavan patogeneettisen<br />
kaskadin [24]. Limakalvossa endogeenisesti<br />
COX-1-välitteisesti syntyvillä prostaglandiineilla<br />
on tärkeä osuus limakalvon suojauksessa.<br />
Prostaglandiinit stimuloivat limakalvon limanja<br />
bikarbonaatineritystä sekä sen hydrofobisen<br />
fosfolipidikerroksen muodostusta vahvistaen limakalvoestettä.<br />
Ne stimuloivat limakalvon ve-<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1917
enkiertoa parantaen sen yleistä hyvinvointia ja<br />
erityisesti sen paranemiskykyä. Limakalvon endogeenisen<br />
prostaglandiinisynteesin esto tulehduskipulääkkeillä<br />
johtaa moniin epäsuotuisiin<br />
vaikutuksiin; se heikentää limakalvon puolustusjärjestelmää<br />
useilla eri tasoilla [25,26]. Lisäksi<br />
tulehduskipulääkkeillä on mahalaukun ja<br />
duodenumin limakalvoon prostaglandiinisynteesistä<br />
riippumaton suora toksinen vaikutus, jonka<br />
voimakkuus riippuu tulehduskipulääkkeestä.<br />
Parhaiten tunnettu ja ilmeisesti myös voimakkain<br />
vaikutus on asetyylisalisyylihapolla.<br />
Limakalvon adaptaatio. Tulehduskipulääkehoidon<br />
pitkittyessä (yli kolme viikkoa) mahalaukun<br />
ja duodenumin akuutit limakalvomuutokset<br />
lievenevät tai paranevat kokonaan osalla<br />
potilaista. Mikäli tämä adaptaatiomekanismi<br />
pettää, muuttuvat akuutit limakalvovauriot<br />
kroonisiksi haavaumiksi. Adaptaation patofysiologiaa<br />
ei tunneta tarkoin, mutta pitkäaikainen<br />
altistus tulehduskipulääkkeelle lisää mahalaukun<br />
ja duodenumin epiteelisolujen DNA-synteesiä<br />
ja mitoottista aktiivisuutta kiihdyttäen solujen<br />
uusiutumista kasvutekijästimulaation vaikutuksesta<br />
[26,27].<br />
Kliininen kuva. Tulehduskipulääkkeet aiheuttavat<br />
etenkin hoidon alkuvaiheessa suurimmalle<br />
osalle potilaista endoskooppisesti todettavia mahalaukun<br />
ja duodenumin pinnallisia limakalvovaurioita,<br />
kuten petekioita, eroosioita tai tihkuvuotoa.<br />
Nämä ovat kuitenkin yleensä oireettomia.<br />
Jonkinasteista verenvuotoa esiintyy lähes<br />
kaikilla, mutta se johtaa vain harvoin kliinisesti<br />
merkittävään anemisoitumiseen. Erilaisia dyspeptisiä<br />
vaivoja esiintyy noin 20 %:lla kaikista<br />
tulehduskipulääkkeiden käyttäjistä, mutta tulehduskipulääkegastropatian<br />
endoskopiassa todetun<br />
vaikeusasteen ja subjektiivisten oireiden (kivun)<br />
tai muiden kliinisten ilmenemismuotojen<br />
välillä ei ole selvää korrelaatiota [28]. Useimmiten<br />
tulehduskipulääkkeen aiheuttama gastropatia<br />
ilmenee kliinisesti vasta muututtuaan<br />
krooniseksi ulkukseksi ja komplisoituessaan ulkusvuotona<br />
tai puhkeamana. Krooninen tulehduskipulääkkeen<br />
aiheuttama ulkus on usein oireeton<br />
tai vähäoireinen. Yli puolella potilaista<br />
komplikaatio esiintyy ilman edeltäviä selviä dyspeptisiä<br />
tai muita ulkustautiin viittaavia vatsaoireita<br />
[29]. Oireettomuutta lukuun ottamatta<br />
tulehduskipulääkeen aiheuttaman ulkuksen kliiniset<br />
ja endoskopialöydökset eivät eroa merkittävästi<br />
Helicobacter pylori -infektioon liittyvästä<br />
ulkuksesta.<br />
Tulehduskipulääkkeen<br />
aiheuttaman ulkuksen hoito<br />
Ulkuspotilaan tulehduskipulääkitys tulee yleensä<br />
aina lopettaa tai korvata pelkällä kipulääkkeellä,<br />
esimerkiksi parasetamolilla. Mikäli lopettaminen<br />
ei ole mahdollista, lääke tulisi mieluiten<br />
vaihtaa COX-2-selektiiviseksi [148,153-<br />
156](D). Ulkus hoidetaan kuten yleensä. Helikobakteeripositiiviselle<br />
annetaan häätöhoito,<br />
jonka jälkeen on tarpeen jatkaa ulkuksen hoitoa<br />
vielä 4–8 viikkoa. Protonipumpun estäjät<br />
ovat jonkin verran tehokkaampia kuin histamiini<br />
2<br />
-salpaajat [30]. Tulehduskipulääkkeen <strong>käyttö</strong><br />
hidastaa ulkuksen parantumista H 2<br />
-salpaajilla<br />
hoidettaessa, mikä on syytä ottaa huomioon<br />
hoidon pituudessa [31]. Omepratsolin tehoa tulehduskipulääke<br />
ei näytä heikentävän [31,<br />
157](B). Misoprostolin teho on heikompi kuin<br />
omepratsolin ulkuksen hoidossa, mutta parempi<br />
eroosiotapauksissa [32]. Haponestolääkkeiden<br />
etuina ovat niiden hyvä siedettävyys ja helppo<br />
<strong>käyttö</strong> verrattuna misoprostoliin.<br />
Taulukko 2. <strong>Tulehduskipulääkkeiden</strong> aiheuttamat suolivauriot.<br />
Ohutsuoli<br />
Tulehduskipulääke-enteropatia<br />
verenvuoto<br />
valkuaisvuoto<br />
Ohusuolen puhkeama<br />
Ohutsuoliperforaatio<br />
Kalvomaiset striktuurat<br />
Paksusuoli<br />
Epäspesifinen koliitti<br />
Eosinofiilinen koliitti<br />
Pseudomembraanoottinen<br />
koliitti<br />
Kollageenikoliitti<br />
Epäspesifiset ulseraatiot<br />
puhkeama, vuoto<br />
Aikaisemman koolonsairauden<br />
komplikaatio<br />
Divertikkeliperforaatio,<br />
-fisteli, -vuoto<br />
Kroonisten tulehduksellisten<br />
suolistosairauksien<br />
aktivoituminen<br />
1918<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
Suolistovauriot<br />
Suolistovaurioiden patogeneesiä on käsitelty artikkeleissa<br />
33-39. Tulehduskipulääkkeet voivat<br />
aiheuttaa vaurioita sekä ohut- että paksusuoleen<br />
[33,38-40](A) (taulukko 2). Jopa kahdella<br />
kolmesta tulehduskipulääkkeen käyttäjistä ilmenee<br />
valkuaisvuotoa ja permeabiliteetin lisääntymistä<br />
sekä valkosolujen lisääntynyttä eritystä<br />
ulosteisiin [158-160](C). Reumapotilaista, joiden<br />
ulosteessa oli piilevää verta, todettiin<br />
47 %:lla enteroskopiassa haavaumia ohutsuolessa<br />
[161,162](C). Pitkään tulehduskipulääkehoitoa<br />
saaneista 8.4 %:lla on todettu obduktiossa<br />
ohutsuolihaavaumia [163](B). Suolen puhkeama<br />
on muista tekijöistä riippumaton tulehduskipulääkehoidon<br />
komplikaatio [164,165](B).<br />
Tulehduskipulääkehoitoa saavilla esiintyy divertikkelivuotoja<br />
ja -puhkeamia [166,167](C).<br />
Ohut- ja paksusuoleen voi kehittyä tulehduskipulääkehoidon<br />
seurauksena kalvomaisia striktuuroita,<br />
joita on vaikea erottaa normaalista<br />
haustraatiosta radiologisessa tutkimuksessa<br />
[168–171](C). Striktuurat, joita voi olla useita<br />
ja jotka saattavat olla pitkiä varsinkin paksusuolessa,<br />
aiheuttavat suolitukoksia ja puhkeamia<br />
[172](C). <strong>Tulehduskipulääkkeiden</strong> <strong>käyttö</strong>ön<br />
liittyvistä koliiteista (pseudomembranoottinen,<br />
kollageeni- ja eosinofiilinen koliitti) on julkaistu<br />
raportteja [173](C). Fulminantin haavaisen paksusuolitulehduksen<br />
tapaan eteneviä kuolemaan<br />
johtaneita tapauksia on kuvattu [174](C). Kyseessä<br />
on voinut olla osassa tapauksista aikaisemmin<br />
diagnosoimaton ulseratiivisen koliitin<br />
pahenemisvaihe, joka kliinisten kokemusten perusteella<br />
voi laueta tulehduskipulääkkeen käytön<br />
seurauksena [175](C).<br />
<strong>Tulehduskipulääkkeiden</strong> aiheuttaman suolivaurion<br />
patogeneesi on epäselvä. Kliinisesti tulehduskipulääkkeiden<br />
aiheuttamat suolivauriot<br />
ilmenevät raudanpuuteanemiana, hypoalbuminemiana,<br />
ripulina, veriulosteina tai rajuina suolistoverenvuotoina<br />
ja puhkeamina [33,38-40](A).<br />
Diagnostiikkaa vaikeuttavat esimerkiksi reumapotilailla<br />
perussairaudesta johtuva anemia ja seerumin<br />
pieni albumiinipitoisuus. Suolivauriot sijaitsevat<br />
usein tavallisen gastroduodenoskoopin<br />
ja kolonoskoopin ulottuvuuden ulkopuolella,<br />
minkä takia niiden diagnostiikassa enteroskooppi<br />
on usein paras väline [40]. Sondityyppisella<br />
enteroskoopilla voidaan tutkia koko ohutsuoli,<br />
ja vaurioita löytyy sen avulla yli 40 %:lta tutkituista<br />
[176](C). Myös työnnettävällä enteroskoopilla,<br />
jolla nähdään noin 2 m ohutsuolen yläosaa,<br />
päästään usein diagnoosiin [177-179](B).<br />
Ohutsuolen läpikulkututkimuksen merkitys<br />
diagnostiikassa on vähäinen [180,181] (C).<br />
Tulehduskipulääkkeistä johtuvia suolivaurioita<br />
voidaan ehkäistä metronidatsolilla ja sulfasalatsiinilla<br />
[182,183](C). Myös misoprostolia<br />
saaneilla anemian on todettu korjaantuvan paremmin<br />
kuin verrokeilla [184](C). Striktuuroita<br />
voidaan laajentaa endoskooppisella toimenpiteellä,<br />
elleivät ne vaadi leikkausta. Tulehduskipulääkkeen<br />
<strong>käyttö</strong>tarve on harkittava tapauskohtaisesti<br />
suolistovaurioiden esiintyessä. COX-<br />
2-selektiivisempien lääkkeiden on todettu aiheuttavan<br />
vähemmän suoliston permeabiliteettihäiriöitä,<br />
ja ne saattavat olla epäselektiivisempiä<br />
turvallisempia [41].<br />
Ruokatorvivauriot<br />
Tulehduskipulääkkeet aiheuttavat ruokatorvivaurioita,<br />
jotka johtuvat joko suoraan korroosiosta<br />
tai refluksitaudin pahenemisesta [185-<br />
188](C). Esofagiittimuutokset ovat tulehduskipulääkkeiden<br />
käyttäjillä vaikeampia kuin muilla,<br />
vaikka toimintahäiriön asteessa ei ole eroa<br />
[42]. Refluksioireiden ilmenemiseen tulehduskipulääkkeiden<br />
käyttäjillä tulisi kiinnittää huomiota<br />
nykyistä enemmän [186,189-192](D).<br />
Munuaishaitat<br />
Munuaisten tuottamilla prostaglandiineilla<br />
(PGE 2<br />
ja PGI 2<br />
), jotka ovat pääasiassa vasodilataattoreita,<br />
on hyvin tärkeitä paikallisvaikutuksia<br />
mm. kiertävän veritilavuuden vähentymisen<br />
laukaisemassa verisuonten supistumisessa [43]<br />
(taulukko 3). Useimmat tulehduskipulääkkeet<br />
asetyylisalisyylihappo mukaan luettuna estävät<br />
sekä COX-1- että COX-2-entsyymejä ja siten<br />
munuaisten paikallista prostaglandiinisynteesiä.<br />
<strong>Tulehduskipulääkkeiden</strong> munuaisiin kohdistuvat<br />
haittavaikutukset on lueteltu taulukossa 3.<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1919
Tavallisin tulehduskipulääkkeiden aiheuttama<br />
haittavaikutus munuaisissa on akuutti vajaatoiminta.<br />
Se voi ilmetä nopeasti lääkityksen aloittamisen<br />
jälkeen mutta korjaantuu yleensä, kun<br />
lääkkeen <strong>käyttö</strong> lopetetaan. Tärkeintä on tunnistaa<br />
mahdollinen syy ajoissa. Riskitekijöitä tulehduskipulääkkeiden<br />
aiheuttaman munuaisten<br />
akuutin vajaatoiminnan kehittymiselle on lueteltu<br />
taulukossa 4.<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>käyttö</strong> lisää munuaisten<br />
akuutin vajaatoiminnan riskin noin nelinkertaiseksi<br />
[193](C). Riski on suurin ensimmäisen<br />
<strong>käyttö</strong>kuukauden aikana, suuria annoksia<br />
käytettäessä etenkin monisairailla vanhuksilla.<br />
Kaikki tulehduskipulääkkeet voivat aiheuttaa<br />
munuaisten vajaatoimintaa, mutta erityisesti<br />
aiemmin käytössä olleet yhdistelmävalmisteet<br />
ovat olleet sellaisia [44-46]. Pelkästään asetyylisalisyylihappo<br />
ei aiheuta vaurioita munuaisten<br />
toiminnan ollessa normaali, eikä pieniannoksisesta<br />
tromboosiprofylaksista ole munuaisille<br />
haittaa [46]. Kipulääkenefropatia, joka tunnetaan<br />
parhaiten fenasetiiniyhdistelmävalmisteiden<br />
käyttäjillä, on yleisesti tunnettu. Vaikka fenasetiinin<br />
myynti on lopetettu useissa maissa, munuaisten<br />
krooniseen vajaatoimintaan johtavaa<br />
sairautta esiintyy edelleen kipulääkkeitä vuosikausia<br />
päivittäin käyttäneillä [47]. <strong>Tulehduskipulääkkeiden</strong><br />
pahentava vaikutus munuaisen<br />
krooniseen vajaatoimintaan on epäselvä [45–<br />
47]. Akuutti interstitiaalinen nefriitti ja siihen<br />
toisinaan liittyvä glomerulusvauriosta johtuva<br />
nefroottinen oireyhtymä ovat harvinaisia [48].<br />
Tila on yleensä korjaantuva. Veden ja natriumin<br />
eritys voi heiketä tulehduskipulääkkeiden käytön<br />
seurauksena, mikä johtaa turvotuksiin, hyponatremiaan<br />
ja hyperkalemiaan (taulukko 5).<br />
Diureettien teho voi heiketä [45]. Huomion arvoista<br />
on myös tulehduskipulääkkeiden verenpainetta<br />
kohottava vaikutus, joka saattaa näkyä<br />
mm. verenpainelääkityksen tehon heikkenemisenä<br />
[194,195](A).<br />
COX-2-selektiivisyys. Vaikka COX-1-isoentsyymiä<br />
pidetään fysiologisten prostaglandiinien<br />
merkittävänä tuottajana, COX-2-isoentsyymi ja<br />
sen tuottamat prostanoidit näyttävät osallistuvan<br />
munuaisten verenkierron säätelyyn ainakin<br />
elimistön stressitilanteissa. COX-2-geenin poistaminen<br />
hiiriltä johtaa vakavan nefropatian kehittymiseen<br />
[49,50], mutta COX-1-poistogeenisten<br />
hiirten munuaiset ovat morfologisesti ja toiminnallisesti<br />
lähes normaalit [51]. Selektiivisilläkin<br />
COX-2-estäjillä on kuvattu olevan vaikutuksia<br />
munuaisten toimintaan erityistilanteissa,<br />
ja on mahdollista, että munuaisiin kohdistuvien<br />
sivuvaikutusten suhteen ne eivät ole epäselektiivisiä<br />
COX-estäjiä turvallisempia [196,197](C).<br />
Käytettäessä tulehduskipulääkkeitä – myös<br />
COX-2-selektiivisiä salpaajia – yhdessä ACE:n<br />
estäjien kanssa tulehduskipulääkkeet voivat<br />
huonontaa ACE:n estäjän verenpainetta alentavaa<br />
vaikutusta. Kliiniset kokemukset uusien<br />
COX-2-selektiivisten salpaajien turvallisuudesta<br />
munuaisten kannalta puuttuvat [52,53].<br />
Maksaan kohdistuvat haittavaikutukset<br />
<strong>Tulehduskipulääkkeiden</strong> aiheuttamista maksavaurioista<br />
on julkaistu useita raportteja<br />
[54,57](A). Vaikka maksahaitat ovat harvinai-<br />
Taulukko 3. <strong>Tulehduskipulääkkeiden</strong> haittavaikutukset munuaisiin.<br />
Munuaisten akuutti hemodynaaminen eli toiminnallinen<br />
vajaatoiminta<br />
Munuaisten erityshäiriö<br />
vesi<br />
natrium<br />
kalium<br />
Akuutti interstitiaalinen nefriitti<br />
Nefroottinen oireyhtymä<br />
Vaikutukset muuhun lääkehoitoon<br />
verenpainelääkeet<br />
diureetit<br />
Krooninen munuaistauti, kipulääkenefropatia<br />
Taulukko 4. Riskitekijöitä tulehduskipulääkkeiden aiheuttaman<br />
munuaisten akuutin toiminnallisen vajaatoiminnan kehittymiselle.<br />
Kiertävän veritilavuuden vajaus<br />
Sydämen vajaatoiminta<br />
Maksakirroosi<br />
Nefroottinen oireyhtymä<br />
Infektiot<br />
Muu lääkehoito (diureetit, aminoglykosidit, syklosporiini A)<br />
Diabetes mellitus<br />
Ateroskleroosi<br />
Korkeä ikä<br />
Anestesia<br />
Munuaissairaus<br />
1920<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
Taulukko 5. Prostaglandiinien vaikutukset munuaisiin sekä vastaavat tulehduskipulääkkeiden käytön mahdolliset haitat.<br />
Prostaglandiinin vaikutus<br />
Munuaisen verenkierron ja glomerulusten<br />
suodattumisnopeden ylläpito vasokonstriktion aikana<br />
Systeemisen vasokonstriktion esto<br />
Reniinin erityksen väheneminen<br />
Antidiureettisen hormonin vastavaikutus<br />
Natriumin erityksen lisääntyminen veritilavuuden vajauksessa<br />
Lääkehaitta<br />
Munuaisten akuutti vajaatoiminta<br />
Verenpaineen nousu<br />
Hyperkalemian mahdollisuus<br />
Voimistaa antidiureettisen hormonin vaikutusta<br />
Natriumin retentio<br />
sia verrattuna muihin tulehduskipulääkkeiden<br />
sivuvaikutuksiin, näistä lääkkeistä johtuvat<br />
maksavauriot muodostavat kuitenkin käytön<br />
laajuuden takia huomattavan osan kaikista lääkeperäisistä<br />
maksavaurioista. Parasetamolimyrkytystä,<br />
joka hoitamattomana johtaa fataaliin<br />
maksanekroosiin, ei käsitellä tässä. <strong>Tulehduskipulääkkeiden</strong><br />
aiheuttama maksavaurion riski on<br />
vähäinen (OR 1.2–1.7). Maha-suolikanavan<br />
vuodon osalta vastaava riskiluku on 4.7 [54].<br />
Sairaalaan joutumisen riski akuutin maksavaurion<br />
vuoksi on pieni (OR 1.2) [198](C). Tanskalaisessa<br />
selvityksessä todettiin tulehduskipulääkkeiden<br />
aiheuttavan noin 9 % kaikista lääkeperäisistä<br />
maksavaurioista [199](C). Akuutin<br />
maksavaurion ilmaantuvuus oli 3.7 sataatuhatta<br />
avohoidossa tulehduskipulääkkeitä käyttänyttä<br />
kohti ja 1.1/100 000 lääkemääräystä, eikä<br />
yksikään tapaus johtanut kuolemaan [55,56].<br />
Nivelreumaa sairastavilla todettiin kymmenkertainen<br />
akuutin maksavaurion vaara verrattuna<br />
nivelrikkopotilaisiin [200](B). Tärkeää on huomata,<br />
että maksaentsyymiarvojen kasvun taustalla<br />
voi olla tulehduskipulääke [58](C).<br />
Mikä tahansa tulehduskipulääke voi aiheuttaa<br />
maksa-arvojen suurenemisen. Muutos on<br />
useimmiten lievä ja korjaantuu normaaliksi hoidon<br />
loputtua [54,57]. Eniten on raportoitu diklofenaakin<br />
ja sulindaakin <strong>käyttö</strong>ön liittyvistä<br />
maksamuutoksista [59-62,201](B). Myös asetyylisalisyylihapon<br />
<strong>käyttö</strong>ön on kuvattu liittyneen<br />
maksavauriota [63](C). <strong>Tulehduskipulääkkeiden</strong><br />
aiheuttama maksavaurio voi olla joko<br />
kolestaattinen, hepatosellulaarinen tai sekamuotoinen<br />
[57-60]. Joskus vaurio on kroonisen hepatiitin<br />
kaltainen [61]. Kolestaattisessa vauriossa<br />
alkalisen fosfataasin aktiivisuus lisääntyy ja<br />
voi kehittyä ikterus, kun taas hepatosellulaarisessa<br />
vauriossa ensisijaisesti aminotransferaasiarvot<br />
suurenevat. Asetyylisalisyylihapon ja ibuprofeenin<br />
aiheuttamat vauriot ovat useimmiten<br />
hepatosellulaarisia ja diklofenaakin, sulindaakin,<br />
piroksikaamin ja naprokseenin <strong>käyttö</strong>ön<br />
liittyvät sekamuotoisia [57,59,60,62,63].<br />
Tulehduskipulääkkeen aiheuttamien maksavaurioiden<br />
patogeneesi tunnetaan huonosti. Lääkeaine<br />
tai sen metaboliitti voi vaurioittaa suoraan<br />
maksasolukkoa [202](B). Reaktio on ennalta<br />
arvaamaton ja annoksesta riippumaton ja<br />
saattaa ilmetä milloin tahansa hoidon aikana.<br />
Koska tulehduskipulääkkeiden aiheuttamat<br />
maksahaitat ovat harvinaisia, jokaisen käyttäjän<br />
maksa-arvojen seuranta ei ole mielekästä (D).<br />
Muut haittavaikutukset<br />
Keuhkoputkien supistuminen. Tulehduskipulääkkeet<br />
aiheuttavat noin 10 %:lle astmaatikoista<br />
eriasteisen keuhkoputkien supistumisen. Kyseessä<br />
ei ole yliherkkyysreaktio johonkin tiettyyn<br />
kipulääkkeeseen vaan vakava, jopa henkeä<br />
uhkaava tulehduskipulääkeryhmään liittyvä sivuvaikutus<br />
[5,64,65]. Yleensä jostakin tulehduskipulääkkeestä<br />
tämän reaktion saanut potilas<br />
saa vastaavan reaktion myös muista, kemiallisesti<br />
täysin erilaisistakin tulehduskipulääkkeistä.<br />
Reaktion syntymekanismia ei tunneta, mutta<br />
ilmeisesti keuhkoputkia supistavat kysteinyylileukotrieenit<br />
välittävät reaktiota. Herkillä astmaatikoilla<br />
tulehduskipulääkkeen estäessä prostanoidisynteesin<br />
osa esiasteesta arakidonihaposta<br />
metaboloituu 5-lipoksigenaasientsyymin vaikutuksesta<br />
keuhkoputkia supistaviksi kysteinyylileukotrieeneiksi<br />
[64,65]. Alustavien tulosten<br />
perusteella osa särkylääkkeille herkistä potilaista<br />
sietää nimesulidia tai meloksikaamia [66-68].<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1921
Koska kyseessä on vakava, jopa henkeä uhkaava<br />
ja usein vaikeasti hoidettava haittavaikutus,<br />
ei näitäkään tulehduskipulääkkeitä tai selektiivisiä<br />
COX-2-estäjiä pidä määrätä potilaille ilman<br />
valvotuissa olosuhteissa tehtyä altistuskoetta.<br />
Toistaiseksi useimmille potilaille <strong>turvallinen</strong><br />
vaihtoehto on parasetamoli, jonka sopivuus on<br />
syytä testata lääkärin vastaanotolla, ei kotona.<br />
Tulehduskipulääkkeet voivat satunnaisesti aiheuttaa<br />
myös muita yliherkkyysreaktioita, kuten<br />
urtikariaa ja muita ihoreaktioita, angioödeemaa<br />
tai jopa anafylaktisen sokin. Myös eosinofiilisia<br />
keuhkoreaktioita on kuvattu. Vakavan<br />
yliherkkyysreaktion saaneen on syytä varoa<br />
kaikkia tulehduskipulääkkeitä. Useimmat sietävät<br />
kuitenkin parasetamolia [5].<br />
Veren hyytyminen. Tulehduskipulääkkeet estävät<br />
verihiutaleiden aggregaatiota ja pidentävät<br />
vuotoaikaa. Erityisesti asetyylisalisyylihapon<br />
osalta tätä ominaisuutta käytetään hyödyksi sydän-<br />
ja verisuonisairauksien hoidossa ja ehkäisyssä.<br />
Lääkkeen COX-2-selektiivisyys näyttää<br />
odotetusti vähentävän vaikutusta verihiutaleiden<br />
aggregaatioon ja vuotoaikaan, sillä meloksikaamin<br />
ja koksibien on raportoitu vaikuttavan niihin<br />
vain vähän tai ei lainkaan (ks. myös kohta<br />
interaktiot) [69–71].<br />
Muut haittavaikutukset. Tulehduskipulääkkeet<br />
voivat hidastaa synnytyksen käynnistymistä<br />
ja pidentää synnytystä ilmeisesti vähentämällä<br />
kohdun supistelua voimistavien prostaglandiinien<br />
synteesiä. Ne ovat aiheuttaneet koe-eläimille<br />
valtimotiehyen ennenaikaisen sulkeutumisen<br />
jo kohdussa. Ihmisen osalta tästä ei ole varmaa<br />
näyttöä [5]. Hiirillä COX-2 on merkittävästi<br />
mukana mm. ovulaation ja hedelmöittymisen<br />
säätelyssä [72]. Selektiivisen COX-2-salpauksen<br />
mahdollisista haitoista hedelmällisyyteen<br />
ei ole tutkimustietoa.<br />
Interaktiot. Metotreksaatti ja litium erittyvät<br />
pääosin munuaisten kautta. Tulehduskipulääkkeet<br />
voivat vähentää glomerulusfiltraatiota erityisesti<br />
munuaissairauden tai esimerkiksi kiertävän<br />
veritilavuuden vajauksen yhteydessä. Tällöin<br />
tulehduskipulääkkeen <strong>käyttö</strong> yhdessä metotreksaatin<br />
tai litiumin kanssa voi johtaa metotreksaatin<br />
tai litiumin pitoisuuden kasvuun ja<br />
niiden toksisuuden lisääntymiseen. Neljällätoista<br />
nivelreumaa sairastavalla naisella tehdyssä<br />
seitsemän päivää kestäneessä tutkimuksessa selekoksibi<br />
(200 mg/vrk) ei vaikuttanut metotreksaatin<br />
kinetiikkaan [73]. Laajemman tutkimustiedon<br />
puuttuessa on COX-2-selektiivisiin estäjiin<br />
kuitenkin syytä suhtautua litiumin tai metotreksaatin<br />
käytön yhteydessä kuten epäselektiivisiin<br />
COX-estäjiin (D).<br />
Tulehduskipulääkkeet, myös uudet COX-2-<br />
selektiiviset estäjät, sitoutuvat plasman proteiineihin<br />
85–99.9-prosenttisesti [74]. Niinpä on<br />
olemassa ainakin teoreettinen mahdollisuus, että<br />
ne syrjäyttävät muita proteiineihin sitoutuvia<br />
lääkeaineita, esimerkkeinä oraaliset antikoagulantit<br />
ja sulfonamidit (oraaliset diabeteslääkkeet),<br />
jolloin näiden lääkkeiden vaikutukset voimistuvat.<br />
Tulehduskipulääkkeen<br />
käytön periaatteet ja valinta<br />
<strong>Tulehduskipulääkkeiden</strong> käytön tärkeimmät aiheet<br />
ovat tuki- ja liikuntaelinsairaudet, vammat<br />
ja kuukautiskivut. Varsinkin käsikaupassa myytäviä<br />
tulehduskipulääkkeitä käytetään yleisesti<br />
myös erilaisten särkyjen, migreenin, akuuttien infektioiden<br />
aiheuttamien oireiden ja kuumeen hoidossa.<br />
Viralliset <strong>käyttö</strong>aiheet ovat useimmilla<br />
lääkkeillä laajat ja lähes samanlaiset. Viime aikoina<br />
indikaatiot ovat olleet joskus rajatummat,<br />
esimerkiksi meloksikaamia ja rofekoksibia käytetään<br />
vain nivelrikkoon. Tämä johtuu siitä, ettei<br />
riittävästä tehosta ja muista <strong>käyttö</strong>ominaisuuksista<br />
ole tarvittavia kokemuksia muiden aiheiden<br />
osalta. Lääkitystä harkittaessa on ensisijaista<br />
miettiä, onko kivun hoidoksi määrättävä kokonaan<br />
muuta kuin tulehduskipulääkettä. Tulehduksellisessa<br />
reumataudissa, vamman aiheuttamassa<br />
kivussa tai akuutissa selkävaivassa tulehduskipulääke<br />
on useimmiten järkevin lääkitys,<br />
mutta esimerkiksi nivelrikon aiheuttamissa vaivoissa<br />
parasetamoli tai sentraalisesti vaikuttava<br />
kipulääke voi olla tehokkaampi ja turvallisempi<br />
vaihtoehto. Kroonisissa selkävaivoissa lukuun ottamatta<br />
selkärankareumaa ei tulehduskipulääkettä<br />
kannata juuri koskaan käyttää [75-79].<br />
Tulehduskipulääkkeen suositeltavin antotapa<br />
on suun kautta. Tavallinen nopeasti imeytyvä<br />
1922<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
tabletti tai kapseli voi olla hitaasti imeytyviä<br />
turvallisempi [80]. Poikkeuksena on ainakin asetyylisalisyylihappo,<br />
joka suolistosta imeytyvänä<br />
valmisteena vähentää mahalaukun paikallista<br />
ärsytystä, ulseraatioita ja ulosteeseen tihkuvaa<br />
verenvuotoa [203–205](B). Antasidilla puskurointi<br />
ei vähennä asetyylisalisyylihapon aiheuttamaa<br />
ulkusvuotojen vaaraa [81]. Myös pieniin<br />
tromboosiprofylaksiassa käytettyihin asetyylisalisyylihappoannoksiin<br />
liittyy lievä ulkusriski<br />
[206](C).<br />
Kaikkien tulehduskipulääkkeiden annoksen<br />
lisääminen suurentaa selvästi riskejä. Erot lääkkeiden<br />
välillä johtuvat osaksi siitä, että joitakin<br />
on totuttu käyttämään pienempinä annoksina<br />
kuin muita [82,83]. Ruiskeina tai peräpuikkoina<br />
annettuina tulehduskipulääkkeet eivät ole<br />
turvallisempia kuin oraalisessa käytössä, mutta<br />
iholta imeytyviin valmisteisiin liittyy harvoin<br />
haittavaikutuksia [84,85]. Tulehduskipulääkeiden<br />
välillä on osoitettu olevan eroja niiden aiheuttamissa<br />
vakavien sivuvaikutusten riskeissä.<br />
Vertailu tulee kuitenkin helposti epätarkaksi, sillä<br />
lääkkeitä ei käytetä teholtaan toisiaan vastaavina<br />
annoksina. Epäselektiivisistä ibuprofeeni<br />
ja diklofenaakki näyttävät verraten turvallisilta<br />
suolikanavan vuotojen suhteen, piroksikaami<br />
taas vaarallisimmalta [207,208](A). Munuaisten<br />
ja verenpainetaudin osalta lääkkeiden<br />
erot ovat vähäisiä [86–88]. Diklofenaakki aiheuttaa<br />
maksan toiminnan häiriöitä muita useammin<br />
[57,54](A). Jos potilaalla on mainittuja<br />
riskejä, lääkkeen valinnassa on otettava nämä<br />
seikat huomioon. Muutaman viime vuoden aikana<br />
Suomessa on tullut <strong>käyttö</strong>ön ns. kohtalaisen<br />
selektiivisesti COX-2-entsyymiä estäviä tulehduskipulääkkeitä<br />
(meloksikaami, nabumetoni,<br />
nimesulidi). Selektiivisyys riippuu annoksesta.<br />
Epidemiologista näyttöä eduista – etenkin<br />
mahasuolikanavan vaurioiden vähentymisen<br />
suhteen – on saatu joissakin tutkimuksissa<br />
[148,153-156](A).<br />
Ensimmäiset selektiivisesti COX-2-entsyymiä<br />
estävät tulehduskipulääkkeet selekoksibi ja rofekoksibi<br />
on rekisteröity Suomessa [89]. Epidemiologista<br />
näyttöä uusimpien lääkkeiden eduista<br />
ei toistaiseksi ole. Gastroskopiatutkimuksissa<br />
havaittu koksibien mahalaukun ulseraatioita aiheuttava<br />
vaikutus ei ole eronnut lumelääkkeen<br />
vaikutuksesta, ei myöskään vaikutus veren hyytymiseen<br />
[90-92]. Seurantatutkimusten mukaan<br />
maha-suolikanavan vuotoja ym. vakavia sivuvaikutuksia<br />
liittyy rofekoksibiin [90,93,94](B) ja<br />
selekoksibiin [14,15,95](B) vähemmän kuin tavanomaisiin<br />
valmisteisiin [14,15,93-95]. Turvotustaipumusta<br />
uudet lääkkeet näyttävän aiheuttavan<br />
yhtä paljon kuin aiemmin käytössä olleet<br />
tulehduskipulääkkeet. Vaikka näyttää siltä, että<br />
koksibit ovat maha-suolikanavaan kohdistuvien<br />
haittavaikutusten suhteen turvallisempia kuin<br />
muut tulehduskipulääkkeet, niiden lopullinen<br />
asema selviää vasta laajemman kliinisen kokemuksen<br />
myötä samoin kuin niiden tehokkuus ja<br />
mahdolliset muihin elimiin (mm. munuaisiin)<br />
kohdistuvat haittavaikutukset [20,22].<br />
Ennen tulehduskipulääkkeen määräämistä on<br />
maha-suolikanavaan kohdistuvat riskit aina arvioitava<br />
jäljempänä esitettyjen periaatteiden mukaisesti.<br />
Myös lääkeaineinteraktioiden mahdollisuus<br />
(esim. antikoagulantit, verenpainelääkkeet)<br />
on otettava huomioon. Munuaisten vajaatoiminta,<br />
sydän- ja verisuonitaudit ja taipumus<br />
astmakohtauksiin ovat myös riskitekijöitä. Potilaalle<br />
annettu tieto haittavaikutusten mahdollisuudesta<br />
ja niiden oireista on tärkeää. Ohjauksella<br />
voidaan myös vähentää tarpeetonta <strong>käyttö</strong>ä<br />
sekä vähentää sivuvaikutusten esiintymistä<br />
[96]. Potilasta on kehotettava ottamaan yhteyttä<br />
lääkäriin vakavaan sivuvaikutukseen viittaavien<br />
oireiden ilmetessä. Ulkuskomplikaatioita<br />
saaneet ovat olleet muita tietämättömämpiä riskeistä<br />
ja oireiden merkityksestä [97,98]. Tulehduskipulääkkeen<br />
määräämisessä voidaan edetä<br />
taulukon 6 mukaisesti.<br />
Tulehduskipulääkkeen<br />
aiheuttaman ulkuksen ehkäisy<br />
Tulehduskipulääkeperäisen ulkuksen riskitekijät<br />
on lueteltu taulukossa 7. <strong>Tulehduskipulääkkeiden</strong><br />
<strong>käyttö</strong> lisää ulkusriskin 3–5-kertaiseksi<br />
iän mukaan. Etenkin ulkuksesta johtuvia komplikaatiota<br />
esiintyy yli 65-vuotiailla [82,105,209]<br />
(A). Aikaisempi ulkusvuoto lisää suhteellisen riskin<br />
saada tulehduskipulääkehoidon aikana uusi<br />
vuoto 13-kertaiseksi [99]. Muuten se on yli 60-<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1923
Taulukko 6. Tulehduskipulääkkeen määräämisen periaatteet.<br />
Harkitse vaihtoehtoista kipulääkitystä (parasetamoli, kodeiini,<br />
tramadoli, paikallishoidot). Arvioi riskit erityisesti mahasuolikanavan<br />
suhteen.<br />
Selvitä muiden vaaratekijöiden ja lääkeaineinteraktioiden<br />
mahdollisuus.<br />
Valitse valmiste, jonka vaikutus sopii ajallisesti ja määrällisesti<br />
potilaan oireisiin. Pitkävaikutteiset sopivat lääkekuureihin,<br />
mutta jatkuvassa käytössä lyhytvaikutteisemmilla voidaan<br />
päästä tarkempiin ja turvallisempiin annoksiin.<br />
Jos maha-suolikanavaan kohdistuvat riskit ovat merkittävät,<br />
valitse COX-2-selektiivinen tulehduskipulääke tai käytä<br />
ulkusprofylaksia, jolloin käytännöllinen vaihtoehto voi olla<br />
diklofenaakkia ja misoprostolia sisältävä yhdistelmävalmiste.<br />
Mieti, ovatko lisääntyneet kustannukset ja parantunut<br />
turvallisuus oikeassa suhteessa.<br />
Huolehdi, että potilas saa tietoa sivuvaikutuksista ja niiden<br />
edellyttämistä toimenpiteistä.<br />
Taulukko 7. Tulehduskipulääkeulkuksen riskitekijät.<br />
Ikä yli 65 vuotta<br />
Aikaisemmin sairastettu ulkus<br />
Glukokortikoidihoito<br />
Usemman kuin yhden tulehduskipulääkkeen samanaikainen<br />
<strong>käyttö</strong><br />
Suuri päivittäinen tulehduskipulääkeannos<br />
Yleiskuntoa heikentävät sairaudet<br />
vuotiaalla 4.5-kertainen [100]. Ulkuskomplikaatioiden<br />
takia sairaalahoitoon joutuneista noin<br />
kolmannes on käyttänyt tulehduskipulääkkeitä<br />
ennen komplikaation ilmaantumista [101]. Tulehduskipulääke<br />
aiheuttaa enemmän maha- kuin<br />
duodenaaliulkuksen komplikaatioita [102]. <strong>Tulehduskipulääkkeiden</strong><br />
käytön aiheuttamat sairaanhoitokustannukset<br />
ikääntyneillä ovat merkittäviä<br />
[103]. Kortisonihoito yksinään ei lisää<br />
ulkusriskiä mutta yhdessä tulehduskipulääkkeen<br />
kanssa ulkusvaara kasvaa noin 4–5-kertaiseksi,<br />
komplikaatioriski kymmenkertaiseksi ja komplikaatioon<br />
liittyvän kuoleman riski jopa 20-kertaiseksi<br />
verrattuna näitä lääkkeitä käyttämättömiin<br />
[210–212](B). Useamman kuin yhden tulehduskipulääkkeen<br />
samoin kuin suurien annosten<br />
<strong>käyttö</strong> lisäävät ulkusriskiä ja komplikaatioita<br />
[82,100,104]. Ulkusriski näyttää olevan<br />
useimpien tutkimusten mukaan suurin tulehduskipulääkehoidon<br />
alkaessa [82,105,106]. Antikoagulanttihoito<br />
lisää ulkusvuotoriskiä [99].<br />
Uusista depressiolääkkeistä, joiden vaikutus perustuu<br />
serotoniinin takaisinoton estoon, on hiljattain<br />
raportoitu aiheutuvan lisääntynyt ruoansulatuskanavan<br />
yläosan vuodon riski varsinkin<br />
käytettäessä yhdessä tulehduskipulääkkeen<br />
kanssa [107].<br />
Helikobakteerin ja tulehduskipulääkkeen yhteisvaikutus<br />
ulkuksen riskitekijänä. Helikobakteeripositiivisella<br />
tulehduskipulääkkeen käyttäjällä<br />
on useammin dyspepsia kuin helikobakteerinegatiivisella<br />
[211,213](C). Käsitykset helikobakteerin<br />
vaikutuksesta tulehduskipulääkehoidon<br />
aikana ilmeneviin ulkuksiin ja komplikaatioihin<br />
ovat ristiriitaisia [108,214-217](C). Tutkimuksia<br />
helikobakteerin häädön vaikutuksesta<br />
tulehduskipulääkevaurioiden esiintymiseen on<br />
niukasti, ja niiden tulokset ovat vaihtelevia, ilmeisesti<br />
ainakin osaksi potilasaineistojen erilaisuuden<br />
takia [109,218,219](C). Tulehduskipulääkettä<br />
käyttävien ulkuspotilaiden haavan on<br />
todettu parantuvan omepratsolihoidossa helikobakteeripositiivisilla<br />
jopa nopeammin kuin -negatiivisilla<br />
[32,108,109]. Helikobakteerin ja tulehduskipulääkkeen<br />
katsotaan olevan kaksi toisistaan<br />
riippumatonta ulkuksen etiologista tekijää<br />
[220](D). Mikäli ulkuspotilaalla todetaan<br />
helikobakteeripositiivinen gastriitti, suositellaan<br />
häätöhoitoa, mutta perusteita kaikkien tulehduskipulääkkeitä<br />
käyttävien helikobakteeritestaukseen<br />
ei ole [221](D).<br />
Tulehduskipulääkeulkuksen riskin arviointi.<br />
Tulehduskipulääkityksen aikana ilmenee endoskooppisia<br />
ulkuksia 20–30 %:lla [110]. Ulkuskomplikaatioita,<br />
kuten vuotoja tai puhkeamia,<br />
saa 2–4 % ulkuspotilaista [111]. Niistä 15–<br />
35 % johtuu tulehduskipulääkkeiden käytöstä<br />
[112]. Ulkusvuoto on tavallisin sairaalahoidon<br />
syy [99,100]. Ulkustaudin takia sairaalahoitoon<br />
joutuvat yleensä ikääntyneet henkilöt, joilla raju<br />
vuoto voi aiheuttaa hemodynamiikan pettämisen<br />
ja iskeemisen sydänsairauden pahentumisen<br />
ja niiden seurauksena sydäninfarktin tai sydämen<br />
vajaatoiminnan [101–103]. Laajan reumapotilailla<br />
tehdyn riskikartoituksen mukaan potilaan<br />
iän, anamneesin, yleiskunnon ja muun lääkityksen<br />
perustella voidaan arvioida tulehduskipulääkehoidon<br />
aloittamisesta johtuvaa ulkuksen<br />
komplisoitumisriskiä [222](C) (taulukko 8).<br />
Tulehduskipulääkeulkuksen ehkäisy. Ehkäisytutkimuksia<br />
on tehty useista ulkuslääkkeistä<br />
1924<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
Taulukko 8. Tulehduskipulääkkeen aiheuttaman ulkuksen komplisoitumisriskin arviointi.<br />
Kerroin<br />
Tekijä<br />
0.3 Jokaisesta viidestä ikävuodesta 50. ikävuoden jälkeen<br />
1.2 Glukokortikoidihoito<br />
1.4 Aikaisempi tulehduskipulääkkeen aiheuttama gastrointestinaalinen haittavaikutus<br />
0.5 Merkittävä raihnaisuus<br />
Pisteet yhteensä = riski joutua ulkustaudin takia sairaalahoitoon seuraavan vuoden aikana (%). Esimerkki: 69-vuotias kortisoni- ja<br />
tulehduskipulääkitystä saava potilas, jolla on aikaisemmin ollut ulkusvuoto, saa pisteitä 0.3 x 3 + 1.2 + 1.4 = 3.5. Riski joutua<br />
sairaalahoitoon vuoden kuluessa ulkustaudin takia on 3.5 %.<br />
Taulukko 9. Tulehduskipulääkkeen aiheuttaman ulkuksen ehkäisyyn käytettäviä lääkkeitä.<br />
Lääke Ehkäisyteho Annos Haittavaikutukset<br />
VU DU<br />
Misoprostoli ++ ++ 200 µg x 2-3 Ripuli, vatsakipu<br />
Ranitidiini - ++ 150 mg x 2 Ei merkittäviä<br />
Famotidiini + ++ 20 mg x 2 Ei merkittäviä<br />
40 mg x 2<br />
Omepratsoli ++ ++ 20 mg x 1 Ei merkittäviä<br />
Pantopratsoli ++ ++ 40 mg x 1 Ei merkittäviä<br />
Lansopratsoli ++ ++ 30 mg x 1 Ei merkittäviä<br />
VU = mahahaava, DU = pohjukaissuolihaava<br />
++ = suuri teho, + = pieni teho, - = ei tehoa<br />
(taulukko 9). Synteettinen prostaglandiini E 1<br />
-<br />
analogi misoprostoli ehkäisee tehokkaasti sekä<br />
mahalaukun että pohjukaissuolen vaurioita tulehduskipulääkkeiden<br />
käyttäjillä [223-226](A).<br />
H 2<br />
-reseptorisalpaajilla voidaan estää hyvin duodenaaliulkukset,<br />
mutta ventrikkeliulkusten ehkäisyyn<br />
tarvitaan usein ulkuksen tavanomaista<br />
hoitoa suuremmat annokset [113–116]. Protonipumpun<br />
estäjien tehokkuus ulkuksen ehkäisyssä<br />
on osoitettu useissa tutkimuksissa [227,<br />
228](A); ks myös [117–121].<br />
Ulkuksen ehkäisyä harkittaessa on otettava<br />
huomioon profylaksin käytännöllisyys, taloudellisuus<br />
ja sen mahdolliset haittavaikutukset, jotka<br />
varsinkin oireettomilla potilailla ovat erityisen<br />
tärkeä hoitomyöntyvyyteen vaikuttava tekijä.<br />
Riittämätön ulkusprofylaksi antasideilla tai<br />
H 2<br />
-salpaajilla saattaa lisätä vakavia ulkuskomplikaatioita<br />
ilmeisesti varoittavien oireiden<br />
puuttumisen takia [122]. Misoprostolilla voidaan<br />
ehkäistä ventrikkeliulkuksia sekä lyhytettä<br />
pitkäaikaisen tulehduskipulääkityksen aikana<br />
merkitsevästi paremmin kuin H 2<br />
-reseptorisalpaajilla<br />
[229](A). Sekä misoprostoli että H 2<br />
-<br />
salpaajat ovat tehokkaita duodenaaliulkuksen<br />
ehkäisyssä niin lyhyt- kuin pitkäaikaisen tulehduskipulääkityksen<br />
aikana [229](A). Omepratsoli<br />
estää tulehduskipulääkkeen aiheuttamien<br />
merkittävien vaurioiden ja etenkin ulkuksien kehittymistä<br />
merkitsevästi paremmin kuin misoprostoli<br />
[32](B). Haittavaikutukset ovat misoprostolihoidon<br />
aikana yleisempiä kuin omepratsolilääkityksen<br />
yhteydessä. Omepratsoli estää<br />
myös ranitidiinia tehokkaammin ulkusrelapseja<br />
tulehduskipulääkeiden käytön aikana [30](B).<br />
Muista protonipumpun estäjistä ei ole julkaistu<br />
yhtä laajoja tutkimuksia. Sukralfaatti on osoittautunut<br />
misoprostolia heikommaksi, eikä sen<br />
tehosta tulehduskipulääkkeen aiheuttaman ulkuksen<br />
ehkäisyssä ole näyttöä [123].<br />
Tromboosiprofylaksi asetyylisalisyylihapolla<br />
ja siihen liittyvät haittavaikutukset. Asetyylisalisyylihappoa<br />
käytetään yleisesti sepelvaltimo- ja<br />
aivoverisuonitromboosin ehkäisyyn [124-127].<br />
Trombosyyttien aggregaatio estyy täydellisesti jo<br />
annoksilla, jotka ovat pienempiä kuin 100 mg/<br />
vrk, varsinkin jos <strong>käyttö</strong> on jatkuvaa [124,127].<br />
Haittavaikutusten riski kasvaa annoksen suuretessa.<br />
Kun annos on alle 100 mg/vrk, ero lumelääkkeeseen<br />
on yleensä ottaen vähäinen, muttei<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1925
olematon [124,128]. Vaikka dyspepsia ja ulkusriski<br />
ovat vähäisiä pieniä annoksia käytettäessä,<br />
ulkusvuodon riski on 2.3–kertainen annoksella<br />
75 mg/vrk, ja se lisääntyy 3.9-kertaiseksi, kun<br />
annosta suurennetaan määrään 300 mg/vrk<br />
[206](C). Pienten asetyylisalisyylihappo- ja tulehduskipulääkeannosten<br />
ei ole todettu lisäävän<br />
aivoverenvuodon riskiä [129].<br />
Tulehduskipulääkitykseen liittyvien limakalvoeroosioiden<br />
ja haavaumien hoidon ja<br />
ehkäisyn kustannusvaikuttavuus<br />
Omepratsolin (20 mg x 1) kustannusvaikuttavuus<br />
on parempi kuin ranitidiinin (150 mg x 2)<br />
mahalaukun tulehduskipulääkeulkuksen hoidossa,<br />
ja misoprostoli (200 µg x 4) on omepratsolia<br />
parempi limakalvoeroosioiden hoidossa<br />
[230](C). Misoprostolin rutiinikäytön kustannusvaikuttavuudesta<br />
tulehduskipulääkityksen<br />
yhteydessä on saatu ristiriitaisia tuloksia, kun<br />
arvion pohjana on käytetty mahalaukun oireisten<br />
haavaumien vähenemistä [130]. Misoprostolilla<br />
päästään hyvään kustannusvaikuttavuuteen<br />
ehkäistäessä tulehduskipulääkityksen vakavia<br />
haittavaikutuksia maha-suolikanavaan potilailla,<br />
joilla on esiintynyt aiemmin peptinen<br />
haavauma. Tämä koskee erityisesti yli 75-vuotiaita<br />
[131,132,225](B). Kustannus-hyötyanalyyseja<br />
protonipumpun estäjien käytöstä tulehduskipulääkityksen<br />
aiheuttamien komplikaatioiden<br />
estossa ei ole käytettävissä.<br />
Tulehduskipulääkitykseen liittyvien haittavaikutusten<br />
taloudellinen merkitys. Tulehduskipulääkitykseen<br />
liittyvällä gastroenteropatialla<br />
on huomattavat taloudelliset vaikutukset. Välittömät<br />
ja välilliset kustannukset huomioiden<br />
Ruotsissa arvioitiin maha-suolikanavaan kohdistuvien<br />
haittavaikutusten hoidon maksaneen<br />
v. 1996 3 420 kruunua yhtä tulehduskipulääkkeen<br />
käyttäjää kohden vuodessa, kun nivelreumasta<br />
aiheutuvat vuotuiset kokonaiskulut potilasta<br />
kohti arvioitiin 60 000 kruunuksi [133].<br />
Täten turvallisempien lääkkeiden kehittämisellä<br />
on huomattava taloudellinen vaikutus.<br />
COX-2-selektiivisten tulehduskipulääkkeiden<br />
kustannusvaikuttavuus ulkuskomplikaatioiden<br />
estossa. Uudet COX-2-selektiiviset tulehduskipulääkkeet<br />
saattavat vähentää ulkuskomplikaatioiden<br />
määrän puoleen [134]. Yhden<br />
komplikaation esto pienen riskin potilailla edellyttää<br />
500 potilaan hoitamista. Näiden valmisteiden<br />
nykyhinnoin (1.12.1999) tästä aiheutuu<br />
huomattavia vuotuisia lisäkustannuksia epäselektiivisillä<br />
tulehduskipulääkkeillä annettuun<br />
hoitoon verrattuna. Sen sijaan hoidettaessa suuren<br />
riskin potilaita (75-vuotta täyttäneet, joilla<br />
on aiemmin esiintynyt ulkus) yhden komplikaation<br />
esto edellyttää vain 40 potilaan hoitamista,<br />
milloin lisäkustannukset ovat kohtuullisia<br />
[134,225,231](D). On huomattava, että kustannusvaikuttavuusanalyysit<br />
ovat herkkiä lääkkeiden<br />
hinnan muutoksille.<br />
Lopuksi<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>käyttö</strong> lisääntyy väestön<br />
ikääntyessä. Maha-suolikanavaan kohdistuvat<br />
haittavaikutukset – etenkin ulkustauti – aiheuttavat<br />
kustannuksia. Varsinkin iäkkäiden riski<br />
saada jopa kuolemaan johtavia ulkuskomplikaatioita<br />
on suuri. Aikaisempi ulkustauti, mahasuolikanavan<br />
verenvuoto ja vaikea yleissairaus<br />
sekä antikoagulantti- ja kortisonihoito altistavat<br />
komplikaatioille. Varoittava dyspepsia saattaa<br />
olla vähäinen tai puuttua. Helikobakteerin<br />
merkitys on kiistanalainen, mutta ulkuspotilaalta<br />
helikobakteeri tulee aina häätää. Haittavaikutuksista<br />
tiedottamiseen tulee kiinnittää huomiota<br />
sekä resepti- että käsikauppamyynnissä.<br />
Kipulääkitystä on harkittava tapauskohtaisesti<br />
vaivan luonteen mukaan. Riskipotilaiden hoidossa<br />
tulee noudattaa erityistä varovaisuutta ja<br />
tarvittaessa liittää hoitoon ulkusprofylaksi.<br />
Maha-suolikanavaan kohdistuvia haittavaikutuksia<br />
liittyy vähemmän COX-2-selektiivisiin<br />
kuin ei-selektiivisiin tulehduskipulääkkeisiin.<br />
Maksaan ja keuhkoihin kohdistuvat haittavaikutukset<br />
voivat olla nopeasti eteneviä ja henkeä<br />
uhkaavia; haittavaikutukset munuaisiin kehittyvät<br />
yleensä hitaammin.<br />
***<br />
Työryhmä kiittää professori Jukka Mustosta (TaY) avusta käsikirjoituksen<br />
laadinnassa.<br />
1926<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
Kirjallisuutta<br />
1. Johnson AG, Day RO. The problems of NSAID therapy in the<br />
elderly (part I). Drugs Aging 1991;1:130-143.<br />
2. Arinen S, Häkkinen U, Klaukka T, Klavus J, Lehtonen R. Aro S.<br />
Suomalaisten terveys ja terveyspalvelujen <strong>käyttö</strong>. Terveydenhuollon<br />
väestötutkimuksen 1995/96 päätulokset ja muutokset vuodesta<br />
1987. Suomen virallinen tilasto. Terveys 1998:5, Helsinki:<br />
Stakes ja KELA 1998.<br />
3. Suomen Lääketilasto 1998. Lääkelaitos ja KELA, 1999.<br />
5. Moilanen E, Vapaatalo H. Tulehdus- ja immunologisia reaktioita<br />
vaimentavat lääkeaineet. Kirjassa: Pelkonen O, Ruskoaho H, toim.<br />
Lääketieteellinen Farmakologia ja toksikologia. Vammala: Kustannus<br />
Oy Duodecim, 1995, s. 346-78.<br />
6. Hawkey CJ. COX-2 inhibitors. Lancet 1999;353:307-14.<br />
7. Kankaanranta H, Vapaatalo H. Kohti tehokkaampia ja turvallisempia<br />
tulehduskipulääkkeitä prostaglandiinien tuoton valikoivalla<br />
vähentämisellä Duodecim 1996;112:419-24.<br />
8. Kankaanranta H, Moilanen E. Flufenamic and tolfenamic acids<br />
inhibit calcium influx in human polymorphonuclear leukocytes.<br />
Mol Pharmacol 1995;47:1006-13.<br />
9. Abramson SB. Treatment of gout and crystal arthropathies and<br />
uses and mechanisms of action of nonsteroidal anti-inflammatory<br />
drugs. Curr Opin Rheumatol 1992;4:295-300.<br />
10. Marnett LJ, Kalgutkar AS. Cyclooxygenase 2 inhibitors: discovery<br />
and the future. Trends Pharmacol Sci 1999;20:465-9.<br />
11. Warner TD, Giuliano F, Vojnovic I, Bukasa A, Mitchell JA, Vane<br />
JR. Nonsteroidal drug selectivities for cyclo-oxygenase-1 rather<br />
than cyclo-oxygenase-2 are associated with human gastrointestinal<br />
toxicity: a full in vitro analysis. Proc Natl Acad Sci USA<br />
1999;96:7563-8.<br />
12. Gierse JK, Koboldt CM, Walker MC, Seibert K, Isakson PC. Kinetic<br />
basis for selective inhibition of cyclo-oxygenases. Biochem J<br />
1999;339:607-14.<br />
13. Chan CC, Boyce S, Brideau C, ym. Rofecoxib (Vioxx, MK-0966; 4-<br />
(4-methylsulfonylphenyl)-3-phenyl-2-(5H)-furanone): a potent and<br />
orally active cyclooxygenase-2 inhibitor. Pharmacological and biochemical<br />
profiles. J Pharm Exp Ther 1999;290:551-60.<br />
14. Simon LS, Weaver AL, Graham DY, ym. Anti-inflammatory and<br />
upper gastrointestinal effects of celecoxib in rheumatoid arthritis.<br />
JAMA 1999;282:1921-8.<br />
15. Emery P, Zeidler H, Kvien TK, ym. Celecoxib versus diclofenac in<br />
long-term management of rheumatoid arthritis: randomised double-blind<br />
comparison. Lancet 1999;354:2106-11.<br />
16. Lipscomb GR, Wallis N, Armstrong G, Rees WDW. Gastrointestinal<br />
tolerability of meloxicam and piroxicam: a double-blind placebo-controlled<br />
study. Br J Clin Pharmacol 1998;46:133-7.<br />
17. Laine L. Nonsteroidal anti-inflammatory drug gastropathy. Gastrointest<br />
Endosc Clin North Am 1996;6:489-504.<br />
18. Soll AH, Weinstein WM, Kurata J, McCarthy D. Nonsteroidal antiinflammatory<br />
drugs and peptic ulcer disease. Ann Intern Med<br />
1991;114:307-19.<br />
19. Porto A, Almeida H, Cunha MJ, Macciocchi A. Double-blind study<br />
evaluating by endoscopy the tolerability of nimesulide and diclofenac<br />
on the gastric mucosa in osteoarthritic patients. Eur J<br />
Rheumatol Inflamm 1994;14:33-8.<br />
20. Mohammed S, Croom II DW. Gastropathy due to celecoxib, a<br />
cyclooxygenase-2 inhibitor. N Engl J Med 1999;340:2005-6.<br />
21. Scott LJ, Lamb HM. Rofecoxib. Drugs 1999;58:499-505.<br />
22. Wallace JL. Selective COX-2 inhibitosr: is the water becoming<br />
muddy Trends Pharmacol Sci 1999;20:4-6.<br />
23. Allen A, Flemström G, Garner A, Kivilaakso E. Gastroduodenal<br />
mucosal protection. Physiol Rev 1993;73:823-57.<br />
24. Wallace JL, Granger N. The cellular and molecular basis of gastric<br />
mucosal defence. FASEB J 1996;10:731-40.<br />
25. Soll A. Pathogenesis of nonsteroidal anti-inflammatory drug-related<br />
upper gastrointestinal toxicity. Am J Med 1998;105:10S-<br />
6S.<br />
26. Wallace J. Prostaglandins, NSAIDs, and cytoprotection. Gastroenterol<br />
Clin North Am 1992;21:631-41.<br />
27. Konturek PCh. Physiological, immunohistochemical and molecular<br />
aspects of gastric adaptation to stress, aspirin and H. pyloriderived<br />
gastrotoxins. J Physiol Pharmacol 1997;48:3-42.<br />
28. Caruso J, Bianchi Borro G. Gastroscopic evaluation of anti-inflammatory<br />
agents. BMJ 1980;280:75-8.<br />
29. Armstrong CP, Blower AL. Non-steroidal anti-inflammatory drugs<br />
and life threatening complications of peptic ulceration. Gut<br />
1987;28:527-32.<br />
30. Yeomans ND, Tulassay Z, Juhasz L, Racz I, Howard JM, van Rensburg<br />
CJ, Swanell AJ, Hawkey CJ for the acid suppression trial:<br />
ranitidine versus omeprazole for NSAID-associated ulcer treatment<br />
(ASTRONAUT) study group. A comparison of omeprazole<br />
with ranitidine for ulcers associated with nonsteroidal anti-inflammatory<br />
drugs. N Engl J Med 1998;338:719-26.<br />
31. Lancaster-Smith MJ, Jaderberg ME, Jackson DA. Ranitidine in the<br />
treatment of non-steroidal anti-inflammatory drug associated<br />
gastric and duodenal ulcers. Gut 1991;32:252-5.<br />
32. Hawkey CJ, Karrasch JA, Szczepanski L, ym. Omeprazole compared<br />
with misoprostol for ulcers associated with nonsteroidal<br />
anti-inflammatory drugs. N Engl J Med 1998;338:727-34.<br />
33. Bjarnason I, Hayllar J, Macpherson AJ, Russell A. Side effects of<br />
nonsteroidal anti-inflammatory drugs on the small and large intestine<br />
in humans. Gastroenterology 1993;104:1832-47.<br />
34. Anthony A. Dhillon AP, Nygard G, ym. Aliment Pharmacol Ther<br />
1993;7:29-39.<br />
35. Robert A, Asano T. Resistance of germfree rats to indomethacininduced<br />
intestinal lesion. Prostaglandins 1977;14:333-41.<br />
36. Collins AJ, Reid J, Soper CJ, Notarianni LJ Characteristic of ulcers<br />
of the small bowel induced by non-steroidal anti-inflammatory<br />
drugs in the rat: implications for clinical practice. Br J Rheumatol<br />
1995;34:727-31.<br />
37. Bjarnason I, Zanelli G, Smith T, ym. The pathogenesis and consequence<br />
of non steroidal anti-inflammatory drug induced small<br />
intestinal inflammation in man. Scand J Rheumatol 1987;64 Suppl:64:55-62.<br />
38. Scheiman JM. NSAIDS, Gastrointestinal injury, and cytoprotection.<br />
Gastroenterol Clin North Am 1996;25:279-98.<br />
39. Kwo PY, Tremaine WJ. Nonsteoidal anti-inflammatory drug-induced<br />
enteropathy: case discussion and review of the literature.<br />
Mayo Clin Proc 1995;70:55-61.<br />
40. Morris AJ. Nonsteroidal anti-inflammatory drug enteropathy.<br />
Gastroenterol Endosc Clin North Am 1999;9:125-33.<br />
41. Bjarnason I, Macpherson A, Rotman H, Schupp J, Hayllar J. A<br />
randomized, double-blind, crossover comparative endoscopy<br />
study on the gastroduodenal tolerability of a highly specific cyclooxygenase-2-inhibitor,<br />
flosulide, and naproxen. Scand J Gastroenterol<br />
1997;32:126-30.<br />
42. Sopena F, Lanas A, Sainz R. Esophageal motility and intraesophageal<br />
pH patterns in patients with esophagitis and chronic nonsteroidal<br />
anti-inflammatory drug use. J Clin Gastroenterol 1998;<br />
27:316-20.<br />
43. Schlondorff D. Renal complications of nonsteroidal anti-inflammatory<br />
drugs. Kidney Int 1993;4:643-53.<br />
44. Aitio M-L. Kipulääkkeet ja munuainen. Duodecim 1998:114:841-8.<br />
45. Bennett WM, Henrich WL, Stoff JS. The renal effects of nonsteroidal<br />
anti-inflammatory drugs: summary and recommendations.<br />
Am J Kidney Dis 1996:28 Suppl 1:S56-S62.<br />
46. Henrich WL, Agoda LE, Barrett B ym. Analgesics and the kidney:<br />
summary and recommendations to the scientific advisory board<br />
of the national kidney foundation from an ad hoc committee of<br />
the national kidney foundation. Am J Kidney Dis 1996;27:162-5.<br />
47. De Broe ME, Elseviers MM. Analgesic nephropathy. N Engl J Med<br />
1998;338:446-52.<br />
48. Helin HJ, Korpela MM, Mustonen JT, Pasternack AI. Renal biopsy<br />
findings and clinicopathologic correlations in rheumatoid arthritis.<br />
Arthritis Rheum 1995;38:242-7.<br />
49. Morham SG, Langenbach R, Loftin CD, ym. Prostaglandin synthase<br />
2 gene disruption causes severe renal pathology in the<br />
mouse. Cell 1995;83:473-82.<br />
50. Dinchuk JE, Car BD, Focht RJ, ym. Renal abnormalities and an<br />
altered inflammatory response in mice lacking cyclooxygenase II.<br />
Nature 1995;378:406-9.<br />
51. Langenbach R, Morham SG, Tiano HF, ym. Prostaglandin synthase<br />
1 gene disruption in mice reduces arachidonic acid-induced<br />
inflammation and indomethacin-induced gastric ulceration. Cell<br />
1995;83:483-92.<br />
52. Breyer MD. COX2 selective NSAIDs and renal function: gain without<br />
pain Kidney Int 1999;55:738-9.<br />
53. Venturini CM, Isakson P, Needleman. Non-steroidal anti-inflammatory<br />
drug-induced renal failure: a brief review of the role of<br />
cyclo-oxygenase isoforms. Curr Opin Nephrol Hypertens<br />
1998;7:79-82.<br />
54. Bjorkman D. Nonsteroidal anti-inflammatory drug-associated toxicity<br />
of the liver, lower gastrointestinal tract, and oesophagus.<br />
Am J Med 1998;105(5A):17-21.<br />
55. Kromann-Andersen H. Pedersen A. Reported adverse reactions<br />
to and consumption of nonsteroidal anti-inflammatory drugs in<br />
Danmark over a 17-year period. Danish Med Bull 1988;35:187-92.<br />
56. Carson JL, Willet LR. Toxicity of nonsteroidal anti-inflammatory<br />
drugs. An overview of the epidemiological evidence. Drugs 1993;<br />
46 Suppl 1:243-8.<br />
57. Fry S, Seeff LB. Hepatotoxicity of analgetics and anti-inflammatory<br />
agents. Gastroenterol Clin North Am 1995;24:875-905.<br />
58. Walker AM, Bortnichak EA, Lanza L, Yood RA. The infrequency<br />
of liver function testing in patients using nonsteroidal anti-inflammatory<br />
drugs. Arch Fam Med 1995;4:24-9.<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1927
59. Banks AT, Zimmerman HJ, Ishak KG, Harter JG. Diclofenac-associated<br />
hepatotoxicity: analysis of 180 cases reported to the Food<br />
and Drug Administration as adverse reactions. Hepatology<br />
1995;22:820-7.<br />
60. Tarazi EM, Harter JG, Zimmerman HJ, Ishak KG, Eaton RA. Sulindac-associated<br />
hepatic injury: analysis of 91 cases reported to the<br />
Food and Drug Administration. Gastroenterology 1993;104:569-<br />
74.<br />
61. Scully LJ, Clarke D, Barr RJ. Diclofenac induced hepatitis. 3 cases<br />
with features of autoimmune chronic active hepatitis. Dig Dis Sci<br />
1993;38:744-51.<br />
62. Purcell P, Henry D, Melville G. Diclofenac hepatitis. Gut<br />
1991;32:1381-5.<br />
63. Zimmerman HJ. Effects of aspirin and acetaminophen on the<br />
liver. Arch Intern Med 1981;141:333-42.<br />
64. Kankaanranta H, Moilanen E, Nieminen MM. Leukotrieenit ja<br />
astma. Suom Lääkäril 1999;54:4097-104.<br />
65. Szczeklik A, Stevenson DD. Aspirin-induced asthma: advances in<br />
pathogenesis and management. J Allergy Clin Immunol<br />
1999;104:5-13.<br />
66. Bianco S, Robuschi M, Petrigni G, ym. Efficacy and tolerability of<br />
nimesulide in asthmatic patients intolerant to aspirin. Drugs<br />
1993;46 Suppl 1:115-20.<br />
67. Andri L, Senna G, Betteli C, ym. Tolerability of nimesulide in<br />
aspirin-sensitive patients. Ann Allergy 1994;72:29-32.<br />
68. Kosnik M, Music E, Matjaz F, Suskovic S. Relative safety of meloxicam<br />
in NSAID-intolerant patients. Allergy 1998;53:1231-3.<br />
69. McAdam BF, Catella-Lawson F, Mardini IA, Kapoor S, Lawson JA,<br />
FitzGerald GA. Systemic biosynthesis of prostacyclin by cyclooxygenase<br />
(COX)-2: the human pharmacology of a selective inhibitor<br />
of COX-2. Proc Natl Acad Sci USA 1999;96:272-7.<br />
70. Stichtenoth DO, Wagner B, Frölich JC. Effects of meloxicam and<br />
indomethacin on cyclooxygenase pathways in healthy volunteers.<br />
J Invest Med 1997;45:44-9.<br />
71. de Meijer A, Vollaard H, de Metz M, Verbruggen B, Thomas C,<br />
Novakova I. Meloxicam, 15 mg/day, spares platelet function in<br />
healthy volunteers. Clin Pharmacol Ther 1999;66:425-30.<br />
72. Wolfe MM. Future trends in the development of safer nonsteroidal<br />
anti-inflammatory drugs. 1998;105:44S-52S.<br />
73. Karim A, Tolbert DS, Hunt TL, Hubbard RC, Harper KM, Geis GS.<br />
Celecoxib, a specific COX-2 inhibitor, has no significant effect on<br />
methotrexate pharmacokinetics in patients with rheumatoid arthritis.<br />
J Rheumatol 1999;26:2539-43.<br />
74. Kaplan-Machlis B, Klostermeyer BS. The cyclooxygenase-2 inhibitors:<br />
safety and effectiveness. Ann Pharmacother 1999;33:979-88.<br />
75. Fries JF. NSAID gastropathy: the second most deadly rheumatic<br />
disease Epidemiology and risk appraisal. J Rheumatol 1991;18<br />
Suppl 28:6-9.<br />
76. Eccles M, Freemantle N, Mason J for the North of England nonsteroidal<br />
non-steroidal anti-inflammatory drug guideline development<br />
group. North of England evidence based guideline development<br />
project: summary guideline for non-steroidal anti-inflammatory<br />
drugs versus basic analgesia in treating the pain of<br />
degenerative arthritis. BMJ 1998;317:526-30.<br />
77. Isomäki H, Martio J. <strong>Tulehduskipulääkkeiden</strong> järkevä <strong>käyttö</strong>.<br />
Suom Lääkäril 1997;52:1927-32.<br />
78. Bradley JD, Brandt KD, Katz BP, Kalanski LA, Ryan SI. Treatment<br />
of knee osteoarthritis: relationship of clinical features of joint<br />
inflammation to the response to a nonsteroidal anti-inflammatory<br />
drug or pure analgesic. J Rheumatol 1992;19:1950-4.<br />
79. Williams HJ, Ward JR, Egger MJ, ym. Comparison of naproxen<br />
and acetaminophen in a two-year study of treatment of osteoarthritis<br />
of the knee. Arthritis Rheum 1993;36:1196-206.<br />
80. MacDonald TM, Morant SV, Robinson GC, ym. Association of<br />
upper gastrointestinal toxicity of non-steroidal anti-inflammatory<br />
drugs with continued exposure. BMJ 1997;315:1333-7.<br />
81. Kelly JP, Kaufman DW. Jurgelon JM, Sheehan J, Koff RS, Shapiro<br />
S. Risk of aspirin-associated major upper-gastointestinal bleeding<br />
with enteric-coated or buffered product. Lancet 1996;348:1413-6.<br />
82. Griffin MR, Piper JM, Daugherty JR, Snowdon M. Ray WA. Nonsteroidal<br />
anti-inflammatory drug use and increased risk for peptic<br />
ulcer disease in elderly persons. Ann Intern Med 1991;114:257-<br />
63.<br />
83. Paakkari P. <strong>Tulehduskipulääkkeiden</strong> turvallisuudesta. Tabu<br />
1996;4(2):12-15.<br />
84. Evans JMM, McMahon AD, McGilchrist MM ym. Topical non-steroidal<br />
anti-inflammatory drugs and admission to hospital for upper<br />
gastrointestinal bleeding and perforation: a record linkage<br />
case-control study. BMJ 1995;311:22-6.<br />
85. Martio J. Iholle annosteltavat tulehduskipulääkkeet - turvallisia<br />
kivunpoistajia vai kalliita lumelääkkeitä Suom Lääkäril<br />
1998;53:569-71.<br />
86. Johnson AG, Nguyen TV, Day RO. Do nonsteroidal anti-inflammatory<br />
drugs affect blood pressure A meta-analysis. Ann Intern<br />
Med 1994;121:289-300.<br />
87. Mene P, Pugliese F, Patrono C. The effects of nonsteroidal antiinflammatory<br />
drugs on human hypertensive vascular disease.<br />
Semin Nephrol 1995;15:244-52.<br />
88. de Leeuw PW. Nonsteroidal anti-inflammatory drugs and hypertension.<br />
The risks in perspective. Drugs 1996;51:179-87.<br />
89. Uudet tulehduskipulääkkeet – tarvitaanko niitä Duodecim<br />
1999;115:2217-24.<br />
90. Lanza FL, Rack MF, Simon TJ, ym. Specific inhibition of cyclooxygenase-2<br />
with MK-0966 (rofecoxib) is associated with less gastroduodenal<br />
damage than either aspirin or ibuprofen. Aliment<br />
Pharmacol Ther 1999;13:761-7.<br />
91. Scott LJ, Lamb HM. Rofecoxib. Drugs 1999;499-507.<br />
92. Fort J. Celecoxib, a COX-2-spesific inhibitor: the clinical data. Am<br />
J Orthop 1999;28 Suppl 3S:13-8.<br />
93. Laine L, Harper S, Simon T, ym. A randomized trial comparing<br />
the effect of rofecoxib, a cyclooxygenase 2-specific inhibitor, with<br />
that of ibuprofen on the gastroduodenal mucosa of patients<br />
with osteoarthritis. Gastroenterology 1999;117:776-83.<br />
94. Langman MJ, Jensen DM, Watson DJ, ym. Adverse upper gastrointestinal<br />
effects of rofecoxib compared with NSAIDs. JAMA<br />
1999;282:1929-33.<br />
95. Simon LS, Lanza FL, Lipsky PE, ym. Preliminary study of the safety<br />
and efficacy of SC-58635, a novel cyclooxygenase 2 inhitor. Arthritis<br />
Rheum 1998;41:1591-602.<br />
96. Kvien TK, Brors O, Staff PH, ym. Improved cost-effectiveness ratio<br />
with a patient self-adjusted naproxen regimen in osteoarthritis<br />
treatment. Scand J Rheumatol 1991;20:280-7.<br />
97. Wynne HA, Long A. Patients awareness of the adverse effects of<br />
non-steroidal anti-inflammatory drugs (NSAIDs). Br J Clin Pharmacol<br />
1996;42:253-6.<br />
98. Pääkirjoitus: Many NSAID users who bleed don’t know when to<br />
stop. BMJ 1998;316:492.<br />
99. Garcia Rodriguez LA, Jick H. Risk of upper gastrointestinal bleeding<br />
and perforation associated with individual non-steroidal antiinflammatory<br />
drugs. Lancet 1994;343:769-72.<br />
100. Langman MJS, Well J, Wainwright P, ym. Risks of bleeding peptic<br />
ulcer associated with individual non-steroidal anti-inflammatory<br />
drugs. Lancet 1994;343:1075-8.<br />
101. Kulber DA, Hartunian S, Schiller D, Morgenstern L. The current<br />
spectrum of peptic ulcer disease in the older age groups. Am<br />
Surg 1990;56:737-41.<br />
102. Smedley FH, Taube M, Leach R, Wastell C. Non-steroidal antiinflammatory<br />
drug ingestion: retrospective study of 272 bleeding<br />
or perforated peptic ulcers. Postgrad Med J 1989;65:892-5.<br />
103. Smalley WE, Griffin MR, Fought RL, Ray WA. Excess costs from<br />
gastrointestinal disease associated with nonsteroidal anti-inflammatory<br />
drugs. J Gen Intern Med 1996;11:461-9.<br />
104. Langman MJS, Weil J, Wainwright P, ym. Risks of bleeding peptic<br />
ulcer associated individual non-steroidal anti-inflammatory drugs.<br />
Lancet 1994;343:1075-8.<br />
105. Gabriel SE, Jaakkimainen L. Bombardier C. Risk for serious gastrointestinal<br />
complications related to use of nonsteroidal antiinflammatory<br />
drugs. Ann Intern Med 1991;115:787-96.<br />
106. Hansen J, Hallas J, Lauritsen JM. Bytzer P. Non-steroidal antiinflammatory<br />
drugs and ulcer complications: a risk factor analysis<br />
for clinical decision-making. Scand J Gastroenterol 1996;31:126-<br />
30.<br />
107. DeAbajo FJ, Garcia Rodriguez LA, Montero D. Association between<br />
selective serotonin re-uptake inhibitors and upper gastrointestinal<br />
bleeding: population based case-control study. BMJ<br />
1999;319:1106-9.<br />
108. Hudson N, Balsitis M, Filipowicz F, Hawkey CJ. Effect of Helicobacter<br />
pylori colonisation on gastric mucosal eicosanoid synthesis<br />
in patients taking nonsteroidal anti-inflammatory drugs. Gut<br />
1993;34:748-51.<br />
109. Hawkey CJ, Tulassay Z, Szczepanski L, ym. Randomised controlled<br />
trial of Helicobacter pylori eradication in patients on non-steroidal<br />
anti-inflammatory drugs: HELP NSAIDs study. Lancet<br />
1998;352:1016-21.<br />
110. Jaszewski R. Frequency of gastroduodenal lesions in asymptomatic<br />
patients on chronic aspirin or nonsteroidal anti-inflammatory<br />
drug therapy. J Clin Gastroenterol 1990;12:10-3.<br />
111. Paulus HE. FDA arthritis advisory committee meeting: serious<br />
gastrointestinal toxicity of nonsteroidal anti-inflammatory drugs;<br />
drug-containing renal and biliary stones; diclofenac and carprofen<br />
approved. Arthritis Rheum 1988;31:1450-1.<br />
112. Griffin MR. Epidemiology of non-steroidal anti-inflammatory<br />
drug-associated gastrointestinal injury. Am J Med 1998;<br />
104(3A):23-29S.<br />
113. Ehsanullah RSB, Page MC, Tidesley G, Wood JR. Prevention of<br />
gastroduodenal damage induced by non-steroidal anti-inflammatory<br />
drugs: controlled trial of ranitidide. BJM 1988;297:1017-21.<br />
114. Taha AS, Hudson N, Hawkey CJ, ym. Famotide for the prevention<br />
of gastric and duodenal ulcers caused by nonsteroidal anti-inflammatory<br />
drugs. N Engl J Med 1996;334:1435-9.<br />
1928<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
115. Hudson N, Taha AS, Russell EI, ym. Famotidine for healing and<br />
maintenance in nonsteroidal anti-inflammatory drug-associated<br />
gastroduodenal ulceration. Gastroenterology 1997;112:1817-22.<br />
116. Levine LR, Cloud ML, Enas NH. Nizatidine prevents peptic ulceration<br />
in high-risk patients taking nonsteroidal anti-inflammatory<br />
drugs. Arch Intern Med 1993;153:2449-54.<br />
117. Bianchi Porro G, Imbesi V. Pantoprazole vs placebo in prevention<br />
of NSAID-induced ulcers. Gastroenterology 1998;114;A74.<br />
118. Simon B, Mueller P, Cain C. Pantoprazole protects against aspirin-induced<br />
damage in the upper-intestinal tract. Can J Gastroenterol<br />
1998;Suppl A12:S48.<br />
119. Singh G. Recent considerations in nonsteroidal anti-inflammatory<br />
drug gastropathy. Am J Med 1998;105:31S-38S.<br />
120. Rose P, Huang B, Lukasik N, Collis C. Evidence that lansoprazole<br />
is effective in preventing NSAID induced ulcers. Gastroenterology<br />
1999;116:A295.<br />
121. Goldstein J, Huang B, Feaheny K, Lukasik NL, Collis CM, Greski-<br />
Rose PA. Healing and prevention of NSAID-associated ulcers in<br />
patients continuing to take NSAIDs. Lansoprazole vs. ranitidine<br />
and lansoprazole vs. misoprostol vs. plasebo. Gut 1999;45:A101.<br />
122. Hawkey CJ. Progress in prophylaxis against nonsteroidal antiinflammatory<br />
drug-associated ulcers and erosions. Am J Med<br />
1998;104:67S-74S.<br />
123. Agrawal NM, Roth S, Graham DY, White RH, Germain B, Brown<br />
JA, Stromatt SC. Misoprostol compared with sucralfate in the<br />
prevention of nonsteroidal anti-inflammatory drug-induced gastric<br />
ulcer. Ann Intern Med 1991;115:195-200.<br />
124. Patrono C. Aspirin as an antiplatelet drug. N Engl J Med<br />
1994;330:1287-94.<br />
125. Steering committee of the Phycisian Health study Research group.<br />
Final report on the aspirin component of the ongoing physician<br />
health study. N Engl J Med 1989;321:129-35.<br />
126. The SALT collaborative group. Swedish aspirin low-dose trial<br />
(SALT) of 75mg aspirin as secondary prophylaxis after cerebrovascular<br />
ischaemic events. Lancet 1991;338:1345-9.<br />
127. Stroke prevention in atrial fibrillation investigators. Stroke prevention<br />
in atrial fibrillation study. Final result. Circulation<br />
1991;84:527-39.<br />
128. Cryer B, Feldman M. Effects of very low dose daily, long term<br />
aspirin therapy on gastric, duodenal, and rectal prostaglandin<br />
levels and on mucosal injury in healthy humans. Gastroenterology<br />
1999;117:17-25.<br />
129. Thrift AG, McNeil JJ, Forbes A, Donnan GA. Risk of primary intracerebral<br />
haemorrhage associated with aspirin and nonsteroidal<br />
anti-inflammatory drugs: case control study. BMJ<br />
1999;318:759-64.<br />
130. Stucki G, Johannesson M, Liang MH. Is misoprostol cost-effective<br />
in prevention of nonsteroidal anti-inflammatory drug-induced<br />
gastropathy in patients with chronic arthritis A review of conflicting<br />
economic evaluations. Arch Intern Med 1994;154:2020-5.<br />
131. Maetzel A, Perraz MB, Bombardier C. The cost-effectiveness of<br />
misoprostol in preventing serious gastrointestinal events associated<br />
with the use of nonsteroidal anti-inflammatory drugs. Arthritis<br />
Rheum 1998;42:16-25.<br />
132. Kristiansen IS,Kvien TK,Nord E. Cost effectiviness of replacing<br />
diclofenac with a fixed combination of misoprostol and diclofenac<br />
in patients with rheumatoid arthritis. Arthritis Rheum<br />
1999;42:2293-309.<br />
133. Walan A, Wahlqvist P. Pharmacoeconomic aspects of nonsteroidal<br />
anti-inflammatory drug gastropathy. Ital J Gastroenterol<br />
Hepatol 1999;31,Suppl 1:S79-S88.<br />
134. Langman MJ, Jensen DM, Watson DJ, ym. Adverse upper gastrointestinal<br />
effects of rofecoxib compared with NSAIDs. JAMA<br />
1999;282:1292-3.<br />
135. Nordic statistics of medicines 1993-1995.NLN Publication No43.<br />
Uppsala: Nordic Council of Medicines, 1996.<br />
136. Myllykangas-Luosujärvi R, Aho K, Kautiainen H, Isomäki H. Nivelreuma<br />
lyhentää ikää. Duodecim 11:1209-15.<br />
137. Young JM, Panah S, Satchawatcharaphong C, Cheung PS. Human<br />
whole blood assays for inhibition of prostaglandin G/H synthases-1<br />
and -2 using A23187 and lipopolysaccharide stimulation of<br />
thromboxane B2 production. Inflamm Res 1996;45:246-53.<br />
138. Giuliano F, Warner TD. Ex vivo assay to determine the cyclooxygenase<br />
selectivity of non-steroidal anti-inflammatory drugs. Br J<br />
Pharmacol 1999;126:1824-30.<br />
139. Blanco FJ, Guitian R, Moreno J, de Toro FJ, Galdo F. Effect of<br />
anti-inflammatory drugs on COX-1 and COX-2 activity in human<br />
articular chondrocytes. J Rheumatol 1999;26:1366-73.<br />
140. Patrignani P, Panara MR, Sciulli MG, Renda G, Patrono C. Differential<br />
inhibition of human prostaglandin endoperoxide synthase-<br />
1 and -2 by nonsteroidal anti-inflammatory drugs. J Physiol Pharmacol<br />
1997;48:623-31.<br />
141. Churchill L, Graham AG, Shih C-K, Pauletti D, Farina PR, Grob PM.<br />
Selective inhibition of human cyclo-oxygenase-2 by meloxicam.<br />
Inflammopharmacology 1996;4:125-35.<br />
142. Gierse JK, Hauser SD, Creely DP, Koboldt C, Rangwala SH, Isakson<br />
PC, Seibert K. Expression and selective inhibition of the constitutive<br />
and inducible forms of human cyclo-oxygenase. Biochem J<br />
1995;305:479-84.<br />
143. Laneuville O, Breuer DK, DeWitt DL, Hla T, Funk CD, Smith WL.<br />
Differential inhibition of human prostaglandin endoperoxide H<br />
synthases-1 and -2 by nonsteroidal anti-inflammatory drugs. J<br />
Pharmacol Exp Ther 1994;271:927-34.<br />
144. Meade EA, Smith WL, De Witt DL. Differential inhibition of prostaglandin<br />
endoperoxide synthase (cyclooxygenase) isozymes by<br />
aspirin and other non-steroidal anti-inflammatory drugs. J Biol<br />
Chem 1993;268:6610-4.<br />
145. Mitchell JA, Akarasereenont P, Thiemermann C, Flower RJ, Vane<br />
JR. Selectivity of nonsteroidal anti-inflammatory drugs as inhibitors<br />
of constitutive and inducible cyclooxygenase. Proc Natl Acad<br />
Sci USA 1994;90:11693-7.<br />
146. O’Neill GP, Mancini JA, Kargman S, ym. Overexpression of human<br />
prostaglandin G/H synthase-1 and -2 by recombinant vaccinia<br />
virus: inhibition by nonsteroidal anti-inflammatory drugs and<br />
biosynthesis of 15-hydroxyeicosatetraenoic acid. Mol Pharmacol<br />
1994;45:245-54.<br />
147. Barnett J, Chow J, Ives D, ym. Purification, characterization and<br />
selective inhibition of human prostaglandin G/H synthase 1 and<br />
2 expressed in the baculovirus system. Biochim Biophys Acta<br />
1994;1209:130-9.<br />
148. Hawkey C, Kahan A, Steinbruck K, Allgre C, Baumelon E, Begaud<br />
B, Degueker J, Isomaki H, Littlejohn G, Mau J, Papazoglou S and<br />
the International Melissa Study group. Gastrointestinal tolerability<br />
of meloxicam compared to diclofenac in osteoarthritis patients.<br />
International MELISSA Study Group. Meloxicam Large-scale<br />
International Study Safety Assessment. Br J Rheumatol 1998;37:<br />
937-45.<br />
149. Patoia L, Santucci L, Furno P, Dionisi MS, Dell’Orso S, Romagnoli<br />
M, Sattarinia A, Marini MG. A 4 week, double-blind, parallelgroup<br />
study to compare the gastrointestinal effects of meloxicam<br />
7.5 mg, meloxicam 15 mg, piroxicam 20 mg and placebo by<br />
means of faecal blood loss, endoscopy and symptom evaluation<br />
in healthy volunteers. Br J Rheumatol 1996;35 Suppl 1:61-7.<br />
150. Dequeker J, Hawkey C, Kahan A, ym. Improvement in gastrointestinal<br />
tolerability of the selective cyclooxygenase (COX)-2 inhibitor,<br />
meloxicam, compared with piroxicam: results of the safety<br />
and efficacy large-scale evaluation of COX-inhibiting therapies<br />
(SELECT) trial in osteoarthritis. Br J Rheumatol 1998;37:946-51.<br />
151. Roth SH. Upper gastrointestinal safety with nabumetone. J Rheumatol<br />
1992;19 Suppl 19:74-9.<br />
152. Lipani JA, Poland M. Clinical update of the relative safety of<br />
nabumetone in long-term clinical trials. Inflammopharmacology<br />
1995;3:351-61.<br />
153. Dequeker J, Hawkey C, Kahan A, Steinbruck K, Alegre C, Baumelou<br />
E, Begaud B, Isomäki H, Littlejohn G, Mau J, Papazoglou S on<br />
behalf of the SELECT Study group. Improvement in gastrointestinal<br />
tolerability of the selective cyclooxygenase (COX)-2 inhibitor<br />
meloxicam, compared with piroxicam:results of the safety and<br />
efficacy large-scale evaluation of cox-inhibiting therapies (SELECT)<br />
trial in osteoarthritis. Br J Rheumatol 1998;37:946-51.<br />
154. Kankaanranta H, Vapaatalo H. Kohti tehokkaampia ja turvallisempia<br />
tulehduskipulääkkeitä prostaglandiinien tuoton valikoivalla<br />
vähentämisellä Duodecim 1996;112:419-24.<br />
155. Lipani JA, Poland M. Clinical update of the relative safety of<br />
nabumetone in long-term clinical trials. Inflammopharmacology<br />
1995;3:351-61.<br />
156. Eversmeyer W, Poland M, DeLapp RE, Jensen CP. Safety experience<br />
with nabumetone versus diclofenac, naproxen, ibuprofen<br />
and piroxicam in osteoarthritis and rheumatoid arthritis. Am J<br />
Med 1993;95(2A):2S-18S.<br />
157. Walan A, Bader J-P, Classen M, ym. Effect of omeprazole and<br />
ranitidine on ulcer healing and relapse rates in patients with<br />
benign gastric ulcer. N Engl J Med 1989;320:69-75.<br />
158. Bjarnason, I, Willams P, So A, ym. Intestinal permeability and<br />
inflammation in rheumatoid arthritis: effect of non-steroidal antiinflammatory<br />
drugs. Lancet 1984;2(8412):1171-4.<br />
159. Bjarnason I, Zanelli G, Prouse P, ym. Blood and protein loss via<br />
small-intestinal inflammation induced by non-steroidal anti-inflammatory<br />
drugs. Lancet 1987:2(8561)711-4.<br />
160. Bjarnasn I, Zanelli G, Smith T, ym. Nonsteroidal anti-inflammatory<br />
drug-induced intestinal inflammation in humans. Gastroenterology<br />
1987;93:480-9.<br />
161. Morris AJ, Madhok R, Sturrock RD, Capell HA, MacKenzie JF.<br />
Enteroscopic diagnosis of small bowel ulceration in patients receiving<br />
non-steroidal anti-inflammatory drugs. Lancet<br />
1991;337:520.<br />
162. Madhok R, MacKenzie JA, Lee FD, Bruckner FE, Terry TR, Sturrock.<br />
Small bowel ulceration in patients receiving non-steroidal<br />
anti-inflammatory drugs for rheumatoid arthritis. Quart J Med<br />
1986;58:53-8.<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1929
163. Allison MC, Howatson AG, Torrance CJ, Lee FD, Russel RI. Gastrointestinal<br />
damage associated with use of nonsteroidal antiinflammatory<br />
drugs. N Engl J Med 1992;327:749-54.<br />
164. Langman MJ, Morgan L, Worrall A. Use of anti-inflammatory<br />
drugs by patients admitted with small or large bowel perforations<br />
and haemorrhage. BMJ 1985;290:347-9.<br />
165. Lanas A, Serrano P, Bajador E, Esteva F, Benito R, Sainz R. Evidence<br />
of Aspirin use in both upper and lower gastrointestinal<br />
perforation. Gastroenterology 1997;112:683-9.<br />
166. Wilson RG, Smith AN, Macintyre IM. Complications of diverticular<br />
disease and non-steroidal anti-inflammatory drugs: a prospective<br />
study. Br J Surg 1990;77:1103-4.<br />
167. Campbell K, Steele RJ. Non-steroidal anti-inflammatory drugs and<br />
complicated diverticular disease. Br J Surg 1991;78:190-1.<br />
168. Lang J, Price AB, Levi AJ, Burke M, Cumpel JM, Bjarnason I.<br />
Diaphragm disease; pathology of disease of the small intestine<br />
induced by non-steroidal anti-inflammatory drugs. J Clin Pathol<br />
1988;41:516-26.<br />
169. Levi S, deLacey G, Price AB, Cumpel MJ, Levi AJ, Bjarnason I.<br />
Diaphragm-like Strictures of the small bowel in patients treated<br />
with non-steroidal anti-inflammatory drugs. Br J Radiol<br />
1990;63:186-9.<br />
170. Fellows IW, Claeke JM, Roberts PF. Non-steroidal anti-inflammatory<br />
drug-induced jejunal and colonic diaphragm disease: a report<br />
of two cases. Gut 1992;33:1424-6.<br />
171. Bjarnason I, Price AB, Zanelli G, ym. Clinicopathological features<br />
of nonsteroidal anti-inflammatory drug-induced small intestinal<br />
strictures. Gastroenterology 1988;94:1070-4.<br />
172. Robinson MHC, Wheatley T, Leach IH. Nonsteroidal anti-inflammatory<br />
dru-induced colonic stricture; an unusual cause of large<br />
bowel obstruction and perforation. Dig Dis Sci 1995;40:315-9.<br />
173. Davies NM. Toxicity of nonsteroidal anti-inflammatory drugs in<br />
the large intestine. Dis Colon Rectum 1995;38:1311-21.<br />
174. Gibson GR, Whitacre FB, Ricotti CA. Colitis induced by nonsteroidal<br />
anti-inflammatory drugs. Report of four cases and review of<br />
the literature. Ann Intern Med 1992;152:625-32.<br />
175. Evans JMM, McMahon AD, Murray FE, McDevitt DG, MacDonald<br />
TM. Non-steroidal anti-inflammatory drugs are associated with<br />
emergency admission to hospital for colitis due to inflammatory<br />
bowel disease. Gut 1994;40:619-22.<br />
176. Morris AJ, Wasson LA, MacKenzie JF. Small bowel enteroscopy in<br />
undiagnosed gastrointestinal blood loss. Gut 1992;33:887-9.<br />
177. Davies GR, Benson MJ, Gertner DJ, van Someren RMN, Rampton<br />
DS, Swein CP. Diagnostic and therapeutic push type enterosopy<br />
in clinical use. Gut 1995;37:346-52.<br />
178. O’Mahony S, Morris AJ, Straiton M, Murray I, MacKenzie JF. Push<br />
enteroscopy in the investigation of small-intestinal disease. Q J<br />
Med 1996;89:685-90.<br />
179. Landi B, Tkoub M, Gaurdic M, ym. Diagnostic yield of push-type<br />
enteroscopy in relation to indication. Gut 1998;42:421-5.<br />
180. Cellier C, Tkoub M, Gaudric M, ym. Comparison of push-type<br />
endoscopy and barium transit study of the small intestine in<br />
digestive bleeding and unexplained iron-deficiency anemia. Gastroenterol<br />
Clin Biol 1998;22:491-4.<br />
181. Collins AJ, Jenkinson T, Notarianni LJ, Virjee J. Barium X-ray study<br />
of the small bowel in patients with rheumatoid arthritis taking<br />
non-steroidal anti-inflammatory drugs did not disclose ulceration.<br />
Br J Rheumatol 1994;33:1195-6.<br />
182. Bjarnason I, Hayllar J, Smethurs P, Price A, Gumpe M. Metronidazole<br />
reduces intestinal inflammation and blood loss in non-steroidal<br />
anti-inflammatory drug induced enteropathy. Gut<br />
1992;33:1204-8.<br />
183. Hayllar J, Smith T, Macpherson A, Price AB, Gumpel M, Bjarnason<br />
I. Nonsteroidal anti-inflammatory drug-induced small intestinal<br />
inflammation and blood loss. Effects of sulfasalazine and other<br />
disease-modifying antirheumatic drugs. Arthritis Rheum<br />
1994;37:1146-50.<br />
184. Morris Aj, Murray L, Sturrock RD, Madhok R, Capell HA, Mackenzie<br />
JF. Short report: the effect of misoprostol on the anemia of<br />
NSAID enteropathy. Alim Pharmacol Ther 1994;8:343-6.<br />
185. Semble EL, Wallace C W, Castell DO. Nonsteroidal anti-inflammatory<br />
drugs and esophageal injury. Semin Arthritis Rheum<br />
1989;19:99-109.<br />
186. Lanas A, Hirschowitz BJ. Significant role of aspirin use in patients<br />
with esophagitis. J Clin Gastroenterol 1991;13:622-7.<br />
187. Heller SR, Fellows IW, Ogilvie AL, Atkinson M. Non-steroidal antiinflammatory<br />
drugs stricture. BMJ 1982;285:167-8.<br />
188. McCord GS, Clouse RE. Pill-induced esophageal strictures: clinical<br />
features and risk factors for development. Am J Med 1990;88:512-8.<br />
189. Santucci L, Patoia L, Fiorucci S, Farroni F, Favero Dei, Morelli A.<br />
Oesophageal lesions during treatment with piroxicam. BMJ<br />
1990;300:1018.<br />
190. Agdal N. Medicinincucerande esophagusskader. En oversigt samt<br />
et tilfaelde of indometacinfremkaldt ulcerations med dödelig<br />
udgang. Ugeskr Laeger 1979;141:3019-21.<br />
191. Scheiman JM, Patel PM, Henson EK, Nostrant TT. Effect of naproxen<br />
on gastroesophageal function: a randomized, double-blind,<br />
placebo-controlled study. Am J Gastroenterol 1995;90:754-7.<br />
192. Taha AS, Dahill S, Nakshabendi I, Lee FD, Sturrock RD, Russell RI.<br />
Oesophageal histology in long-term users of nonsteroidal antiinflammatory<br />
drugs. J Clin Pathol 1994;47:705-8.<br />
193. Perez Gutthann SP, Garcia Rodriguez LAG, Raiford DS, Duque<br />
Oliart AD, Ris Romeu JR. Nonsteroidal anti-inflammatory drugs<br />
and the risk of hospitalization for acute renal failure. Arch Intern<br />
Med 1996;156:2433-9.<br />
194. Johnson AG, Ngyen TV, Day RO. Do non-steroidal anti-inflammatory<br />
drugs affect blood pressure: a meta-analysis. Ann Intern<br />
Med 1994;121:289-300.<br />
195. The Database of Abstracts of Reviews of Effectiveness (University<br />
of York), Database no.: DARE-948074. In: The Cochrane Library,<br />
Issue 4. Oxford: Update Software, 1999.<br />
196. Rossat J, Maillard M, Nussberger J, Brunner HR, Burnier M. Renal<br />
effects of selective cyclooxygenase-2 inhibition in normotensive<br />
salt-depleted subjects. Clin Pharmacol Ther 1999;66:76-84.<br />
197. Steinhauslin F, Munafo A, Buclin T, Macciocchi A, Biollaz J. Renal<br />
effects of nimesulide in furosemide-treated subjects. Drugs<br />
1993;46 Suppl 1:257-62.<br />
198. Carson JL, Strom BL, Duff A, Gypta A, Das K. Safety of nonsteroidal<br />
anti-inflammatory drugs with respect to acute liver disease.<br />
Arch Intern Med 1993;153:1331-6.<br />
199. Friis H, Andreasen PB. Drug-induced hepatic injury: an analysis of<br />
1100 cases reported to the Danish Committee on Adverse Drug<br />
Reactions between 1978 and 1987. J Intern Med 1992;232:133-8.<br />
200. Garcia Rodriguez LA, Williams R, Derby LE, Dean AD, Jick H.<br />
Acute liver injury associated with nonsteroidal anti-inflammatory<br />
drugs and role of risk factors. Arch Int Med 1994;154:311-6.<br />
201. Manoukian AV, Carson JL. Nonsteroidal anti-inflammatory drugassociated<br />
drug-induced hepatic disorders. Incidence and prevention.<br />
Drug Safety 1996;15:64-71.<br />
202. Boelsterli UA, Zimmerman HJ, Kretz-Rommel A. Idiosyncratic liver<br />
toxicity on nonsteroidal anti-inflammatory drugs: molecular<br />
mechanism and pathology. Cr Rev Toxicol 1995;25:207-35.<br />
203. Hoftietzer JW, Silvoso GR, Burks M, Ivey KJ. Comparison of the<br />
effects of regular and enteric-coated aspirin on gastroduodenal<br />
mucosa of man. Lancet 1980;2:609.<br />
204. Isomäki H, v. Essen R. Magblödning förorsakad av acetylsalicylsyra<br />
- tarmlösligt preparat jämfört med ett buffrat. Läkartidningen<br />
1975;1561:1561.<br />
205. Martio J. The influence of antirheumatic drugs on the occurrence<br />
of peptic ulcers. Scand J Rheumatol 1980;9:55-9.<br />
206. Weil J, Colin-Jones D, Langman M, ym. Profylactic aspirin and risk<br />
of peptic ulcer bleeding. BMJ 1995;310:827-30.<br />
207. De Craen AJM, DiGiulio G, Lampe-Schoenmaeckers AJEM, Kessels<br />
AGH, Kleijnen J. Analgesic efficacy and safety of paracetamolcodeine<br />
combinations versus paracetamol alone: a systemic review.<br />
BMJ 1996;313:321-5.<br />
208. Henry D, Lim L L-Y, Garcia Rodrigues LA, ym. Variability in risk of<br />
gastrointestinal complications with individual non-steroidal antiinflammatory<br />
drugs: results of a collaborative meta-analysis. BMJ<br />
1996;312:1563-6.<br />
209. Hallas J, Lauritsen J, Dahlsgård Villadsen H, Frenggram L. Nonsteroidal<br />
anti-inflammatory drugs and upper gastrointestinal<br />
bleeding, identifying high-risk groups by excess risk estimates.<br />
Scand J Gastroenterol 1995;30:438-44.<br />
210. Conn HG, Poynard T. Corticosteroid and peptic ulcer: meta-analysis<br />
of adverse events during steroid therapy. J Intern Med<br />
1994;236:619-32.<br />
211. Jones STM, Clague RB, Eldridge J, Jones DM. Serological evidence<br />
of infections with Helicobacter pylori may predict gastrointestinal<br />
intolerance to non-steroidal anti-inflammatory drug<br />
(NSAID) treatment in rheumatoid arthritis. Br J Rheumatol 1991;<br />
30:16-20.<br />
212. Piper JM, Wayne AR, Daugherty JR, Griffin MR. Corticosteroid<br />
use and peptic ulcer disease: role of nonsteroidal anti-inflammatory<br />
drugs. Ann Intern Med 1991;114:735-40.<br />
213. Goggin PM. Collins DA, Jazeawi RP, ym. Prevalence of Helicobacter<br />
pylori infection and its effects on symptoms and nonsteroidal<br />
anti-inflammatory drug induced gastrointestinal damage<br />
in patients with rheumatoid arthritis. Gut 1993;34:1677-80.<br />
214. Taha AS, Sturrock RD, Rusell RI. Mucosal erosions in long-term<br />
non-steroidal anti-inflammatory drug users: predisposition to<br />
ulceration and relation to Helicobacter pylori. Gut 1995;36:334-6.<br />
215. Lanza FL, Evans DG, Graham DY. Effect of Helicobacter pylori<br />
infection on the severity of gastroduodenal mucosal injury after<br />
the acute administration of naproxen or aspirin to normal volunteers.<br />
Am J Gastroenterol 1991;86:735-7.<br />
216. Pilotto A, Franceschi M, Leandro G, DiMario F, Valerio G. The<br />
effect of Helicobacter pylori infection on NSAID-related gastroduodenal<br />
damage in the elderly. Eur J Gastroenterol Hepatol<br />
1997;9:951-6.<br />
1930<br />
Suomen Gastroenterologiayhdistys ja Suomen Reumatologinen Yhdistys
217. Aalykke C. Lauritsen JM, Hallas J, Reinholdt S, Krogfelt K, Lauritsen<br />
K. Helicobacter pylori and risk of ulcer bleeding among users<br />
of nonsteroidal anti-inflammatory drugs: a case-control study.<br />
Gastroenterology 1999;116:1305-9.<br />
218. Chan FKL, Sung JJY, Chan CSY, ym. Randomised trial of eradication<br />
of Helicobacter pylori before non-steroidal anti-inflammatory<br />
drug therapy to prevent peptic ulcers. Lancet 1997;350:975-9.<br />
219. Bianchi-Porro G, Parente F, Imbesi V, Montrone F, Caruso I. Role<br />
of Helicobacter pylori in ulcer healing and recurrence of gastric<br />
and duodenal ulcers in long-term NSAID users. Response to omeprazole<br />
dual therapy. Gut 1996;39:22-6.<br />
220. Cullen DJE, Hawkey GM. Greewood DC, ym. Peptic ulcer bleeding<br />
in the elderly: relative roles of Helicobacter pylori and nonsteroidal<br />
anti-inflammatory drugs. Gut 1997;41:459-62.<br />
221. Malfertheiner P, Labenz J. Does Helicobacter pylori status affect<br />
non-steroidal anti-inflammatory drug-associated gastroduodenal<br />
pathology. Am J Med 1998;104(3A):35S-40S.<br />
222. Fries JF, Williams CA, Bloch DA, Michel BA. Nonsteroidal antiinflammatory<br />
drug-associated gastropathy: incidence and risk factor<br />
models. Am J Med 1991;91:213-23.<br />
223. Graham DY, Agrawal NM, Roth SH. Prevention of NSAID-induced<br />
gastric ulcer with misoprostol: multicentre, double-blind, plasebo-controlled<br />
trial. Lancet 1998;II:1277-80.<br />
224. Graham DY, White RH, Moreland W, Schubert TT. Katz R. Jaszemski<br />
R, Tindall E. Triandafilopoulos G, Stromall SC, Teoh LS<br />
and the Misoprostol Study Group. Duodenal and gastric ulcer<br />
prevention with misoprostol in arthritis patients taking NSAIDs.<br />
Ann Intern Med 1993;119:257-62.<br />
225. Silverstein FE, Graham DY, Senior JR, ym. Misoprostol reduces<br />
serious gastrointestinal complications in patients with rheumatoid<br />
arthritis receiving nonsteroidal anti-inflammatory drugs. Ann<br />
Intern Med 1995;123:241-9.<br />
226. Mc Kenna F. Efficacy and gastroduodenal safety of a fixed combination<br />
of diclofenac and misoprostol in the treatment of arthritis.<br />
Br J Rheumatol 1995;34 Suppl 1:11-8.<br />
227. Collen D, Bradham KD, Eisner M, ym. Primary gastroduodenal<br />
profylaxis with omeprazole for non-steroidal-anti-inflammatory<br />
drug users. Alim Pharmacol Ther 1998;12:135-40.<br />
228. Ekström P, Carling L, Wetterhus S, ym. Prevention of peptic ulcer<br />
and dyspeptic symptoms with omeprazole in patients receiving<br />
continuous non-steroidal anti-inflammatory drug therapy. Scand<br />
J Gastroenterol 1996;31:753-8.<br />
229. Koch M, Dezi A, Ferrario F, Capurso L. Prevention of nonsteroidal<br />
anti-inflammatory drug-induced gastroinestinal mucosal injury.<br />
A meta-analysis of randomized controlled clinical trials. Arch Intern<br />
Med 1996;156:2321-32.<br />
230. Jönsson B. Management of nonsteroidal anti-inflammatory drugassociated<br />
lesions: a cost-effectiveness perspective. Am J Med<br />
1998;104 (3A):81S-88S.<br />
231. Peterson WL, Cryer B. COX-1-sparing NSAIDs. Is the enthusiasm<br />
justified JAMA 1999;282:1961-3.<br />
232. Luomanmäki K, Elonen E, Vuoristo M, toim. Meilahden akuuttihoito-opas.<br />
Vammala: Kustannus Oy Duodecim, 1997.<br />
233. Vane JR, Botting RM. Mechanism of action of nonsteroidal antiinflammatory<br />
drugs. Am J Med 1998;104:2S-8S.<br />
234. Mitchell JA, Warner TD. Cyclo-oxygenase-2: pharmacology, physiology,<br />
biochemistry and relevance to NSAID therapy. Br J Pharmacol<br />
1999;128:1121-32.<br />
235. Frölich JC. A classification of NSAIDs according to the relative<br />
inhibition of cyclooxygenase isoenzymes. Trends Pharmacol Sci<br />
1997;18:30-4.<br />
236. Lanza F, Rack MF, Simon TJ, ym. Specific inhibition of cyclooxygenase-2<br />
with MK-0966 (rofecoxib) is associated with less gastroduodenal<br />
damage than either aspirin or ibuprofen. Aliment Pharmacol<br />
Ther 1999;13:761-7.<br />
237. Ehrich EW, Dallob A, De Lepeleire I, ym. Characterization of rofecoxib<br />
as a cyclooxygenase-2 isoform inhibitor and demonstration<br />
of analgesia in the dental pain model. Clin Pharmacol Ther<br />
1999;65:336-47.<br />
238. Gilroy DW, Tomlinson A, Willoughby DA. Differential effects of<br />
inhibitors of cyclooxygenase (cyclooxygenase 1 and cycloogygenase<br />
2) in acute inflammation. Eur J Pharmacol 1998;355:211-7.<br />
239. Tegeder I, Lötsch J, Krebs S, Muth-Selbach U, Brune K, Geisslinger<br />
G. Comparison of inhibitory effects of meloxicam and diclofenac<br />
on human thromboxane biosynthesis after single doses<br />
and at steady state. Clin Pharmacol Ther 1999;65:533-44.<br />
240. Panara MR, Renda G, Sciulli MG, ym. Dose-dependent inhibition<br />
of platelet cyclooxygenase-1 and monocyte cyclooxygenase-2 by<br />
meloxicam in healthy subjects. J Pharm Exp Ther 1999;290:276-<br />
80.<br />
241. Panara MR, Padovano R, Sciulli MG, ym. Effects of nimesulide on<br />
constitutive and inducible prostanoid biosynthesis in human<br />
beings. Clin Pharmacol Ther 1998;63:672-81.<br />
242. Cullen L, Kelly L, Connor SO, Fitzgerald DJ. Selective cyclooxygenase-2<br />
inhibition by nimesulide in man. J Pharm Exp Ther 1998;<br />
287:578-82.<br />
243. Anonymous. Celecoxib for arthritis. Med Lett 1999;41:11-2.<br />
SUOMEN GASTROENTEROLOGIAYHDISTYKSEN JA SUOMEN REUMATOLOGISEN YHDISTYKSEN ASETTAMA<br />
HOITOSUOSITUSTYÖRYHMÄ<br />
Vetäjä<br />
ANNA-LIISA KARVONEN, dosentti, TAYS<br />
Jäsenet<br />
MARKKU HAKALA, dosentti, OYS<br />
HANNU KANKAANRANTA, dosentti, Tampereen yliopisto<br />
EERO KIVILAAKSO, professori, HYKS<br />
ILKKA KUNNAMO, LKT, Saarijärven-Karstulan seudun terveyskeskus<br />
(Käypä hoito -toimittaja)<br />
JUHANI LEHTOLA, dosentti, OYS<br />
JUKKA MARTIO, dosentti, Reumasäätiön sairaala<br />
<strong>Tulehduskipulääkkeiden</strong> <strong>turvallinen</strong> <strong>käyttö</strong><br />
1931