HYDROMÉTALLURGIE DU ZINC
HYDROMÉTALLURGIE DU ZINC
HYDROMÉTALLURGIE DU ZINC
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Page 2 sur 5<br />
<strong>HYDROMÉTALLURGIE</strong> <strong>DU</strong> <strong>ZINC</strong>.<br />
En pratique, la lixiviation est une attaque acido-basique d'un minerai et suivant le domaine de<br />
pH dans lequel on opère, on parlera de lixiviation acide, neutre ou basique. Parfois, plusieurs lixiviations sont<br />
nécessaires pour éliminer des produits non voulus (impuretés, autres cations métalliques).<br />
La mise en solution effectuée industriellement n’est pas aussi simple car, dans la<br />
calcine, il y d’autres éléments métalliques qu’on veut éliminer au mieux, et quelquefois,<br />
des métaux importants qu’on veut récupérer ! Dans la chimie du zinc, on réalise deux<br />
lixiviations :<br />
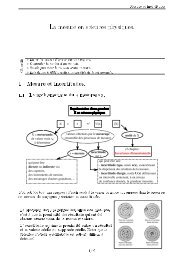
1. Lixiviation neutre.<br />
On traite d’abord la calcine provenant du grillage (ZnO impur) par une solution d’acide sulfurique à 2<br />
mol.L -1 , en présence d’air (parfois même de dioxygène)<br />
Le zinc passe en solution (pendant plusieurs heures) sous la forme d’ions Zn 2+ selon la réaction :<br />
2<br />
ZnO 2H<br />
Zn H O<br />
( s) aq ( aq)<br />
2<br />
Cette réaction acide-base exothermique élève la température vers 60 °C et augmente le pH.<br />
Ainsi, à ce stade :<br />
La solution aqueuse, vers pH = 5, contient les ions<br />
Zn 2+ , mais aussi des ions Cd 2+ , Ni 2+ , Cu 2+ , Co 2+<br />
chimiquement proches des ions zinc, ainsi que des<br />
ions Fe 2+ qui proviennent du grillage de la pyrite<br />
? Ces ions ferreux sont en faible quantité, du<br />
fait de leur oxydation par le dioxygène de l’air et<br />
de la précipitation de l’hydroxyde de fer III qui en<br />
résulte.<br />
Le solide, lui, contient le complément de zinc (> 10<br />
%) sous la forme d’un oxyde associé à l’oxyde de<br />
fer Fe 2 O 3 dans une structure stable et complexe,<br />
une ferrite de zinc de formule (ZnO, Fe 2 O 3 ).<br />
2. Lixiviation acide.<br />
Pour récupérer au maximum le zinc, le résidu solide est attaqué à chaud (vers 90 °C) par la solution<br />
aqueuse provenant de l’électrolyse : celle-ci contient en effet de l’acide sulfurique formé par l’électrolyse<br />
et encore quelques ions Zn 2+ qui n’ont pas été réduits. La ferrite est dissoute et la solution contient maintenant<br />
des ions Zn 2+ et des ions Fe 3+ . Elle contient aussi les ions métalliques qui avaient initialement précipités<br />
sous formes d’hydroxydes.<br />
De la partie solide, on peut récupérer du plomb, de l’argent et de l’or (en quantités<br />
faibles mais non négligeables).<br />
À ce stade, la solution acide contient des ions Zn 2+ et des ions Fe 3+ , dont<br />
l’élimination est difficile !<br />
Pour résoudre cette difficulté, plusieurs procédés sont utilisés qui permettent tous d’obtenir des précipités<br />
plus complexes, mais facilement filtrables, ce qui n’était pas le cas de l’hydroxyde de fer III.<br />
Après les lixiviations, la solution (acide) contient, outre les ions Zn 2+ , un certain<br />
nombre de cations métalliques : Cd 2+ , Ni 2+ , Cu 2+ , Co 2+ , Mn 2+<br />
II. Cémentation de la solution.<br />
L’élimination des impuretés est nécessaire, d’abord pour obtenir du zinc très pur, et aussi parce que<br />
les aspects cinétiques des réactions d’électrolyse pourraient se trouver modifiés du fait de leur présence<br />
!<br />
L’élimination de la plupart d’entre eux est effectuée par cémentation, c’est à dire par réduction des<br />
cations métalliques par un autre métal. Comme on ne veut pas introduire d’autres ions métalliques en<br />
solution, il faut utiliser du zinc, lui même comme réducteur.<br />
Le terme cémentation définit (du moins dans ce contexte d'hydrométallurgie) une<br />
opération qui consiste à faire précipiter un métal en solution à l'aide d'un autre<br />
métal.