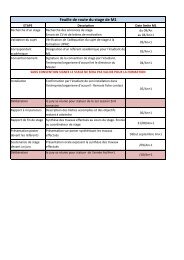
Master Energétique et Environnement : TP Energie Solaire
Master Energétique et Environnement : TP Energie Solaire
Master Energétique et Environnement : TP Energie Solaire
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Master</strong> Energétique <strong>et</strong> <strong>Environnement</strong> : <strong>TP</strong> <strong>Energie</strong> <strong>Solaire</strong><br />
Page |<br />
25<br />
La batterie au plomb acide est la forme de stockage de l’énergie électrique la pluscourante, en<br />
raison de son coût qui est relativement faible <strong>et</strong> d’une large disponibilité. Parcontre, lesbatteries<br />
nickel-cadmium sont plus chères, elles sont utilisées dans lesapplications ou la fiabilité est vitale.<br />
Composition d'une batterie solaire plomb- Acide [14] :<br />
Ces batteries sont composées de plusieurs plaques de plomb dans une solution<br />
d'acidesulfurique. La plaque consiste en une grille d'alliage de Plomb avec une pâte d'oxyde deplomb<br />
marqu<strong>et</strong>ée sur la grille. La solution acide sulfurique <strong>et</strong> l’eau est appelée électrolyte.<br />
Figure 34: Construction d'une batterie monobloc<br />
Les plaques sont alternées dans la batterie, avec des séparateurs entre elles, qui sontfabriqués<br />
d'un matériel poreux qui perm<strong>et</strong> le flux de l'électrolyte. Ils sont électriquementnon conducteurs, ils<br />
peuvent être des mélanges de silice <strong>et</strong> de matières plastiques ougommes.<br />
Un groupe de plaques positives <strong>et</strong> négatives, avec des séparateurs, constituent un"élément".<br />
Un élément dans un container plongé dans un électrolyte constitue une "cellule"de batterie.<br />
Indépendamment de la taille des plaques, une cellule fournira une tension variant entre 1,7<strong>et</strong><br />
2 volts suivant l’état de charge en conductions nominales de fonctionnement, <strong>et</strong> unrendement<br />
énergétique de l’ordre de 70% à 85%(pour plomb- Acide).Une batterie est constituée par plusieurs<br />
cellules ou des éléments reliés en série, interneou externe, pour augmenter le voltage à des valeurs<br />
normales aux applications électriques.<br />
Principe de fonctionnement :<br />
Une réaction chimique intervient lorsque la batterie alimente une charge connectée à cesdeux<br />
électrodes. Pendant la décharge, il y a une oxydation à la plaque négative qui s<strong>et</strong>raduit par une perte<br />
d'électrons <strong>et</strong> réduction à la plaque positive ou gain d'électrons.L'électrolyte en présence dans la<br />
batterie facilite le déplacement des chargesélectrochimiques sous forme d'ions. Le processus inverse<br />
se produit quand la batterie serecharge on voit apparaître immédiatement une force électromotrice<br />
entre les deuxélectrodes. Les équations des réactions suivantes décrivent la réaction principale:<br />
Electrode Positive:<br />
+ − − Déch arge<br />
PbO 2+ 3H3O + HSO<br />
4<br />
+ 2e ←⎯⎯ ⎯⎯⎯⎯→ ⎯ P<br />
Ch arge<br />
bSO 4+<br />
5H2O<br />
dioxyde de plomb + acide sulfurique + 3 ions hydrogène + 2 électrons = sulfate de plomb +<br />
2eau<br />
Electrode négative:<br />
− Déch arge<br />
+ −<br />
P<br />
b+ HSO<br />
4<br />
+H2O ←⎯⎯ ⎯⎯⎯⎯→ ⎯ P<br />
Ch arge<br />
bSO 4+<br />
H3O +2e<br />
plomb + acide sulfurique = sulfate de plomb + 2 électrons + ion hydrogène<br />
Equation bilan:<br />
Déch arge<br />
Pb + PO<br />
b 2+ 2HSO<br />
2 4 ←⎯⎯ ⎯⎯⎯⎯→ ⎯ 2PSO<br />
Ch arge<br />
b 4+<br />
2HO<br />
2<br />
L'équation bilan de l'élément traduit une consommation d'acide sulfurique<strong>et</strong> une production<br />
d'eau lors de la décharge d'un élément.<br />
UPMC | Contact : philippe.guibert@upmc.fr<br />
Exemplaire provisoire