Etude de fonctionnement de l'écosystème prairial en conditions de ...
Etude de fonctionnement de l'écosystème prairial en conditions de ...
Etude de fonctionnement de l'écosystème prairial en conditions de ...
- No tags were found...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
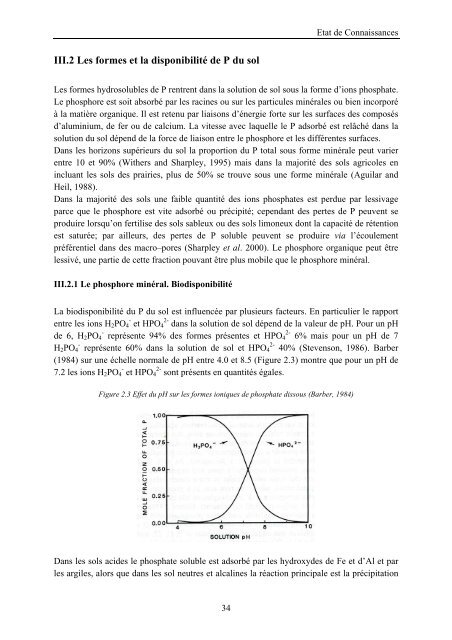
Etat <strong>de</strong> ConnaissancesIII.2 Les formes et la disponibilité <strong>de</strong> P du solLes formes hydrosolubles <strong>de</strong> P r<strong>en</strong>tr<strong>en</strong>t dans la solution <strong>de</strong> sol sous la forme d’ions phosphate.Le phosphore est soit absorbé par les racines ou sur les particules minérales ou bi<strong>en</strong> incorporéà la matière organique. Il est ret<strong>en</strong>u par liaisons d’énergie forte sur les surfaces <strong>de</strong>s composésd’aluminium, <strong>de</strong> fer ou <strong>de</strong> calcium. La vitesse avec laquelle le P adsorbé est relâché dans lasolution du sol dép<strong>en</strong>d <strong>de</strong> la force <strong>de</strong> liaison <strong>en</strong>tre le phosphore et les différ<strong>en</strong>tes surfaces.Dans les horizons supérieurs du sol la proportion du P total sous forme minérale peut varier<strong>en</strong>tre 10 et 90% (Withers and Sharpley, 1995) mais dans la majorité <strong>de</strong>s sols agricoles <strong>en</strong>incluant les sols <strong>de</strong>s prairies, plus <strong>de</strong> 50% se trouve sous une forme minérale (Aguilar andHeil, 1988).Dans la majorité <strong>de</strong>s sols une faible quantité <strong>de</strong>s ions phosphates est perdue par lessivageparce que le phosphore est vite adsorbé ou précipité; cep<strong>en</strong>dant <strong>de</strong>s pertes <strong>de</strong> P peuv<strong>en</strong>t seproduire lorsqu’on fertilise <strong>de</strong>s sols sableux ou <strong>de</strong>s sols limoneux dont la capacité <strong>de</strong> rét<strong>en</strong>tionest saturée; par ailleurs, <strong>de</strong>s pertes <strong>de</strong> P soluble peuv<strong>en</strong>t se produire via l’écoulem<strong>en</strong>tpréfér<strong>en</strong>tiel dans <strong>de</strong>s macro–pores (Sharpley et al. 2000). Le phosphore organique peut êtrelessivé, une partie <strong>de</strong> cette fraction pouvant être plus mobile que le phosphore minéral.III.2.1 Le phosphore minéral. BiodisponibilitéLa biodisponibilité du P du sol est influ<strong>en</strong>cée par plusieurs facteurs. En particulier le rapport<strong>en</strong>tre les ions H 2 PO - 4 et HPO 2- 4 dans la solution <strong>de</strong> sol dép<strong>en</strong>d <strong>de</strong> la valeur <strong>de</strong> pH. Pour un pH-<strong>de</strong> 6, H 2 PO 4 représ<strong>en</strong>te 94% <strong>de</strong>s formes prés<strong>en</strong>tes et HPO 2- 4 6% mais pour un pH <strong>de</strong> 7H 2 PO - 4 représ<strong>en</strong>te 60% dans la solution <strong>de</strong> sol et HPO 2- 4 40% (Stev<strong>en</strong>son, 1986). Barber(1984) sur une échelle normale <strong>de</strong> pH <strong>en</strong>tre 4.0 et 8.5 (Figure 2.3) montre que pour un pH <strong>de</strong>7.2 les ions H 2 PO - 4 et HPO 2- 4 sont prés<strong>en</strong>ts <strong>en</strong> quantités égales.Figure 2.3 Effet du pH sur les formes ioniques <strong>de</strong> phosphate dissous (Barber, 1984)Dans les sols aci<strong>de</strong>s le phosphate soluble est adsorbé par les hydroxy<strong>de</strong>s <strong>de</strong> Fe et d’Al et parles argiles, alors que dans les sol neutres et alcalines la réaction principale est la précipitation34