PEDOMAN PENILAIAN REGISTRASI - Direktorat Jenderal Bina ...
PEDOMAN PENILAIAN REGISTRASI - Direktorat Jenderal Bina ...
PEDOMAN PENILAIAN REGISTRASI - Direktorat Jenderal Bina ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
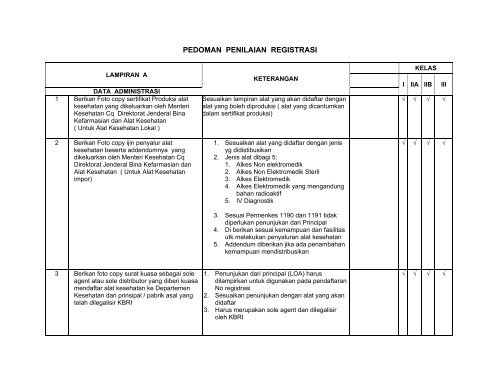
<strong>PEDOMAN</strong> <strong>PENILAIAN</strong> <strong>REGISTRASI</strong><br />
LAMPIRAN A<br />
DATA ADMINISTRASI<br />
1 Berikan Foto copy sertifikat Produksi alat<br />
kesehatan yang dikeluarkan oleh Menteri<br />
Kesehatan Cq <strong>Direktorat</strong> <strong>Jenderal</strong> <strong>Bina</strong><br />
Kefarmasian dan Alat Kesehatan<br />
( Untuk Alat Kesehatan Lokal )<br />
2 Berikan Foto copy ijin penyalur alat<br />
kesehatan beserta addendumnya yang<br />
dikeluarkan oleh Menteri Kesehatan Cq<br />
<strong>Direktorat</strong> <strong>Jenderal</strong> <strong>Bina</strong> Kefarmasian dan<br />
Alat Kesehatan ( Untuk Alat Kesehatan<br />
impor)<br />
KETERANGAN<br />
Sesuaikan lampiran alat yang akan didaftar dengan<br />
alat yang boleh diproduksi ( alat yang dicantumkan<br />
dalam sertifikat produksi)<br />
1. Sesuaikan alat yang didaftar dengan jenis<br />
yg didistibusikan<br />
2. Jenis alat dibagi 5:<br />
1. Alkes Non elektromedik<br />
2. Alkes Non Elektromedik Steril<br />
3. Alkes Elektromedik<br />
4. Alkes Elektromedik yang mengandung<br />
bahan radioaktif<br />
5. IV Diagnostik<br />
3. Sesuai Permenkes 1190 dan 1191 tidak<br />
diperlukan penunjukan dari Principal<br />
4. Di berikan sesuai kemampuan dan fasilitas<br />
utk melakukan penyaluran alat kesehatan<br />
5. Addendum diberikan jika ada penambahan<br />
kemampuan mendistribusikan<br />
KELAS<br />
I IIA IIB III<br />
√ √ √ √<br />
√ √ √ √<br />
3 Berikan foto copy surat kuasa sebagai sole<br />
agent atau sole distributor yang diberi kuasa<br />
mendaftar alat kesehatan ke Departemen<br />
Kesehatan dari prinsipal / pabrik asal yang<br />
telah dilegalisir KBRI<br />
1. Penunjukan dari principal (LOA) harus<br />
dilampirkan untuk digunakan pada pendaftaran<br />
No registrasi<br />
2. Sesuaikan penunjukan dengan alat yang akan<br />
didaftar<br />
3. Harus merupakan sole agent dan dilegalisir<br />
oleh KBRI<br />
√ √ √ √
4 Berikan certificate of free sale dari lembaga<br />
yang berwewenang<br />
• Certificate of free sale adalah bukti bahwa alat<br />
tersebut telah beredar di Negara dimana alat<br />
tersebut dibuat<br />
• CFS harus mencantumkan nama alat<br />
kesehatan dan nama pabrik dan masih<br />
berlaku ( max 2 tahun jika tidak<br />
mencantumkan batas waktu)<br />
• CFS tidak perlu dilegalisir KBRI<br />
• Certificate Of Export dimana alat tersebut<br />
hanya khusus di ekspor dan tidak diregistrasi<br />
di negaranya , TIDAK DAPAT DIANGGAP<br />
SEBAGAI CFS.<br />
• Beberapa negara mencantumkan Cert of<br />
export tetapi didalamnya tertulis telah<br />
diregistrasi - boleh dianggap sbg CFS<br />
• CFS dari Commerce setempat boleh diterima<br />
utk alat tertentu jika ada pernyataan dari<br />
instansi berwenang di negaranya bahwa alat<br />
tersebut tidak didaftar<br />
• Untuk Principal dari negara Europa, CE dapat<br />
menggantikan CFS.<br />
• Utk negara lain ( India, China dll) CE harus<br />
diberikan bersama dengan keterangan lain<br />
dari FDA setempat<br />
• CFS boleh dari negara bukan pembuat tapi<br />
negara tempat legal manufacturenya<br />
- √ √ √
6 Ringkasan eksekutif alat kesehatah :<br />
− Tinjauan ringkas mengenai deskripsi alat<br />
kesehatan beserta mekanisme kerjanya<br />
bila ada<br />
−<br />
−<br />
−<br />
−<br />
Sejarah pemasaran<br />
Tujuan penggunaan dan indikasi pada<br />
label<br />
Jika belum memiliki ijin edar dari negara<br />
lain yang diakui harus memberikan<br />
informasi tentang status tunggu tersebut<br />
Informasi penting tentang keamanan atau<br />
kinerja alat<br />
7 Salinan /fotokopi sertifikasi dan dokumen<br />
yang menyebutkan kesesuaian terhadap<br />
standar produk, persyaratan keamanan,<br />
efektivitas dan sistem mutu dalam desain<br />
dan proses pembuatan<br />
Adalah ringkasan umum dari alat kesehatan<br />
termasuk didalam nya al: :<br />
1. Prinsip penggunaan.<br />
2. Penjelasan fungsi dari setiap komponen,<br />
komponen atau material yang digunakan<br />
terutama yang langsung bersentuhan<br />
dengan pasien atau pengguna.<br />
3. Jika alat kesehatan mengandung obat maka<br />
harus dijelaskan hasil evaluasi dari institusi<br />
yang bertanggung jawab terhadap<br />
keamanan dan kemanfaatan dari obat yang<br />
di gunakan ( data dari Principal kecuali jika<br />
dibutuhkan data dari institusi yang<br />
bertanggung jawab di Indonesia)<br />
4. Dokumen berupa hasil pengujian produk<br />
.<br />
• ISO 13485 untuk Quality System<br />
• GMP<br />
• Kecuali untuk alat kesehtan kelas I tertentu<br />
( sikat Gigi) boleh digantikan dengan ISO<br />
9000<br />
• ISO 14921 tentang Risk maagement khusus<br />
produk dengan resiko tinggi<br />
• IEC 60-601 untuk keamanan Listrik<br />
• COA Produk jadi<br />
• Wire design utk Alkes Elek resiko tinggi<br />
√ √ √ √<br />
√ √ √ √<br />
• Dokumen harus menjelaskan metode umum<br />
yang digunakan untuk deklarasi kesesuain<br />
terhadap prinsip dasar dari keamanan dan<br />
kinerja alat kesehatan.<br />
• Dapat menggunakan standar internasional<br />
atau standar lain yang diakui, teknologi terkini<br />
atau metode yang digunakan oleh industri itu<br />
sendiri, perbandingan dengan produk sejenis<br />
di pasaran dan lain-lain.
• Harus mencantumkan seluruh judul dari<br />
standar yang diacu, nomor dan tanggal<br />
penetapan standar, serta organisasi yang<br />
membuat standar tersebut<br />
• Jika pabrik menggunakan standar lain seperti<br />
standar internal maka harus mencantumkan<br />
sumbernya<br />
• Bukti kesesuaian dapat dibuat dalam bentuk<br />
tabel dengan dokumen pendukung yang<br />
mungkin untuk penilaian sesuai dengan<br />
persyaratan. Contoh daftar pemeriksaan<br />
kesesuaian dengan Prinsip Utama terdapat<br />
pada Lampiran (1)<br />
8 Berikan standar yang digunakan dan bukti<br />
kesesuaian terhadap standar tersebut<br />
• Mengacu pada standart produk misal SNI,<br />
ISO Produk dll<br />
LAMPIRAN B<br />
KELAS<br />
KETERANGAN<br />
INFORMASI ALAT KESEHATAN I IIA IIB III<br />
1 Uraian alat (Menurut Klasifikasi) √ √ √ √<br />
Uraian A B C D<br />
Uraian alat termasuk<br />
− cara penggunaan<br />
− indikasi penggunaan alat<br />
− brosur<br />
− material produk<br />
− kadaluwarsa ( hanya untuk produk steril)<br />
2 Deskripsi dan fitur Alat Kesehatan • Gambaran yang lebih detail untuk menjelaskan:<br />
fungsi dari alat, konsep ilmiah dasar yang<br />
digunakan untuk mendasari penggunaan alat<br />
(termasuk wiring untuk alkes elektromedik),<br />
• komponen material dan aksesori yang<br />
digunakan pada pengoperasian alat<br />
pengemasan<br />
√<br />
Jika<br />
ada<br />
√<br />
Jika<br />
ada<br />
√<br />
Jika<br />
ada<br />
√<br />
Jika<br />
ada
• uraian lengkap dari fungsi setiap komponen,<br />
material atau bahan dari alat, dilengkapi<br />
dengan penandaan, diagram, foto, gambar<br />
teknis atau sejenisnya jika diperlukan<br />
3 Tujuan Penggunaan • Yang dimaksud di sini adalah penggunaan<br />
yang sesuai dengan tujuan penggunaan alat,<br />
yang dilengkapi dengan data yang disediakan<br />
oleh pabrik alat kesehatan dalam bentuk<br />
petunjuk penggunaan serta kemampuan<br />
fungsional dari alat<br />
4 Indikasi • Uraian umum dari penyakit atau kondisi dimana<br />
alat kesehatan dapat mendiagnosa, merawat,<br />
mencegah, atau meringankan, serta meliputi<br />
uraian dari target pasien yang dituju.<br />
5 Petunjuk penggunaan • Semua informasi yang diperlukan dari pabrik<br />
alat kesehatan terkait penggunaan, termasuk<br />
prosedur, metode, frekuensi, durasi , jumlah<br />
dan cara penyiapan yang harus diikuti untuk<br />
keamanan.<br />
√ √ √ √<br />
√ √ √ √<br />
√ √ √ √<br />
• Petunjuk yang diperlukan untuk dapat<br />
menggunakan alat dengan cara yang<br />
aman.yang terdapat pada alat atau kemasan<br />
6 Kontra indikasi • Kontra indikasi adalah kondisi dimana alat tidak<br />
dapat digunakan karena dapat menimbulkan<br />
resiko yang lebih besar dari keuntungannya.<br />
√ √ √ √<br />
• Merupakan uraian umum dari penyakit atau<br />
kondisi pasien yang tidak boleh menggunakan<br />
alat tersebut untuk tujuan diagnosa, perawatan,<br />
penyembuhan atau meringankan penyakit<br />
• Misal: IUD tidak boleh digunakan utk wanita<br />
hamil
7 Peringatan • Informasi mengenai bahaya yang mungkin<br />
dapat terjadi, yang harus diketahui oleh<br />
pengguna sebelum menggunakan alat.<br />
Misal : penggunaan Stent Jantung dapat<br />
terjadi restenosis<br />
√ √ √ √<br />
• Peringatan termasuk siapa yang boleh<br />
menggunakan alat tersebut<br />
• Misal : Filler, Silikon hanya boleh dikerjakan<br />
oleh dokter ahli<br />
8 Perhatian • Perhatian kepada pengguna mengenai hal-hal<br />
yang perlu diperhatikan untuk menjamin<br />
keamanan dan kemanfaatan alat dalam<br />
penggunaan<br />
√ √ √ √<br />
• Perhatian ini termasuk hal-hal yang perlu<br />
dilakukan untuk menghindari efek terhadap<br />
pasien/ pengguna alat yang tidak berpotensi<br />
mengancam jiwa atau menimbulkan cidera<br />
serius, tetapi perlu diketahui oleh pengguna<br />
alat.<br />
• Perhatian ini dapat membuat pengguna<br />
waspada terhadap efek yang tidak diinginkan<br />
dari penggunaan atau kesalahan penggunaan<br />
alat dan hal-hal yang diperlukan untuk<br />
menghindari efek tersebut<br />
• Misalnya: Jangan digunakan jika kemasan<br />
sudah rusak.
9 Potensi efek yang tidak diinginkan • Potensi efek yang tidak diinginkan dan<br />
berakibat serius (kematian, cidera atau<br />
kejadian serius lainnya) terhadap pasien atau<br />
pengguna atau efek samping yang ditimbulkan<br />
pada penggunaan alat kesehatan secara<br />
normal<br />
√<br />
√<br />
10 Alternatif Terapi • Merupakan uraian dari cara atau prosedur<br />
alternatif untuk mendiagnosa, merawat,<br />
mengobati atau meringankan penyakit yang<br />
merupakan tujuan penggunaan alat tersebut<br />
11 Material • Uraian dari material penyusun alat kesehatan<br />
serta sifat fisik yang diperlukan untuk<br />
membuktikan kesesuaian dengan Prinsip<br />
utama yang berhubungan dengan keamanan<br />
dan kinerja alat<br />
√ √ √ √<br />
√ √ √<br />
• Informasi yang diberikan harus meliputi bahan<br />
kimia, biologis, dan karakter fisik dari<br />
komponen alat kesehatan secara lengkap<br />
12 Informasi pabrik • Merupakan ringkasan berisi dokumentasi yang<br />
berhubungan dengan proses produksi,<br />
termasuk pengukuran jaminan mutu, yang<br />
memadai sesuai dengan tingkat kerumitan dan<br />
tingkat resiko alat.<br />
13 Proses produksi • Proses pembuatan alat harus mencakup<br />
sumber daya dan kegiatan yang dilakukan<br />
untuk mengubah masukan menjadi keluaran<br />
yang diinginkan<br />
√ √ √ √<br />
√ √ √ √<br />
• Proses pembuatan alat harus meliputi metode<br />
dan cara pembuatan, kondisi, lingkungan<br />
pembuatan, fasilitas dan pengendalian yang<br />
digunakan untuk pembuatan, pemprosesan,<br />
pengemasan, penandaan dan penyimpanan<br />
alat.
• Sertakan ringkasan tentang metode dan<br />
proses sterilisasi (untuk produk steril) .<br />
• Perusahaan yang dikontrak oleh pabrik alat<br />
kesehatan untuk membuat atau memproses<br />
alat harus menyerahkan semua atau<br />
sebagian dari informasi pembuatan yang<br />
sesuai dengan fasilitas mereka kepada<br />
pemerintah<br />
LAMPIRAN C<br />
KELAS<br />
KETERANGAN<br />
SPESIFIKASI DAN JAMINAN MUTU I IIA IIB III<br />
1 Spesifikasi Karakteristik fungsional dan spesifikasi kinerja<br />
teknis alat untuk membuktikan kesesuaian dengan<br />
Prinsip utama meliputi:<br />
• akurasi,, sensitivitas,,spesifisitas alat ukur dan<br />
alat diagnostik<br />
• keandalan (reliabilitias)<br />
• spesifikasi lain yang terkait termasuk kimia,<br />
fisika, elektrik, mekanis, biologi, piranti lunak,<br />
sterilitas, stabilitas, penyimpanan,<br />
pengangkutan dan pengemasan<br />
2 Informasi tambahan • Informasi penting tentang karakteristik alat<br />
yang belum dicantumkan pada bagian<br />
sebelumnya, yang diperlukan untuk<br />
membuktikan kesesuaian terhadap Prinsip<br />
utama (contoh: kategori biokompatibilitas<br />
untuk produk jadi)<br />
√ √ √ √<br />
√ √ √<br />
• CATATAN : Untuk alat kesehatan sederhana<br />
dengan resiko rendah, informasi di atas<br />
umumnya sudah tercakup dalam brosur<br />
penjualan, petunjuk penggunaan dan lain-lain<br />
3 Ringkasan dari verifikasi rancangan dan<br />
dokumen validasi<br />
• Ringkasan atau referensi atau verifikasi √<br />
Steri<br />
√<br />
√
desain dan data validasi desain yang<br />
diperlukan, sesuai dengan tingkat kerumitan<br />
dan resiko dari alat<br />
l<br />
• Validasi data report meliputi<br />
• test design description<br />
• complete test or study protocols<br />
• methods of data analysis<br />
• data summaries<br />
• test conclusions<br />
• Verifikasi dan validasi data alat kes juga<br />
meliputi:<br />
1. Pernyataan/sertifikat kesesuaian<br />
terhadap standar yang sudah diakui,<br />
yang digunakan oleh pabrik alat<br />
kesehatan, dan/ atau<br />
2. Ringkasan/ hasil pengujian dan<br />
evaluasi yang berdasarkan standar,<br />
metode dan pengujian dari pabrik atau<br />
cara lain untuk membuktikan<br />
kesesuaian<br />
3. pernyataan kesesuaian terhadap<br />
standar atau sertifikat lain yang<br />
diberikan oleh regulator yang<br />
berwenang dan ringkasan data hasil<br />
pengujian,<br />
4 Studi pre-klinis Studi Klinis harus meliputi :<br />
• uji biokompatibilitas yang dilakukan terhadap<br />
material dari alat kesehatan.<br />
• dilakukan pada produk jadi dan produk steril.<br />
Informasi pengujian, hasil dan analisa data<br />
harus diberikan<br />
• tujuan, metodologi, hasil dan kesimpulan dari<br />
pabrik alat kesehatan terhadap keseluruhan<br />
penelitian fisik alat kesehatan dan komponen<br />
√<br />
√
• Pengujian fisik harus dilakukan untuk<br />
memperkirakan kemampuan respon alat<br />
terhadap tekanan fisiologi, kondisi dan gaya<br />
yang tidak diinginkan, penggunaan jangka<br />
panjang dan semua hal yang dapat<br />
menyebabkan kegagalan<br />
• Uji pre-klinis pada hewan yang mendukung<br />
kemungkinan efektifitas pada manusia harus<br />
dilaporkan<br />
• Kesimpulan penelitian harus memuat interaksi<br />
alat kesehatan dengan cairan dan jaringan<br />
hewan serta efektivitas fungsional alat pada<br />
hewan percobaan. Alasan (dan keterbatasan)<br />
dari pemilihan hewan percobaan tertentu<br />
harus dijelaskan<br />
5 Pengujian Validasi piranti lunak ( jika<br />
dapat diterapkan)<br />
• Pabrik harus memberikan bukti validasi<br />
desain dan proses pengembangan piranti<br />
lunak.<br />
√<br />
√<br />
• Informasi harus meliputi hasil seluruh<br />
verifikasi, validasi dan uji yang dilakukan<br />
internal dan pada lingkungan pengguna,<br />
sebelum pelepasan akhir, untuk semua<br />
konfigurasi piranti keras yang berbeda<br />
dicantumkan pada penandaan, serta datadata<br />
yang mewakili dari kedua lingkungan uji.<br />
6 Alat yang mengandung material biologi Berikan hasil penelitian yang meliputi:<br />
• Kecukupan pengukuran yang berhubungan<br />
dengan material yang mempunyai resiko<br />
dapat menularkan. Pernyataan bebas virus<br />
dari bahaya yang sudah diketahui.<br />
• Penjelasan penapisan donor dan metode<br />
pengambilannya<br />
• Hasil validasi proses untuk menunjukan<br />
proses produksi sudah dapat meminimalkan<br />
resiko biologis
7 Bukti Klinis • Investigasi klinis terutama diperlukan oleh alat<br />
kesehatan dengan resiko yang lebih tinggi atau<br />
untuk alat kesehatan yang tidak atau sedikit<br />
sekali memiliki bukti klinis.<br />
- - √ √<br />
• Bukti klinis berupa:<br />
‣ Studi klinik ( melalui investigasi Klinik yang<br />
dilakukan di dalam atau diluar negeri.<br />
Meliputi tujuan, metodologi dan hasil yang<br />
sesuai cakupan uji klinis, jelas dan<br />
bermakna. Kesimpulan dari hasil uji klinis<br />
harus didahului dengan pembahasan sesuai<br />
literatur yang sudah dipublikasikan<br />
‣ Daftar Pustaka /Literatur .Lampirkan semua<br />
salinan literatur/Pustaka. Harus spesifik<br />
untuk alat tersebut berdasarkan kronologis<br />
dan masih berlaku<br />
‣ Bukti klinis dapat diperoleh dari publikasi<br />
yang berhubungan dengan literatur ilmiah<br />
hasil penelaahan bersama<br />
9 Hasil analisa resiko ‣ Uraian kemungkinan bahaya yang dapat<br />
terjadi pada penggunaan alat .<br />
- - √ √<br />
‣ Meliputi resiko tidak langsung dari alat<br />
kesehatan yang diakibatkan oleh :<br />
1. bahaya dari alat penyerta seperti bagian<br />
bergerak yang dapat menyebabkan cidera<br />
yang berkelanjutan,<br />
2. bahaya yang berhubungan dengan<br />
pengguna, misalkan radiasi ionisasi dari<br />
mesin X-ray.<br />
‣ Penilaian terhadap resiko dibandingkan<br />
dengan keuntungan dari alat dan metode<br />
yang digunakan untuk mengurangi resiko<br />
sampai ke tingkat yang dapat diterima harus
dijabarkan.<br />
‣ Teknik yang digunakan untuk melakukan<br />
analisa resiko harus disebutkan secara rinci<br />
‣ Orang/organisasi yang melakukan analisis<br />
resiko harus disebutkan dengan jelas.<br />
LAMPIRAN D<br />
KELAS<br />
KETERANGAN<br />
PENANDAAN DAN PETUNJUK PENGGUNAAN I IIA IIB III<br />
1 Penandaan Merupakan uraian dan informasi produk yang<br />
melekat pada alat, selama alat tersebut dijual atau<br />
dikirimkan, seperti manual untuk dokter, penandaan<br />
pada kemasan, materi promosi, brosur produk dan<br />
sebagainya.<br />
Contoh penandaan pada alat dan kemasannya<br />
− Petunjuk penggunaan<br />
− Literatur lain atau bahan pelatihan<br />
− Petunjuk pemasangan dan pemeliharaan ( jika<br />
dapat diterapkan)<br />
Setiap informasi dan petunjuk yang diberikan<br />
kepada pasien, termasuk petunjuk untuk setiap<br />
prosedur yang harus dilakukan oleh pasien<br />
√ √ √ √<br />
2 Contoh penandaan pada alat dan<br />
kemasannya<br />
• Informasi produk dalam bentuk cetakan,<br />
tulisan atau grafik pada atau melekat pada<br />
satu atau lebih kemasan, termasuk kemasan<br />
luar atau pembungkus wadah luar.<br />
• Setiap penandaan kemasan yang tidak<br />
tersedia pada kemasan luar harus mudah<br />
dilihat dari kemasan luar<br />
• Jika tidak dimungkinkan untuk menyertakan<br />
contoh dari penandaan (misal penandaan<br />
peringatan berukuran besar yang direkatkan<br />
pada mesin X-ray), maka cukup diberikan<br />
√ √ √ √
3 Petunjuk penggunaan, materi<br />
pelatihan & petunjuk pemasangan<br />
dan pemeliharaan<br />
contoh dengan menggunakan metode<br />
alternatif (seperti foto atau gambar teknis),<br />
• Petunjuk penggunaan umumnya merujuk pada<br />
buku panduan dokter, panduan pengguna,<br />
panduan operator, panduan pemberi resep<br />
atau panduan rujukan dan pengguna akhir<br />
dapat menggunakan alat dengan aman dan<br />
sesuai dengan tujuan<br />
• Bagian ini harus berisi informasi tentang<br />
indikasi, kontraindikasi, peringatan, perhatian,<br />
kemungkinan adanya efek yang tidak<br />
diinginkan , alternatif terapi dan kondisi yang<br />
harus diatur selama penggunaan normal untuk<br />
mempertahankan keamanan dan efektifitas<br />
alat. Jika dapat diterapkan, bagian ini harus<br />
termasuk petunjuk untuk pelatihan bagi<br />
pengguna akhir agar mampu menggunakan<br />
alat sesuai dengan tujuannya, serta melakukan<br />
pemasangan dan pemeliharaan alat.<br />
√ √ √ √<br />
LAMPIRAN E<br />
KELAS<br />
KETERANGAN<br />
POST MARKET EVALUATION I IIA IIB III<br />
1 Berikan Prosedur yang digunakan dan<br />
sistem Pencatatan, Penanganan<br />
komplain , Laporan Kejadian Efek yang<br />
tidak diinginkan dan prosedur Recall