12 - Proteine fosfatasi pp 158-218.pdf - Corso di Laurea in Biologia
12 - Proteine fosfatasi pp 158-218.pdf - Corso di Laurea in Biologia
12 - Proteine fosfatasi pp 158-218.pdf - Corso di Laurea in Biologia
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong><br />
Ora che abbiamo completato la rassegna delle prote<strong>in</strong>e c<strong>in</strong>asi, ve<strong>di</strong>amo <strong>in</strong> dettaglio gli enzimi che<br />
determ<strong>in</strong>ano la rimozione del fosfato da prote<strong>in</strong>e. L’attività <strong>di</strong> tali enzimi è <strong>in</strong><strong>di</strong>spensabile per<br />
assicurare fenomeni ciclici <strong>di</strong> attivazione – <strong>di</strong>sattivazione <strong>di</strong> prote<strong>in</strong>e bersaglio. Si pensi alla<br />
glicogeno fosforilasi, che da b viene portata nella forma a (attiva) me<strong>di</strong>ante fosforilazione della<br />
Ser14 della glicogeno fosforilasi. L’attività <strong>fosfatasi</strong>ca garantisce il ritorno della a nella forma b e,<br />
pertanto, è <strong>in</strong>staurato un ciclo.<br />
Anche la p34 cdc-2 va <strong>in</strong>contro a tali meccanismi fosfo-defosfo (defosfo Tyr-15 ≡ cdc-2 attiva; forma<br />
fosfo Tyr-15 ≡ cdc-2 <strong>in</strong>attiva).<br />
Le prote<strong>in</strong>e <strong>fosfatasi</strong> ra<strong>pp</strong>resentano una famiglia molto numerosa <strong>di</strong> prote<strong>in</strong>e. (Nel 2000 si sa che<br />
nel genoma umano: circa 2000 prote<strong>in</strong>e c<strong>in</strong>asi e poche prote<strong>in</strong>e <strong>fosfatasi</strong>). (Nel lievito <strong>12</strong>4 c<strong>in</strong>asi e<br />
37 <strong>fosfatasi</strong> subunità catalitica). Per razionalizzare lo stu<strong>di</strong>o è stato stabilito un criterio <strong>di</strong><br />
classificazione. È stato scelto un substrato ben conosciuto: la glicogeno fosforilasi c<strong>in</strong>asi (GPK).<br />
In particolare:<br />
<strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong> tipo 1 (PP1) sono quelle <strong>fosfatasi</strong> che determ<strong>in</strong>ano la rimozione idrolitica del P<br />
dalla subunità β della GPK (ve<strong>di</strong> pag.<strong>12</strong>3). PP1 agiscono su β.<br />
<strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong> tipo 2 (PP2) sono gli enzimi <strong>fosfatasi</strong> che determ<strong>in</strong>ano la rimozione idrolitica<br />
del P dalla subunità α della GPK. PP2 agiscono su α.<br />
Questo criterio era già stato <strong>in</strong>trodotto quando si è parlato del ciclo della GPK (ve<strong>di</strong> pag.<strong>12</strong>3).<br />
Sono stati <strong>in</strong>oltre identificati pepti<strong>di</strong> che sono <strong>in</strong>ibitori solo delle PP1. Sono prote<strong>in</strong> phosphatase<br />
<strong>in</strong>ibitor 1 e prote<strong>in</strong> phosphatase <strong>in</strong>ibitor 2 – PPI1 e PPI2 – con PM 19000 e 23000.<br />
<strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong> 1 (PP1)<br />
La PP1 è <strong>di</strong>rettamente implicata nell’<strong>in</strong>terconversione della glicogeno fosforilasi e della glicogeno<br />
s<strong>in</strong>tetasi. L’attività della PP1 è <strong>di</strong>rettamente collegata alla presenza o meno <strong>di</strong> <strong>in</strong>ibitori proteici che<br />
possono, a loro volta, essere fosforilati o defosforilati. In particolare, solo PPI1 può essere<br />
fosforilato <strong>in</strong> una treon<strong>in</strong>a dalla PKA (ve<strong>di</strong> pag.<strong>12</strong>2; sequenza estremamente basica):<br />
Gln-Ile-Arg-Arg-Arg-Arg-Pro-Thr-Pro-Ala-Thr<br />
Residui basici fosforilazione<br />
PPI1, nella forma fosforilata, è attivo come <strong>in</strong>ibitore. Per comprendere il significato fisiologico<br />
occorre fare il punto della situazione:<br />
L’<strong>in</strong>ibitore fosforilato si lega alla prote<strong>in</strong>a <strong>fosfatasi</strong> 1 e la <strong>in</strong>attiva, per cui tale <strong>fosfatasi</strong> non può<br />
rimuovere il fosfato dalla Ser14 della glicogeno fosforilasi.<br />
L’AMP ciclico blocca pertanto il meccanismo <strong>di</strong> <strong>di</strong>sattivazione della glicogeno fosforilasi. Qu<strong>in</strong><strong>di</strong><br />
mentre AMPc attiva la glicogeno fosforilasi c<strong>in</strong>asi e la conseguente attivazione della fosforilasi,<br />
contemporaneamente blocca (con questo meccanismo me<strong>di</strong>ato dall’<strong>in</strong>ibitore PPI1 fosforilato)<br />
l’<strong>in</strong>attivazione dello stesso enzima, evitando un assurdo ciclo futile (quello della cont<strong>in</strong>ua<br />
attivazione e <strong>di</strong>sattivazione della glicogeno fosforilasi).<br />
E’ noto che l’<strong>in</strong>sul<strong>in</strong>a promuove (<strong>in</strong><strong>di</strong>rettamente) la defosforilazione del PPI 1 (≡ <strong>in</strong>attivazione della<br />
glicogeno fosforilasi ≡ stop alla scissione del glicogeno ≡ prote<strong>in</strong>a <strong>fosfatasi</strong> 1 attiva ≡ glicogeno<br />
s<strong>in</strong>tetasi attiva). Viene qu<strong>in</strong><strong>di</strong> bloccata dall’<strong>in</strong>sul<strong>in</strong>a una reazione catabolica, e viene promossa<br />
un’azione anabolica.<br />
<strong>158</strong>
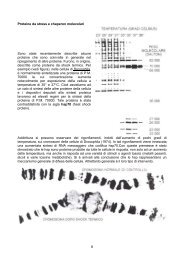
Per quanto concerne la PP1 (qu<strong>in</strong><strong>di</strong> la prote<strong>in</strong>a <strong>fosfatasi</strong> e non l’<strong>in</strong>ibitore), occorre ricordare che<br />
esiste anche una prote<strong>in</strong>a accessoria G (perché legata al glicogeno), <strong>di</strong> PM 135000 descritta<br />
recentemente da Philip Cohen. Questa è <strong>di</strong> fatto un attivatore della prote<strong>in</strong>a <strong>fosfatasi</strong> 1. Infatti<br />
l’<strong>in</strong>sul<strong>in</strong>a (con un meccanismo non ancora del tutto decifrato) porta alla fosforilazione della<br />
subunità G (non chiamiamola prote<strong>in</strong>a G per evitare confusione con le ben note prote<strong>in</strong>e G,<br />
traduttrici del segnale), che rende la PP1 più attiva ( = defosforilazione della GS con conseguente<br />
attivazione, etc.). Inoltre la subunità G tiene la PP1 legata normalmente ai granuli <strong>di</strong> glicogeno,<br />
impedendo che questa PP1 possa agire senza controllo (questo è stato <strong>di</strong>mostrato nel muscolo<br />
scheletrico). Ne consegue che la fosforilazione della G porta al <strong>di</strong>stacco della PP1 dal glicogeno:<br />
perché la PP1 è unita alla G, si stacca la G e porta con sé la PP1.<br />
Adrenal<strong>in</strong>a ≡ stimolo catabolico (degradazione del glicogeno) ≡ PKA attiva ≡ fosforilazione della<br />
β della GFK e qu<strong>in</strong><strong>di</strong> attivazione GP ≡ fosforilazione dell’<strong>in</strong>ibitore PPI 1b e conseguente <strong>in</strong>ibizione<br />
della prote<strong>in</strong>a <strong>fosfatasi</strong> PP1<br />
<strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong> 2 (PP2)<br />
Le prote<strong>in</strong>e <strong>fosfatasi</strong> 2 sono caratterizzate dall’essere attive sulla subunità α della glicogeno<br />
fosforilasi c<strong>in</strong>asi. Ne sono state descritte tre (PP2A, PP2B, PP2C). Nessuna delle tre forme è<br />
<strong>in</strong>ibita da <strong>in</strong>ibitori proteici (abbiamo visto che PPI 1 e PPI 2 sono attivi solo su PP1). Sono noti però<br />
<strong>in</strong>ibitori proteici, come l’acido okadaico.<br />
Tabuliamo alcune proprietà:<br />
PP2A (o INH) PP2B PP2C<br />
Substrato: subunità<br />
α o β della GPK<br />
α α α<br />
Inibizione da PPI 1 o<br />
PPI2<br />
no* no no<br />
Dipendenza assoluta<br />
da cationi bivalenti<br />
no Ca ++ Mg ++<br />
Stimolazione da CaM no sì no<br />
*(ma è <strong>in</strong>ibita da acido okadaico; ve<strong>di</strong> pag.132 la INH che è una PP2A)<br />
Prote<strong>in</strong>a <strong>fosfatasi</strong> 2A:<br />
Si lega all’antigene T piccolo del polyoma e dell’SV-40. Tale T<br />
piccolo <strong>in</strong>ibisce la defosforilazione <strong>di</strong> MEK ad opera <strong>di</strong> PP2A.<br />
E’ una famiglia numerosa. In genere è formata da 3 subunità.<br />
E’ anch’essa implicata nel ciclo del glicogeno, anche se l’attività della PP1 è <strong>in</strong> larga maggioranza<br />
nel muscolo. Nel fegato è maggiore l’attività della PP2A.<br />
È implicata (nel muscolo) nella defosforilazione delle catene leggere della mios<strong>in</strong>a (anche una PP1<br />
lo è, quella <strong>di</strong> tipo C, cioè la PP1C).<br />
L’acido okadaico è un importante <strong>in</strong>ibitore della prote<strong>in</strong>a <strong>fosfatasi</strong> 2A ! E’ ben documentato a<br />
pag.132, dove l’acido okadaico è citato come <strong>in</strong>ibitore della INH (una PP2A).<br />
159
<strong>Prote<strong>in</strong>e</strong> Fosfatasi 2 A [da Curr. Op. <strong>in</strong> Cell Biol. <strong>12</strong> (2) 180 (2000)]<br />
Le forme attive delle PP2A sono eterotrimeriche, formate da una subunità catalitica (C), e due<br />
subunità regolatorie, una subunità A, che <strong>in</strong>teragisce sia con C che con B, ed una subunità B, che<br />
è co<strong>di</strong>ficata da almeno 13 geni.<br />
La subunità A è più grande <strong>di</strong> B e C, e <strong>in</strong>teragisce con la zona N term<strong>in</strong>ale con B, mentre con la Cterm<strong>in</strong>ale<br />
<strong>in</strong>teragisce con la subunità C.<br />
La subunità A è costituita da 15 ripetizioni (repeat) <strong>di</strong> 39 am<strong>in</strong>oaci<strong>di</strong>. Tale repaeat è denom<strong>in</strong>ato<br />
dom<strong>in</strong>io HEAT ( da Hunt<strong>in</strong>gt<strong>in</strong> Elongation factor PP2A and Tor k<strong>in</strong>ase).<br />
Questo dom<strong>in</strong>io è importante. E’ stato trovato recentemente nell’import<strong>in</strong>a β.<br />
In molti tumori della pelle si trova una subunità A mutata.<br />
Sia l’antigene T piccolo che il T me<strong>di</strong>o possono sostituire la subunità B.<br />
Nella prostata si ha un’elevata espressione del gene per la prote<strong>in</strong>a <strong>pp</strong>32, che co<strong>di</strong>fica per la<br />
prote<strong>in</strong>a <strong>in</strong>ibitrice (<strong>di</strong> PP2A): I1/PHAP-1. Nelle forme tumorali della prostata la normale <strong>pp</strong>32 non è<br />
più espressa, per essere sostituita da <strong>pp</strong>32r1 e <strong>pp</strong>32r2.<br />
Prote<strong>in</strong>a <strong>fosfatasi</strong> 2B:<br />
Presenta un particolare <strong>in</strong>teresse perché è stimolata da Ca ++ . Quando è estratta da tessuti nervosi<br />
è un etero<strong>di</strong>mero, formato da una subunità A (61000, subunità catalitica) e da una subunità B<br />
(19000, subunità regolatoria).<br />
Da tempo era nota una prote<strong>in</strong>a <strong>fosfatasi</strong> Ca-<strong>di</strong>pendente denom<strong>in</strong>ata Calc<strong>in</strong>eur<strong>in</strong>a, che è molto<br />
abbondante nell’encefalo (anche 1% delle prote<strong>in</strong>e totali). Quando furono meglio def<strong>in</strong>iti i criteri <strong>di</strong><br />
classificazione delle prote<strong>in</strong>e <strong>fosfatasi</strong>, si scoprì che la calc<strong>in</strong>eur<strong>in</strong>a è la PP2B.<br />
La subunità B presenta omologia <strong>di</strong> sequenza con la calmodul<strong>in</strong>a (possiede anch’essa 4 EF-hand,<br />
ve<strong>di</strong> pag.45). tra l’altro ha l’N-term<strong>in</strong>ale miristoilato, per consentire l’<strong>in</strong>serimento <strong>in</strong> membrana.<br />
L’omologia riguarda solo le “chele” che legano il calcio. La restante parte della molecola è molto<br />
<strong>di</strong>versa. Nel complesso l’identità riguarda solo il 30% della sequenza.<br />
La subunità B della PP2B ha un ruolo s<strong>in</strong>golare. Possiamo, <strong>in</strong> prima a<strong>pp</strong>rossimazione, <strong>di</strong>re che è<br />
un <strong>in</strong>ibitore dell’attività <strong>fosfatasi</strong>ca. Se la subunità B è sostituita dalla CaM, si ha un forte aumento<br />
dell’attività prote<strong>in</strong>a <strong>fosfatasi</strong>ca Ca-<strong>di</strong>pendente. Stranamente la PP2B è stimolata anche dal solo<br />
Ca ++ (A0.5 ≅ 1 µM). Con CaM saturante A0.5 non varia, ma Vmax aumenta <strong>di</strong> ben 10 volte.<br />
Questo fenomeno viene <strong>in</strong>terpretato nel seguente modo: la subunità B stimola la subunità catalitica<br />
A via Ca ++ . Con CaM si forma un complesso ternario, con extra stimolazione da Ca ++ . La subunità<br />
B sembra co<strong>in</strong>volta nel riconoscimento della prote<strong>in</strong>a substrato che deve subire la defosforilazione.<br />
Possiamo qui citare questo fenomeno comune ad altre prote<strong>in</strong>e <strong>fosfatasi</strong>: esistono, per le prote<strong>in</strong>e<br />
<strong>fosfatasi</strong>, delle zone che riconoscono il substrato e che, pertanto, “convogliano” la prote<strong>in</strong>a<br />
<strong>fosfatasi</strong> su tale substrato. Tali dom<strong>in</strong>i sono denom<strong>in</strong>ati “ZIP – Code”. Vedremo che una PTB<br />
(Prote<strong>in</strong>a Tiros<strong>in</strong>a Fosfatasi), la PTB1 D o Syp, contiene 2 SH2 che la “spe<strong>di</strong>scono” sulla tiros<strong>in</strong>a<br />
fosforilata. Infatti, f<strong>in</strong> tanto che la tiros<strong>in</strong>a è defosforilati, i dom<strong>in</strong>i SH2 non la riconoscono. Quando<br />
<strong>in</strong>vece la Tyr è fosforilata, essa “arruola” prote<strong>in</strong>e tramite gli essenziali SH2 (ve<strong>di</strong> Syp a pag.117,<br />
che si lega al recettore per PDGF).(ve<strong>di</strong> <strong>in</strong>serto zip – code a pag.167).<br />
160
Ruolo della calc<strong>in</strong>eur<strong>in</strong>a (CN) nell’attivazione delle cellule T:<br />
L’aumento <strong>di</strong> Ca ++ determ<strong>in</strong>a il legame<br />
<strong>di</strong> Ca/CaM (calcio/calmodul<strong>in</strong>a) alla CN<br />
(calc<strong>in</strong>eur<strong>in</strong>a), che si attiva e<br />
defosforila NF-AT (Nuclear Factor –<br />
Activation T cells), che può trasferirsi al<br />
nucleo (nella forma defosforilati) dove,<br />
<strong>in</strong>sieme ad altri fattori <strong>di</strong> trascrizione<br />
(per es. Jun e Fos), si lega a siti<br />
promotori sul DNA (per esempio al sito<br />
AP-1), con trascrizione del gene per IL-<br />
2 (Interleuch<strong>in</strong>a 2; ve<strong>di</strong> pagg.267 e<br />
270), uno dei primi geni stu<strong>di</strong>ati<br />
nell’attivazione delle cellule T.<br />
Ciclospor<strong>in</strong>e ed attività immunoso<strong>pp</strong>ressiva:<br />
Le ciclospor<strong>in</strong>e (ve<strong>di</strong> pag.7) sono importanti<br />
agenti immunoso<strong>pp</strong>ressori. Si sa che sono<br />
composti (non proteici) <strong>di</strong> basso peso<br />
molecolare che <strong>in</strong>ibiscono le ciclofil<strong>in</strong>e (o<br />
pepti<strong>di</strong>l-prolil-cis-trans-isomerasi). Non era<br />
chiara la loro azione immunoso<strong>pp</strong>ressiva.<br />
Oggi [ve<strong>di</strong> TIBS 21, (11) 407-1996] è stato<br />
chiarito che la ciclospor<strong>in</strong>a forma un<br />
complesso stabile con la ciclofil<strong>in</strong>a che si lega<br />
alla PP2B legata, a sua volta, alla subunità B<br />
della calc<strong>in</strong>eur<strong>in</strong>a stessa. Si tratta qu<strong>in</strong><strong>di</strong> <strong>di</strong> un<br />
complesso quaternario che blocca la<br />
calc<strong>in</strong>eur<strong>in</strong>a (CN) impedendole <strong>di</strong> legare il<br />
naturale attivatore (la CaM). Non avviene<br />
pertanto l’attivazione della CN e viene a<br />
mancare l’essenziale defosforilazione <strong>di</strong> NF-<br />
AT, con attivazione delle cellule T (ve<strong>di</strong><br />
schema <strong>in</strong> precedente).<br />
Prote<strong>in</strong>a <strong>fosfatasi</strong> 2C:<br />
Dipende strettamente dal Mg ed anche dal Mn (è detta anche famiglia PPM). La Piruvato<br />
Deidrogenasi Fosfatasi è una PP2C. Negli Eucarioti la PP2C ribalta la cascata <strong>di</strong> prote<strong>in</strong>e c<strong>in</strong>asi<br />
che si attiva <strong>in</strong> risposta a stress o elevati ra<strong>pp</strong>orti AMP/ATP. Defosforilazione piruvico deidrogenasi<br />
= aumento decarbossilazione ossidativa del piruvato = produzione ATP via catena respiratoria.<br />
161
<strong>Prote<strong>in</strong>e</strong> Tiros<strong>in</strong> – Fosfatasi (PTP)<br />
Si è già detto che le prote<strong>in</strong>e <strong>fosfatasi</strong> sono molto importanti: sono la naturale controparte delle<br />
prote<strong>in</strong>e c<strong>in</strong>asi. Le prote<strong>in</strong>e c<strong>in</strong>asi sono state classificate <strong>in</strong> Ser<strong>in</strong>/Treon<strong>in</strong> c<strong>in</strong>asi, Tiros<strong>in</strong>-C<strong>in</strong>asi e<br />
miste (si ricor<strong>di</strong>, per esempio, che MEK, detta anche MAPKK, che fosforila la MAP-c<strong>in</strong>asi sia su<br />
treon<strong>in</strong>a che su tiros<strong>in</strong>a <strong>in</strong> corrispondenza della sequenza TEY del subdom<strong>in</strong>io VIII). Anche le<br />
prote<strong>in</strong>e <strong>fosfatasi</strong> sono classificabili <strong>in</strong> tre gran<strong>di</strong> famiglie:<br />
• Ser/Thr prote<strong>in</strong>e <strong>fosfatasi</strong>, contrad<strong>di</strong>st<strong>in</strong>te dalla sigla PP (abbiamo visto PP1 e PP2).<br />
• Tyr prote<strong>in</strong>e <strong>fosfatasi</strong>, che sono prote<strong>in</strong>e <strong>fosfatasi</strong> specifiche per residui tiros<strong>in</strong>ici <strong>di</strong> prote<strong>in</strong>e<br />
(sono contrad<strong>di</strong>st<strong>in</strong>te dalla sigla PTP).<br />
• <strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong> a funzione mista, nel senso che staccano con meccanismo idrolitico un<br />
residuo <strong>di</strong> acido ortofosforico sia da ser<strong>in</strong>/treon<strong>in</strong>e che da tiros<strong>in</strong>e. Anche <strong>in</strong> questo caso<br />
possiamo citare l’esempio della Cdc-25 (ve<strong>di</strong> pag.132), che stacca il fosfato sia dalla Treon<strong>in</strong>a-<br />
14 che dalla Tiros<strong>in</strong>a-15 del Rossman motiv della Cdc-2.<br />
Il “capitolo” delle prote<strong>in</strong>-tiros<strong>in</strong> <strong>fosfatasi</strong> (PTP) è della massima importanza, ed è <strong>in</strong> cont<strong>in</strong>uo<br />
aggiornamento. Gli stu<strong>di</strong> sulle PTP <strong>in</strong>iziarono, <strong>in</strong> pratica, nel 1988, quando una PTP fu purificata<br />
da placenta umana da un gru<strong>pp</strong>o <strong>di</strong> ricercatori coor<strong>di</strong>nato dal Prof. Edmond H. Fischer (che<br />
conseguì, <strong>in</strong>sieme ad Edw<strong>in</strong> G. Krebs, il premio Nobel nel 1992 per la Me<strong>di</strong>c<strong>in</strong>a e la Fisiologia). Fu<br />
una realizzazione importante, e per un certo verso <strong>in</strong>usuale, nell’ambito degli enzimi che<br />
partecipano al metabolismo regolatorio. Infatti tali enzimi sono normalmente presenti <strong>in</strong> quantità<br />
molto limitata e sfuggono, <strong>in</strong> pratica, ai tentativi <strong>di</strong> purificazione ed isolamento <strong>in</strong> forma omogenea:<br />
gran parte degli enzimi che partecipano al metabolismo regolatorio e che sono stati stu<strong>di</strong>ati<br />
provengono, <strong>in</strong> genere, da a<strong>pp</strong>licazioni <strong>di</strong> tecnologie biomolecolari. Con la purificazione <strong>di</strong> una PTP<br />
(si trattava della PTP-1B), fu <strong>di</strong>sponibile la sequenza <strong>di</strong> una prote<strong>in</strong>a tiros<strong>in</strong>a <strong>fosfatasi</strong>, e fu<br />
possibile constatare, me<strong>di</strong>ante una ricerca su banche dati, che non aveva omologia <strong>di</strong> sequenza<br />
con altre ser/thr prote<strong>in</strong>e <strong>fosfatasi</strong>. Oggi è anche <strong>di</strong>sponibile (ve<strong>di</strong> più avanti) la struttura completa,<br />
me<strong>di</strong>ante l’analisi ai raggi X, della PTP-1B.<br />
Me<strong>di</strong>ante la stessa ricerca su banche dati, fu possibile constatare che parte della PTP-1B aveva<br />
omologia <strong>di</strong> sequenza con una prote<strong>in</strong>a transmembrana già nota: si tratta della CD45 che, <strong>in</strong>torno<br />
alla metà degli anni ’70, era stata caratterizzata quale maggior componente delle glicoprote<strong>in</strong>a<br />
trans-membrana <strong>di</strong> tutte le cellule della l<strong>in</strong>ea ematopoietica. Poiché la CD45 era posseduta solo da<br />
tali cellule, fu utilizzata come marker importante a livello cl<strong>in</strong>ico, anche se la sua funzione restava<br />
completamente ignota. Per esempio la <strong>di</strong>agnosi <strong>di</strong> l<strong>in</strong>fomi non-<strong>di</strong>fferenziati passa anche attraverso<br />
la determ<strong>in</strong>azione della CD45. Seguì l’identificazione <strong>di</strong> altre importanti prote<strong>in</strong>e <strong>fosfatasi</strong><br />
specifiche per il residuo tiros<strong>in</strong>ico e, a tutt’oggi, le prote<strong>in</strong>e stu<strong>di</strong>ate sono più <strong>di</strong> 35.<br />
K.M. Walton & J.E. Dixon, Ann. Rev. Biochem., 62, 101-20, 1993<br />
I.S. Towbridge, J. Biol. Chem., 266, 23517, 1991<br />
Inserto: NiceProt View of SWISS-PROT: P08575 (CD45)<br />
Le PTP presentano, <strong>in</strong> generale, un’elevata attività: si ritiene che per tale elevata attività i residui<br />
tiros<strong>in</strong>ici delle prote<strong>in</strong>e (oggetto <strong>di</strong> fosforilazione) siano, “<strong>di</strong> norma”, defosforilati. Le tiros<strong>in</strong>-c<strong>in</strong>asi<br />
possono <strong>in</strong> effetti determ<strong>in</strong>are una fosforilazione transiente.<br />
Struttura primaria delle <strong>Prote<strong>in</strong>e</strong> Tiros<strong>in</strong> Fosfatasi e loro pr<strong>in</strong>cipali proprietà<br />
Dalla monografia <strong>di</strong> Walton & Dixon è qui sotto riportato lo schema delle PTP più stu<strong>di</strong>ate. Si fa<br />
riferimento alla PTP-1B con un dom<strong>in</strong>io ben caratterizzato, specifico dell’attività prote<strong>in</strong>a tiros<strong>in</strong><strong>fosfatasi</strong>ca,<br />
e, qu<strong>in</strong><strong>di</strong>, l’esistenza del dom<strong>in</strong>io <strong>fosfatasi</strong>co accomuna tutte le prote<strong>in</strong>e riportate <strong>in</strong><br />
figura. Interessante che tale dom<strong>in</strong>io PTP può essere presente anche due volte (come <strong>in</strong> CD45).<br />
La presenza <strong>di</strong> altri dom<strong>in</strong>i a funzione nota <strong>in</strong> varie prote<strong>in</strong>e del gru<strong>pp</strong>o PTP può guidare nella<br />
ricerca della funzione delle PTP stesse, funzione che, d’altronde, è <strong>in</strong>sc<strong>in</strong><strong>di</strong>bile dalla localizzazione<br />
subcellulare delle medesime, localizzazione ottenuta con sequenze che “spe<strong>di</strong>scono” la PTP nel<br />
suo sito(denom<strong>in</strong>ate ZIP-code). Infatti la PTP-1B al C-term<strong>in</strong>ale possiede una sequenza che ne<br />
giustifica l’adesione al reticolo endoplasmatico, con la PTP-1B che è rivolta al citoplasma. In tale<br />
sede potrà agire su particolari substrati. La PTP-1B presenta ser<strong>in</strong>e fosforilabili da Cdc-2 (cioè Ser<br />
seguite imme<strong>di</strong>atamente da Pro) e il suo co<strong>in</strong>volgimento è stato <strong>di</strong>mostrato nel ciclo cellulare ed<br />
anche come me<strong>di</strong>atore dell’azione dell’<strong>in</strong>sul<strong>in</strong>a.<br />
162
Altre PTP possiedono extra-dom<strong>in</strong>i a funzione nota.<br />
La PTP-MEG presenta, all’N-term<strong>in</strong>ale, un dom<strong>in</strong>io simile ad altre prote<strong>in</strong>e del citoscheletro. In<br />
particolare alla prote<strong>in</strong>a della banda 4.1 dei globuli rossi umani. Tale 4.1 collega l’act<strong>in</strong>a alla<br />
“rete” adesa al lato <strong>in</strong>terno della membrana che è formata dalle molecole <strong>di</strong> spettr<strong>in</strong>a. Ma la 4.1 è<br />
omologa della tal<strong>in</strong>a (che a sua volta è substrato della Src-prote<strong>in</strong>a c<strong>in</strong>asi; ve<strong>di</strong> pag.117). È del<br />
tutto proponibile il seguente sillogismo: come la 4.1 sta unita al citoscheletro, così può farlo anche<br />
la PTP-MEG, ed i suoi substrati andranno ricercati tra le prote<strong>in</strong>e del citoscheletro stesso.<br />
La PTP-1C è stata isolata da tessuti umani e <strong>di</strong> topo: contiene il consueto dom<strong>in</strong>io PTP nella parte<br />
C-term<strong>in</strong>ale, mentre all’N-term<strong>in</strong>ale contiene due dom<strong>in</strong>i <strong>di</strong> tipo SH2. Questi dom<strong>in</strong>i “Src Homology”<br />
<strong>di</strong> tipo 2 sono <strong>di</strong> grande importanza. Abbiamo già visto (pag.117) che riconoscono una tiros<strong>in</strong>a<br />
della stessa prote<strong>in</strong>a che porta T/SH2 o <strong>di</strong> un’altra prote<strong>in</strong>a (per es. il recettore per il PDGF) solo<br />
se è nello stato fosforilato. Abbiamo visto che è stato anche decifrato il co<strong>di</strong>ce con il quale sono<br />
riconosciute tali tiros<strong>in</strong>e fosforilate (sono gli amm<strong>in</strong>oaci<strong>di</strong> che imme<strong>di</strong>atamente seguono la tiros<strong>in</strong>a).<br />
Ricor<strong>di</strong>amo che gli SH2 su prote<strong>in</strong>e non si legano alla tiros<strong>in</strong>a se questa non è nello stato<br />
fosforilato (<strong>in</strong> genere autofosforilato). (Già considerato a pag.160).<br />
La presenza <strong>di</strong> dom<strong>in</strong>i SH2 su prote<strong>in</strong>e tiros<strong>in</strong> <strong>fosfatasi</strong> è estremamente pert<strong>in</strong>ente alla funzione<br />
della tiros<strong>in</strong>a <strong>fosfatasi</strong> stessa: <strong>in</strong>fatti gli SH2 consentono <strong>di</strong> “pilotare” la PTP sulla tiros<strong>in</strong>a da<br />
defosforilare.<br />
Esistono <strong>di</strong>verse altre prote<strong>in</strong>e riconducibili alla struttura della PTP-1C, alcune delle quali<br />
partecipano allo svilu<strong>pp</strong>o dell’embrione della Drosophila. A pag.117 era stata <strong>in</strong>trodotta la prote<strong>in</strong>a<br />
Syp, che è simile alla PTP-1C, che è anche denom<strong>in</strong>ata PTP-1D e che ha aff<strong>in</strong>ità per una<br />
particolare tiros<strong>in</strong>a <strong>in</strong> forma fosforilata del recettore per il PDGF.<br />
La YOP51 a<strong>pp</strong>artiene alla famiglia <strong>di</strong> prote<strong>in</strong>e tossiche prodotte da batteri del genere Yers<strong>in</strong>ia. È<br />
sorprendente che i batteri possiedano attività PTP. Infatti non è nota la presenza <strong>di</strong> toss<strong>in</strong>e<br />
fosforilate nei batteri. Ma l’attività enzimatica prote<strong>in</strong>a tiros<strong>in</strong>a <strong>fosfatasi</strong>ca è presente su prote<strong>in</strong>e<br />
prodotte dai batteri per attaccare cellule eucariote.<br />
163
Vedremo più avanti che altri batteri patogeni producono enzimi che producono AMP-ciclico<br />
(pertosse ed antrace), e ciò rientra nel medesimo tipo <strong>di</strong> strategia: l’attacco alle cellule bersaglio<br />
degli organismi eucarioti mira a <strong>di</strong>sarticolare qualche punto importante della fitta rete dei segnali<br />
<strong>in</strong>tracellulari. Del genere Yers<strong>in</strong>ia sono stu<strong>di</strong>ate <strong>in</strong> particolare tre specie:<br />
▪ Yers<strong>in</strong>ia pseudotuberculosis: prima specie identificata per essere produttrice <strong>di</strong> PTP<br />
▪ Yers<strong>in</strong>ia enterocolitica: produce PTP contrad<strong>di</strong>st<strong>in</strong>ta dalla sigla YOP51<br />
▪ Yers<strong>in</strong>ia pestis: agente eziologico della peste bubbonica. Produce una PTP dalla sigla YOP2b<br />
La YOP51, che è stata molto stu<strong>di</strong>ata, possiede un’attività PTP da 20 a 1000 volte più elevata <strong>di</strong><br />
altre PTP. Alcune specie mutanti <strong>di</strong> Y. enterocolitica, con il gene co<strong>di</strong>ficante per YOP51 mutato <strong>in</strong><br />
modo tale da co<strong>di</strong>ficare una PTP mancante dell’AA essenziale nel sito attivo (una ciste<strong>in</strong>a), non<br />
sono più patogene! La PTP mutata è <strong>in</strong>attiva cataliticamente ma riconosce ugualmente i substrati e<br />
resta associata ad essi. Questo è stato molto utile per identificare i substrati <strong>di</strong> questa PTP (ve<strong>di</strong><br />
pag.165: ciste<strong>in</strong>a-215 del sito attivo).<br />
VH1. E’ la prote<strong>in</strong>a con attività PTP dal peso molecolare più basso: 20000 Da. Una parte del<br />
genoma del Vaiolo Bov<strong>in</strong>o, denom<strong>in</strong>ata H1, co<strong>di</strong>fica per la prote<strong>in</strong>aVH1. Tale prote<strong>in</strong>a ha la<br />
proprietà <strong>di</strong> essere, non solo <strong>fosfatasi</strong>ca per residui <strong>di</strong> fosfo-tiros<strong>in</strong>a, ma idrolizza anche fosfoser<strong>in</strong>e<br />
e fosfo-treon<strong>in</strong>e. Qu<strong>in</strong><strong>di</strong> a<strong>pp</strong>artiene alle PTP a “funzione mista”.<br />
Cdc-25. Abbiamo già parlato <strong>di</strong> tale importante PTP, che <strong>in</strong> realtà fosforila anche treon<strong>in</strong>a-14 oltre<br />
alla tiros<strong>in</strong>a-15 della Cdc-2. Qu<strong>in</strong><strong>di</strong>, come VH1, è una PTP a funzione mista.<br />
Importante proprietà (già considerata): la cdc-25 è attiva, come <strong>fosfatasi</strong> quando è, a sua volta,<br />
fosforilata.<br />
S<strong>in</strong>o a questo punto abbiamo parlato <strong>di</strong> PTP <strong>in</strong>tracellulari, o, comunque, <strong>in</strong>teragenti con la<br />
membrana. Ora occupiamoci <strong>di</strong> PTP transmembrana (qualche notizia è già stata fornita per la<br />
CD45) ed è <strong>in</strong>teressante esam<strong>in</strong>are la parte extra-cellulare che scatena (all’<strong>in</strong>terno della cellula)<br />
una serie <strong>di</strong> fenomeni me<strong>di</strong>ati da attività PTP. Iniziamo dalla nota:<br />
CD45. All’<strong>in</strong>izio <strong>di</strong> questo capitolo abbiamo già accennato alla CD45, che è una glicoprote<strong>in</strong>a<br />
transmembrana presente <strong>in</strong> tutte le cellule ematopoietiche. Era nota da tempo, ma solo con la<br />
def<strong>in</strong>izione della struttura della PTP-1B e della <strong>in</strong>tr<strong>in</strong>seca attività PTP, fu possibile scoprire che la<br />
CD45, <strong>in</strong> effetti, è una PTP. È da considerarsi come prototipo delle PTP transmembrana.<br />
La CD45 era già nota come LCA (Leucocite Common Antigen) ed ha una struttura compatibile con<br />
il ruolo <strong>di</strong> ipotetico recettore. E’ importantissima per la risposta contro antigeni (produzione <strong>di</strong><br />
anticorpi), sia da parte <strong>di</strong> l<strong>in</strong>fociti B che T. Cellule mancanti solo <strong>di</strong> CD45 non proliferano <strong>in</strong> risposta<br />
all’antigene. Lo stu<strong>di</strong>o dettagliato della ricerca dei substrati defosforilati dalla CD45 è <strong>in</strong> corso.<br />
Nella parte esterna alla cellula troviamo una regione N-term<strong>in</strong>ale (1-177) ricca <strong>di</strong> gluci<strong>di</strong> legati all’O.<br />
Dal residuo 177 al 542 c’è un dom<strong>in</strong>io ricco <strong>in</strong> ciste<strong>in</strong>a con ben 15 siti <strong>di</strong> glicosilazione all’N. La<br />
parte extracellulare della CD45 me<strong>di</strong>a <strong>in</strong>terazioni con altre prote<strong>in</strong>e <strong>di</strong> adesione (per es.CD22).<br />
Nella parte citoplasmatica, la CD45 è <strong>in</strong>teressante perché presenta ben due dom<strong>in</strong>i <strong>di</strong> tipo PTP,<br />
ripetuti <strong>in</strong> tandem. Lo stu<strong>di</strong>o dettagliato della struttura primaria <strong>di</strong> tali dom<strong>in</strong>i ha rivelato una buona<br />
omologia con PTP-1B. Tale omologia è esaltata <strong>in</strong> un tratto <strong>di</strong> 11 residui che contengono<br />
l’amm<strong>in</strong>oacido del sito attivo (una ciste<strong>in</strong>a, che forma un tio-estere con il gru<strong>pp</strong>o fosforico del<br />
substrato, cioè con il gru<strong>pp</strong>o fosforico che va <strong>in</strong>contro a rimozione). Più avanti ci occuperemo della<br />
struttura del sito attivo della PTP.<br />
HLAR. Nella ricerca <strong>di</strong> prote<strong>in</strong>e simili alla CD45 (detta anche LCA, Leucocite Common Antigen),<br />
sono state identificate <strong>di</strong>verse LAR (LCA – Related molecole), tra cui, nell’uomo (Human), la<br />
HLAR. Questa ha un dom<strong>in</strong>io extracellulare estremamente articolato. Infatti presenta (a partire<br />
dall’estremità N-term<strong>in</strong>ale):<br />
- 3 dom<strong>in</strong>i tipo Immunoglobul<strong>in</strong>a: si tratta <strong>di</strong> una struttura ridondante fra le prote<strong>in</strong>e <strong>di</strong> membrana.<br />
Ricor<strong>di</strong>amo i complessi maggiori <strong>di</strong> istocompatibilità <strong>di</strong> classe I e II (MHCI e MHCII), i recettori<br />
delle cellule T, le IgG e le IgM.<br />
- 9 dom<strong>in</strong>i <strong>di</strong> tipo III della fibronect<strong>in</strong>a: li abbiamo già visti a pag.65 (il decimo residuo <strong>di</strong> tipo III<br />
della fibronect<strong>in</strong>a contiene la sequenza RGD che è essenziale per il legame alle cellule, <strong>in</strong><br />
genere alle <strong>in</strong>tegr<strong>in</strong>e).<br />
164
Tale struttura è molto simile, nel suo <strong>in</strong>sieme, alle N-CAM (Neuronal Cellular Adesion Molecule) e<br />
si ritiene che la HLAR partecipi alla crescita dell’assone verso le cellule bersaglio. In tale processo<br />
vedremo che è importantissimo il ruolo svolto dal Fattore <strong>di</strong> Crescita delle Cellule Nervose (NGF).<br />
Conformazione delle <strong>Prote<strong>in</strong>e</strong> Tiros<strong>in</strong> Fosfatasi e sequenza del sito attivo<br />
Nel marzo del 1994 è comparsa sulla rivista Science un articolo <strong>di</strong> D. Barbord e coll. con la<br />
struttura dettagliata della PTP-1B, def<strong>in</strong>ita me<strong>di</strong>ante cristallografia a raggi-X. Tutto lo stu<strong>di</strong>o è stato<br />
portato avanti su <strong>di</strong> un s<strong>in</strong>golo cristallo <strong>di</strong> tale prote<strong>in</strong>a, <strong>di</strong> <strong>di</strong>mensioni: 0.8x0.15x0.15 mm, che era<br />
impregnato <strong>di</strong> tungsteno <strong>di</strong> so<strong>di</strong>o.<br />
La prote<strong>in</strong>a presenta <strong>di</strong>versi tratti ad α-elica e tratti a β-struttura antiparallela.<br />
La sequenza <strong>di</strong> amm<strong>in</strong>oaci<strong>di</strong> tra la posizione 213 e la 223 è essenziale per l’attività <strong>fosfatasi</strong>ca,<br />
con un residuo <strong>di</strong> ciste<strong>in</strong>a che forma un tioestere fosforico. Anche un residuo basico <strong>di</strong> arg<strong>in</strong><strong>in</strong>a (R)<br />
è essenziale.<br />
Conoscendo la sequenza <strong>di</strong> numerose altre PTP, è stato confermato che tale successione <strong>di</strong> 10<br />
amm<strong>in</strong>oaci<strong>di</strong> è importante, con alcuni residui <strong>in</strong>varianti. Gli amm<strong>in</strong>oaci<strong>di</strong> essenziali sono i seguenti:<br />
Rossmann motiv<br />
I/V – H – C215 – X – A – G – X – X – R221 – S/T – G<br />
↑<br />
Gly <strong>in</strong> PTP-1B<br />
È <strong>di</strong>ffusa la sigla Cx5R, perché, <strong>in</strong> realtà, tra C ed R possono essere compresi 5 AA (qualsiasi/X).<br />
Nella PTP-1B l’AA 220 è Gly (anche <strong>in</strong> altre PTP), per cui è presente il noto Rossmann motiv Gly –<br />
X – Gly – X – X – Gly che è ideale per “avvolgere” il gru<strong>pp</strong>o fosforico. Normalmente, nelle prote<strong>in</strong>e<br />
c<strong>in</strong>asi, il Rossmann motiv “avvolge” i tre residui fosforici dell’ATP. È <strong>in</strong>teressante che prote<strong>in</strong>e dalla<br />
funzione antitetica (le prote<strong>in</strong>e c<strong>in</strong>asi da una parte e le <strong>fosfatasi</strong> dall’altra) ricorrono agli stessi<br />
elementi strutturali anche per assolvere a funzioni così <strong>di</strong>verse.<br />
È anche importante (<strong>in</strong>fatti è sempre presente <strong>in</strong> PTP-1B), un residuo D (aspartico), che precede <strong>in</strong><br />
genere la C circa 25 residui prima.<br />
<strong>Prote<strong>in</strong>e</strong> <strong>di</strong> Adesione Cellulare e attività prote<strong>in</strong>a-tiros<strong>in</strong>-<strong>fosfatasi</strong>ca<br />
[CB- 5 (<strong>12</strong>) 1368 (1995)]<br />
Le prote<strong>in</strong>e d’adesione cellulare (CAM – ve<strong>di</strong> pag.73-74) sono importantissime per la realizzazione<br />
<strong>di</strong> tanti tipi d’<strong>in</strong>terazione cellula-cellula. Abbiamo visto che le CAM con caratteristiche Ca<strong>di</strong>pendenti<br />
sono le CADERINE (ve<strong>di</strong> pag.73), che presentano una caratteristica struttura a moduli<br />
<strong>di</strong> tipo <strong>in</strong> l<strong>in</strong>e (ve<strong>di</strong> pag.2), come del resto anche le CAM stesse. Le due HLAR e DPTP 10 D,<br />
a<strong>pp</strong>ena citate, sono CAM con, <strong>in</strong> più, la caratteristica attività Prote<strong>in</strong>a Tiros<strong>in</strong> Fosfatasica (PTP).<br />
Per la DPTP10D (con <strong>12</strong> dom<strong>in</strong>i tipo Fibronect<strong>in</strong>a III) è stato trovato un substrato. Si tratta della<br />
gp-150 (gp=glico prote<strong>in</strong>a), che è una CAM della Drosophila, con 18 dom<strong>in</strong>i extracellulari ricchi <strong>di</strong><br />
leuc<strong>in</strong>a (non ne abbiamo ancora parlato), ed un tratto <strong>in</strong>tra-cellulare dove esistono 4 residui <strong>di</strong><br />
tiros<strong>in</strong>a fosforilabili, <strong>in</strong>seriti <strong>in</strong> sequenze identificabili da dom<strong>in</strong>i SH2. E’ stato <strong>di</strong>mostrato che la gp-<br />
150 è substrato dell’attività PTP, sia <strong>in</strong> vitro che <strong>in</strong> vivo. In questo caso ha particolare significato la<br />
presenza ridondante <strong>di</strong> dom<strong>in</strong>i ricchi <strong>di</strong> leuc<strong>in</strong>a della gp-150. Tali dom<strong>in</strong>i sono stati trovati <strong>in</strong><br />
numerose altre prote<strong>in</strong>e della Drosophila, che controllano importanti processi cellulari, come<br />
l’aggregazione dei fotorecettori, dei neuroni motori, dove le <strong>in</strong>terazioni omofiliche (ve<strong>di</strong> pag.73) tra i<br />
dom<strong>in</strong>i ricchi <strong>di</strong> leuc<strong>in</strong>a potrebbero co<strong>in</strong>volgere la attività PTP ad esse collegate.<br />
Citiamo un’altra importante CAM con attività PTP:<br />
PTPµ: è una CAM che <strong>in</strong>izia, nella zona extra-cellulare, con un dom<strong>in</strong>io particolare (MAM-<br />
Mepr<strong>in</strong>/a5/µ), seguito dal “classico” dom<strong>in</strong>io tipo immunoglobul<strong>in</strong>a -uno solo- seguito, a sua volta,<br />
da 4 residui Fibronect<strong>in</strong>a <strong>di</strong> tipo III (FN3) <strong>in</strong> successione. Esiste il tratto transmembrana, qu<strong>in</strong><strong>di</strong>,<br />
nella parte citosolubile, ritroviamo 2 dom<strong>in</strong>i Prote<strong>in</strong>a Tiros<strong>in</strong> Fosfatasi (PTP). E’ un caso un po’<br />
analogo alla già citata HLAR (ve<strong>di</strong> pag.164).<br />
Le <strong>in</strong>terazioni omofiliche tra le zone extracellulari <strong>di</strong> PTPµ, e la zona extracellulare <strong>di</strong> alcuni tipi <strong>di</strong><br />
cader<strong>in</strong>e, determ<strong>in</strong>a de-fosforilazione <strong>di</strong> tiros<strong>in</strong>e delle cader<strong>in</strong>e stesse.<br />
165
Infatti esiste una cader<strong>in</strong>a caratterizzata dalla presenza <strong>di</strong> una tiros<strong>in</strong>a fosforilabile nel dom<strong>in</strong>io<br />
<strong>in</strong>tra-cellulare. Tale cader<strong>in</strong>a è normalmente legata, attraverso le caten<strong>in</strong>e, ai microfilamenti <strong>di</strong><br />
act<strong>in</strong>a del citoscheletro (ve<strong>di</strong> pag.73). Qu<strong>in</strong><strong>di</strong> le <strong>in</strong>terazioni omofiliche tra dom<strong>in</strong>i extra-cellulari <strong>di</strong><br />
PTPµ e dom<strong>in</strong>i extracellulari delle cader<strong>in</strong>e determ<strong>in</strong>a la veicolazione dell’attività PTP sulla tiros<strong>in</strong>a<br />
che deve essere defosforilata. E’ una forma <strong>di</strong> “zip code”.<br />
166
Inserto: ZIP - code<br />
Il term<strong>in</strong>e zip-code <strong>in</strong><strong>di</strong>ca un co<strong>di</strong>ce, ovvero un particolare dom<strong>in</strong>io proteico, che <strong>in</strong><strong>di</strong>rizza una<br />
prote<strong>in</strong>a, che contiene tale dom<strong>in</strong>io, verso particolari dest<strong>in</strong>azioni cellulari. Le PTP (prote<strong>in</strong>e-tiros<strong>in</strong><strong>fosfatasi</strong>)<br />
presentano una molteplicità <strong>di</strong> zip-code. Ricor<strong>di</strong>amoci, tuttavia, <strong>di</strong> non confondere questi<br />
zip-code con i leuc<strong>in</strong>e-Zi<strong>pp</strong>er (anch’essi contrad<strong>di</strong>st<strong>in</strong>ti dalla sigla ZIP; sono detti anche cerniere <strong>di</strong><br />
leuc<strong>in</strong>a) presenti <strong>in</strong> <strong>di</strong>versi fattori <strong>di</strong> trascrizione (ve<strong>di</strong> pag.242; per esempio CREB, Cyclic AMP<br />
Element B<strong>in</strong><strong>di</strong>ng, che è una prote<strong>in</strong>a b-ZIP; b=basica).<br />
Gli zip-code <strong>di</strong> PTP comprendono:<br />
1) dom<strong>in</strong>i <strong>di</strong> associazione a membrana;<br />
2) dom<strong>in</strong>i <strong>di</strong> localizzazione nucleare;<br />
3) dom<strong>in</strong>i SH2 (Src Homology <strong>di</strong> tipo 2)<br />
4) dom<strong>in</strong>i <strong>di</strong> associazione al citoscheletro.<br />
Nella figura <strong>di</strong> fondo pag<strong>in</strong>a (riprodotta da TIBS<br />
19-4, 153, aprile ’94) sono <strong>in</strong><strong>di</strong>cate alcune <strong>di</strong><br />
queste dest<strong>in</strong>azioni.<br />
Situazione 1): esistono le prote<strong>in</strong>e tiros<strong>in</strong> c<strong>in</strong>asi <strong>di</strong> adesioni focali (FAK), che possono trovarsi <strong>in</strong><br />
competizione con una PTP (<strong>in</strong><strong>di</strong>cata con ?), per esempio la PTP1.<br />
Situazione 2): nel nucleo è possibile trovare una DPTP 61 F [p61/62n, che nasce per splic<strong>in</strong>g<br />
alternativo <strong>di</strong> un’altra, la DPTP 61 F (p61/62m)].La prima, contrad<strong>di</strong>st<strong>in</strong>ta da n f<strong>in</strong>ale- n=nucleo, ha<br />
una sequenza <strong>di</strong> 11 AA idrofilici che assomiglia alla sequenza <strong>di</strong> dest<strong>in</strong>azione al nucleo. Infatti è<br />
KRRRGNRLKKSKTK (<strong>in</strong> grassetto sono <strong>in</strong><strong>di</strong>cati gli AA nettamente basici K-lis<strong>in</strong>a o R-arg<strong>in</strong><strong>in</strong>a).<br />
Ve<strong>di</strong> anche <strong>in</strong><strong>di</strong>cazioni <strong>di</strong> pag.6, ovvero alcune sequenze altamente basiche determ<strong>in</strong>ano<br />
l’importazione nel nucleo delle prote<strong>in</strong>e che le contengono.<br />
Situazione 3): sempre nell’ambito <strong>di</strong> associazione a membrana, la PTP2 può legarsi ad un<br />
recettore per fattore <strong>di</strong> crescita (GFR-Growth Factor Receptor), fosforilato su tiros<strong>in</strong>a, tramite il<br />
proprio SH2; ve<strong>di</strong> pag.163 caso comune a PTP1D o Syp.<br />
Situazione 4): è possibile un legame alla matrice, come PTPH1, ma anche all’ER, o<strong>pp</strong>ure alla<br />
matrice mitocondriale. Infatti esiste la sopra citata DPTP 61F8p61/62m - m=matrice - che al posto<br />
degli 11 AA sopra citati presenta la sequenza KRRSLLTYIAAGVVVGICAYAYTKLG, che è<br />
tipicamente idrofobica, e adatta ad attraversare la membrana ER ed anche quella mitocondriale<br />
<strong>in</strong>terna.<br />
167
Interazione: Cader<strong>in</strong>e - Tiros<strong>in</strong> C<strong>in</strong>asi - Tiros<strong>in</strong> Fosfatasi<br />
[da Curr.Op<strong>in</strong>.Cell.Biol. 11 (5) 554 (ott.1999)]<br />
In relazione alle molecole d’adesione (CAM), che costituiscono una famiglia assai articolata,<br />
possiamo oggi comprendere nei particolari il funzionamento delle cader<strong>in</strong>e, che ra<strong>pp</strong>resentano<br />
certamente una classe importante <strong>di</strong> CAM. Ricor<strong>di</strong>amo che le cader<strong>in</strong>e sono CAM calcio<strong>di</strong>pendenti.<br />
Possiamo far riferimento a quanto già trattato a pag.73 per a<strong>pp</strong>rofon<strong>di</strong>rlo con la seguente figura.<br />
In alto è schematizzata la struttura primaria delle cader<strong>in</strong>e, con i seguenti dom<strong>in</strong>i (com<strong>in</strong>ciando da<br />
s<strong>in</strong>istra):<br />
CYTO - è il dom<strong>in</strong>io citoplasmatico, che contiene, a sua volta, le zone <strong>di</strong> legame a β-caten<strong>in</strong>e o<br />
alla plakoglob<strong>in</strong>a (β-cat/plak), che a sua volta lega la α-caten<strong>in</strong>a. Quest’ultima lega, ancora, l’act<strong>in</strong>a<br />
o <strong>di</strong>rettamente, o<strong>pp</strong>ure attraverso l’<strong>in</strong>terposizione <strong>di</strong> α-act<strong>in</strong><strong>in</strong>a, v<strong>in</strong>cul<strong>in</strong>a e altre (ve<strong>di</strong> figura <strong>di</strong><br />
pag<strong>in</strong>a seguente). Tutte queste prote<strong>in</strong>e, nel loro <strong>in</strong>sieme, costituiscono il CAC (Cadher<strong>in</strong>-<br />
Associated Complex).<br />
Il dom<strong>in</strong>io CYTO comprende anche la zona <strong>di</strong> legame ad una famiglia <strong>di</strong> caten<strong>in</strong>e, le p<strong>12</strong>0.<br />
Queste ultime furono isolate <strong>in</strong>izialmente come substrati dell’azione della tiros<strong>in</strong>-c<strong>in</strong>asi Src. In<br />
particolare la prote<strong>in</strong>a p<strong>12</strong>0 ctn (la più nota) contiene 10 copie del dom<strong>in</strong>io arma<strong>di</strong>llo (formato da 42<br />
amm<strong>in</strong>oaci<strong>di</strong>). La p<strong>12</strong>0 è fosforilabile e <strong>di</strong>versi riscontri sperimentali depongono a favore <strong>di</strong> un suo<br />
stato de-fosforilato e coesivo <strong>in</strong> antitesi ad uno stato fosforilato e <strong>di</strong>ssociato, per il contributo<br />
(ovvio) della repulsione elettrostatica tra cariche negative portate dal gru<strong>pp</strong>o fosforico.<br />
TM - è il tratto transmembrana formato <strong>in</strong> prevalenza da amm<strong>in</strong>oaci<strong>di</strong> idrofobici.<br />
C5, C4, C3, C2, C1 - sono i dom<strong>in</strong>i costituenti l’ecto-doma<strong>in</strong>, che legano (non sempre) calcio.<br />
L’ultimo <strong>di</strong> questi dom<strong>in</strong>i, il C1, vic<strong>in</strong>o all’N-term<strong>in</strong>ale, presenta la sequenza HAV tipica delle<br />
cader<strong>in</strong>e (ve<strong>di</strong> figura sopra e pag.73) che è importante per i legami <strong>di</strong> tipo omofilico.<br />
Nella figura (sopra) sono illustrati i dom<strong>in</strong>i leganti calcio, ed il calcio stesso.<br />
168
E’ altresì illustrata l’<strong>in</strong>terazione <strong>di</strong> tipo cis, tra cader<strong>in</strong>e cioè della stessa cellula, che si realizza alle<br />
<strong>in</strong>terconnessioni tra C2 e C1. Il Calcio determ<strong>in</strong>a una maggiore rigi<strong>di</strong>tà della catena e consente lo<br />
stabilirsi del legame cis. Importanti sono i legami trans (tra cader<strong>in</strong>e <strong>di</strong> cellule <strong>di</strong>verse) che sono<br />
promossi da un <strong>in</strong>serimento del triptofano-2 (W2 - secondo amm<strong>in</strong>oacido della caten<strong>in</strong>a, qu<strong>in</strong><strong>di</strong><br />
praticamente all’N-term<strong>in</strong>ale), che <strong>in</strong>teragisce con l’alan<strong>in</strong>a-80, che è al centro della terna HAV. La<br />
struttura HAV-W è essenziale per le <strong>di</strong>merizzazioni <strong>di</strong> tipo trans, ma non per quelle <strong>di</strong> tipo cis.<br />
Completiamo ora l’analisi <strong>di</strong> quanto accade nella zona citosolica, che <strong>in</strong>teressa per le connessioni<br />
al citoscheletro, e per comprendere il ruolo centrale delle tiros<strong>in</strong>-c<strong>in</strong>asi (come Src e, più <strong>in</strong> generale<br />
le RTK- attività tiros<strong>in</strong> c<strong>in</strong>asica associata a recettori), nonché delle prote<strong>in</strong>e-tiros<strong>in</strong>-<strong>fosfatasi</strong> (PTP)<br />
che sono trattate a pag.162 e seguenti.<br />
L’aggregato che si forma nella parte citosolica è denom<strong>in</strong>ato CAC (Cadher<strong>in</strong>-Associated-Complex)<br />
e alla sua formazione contribuiscono una molteplicità <strong>di</strong> macromolecole. Comunque nella figura qui<br />
sotto sono illustrate la β-caten<strong>in</strong>a e la Plakoglob<strong>in</strong>a, fosforilabili <strong>in</strong> ser<strong>in</strong>a (S), tiros<strong>in</strong>a (Y) e treon<strong>in</strong>a<br />
(T). Ma l’attività più importante è la fosforilazione a carico delle tiros<strong>in</strong>e. La fosforilazione, <strong>in</strong><br />
generale, <strong>di</strong>ssocia la β-caten<strong>in</strong>a e la Plakoglob<strong>in</strong>a dal CAC, annullando l’adesione. Infatti<br />
l’esposizione ad un certo numero <strong>di</strong> fattori <strong>di</strong> crescita (EGF, TGF-β, PDGF, CSF1, HGF) si traduce<br />
nella fosforilazione <strong>di</strong> tiros<strong>in</strong>e <strong>di</strong>retta (ad opera <strong>di</strong> recettori con attività RTK) o<strong>pp</strong>ure <strong>in</strong><strong>di</strong>retta<br />
(attraverso attività tiros<strong>in</strong> c<strong>in</strong>asica non-recettoriale come src).<br />
Al contrario l’azione <strong>di</strong> tiros<strong>in</strong>-<strong>fosfatasi</strong> (PTP) come PTPµ (ve<strong>di</strong> figura b <strong>di</strong> pag.166) <strong>in</strong><strong>di</strong>rizzate alle<br />
tiros<strong>in</strong>e fosforilate dai propri zip-code (il dom<strong>in</strong>io PTP stesso è uno zip-code) porta alla defosforilazione<br />
<strong>di</strong> prote<strong>in</strong>e della famiglia arma<strong>di</strong>llo, ed al conseguente aumento <strong>di</strong> coesività.<br />
CAC: Cader<strong>in</strong> Associated Complex<br />
169
<strong>Prote<strong>in</strong>e</strong> <strong>fosfatasi</strong> a funzione mista<br />
Con quest’a<strong>pp</strong>rofon<strong>di</strong>mento delle prote<strong>in</strong>e tiros<strong>in</strong> <strong>fosfatasi</strong>, possiamo riprendere il <strong>di</strong>scorso con la<br />
MAP-c<strong>in</strong>asi <strong>fosfatasi</strong>, che era stata <strong>in</strong>trodotta a pag.151. In particolare era prevista, per tale<br />
<strong>fosfatasi</strong>, la funzione mista, cioè la possibilità <strong>di</strong> idrolizzare sia tiros<strong>in</strong>e che ser<strong>in</strong>e/treon<strong>in</strong>e. Diverse<br />
<strong>fosfatasi</strong> con tali proprietà sono state sequenziale, ed ora possiamo confrontare la loro sequenza.<br />
Riassumiamo brevemente una serie <strong>di</strong> esperimenti, condotti peraltro <strong>in</strong> laboratori <strong>di</strong>fferenti:<br />
1) Se fibroblasti NIH 3T3 sono stimolati da siero, si ha una rapida attivazione (5 m<strong>in</strong>uti circa) della<br />
MAP-c<strong>in</strong>asi, ma la sua attività com<strong>in</strong>cia a scendere dopo circa 60 m<strong>in</strong>uti. È stato accertato che<br />
l’espressione della do<strong>pp</strong>ia <strong>fosfatasi</strong> 3CH134 co<strong>in</strong>cide, nel tempo, con la defosforilazione ed <strong>in</strong><br />
attivazione della MAP-c<strong>in</strong>asi. Inoltre <strong>in</strong> cellule <strong>di</strong> scimmia<br />
2) COS trasfettate ed arricchite con la do<strong>pp</strong>ia <strong>fosfatasi</strong> 3CH134 si aveva selettivo blocco<br />
dell’attivazione della MAP-c<strong>in</strong>asi.<br />
3) Anche nel bud<strong>di</strong>ng yeast Saccharomyces cerevisiae è stata stu<strong>di</strong>ata e sequenziata una MSG5<br />
con analoghe proprietà <strong>di</strong> do<strong>pp</strong>ia attività prote<strong>in</strong>-<strong>fosfatasi</strong>ca.<br />
È stata stu<strong>di</strong>ata anche la PAC1, che è presente nei Mammiferi ed è omologa della 3CH134.<br />
Una do<strong>pp</strong>ia prote<strong>in</strong>a <strong>fosfatasi</strong>, già presa <strong>in</strong> considerazione, è la Cdc-25, che rimuove il fosfato dai<br />
residui Thr-14 e Tyr-15 <strong>in</strong>seriti nel Rossmann motiv della Cdc-2. Ricor<strong>di</strong>amo (ve<strong>di</strong> pag.152) che si<br />
tratta <strong>di</strong> un subdom<strong>in</strong>io (il I) <strong>di</strong>verso dal subdom<strong>in</strong>io (l’VIII) fosforilato nelle MAP-c<strong>in</strong>asi,<br />
do<strong>pp</strong>iamente defosforilati dalle MAP-c<strong>in</strong>asi <strong>fosfatasi</strong>.<br />
Nella seguente figura (da Current Biology, 4, 647, 1994), è riportata la sequenza amm<strong>in</strong>oaci<strong>di</strong>ca<br />
nei <strong>di</strong>ntorni del sito attivo <strong>di</strong> <strong>di</strong>verse PTP, sia solo tiros<strong>in</strong> <strong>fosfatasi</strong> che con do<strong>pp</strong>ia aff<strong>in</strong>ità.<br />
La PTP-1B è stata stu<strong>di</strong>ata per prima.<br />
La VHI (co<strong>in</strong>volta nel vaiolo bov<strong>in</strong>o) ha do<strong>pp</strong>ia specificità.<br />
La CL100 e la MAP-c<strong>in</strong>asi <strong>fosfatasi</strong> umana, omologa della 3CH134 espressa dal topo (ambedue<br />
presentano do<strong>pp</strong>ia specificità).<br />
La Pac1 è presente nei mammiferi ed è omologa delle due precedenti.<br />
La MSG25 è del lievito, con do<strong>pp</strong>ia specificità.<br />
La Cdc-25 umana è nota.<br />
Si può constatare che non esistono elementi strutturali <strong>di</strong> tale breve tratto <strong>di</strong> sequenza per<br />
prevedere la semplice o do<strong>pp</strong>ia specificità come prote<strong>in</strong>a <strong>fosfatasi</strong>.<br />
Possiamo concludere che tale sequenza è caratteristica <strong>di</strong> tiros<strong>in</strong> prote<strong>in</strong>e <strong>fosfatasi</strong>, che, <strong>in</strong> alcuni<br />
casi, possono essere anche tiros<strong>in</strong>a e ser<strong>in</strong>a <strong>fosfatasi</strong>.<br />
Si può constatare la sequenza Cx5R caratteristica <strong>di</strong> tutte le PTP.<br />
170
Enzimi che producono AMPciclico e GMPciclico<br />
Abbiamo completato lo stu<strong>di</strong>o delle prote<strong>in</strong>e c<strong>in</strong>asi e delle prote<strong>in</strong>e <strong>fosfatasi</strong>, che sovente<br />
partecipano a reazioni <strong>in</strong> sequenza o cascata, dalla formulazione anche molto complessa. Nel<br />
flusso <strong>di</strong> <strong>in</strong>formazioni che lega un evento extracellulare ad un processo endocellulare, <strong>in</strong> genere<br />
metabolico (per esempio s<strong>in</strong>tesi o degradazione <strong>di</strong> glicogeno), troviamo gli importanti nucleoti<strong>di</strong><br />
ciclici AMPC e GMPC, che possono stimolare specifiche prote<strong>in</strong>e c<strong>in</strong>asi. Ve<strong>di</strong>amo <strong>in</strong> dettaglio i<br />
sistemi enzimatici implicati nella s<strong>in</strong>tesi <strong>di</strong> tali importanti “secon<strong>di</strong> messaggeri”.<br />
Adenilato ciclasi (A.C.)<br />
Ne sono conosciute 9 forme. Le più stu<strong>di</strong>ate sono 2:<br />
⇒ Adenilato ciclasi calmodul<strong>in</strong>a <strong>in</strong><strong>di</strong>pendente.<br />
⇒ Adenilato ciclasi calmodul<strong>in</strong>a <strong>di</strong>pendente.<br />
Occupiamoci prima della CaM – <strong>di</strong>pendente, che è stata clonata da cDNA. È nota altresì la<br />
sequenza ricavata <strong>di</strong>rettamente dall’analisi <strong>di</strong> alcuni pepti<strong>di</strong>, che risultano sottol<strong>in</strong>eati a pag.172.<br />
Infatti l’Adenilato Ciclasi CaM – <strong>di</strong>pendente è stata purificata con il metodo della cromatografia per<br />
aff<strong>in</strong>ità, con colonne cromatografiche portanti calmodul<strong>in</strong>a o forscol<strong>in</strong>a (ve<strong>di</strong> dopo). Facilmente la<br />
A.C. purificata porta a sé strettamente legata la subunità α della prote<strong>in</strong>a-G stimolatoria. È stata<br />
verificata, qu<strong>in</strong><strong>di</strong>, una perfetta corrispondenza fra una parte della prote<strong>in</strong>a effettivamente estratta<br />
da cervello bov<strong>in</strong>o ed il gene che co<strong>di</strong>fica per l’Adenilato Ciclasi (A.C.) CaM – <strong>di</strong>pendente.<br />
È <strong>in</strong>teressante che non presenta omologia <strong>di</strong> sequenza con l’A.C. CaM – <strong>in</strong><strong>di</strong>pendente, qu<strong>in</strong><strong>di</strong><br />
sono due enzimi <strong>di</strong>st<strong>in</strong>ti.<br />
In riferimento, qu<strong>in</strong><strong>di</strong>, alla struttura primaria putativa (pag.172) ve<strong>di</strong>amo <strong>di</strong> estrapolare alcune<br />
proprietà dell’A.C. CaM – <strong>di</strong>pendente.<br />
▪ È formata da 1134 AA (P.M. <strong>12</strong>0000 Da circa) e contiene <strong>12</strong> tratti idrofobici transmembrana<br />
(ve<strong>di</strong> schema), che sono ripartiti <strong>in</strong> 2 gru<strong>pp</strong>i da 6 ciascuno. I due gru<strong>pp</strong>i <strong>di</strong> 6 tratti sono separati da<br />
un dom<strong>in</strong>io idrofilico <strong>di</strong> P.M. 43000 Da (dall’AA 236 all’AA 613). Al C-term<strong>in</strong>ale esiste un’altra zona<br />
idrofilia (36 KDa). Anche l’amm<strong>in</strong>o-term<strong>in</strong>ale è idrofilico. Queste tre zone sono co<strong>in</strong>volte nel<br />
legame con l’ATP ed il suo processamento ad AMP – ciclico.<br />
Poiché la prote<strong>in</strong>a lega ATP, dovrà contenere alcuni elementi strutturali comuni alle prote<strong>in</strong>e c<strong>in</strong>asi<br />
(ve<strong>di</strong> classificazione HQH pag.82 e seguenti). Analizziamo <strong>in</strong>fatti i residui amm<strong>in</strong>oaci<strong>di</strong>ci presenti<br />
da 16 a 21 e osserviamo la “curiosità” dovuta a ben 7 glic<strong>in</strong>e <strong>in</strong> successione che precedono:<br />
⇓ ⇓ ⇓<br />
− Gly16 – Ala17 – Gly18 – Glu19 – Ser20 – Gly21 –<br />
Sono evidenziati i residui <strong>di</strong> glic<strong>in</strong>a, che si susseguono secondo il “classico” Rossmann motiv Gly-<br />
X-Gly-X-X-Gly, e qu<strong>in</strong><strong>di</strong> questa è, teoricamente, la zona dest<strong>in</strong>ata al legame con l’ATP.<br />
From Krup<strong>in</strong>sky et all. Science 244, 1558, 1989<br />
171
172
▪ Contiene un sito <strong>di</strong> glicosilazione extracellulare. Infatti, <strong>in</strong> posizione 706 esiste l’asparag<strong>in</strong>a (N)<br />
seguita, <strong>in</strong> seconda posizione, dalla ser<strong>in</strong>a. Trattasi della tipica sequenza Asn-X-Ser, sito <strong>di</strong><br />
glicosilazione all’N (ve<strong>di</strong> pag.28).<br />
▪ Contiene due ser<strong>in</strong>e fosforilabili. Infatti la Ser-481 è seguita, <strong>in</strong> seconda posizione, da Arg-Arg-<br />
Lys, e questo è un requisito essenziale per la fosforilabilità da PKC (<strong>in</strong> realtà possono essere<br />
presenti anche AA basici prima del residuo fosforilabile). Infatti una A.C. da globuli rossi <strong>di</strong> rana, <strong>di</strong><br />
P.M. <strong>12</strong>0000 è fosforilata da PKC.<br />
Anche la Ser-1035 è fosforilabile da PKA (è preceduta, <strong>in</strong> seconda e terza posizione, da Arg-Arg).<br />
Queste fosforilazioni sono previste come <strong>in</strong>ibizioni a feed-back. La PKA è attivata, per def<strong>in</strong>izione,<br />
da AMPC e può essere regolata dall’<strong>in</strong>ibizione dell’enzima che produce l’AMP – ciclico stesso.<br />
Anche il recettore β-adrenergico è estensivamente fosforilato e <strong>in</strong>attivato da prote<strong>in</strong>e c<strong>in</strong>asi.<br />
▪ Contiene un dom<strong>in</strong>io legante CaM al C-term<strong>in</strong>ale. È situato tra la Val<strong>in</strong>a-987 e la Glic<strong>in</strong>a-1050.<br />
Possiede proprietà comuni ad altri dom<strong>in</strong>i leganti CaM <strong>di</strong> altre prote<strong>in</strong>e. Come tale, l’A.C. CaM –<br />
<strong>di</strong>pendente sarà proteolizzata dalla calpa<strong>in</strong>a (questo è un tema ricorrente <strong>di</strong> tutte le prote<strong>in</strong>e che<br />
legano calmodul<strong>in</strong>a; per es.: Fosfo<strong>di</strong>esterasi per AMPC, Ca-ATPasi <strong>di</strong> membrane plasmatiche,<br />
Calc<strong>in</strong>eur<strong>in</strong>a, Prote<strong>in</strong>a C<strong>in</strong>asi CaM – <strong>di</strong>pendente).<br />
Nel complesso esistono strette omologie con altre GuanilatoCiclasi, mentre esistono nette<br />
<strong>di</strong>fferenze tra A.C. CaM – <strong>di</strong>pendenti e <strong>in</strong><strong>di</strong>pendenti.<br />
La maggior parte delle Adenilato Ciclasi sono attivate da concentrazioni micro-molari del <strong>di</strong>terpene<br />
Forscol<strong>in</strong>a (isolato dalla pianta Coleus forskohlii). Infatti, come è stato detto all’<strong>in</strong>izio del<br />
paragrafo, la cromatografia per aff<strong>in</strong>ità con forscol<strong>in</strong>a consente la purificazione dell’A.C. CaM –<br />
<strong>di</strong>pendente dal cervello bov<strong>in</strong>o.<br />
L’Adenilato Ciclasi CaM – <strong>in</strong><strong>di</strong>pendente è stata clonata ed è formata da 834 AA (P.M. 92000 da),<br />
qu<strong>in</strong><strong>di</strong> ha un P.M. <strong>in</strong>feriore alla CaM –<strong>di</strong>pendente. Non presenta omologie con la CaM –<br />
<strong>di</strong>pendente.<br />
Funzioni dell’Adenilato Ciclasi CaM – <strong>di</strong>pendente<br />
È alquanto <strong>in</strong>comprensibile l’attivabilità da CaM dell’A.C., <strong>in</strong> relazione soprattutto al fatto che la<br />
CaM è anche un noto attivatore dell’enzima Fosfo<strong>di</strong>esterasi, l’enzima cioè che sc<strong>in</strong>de l’AMPC<br />
(ricor<strong>di</strong>amo che la CaM fu scoperta per tale proprietà, ed ancora oggi viene denom<strong>in</strong>ata “attivatore<br />
della fosfo<strong>di</strong>esterasi”). Qu<strong>in</strong><strong>di</strong> la CaM, contemporaneamente, attiva sia l’enzima che produce<br />
l’AMPC che l’enzima che lo sc<strong>in</strong>de (cioè la fosfo<strong>di</strong>esterasi) e qu<strong>in</strong><strong>di</strong> s’<strong>in</strong>staurerebbe un ciclo futile.<br />
In realtà l’A.C. non può essere attivata dalla sola CaM e, come è oggi ben noto (ritorneremo<br />
sull’argomento), svolgono un ruolo importante le prote<strong>in</strong>e-G, cioè attivate da GTP, che sono<br />
classici trasduttori del segnale.<br />
Interessante è la struttura transmembrana dell’A.C., tipica <strong>di</strong> una prote<strong>in</strong>a che forma canali. È<br />
particolarmente marcata la somiglianza tra A.C. e la prote<strong>in</strong>a “multidrug resistence”, che vedremo<br />
più avanti. Può comunque essere ipotizzato che tale A.C. sia anche implicata nell’esportazione <strong>di</strong><br />
AMPC dalle cellule, come nel Dictyostelum <strong>di</strong>scoideum, che lo s<strong>in</strong>tetizza e lo esporta per<br />
controllare la chemiotassi, l’aggregazione e la <strong>di</strong>fferenziazione.<br />
AMP – ciclico <strong>in</strong> Eucarioti semplici e <strong>in</strong> Procarioti<br />
Negli organismi superiori, l’AMPC me<strong>di</strong>a, come abbiamo già visto, segnali <strong>in</strong>tracellulari: attiva una<br />
PKA. Nel Dictyostelium <strong>di</strong>scoideum (D.D.), me<strong>di</strong>a <strong>in</strong>vece segnali <strong>in</strong>tercellulari ed è prodotto come<br />
“segnale <strong>di</strong> carenza <strong>di</strong> nutrienti” e promuove l’aggregazione <strong>di</strong> cellule. In situazione d’emergenza, il<br />
D.D. produce nel mezzo AMPC, che è percepito da altre cellule le quali, per chemiotassi, si<br />
aggregano alla cellula “fondatrice” e sono, qu<strong>in</strong><strong>di</strong>, da questa “reclutate”. Il D.D. è un eucariote<br />
semplice e, quando i nutrienti sono abbondanti, il D.D. esiste come cellula <strong>in</strong><strong>di</strong>pendente.<br />
173
D’altra parte abbiamo visto che, <strong>in</strong> procarioti, l’AMPC si lega alla prote<strong>in</strong>a CAP (ve<strong>di</strong> pag.88), che si<br />
lega al DNA <strong>in</strong> corrispondenza <strong>di</strong> certi siti promotori, con conseguente trascrizione <strong>di</strong> geni che<br />
consentono l’utilizzo <strong>di</strong> nutrienti alternativi (per esempio lattosio) ad un nutriente <strong>di</strong> base (per<br />
esempio glucosio).<br />
Do<strong>pp</strong>ia azione della CaM su Adenilato Ciclasi (A.C.) e Fosfo<strong>di</strong>esterasi (PDE)<br />
Effetto paradosso della Calmodul<strong>in</strong>a:<br />
→ Attiva l’Adenilato Ciclasi (che produce AMPC)<br />
→ Attiva la Fosfo<strong>di</strong>esterasi (PDE) che idrolizza l’AMPC<br />
→ Potrebbe essere assicurata la transitorietà nella formazione <strong>di</strong> AMPC<br />
→ Potrebbe, l’aumento <strong>di</strong> calcio, smorzare i segnali da AMPC per far risaltare i segnali Ca –<br />
<strong>di</strong>pendenti<br />
174
Inserto: generalità su toss<strong>in</strong>e batteriche<br />
Toss<strong>in</strong>e<br />
batteriche<br />
Esotoss<strong>in</strong>e<br />
Endotoss<strong>in</strong>e<br />
L<br />
I<br />
P<br />
O<br />
P<br />
O<br />
L<br />
I<br />
S<br />
A<br />
C<br />
C<br />
A<br />
R<br />
I<br />
D<br />
E<br />
polisaccaride<br />
lipide A<br />
Per es.: fattore ADP-ribosilante del Colera e<br />
Adenilato ciclasi <strong>di</strong> Pertosse e Antrace (ve<strong>di</strong><br />
pag.176)<br />
Botulismo<br />
da “Le Scienze” 290, 34, (1992)<br />
175<br />
- determ<strong>in</strong>a l’antigenicità (catena Ospecifica)<br />
- segmento <strong>in</strong>terno<br />
- segmento <strong>in</strong>terno con Kdo<br />
- causa <strong>di</strong> tutti gli effetti nocivi delle<br />
endotoss<strong>in</strong>e. Per esempio E. coli e<br />
Salmonella typhimurium possiedono lo<br />
stesso lipide A.
Adenilato ciclasi toss<strong>in</strong>e<br />
Già avevamo parlato <strong>di</strong> questa toss<strong>in</strong>a (ve<strong>di</strong> pag.88). Analizziamo ora l’Adenilato ciclasi prodotta<br />
dal batterio Bordetella pertussis (che causa la pertosse) e dal Bacillus anthracis (che causa il<br />
carbonchio).<br />
La Bordetella pertussis produce una miscela <strong>di</strong> toss<strong>in</strong>e, tra cui la Pertussis Tox<strong>in</strong> propriamente<br />
detta (che è un enzima che ADP-ribosila le subunità α delle Gi).<br />
Contiene <strong>in</strong>oltre un’<strong>in</strong>solita Adenilato ciclasi, che è CaM stimolata (dec<strong>in</strong>e <strong>di</strong> volte). Il batterio non<br />
possiede Calmodul<strong>in</strong>a. Viceversa questa Adenilato Ciclasi (A.C.) penetra facilmente nelle cellule<br />
ospiti e <strong>in</strong> esse trova la CaM, che la stimola. La sovra<strong>pp</strong>roduzione <strong>di</strong> AMPC blocca la chemiotassi,<br />
la fagocitosi dei macrofagi. La malattia è caratterizzata da assenza <strong>di</strong> febbre (perché i neutrofili<br />
non rispondono) e da elevata <strong>in</strong>cidenza <strong>di</strong> batteri della polmonite, grazie alla scarsa risposta<br />
immunitaria. Esiste una prova <strong>di</strong> questo comportamento.<br />
Un mutante <strong>di</strong> Bordetella pertussis, mancante <strong>di</strong> A.C. è non patologico. Questa A.C. produce molto<br />
AMPC, avendo un elevato numero <strong>di</strong> turnover.<br />
Qui a lato è riportato lo<br />
schema della struttura<br />
primaria dell’A.C. <strong>di</strong><br />
Bordetella pertussis. Nei<br />
primi 450 AA c’è l’attività<br />
A.C., più, molto<br />
importante, un dom<strong>in</strong>io<br />
legante CaM.<br />
Proseguendo, dall’AA 450<br />
al 1600, abbiamo una<br />
catena polipepti<strong>di</strong>ca che<br />
ha omologia <strong>di</strong> sequenza<br />
con l’α-emolis<strong>in</strong>a <strong>di</strong> E.coli<br />
(è una esotoss<strong>in</strong>a che lisa i<br />
globuli rossi). L’omologia è<br />
particolarmente<br />
pronunciata tra i residui<br />
640 e 910 (zona a<br />
tratteggio orizzontale).<br />
Inoltre, tra l’AA 1000 e 1600, esiste una sequenza Gly – Gly – Asp – Gly – Asp – Asp – Thr – Leu<br />
– X (9 AA) ripetuta un numero rilevante <strong>di</strong> volte (sempre omologa con l’α-emolis<strong>in</strong>a).<br />
Essendo nota la sequenza putativa è possibile costruire un grafico <strong>di</strong> idrofobicità e sono<br />
<strong>in</strong><strong>di</strong>viduabili 4 tratti idrofobici. Se ne ipotizza la partecipazione al processo <strong>di</strong> penetrazione della<br />
prote<strong>in</strong>a nella cellula ospite. Se si opera la delezione <strong>in</strong><strong>di</strong>cata <strong>in</strong> figura, non si ha più penetrazione<br />
all’<strong>in</strong>terno della cellula ospite.<br />
È cruciale la capacità <strong>di</strong> essere attivata da CaM. Infatti la CaM è una prote<strong>in</strong>a presente <strong>in</strong> tutte le<br />
cellule eucariote con una struttura molto ben conservata. Qu<strong>in</strong><strong>di</strong> CaM è un ottimo marker<br />
endocellulare <strong>di</strong> qualsiasi cellula eucariotica. Pertanto l’A.C., una volta penetrata all’<strong>in</strong>terno <strong>di</strong> una<br />
cellula, viene gradualmente attivata. Tale A.C. ha un numero <strong>di</strong> turnover molto più alto dell’A.C.<br />
endogena, e si ha sovra<strong>pp</strong>roduzione <strong>di</strong> AMPC, con sbilanciamento <strong>di</strong> delicati cicli regolatori.<br />
Anche Bacillus anthracis genera una toss<strong>in</strong>a del tutto analoga a quella <strong>di</strong> Bordetella pertussis.<br />
Anch’essa contiene all’N-term<strong>in</strong>ale l’attività A.C. stimolata da CaM. Entra nelle cellule per<br />
endocitosi.<br />
176
From E.Hanski TIBS 14 459 (1989)<br />
177<br />
Qui a lato è riprodotto lo schema<br />
d’azione <strong>di</strong> questa toss<strong>in</strong>a. Le parti (a)<br />
e (b) non richiedono commenti.<br />
(c): per l’<strong>in</strong>attivazione si è visto che è<br />
strettamente ATP <strong>di</strong>pendente. È<br />
ipotizzabile anche l’<strong>in</strong>tervento delle<br />
calpa<strong>in</strong>e endocellulari (come<br />
meccanismo d’azione comune a tutte le<br />
prote<strong>in</strong>e che legano CaM; ve<strong>di</strong> pag.44).<br />
Essendo ATP-<strong>di</strong>pendente, la proteolisi<br />
potrebbe essere <strong>di</strong>pendente da<br />
ubiquit<strong>in</strong>a (ve<strong>di</strong> pag.36).<br />
Si può constatare che questo<br />
meccanismo d’azione <strong>di</strong> una toss<strong>in</strong>a<br />
batterica ha analogie <strong>di</strong> funzionamento<br />
con il batterio patogeno Yers<strong>in</strong>ia pestis<br />
(ve<strong>di</strong> pag.164), che <strong>in</strong>troduceva<br />
nell’organismo <strong>in</strong>fettato una potente<br />
attività prote<strong>in</strong>a tiros<strong>in</strong> <strong>fosfatasi</strong>ca<br />
(PTP).
Il GMPciclico (GMPC)<br />
Qui sotto è riportata la struttura dell’AMP – ciclico e del GMP – ciclico. Trattasi <strong>di</strong> esteri fosforici<br />
ciclici, che per semplice idrolisi possono convertirsi nei comuni aci<strong>di</strong> adenilici (AMP) o guanilici<br />
(GMP).<br />
AMPc<br />
GMPc<br />
Del ruolo dell’AMPC quale secondo messaggero abbiamo già parlato. Dell’esistenza <strong>di</strong> un GMPC si<br />
è com<strong>in</strong>ciato a parlare solo <strong>in</strong> tempi più recenti, anche perché la sua concentrazione, <strong>in</strong> generale,<br />
nelle cellule eucariote è <strong>di</strong> gran lunga <strong>in</strong>feriore all’AMPC. L’AMPC, <strong>in</strong> genere, è presente a<br />
concentrazioni <strong>in</strong>torno all’1 micromolare, mentre il GMPC oscilla <strong>in</strong>torno allo 0.1 - 0.001<br />
micromolare. Il GMPC fu scoperto come importante componente del processo <strong>di</strong> fototrasduzione<br />
<strong>in</strong>torno alla metà degli anni ’80 (ve<strong>di</strong> <strong>in</strong>serto pag.292). Intorno alla metà degli anni ’80, furono<br />
scoperti gli importanti fattori natriuretici (ormoni), che <strong>in</strong>ducono la produzione <strong>di</strong> GMPC<br />
<strong>in</strong>tracellulari. Tutto lascia <strong>in</strong>tendere che il GMPC sia implicato <strong>in</strong> una varietà <strong>di</strong> altri importanti<br />
processi cellulari.<br />
Ve<strong>di</strong>amo ora le proprietà degli enzimi che lo producono (guanilato ciclasi) che, a <strong>di</strong>fferenza delle<br />
adenilato ciclasi, sono note <strong>in</strong> più <strong>di</strong> due forme (ne descriveremo 4).<br />
Guanilato ciclasi <strong>di</strong>pendente da calcio – recover<strong>in</strong>a<br />
Com<strong>in</strong>ciamo da questa forma perché connessa al processo <strong>di</strong> foto-trasduzione nei vertebrati, dove<br />
il ruolo del GMPC è stato completamente def<strong>in</strong>ito. Vedremo <strong>in</strong> dettaglio più avanti tutto il processo.<br />
Ora ricor<strong>di</strong>amo solo che il GMPC tiene aperti i canali per il so<strong>di</strong>o della membrana del segmento<br />
esterno dei bastoncelli. Uno stimolo lum<strong>in</strong>oso porta ad un calo massiccio del GMPC con<br />
conseguente chiusura dei canali stessi. Nella fase <strong>di</strong> riposo, il GMPC deve essere ris<strong>in</strong>tetizzato<br />
dalla guanilato ciclasi (G.C.), che è calcio <strong>di</strong>pendente. Si pensava (<strong>in</strong> analogia con quanto succede<br />
con l’Adenilato Ciclasi) che anche la G.C. <strong>di</strong>pendesse dalla calmodul<strong>in</strong>a. Invece è stato scoperto<br />
da Stryer che è co<strong>in</strong>volta una prote<strong>in</strong>a della famiglia della CaM, nota con il nome <strong>di</strong> recover<strong>in</strong>a.<br />
Tale prote<strong>in</strong>a assicura una stimolazione dell’attività G.C. quando il calcio <strong>in</strong>tracellulari (che pure è<br />
molto basso, circa 0.1 – 0.3 µM) scende ulteriormente. È stato accettato uno schema <strong>di</strong><br />
funzionamento del tipo:<br />
178
La Recover<strong>in</strong>a (con P.M. 23000: possiede 4 EF hand come la CaM) a calcio elevato lo lega,<br />
secondo un equilibrio <strong>di</strong> associazione-<strong>di</strong>ssociazione e, <strong>in</strong> tale forma, si lega alla G.C.,<br />
<strong>di</strong>sattivandola. Se il calcio scende, la recover<strong>in</strong>a perderà lo ione calcio e, nella forma che non lega<br />
calcio, si <strong>di</strong>ssocerà da G.C., lasciandola libera <strong>di</strong> esprimere attività catalitica. Premettiamo che<br />
questo è soltanto un modello. È accertato che sono co<strong>in</strong>volti anche altri elementi ancora da<br />
identificare, ma, nelle l<strong>in</strong>ee generali, è accettato.<br />
Interessante che la recover<strong>in</strong>a è un po’ la controparte della calmodul<strong>in</strong>a. In genere, la calmodul<strong>in</strong>a<br />
attiva gli enzimi ai quali si lega (ve<strong>di</strong> calcio – ATPasi e Adenilato Ciclasi). Qui la recover<strong>in</strong>a<br />
<strong>di</strong>sattiva l’enzima al quale si lega.<br />
La recover<strong>in</strong>a è stata scoperta e clonata nel 1991 da Lubert Stryer ed è presente nei bastoncelli.<br />
Nei coni è contenuta una prote<strong>in</strong>a omologa (la vis<strong>in</strong><strong>in</strong>a), con struttura leggermente <strong>di</strong>versa,<br />
co<strong>di</strong>ficata da un gene <strong>di</strong>st<strong>in</strong>to da quello che co<strong>di</strong>fica per la recover<strong>in</strong>a, ma con funzioni<br />
sostanzialmente analoghe alla recover<strong>in</strong>a.<br />
Nei bastoncelli potrebbe essere implicata anche un’altra Guanilato Ciclasi, del tipo “solubile” e<br />
stimolata da ossido d’azoto (ve<strong>di</strong> più avanti). La G.C. dei bastoncelli è legata all’assonema che sta<br />
alla base del segmento esterno.<br />
Guanilato ciclasi attivata da fattori natriuretici<br />
L’Atrial Natriuretic Peptide (ANP) è una prote<strong>in</strong>a ormonale secreta da <strong>di</strong>versi tipi cellulari. È<br />
prodotta dai miociti atriali <strong>in</strong> situazione <strong>di</strong> sovraccarico per il muscolo car<strong>di</strong>aco. L’ANP viene<br />
immesso <strong>in</strong> circolo e, come tutti gli ormoni, <strong>in</strong>teragisce con tutte le cellule <strong>di</strong> un organismo<br />
superiore. In particolare, nel rene, determ<strong>in</strong>a un’aumentata estrusione <strong>di</strong> ione so<strong>di</strong>o, con<br />
conseguente calo <strong>di</strong> pressione. L’ANP possiede anche proprietà rilassanti sul muscolo liscio (come<br />
l’ossido <strong>di</strong> azoto; ve<strong>di</strong> più avanti).<br />
In realtà, non esiste un unico ANP (ne sono stati<br />
descritti tre: ANP A, B, C). Gli ANP si legano a<br />
specifici recettori delle cellule sulle quali<br />
agiscono <strong>in</strong>ducendo, <strong>in</strong> generale, la s<strong>in</strong>tesi <strong>di</strong><br />
GMPC all’<strong>in</strong>terno della cellula. Qu<strong>in</strong><strong>di</strong> tali<br />
recettori sono, ad un tempo, recettori<br />
propriamente detti ed enzimi produttori del<br />
secondo messaggero.<br />
Per la s<strong>in</strong>tesi <strong>di</strong> AMPC, <strong>in</strong>vece, esiste il recettore che si lega all’ormone (una prote<strong>in</strong>a con la sua<br />
identità), il trasduttore del segnale (la prote<strong>in</strong>a-G), e l’enzima (Adenilato Ciclasi), che produce il<br />
secondo messaggero. Per i fattori natriuretici, <strong>in</strong>vece, <strong>in</strong> una sola prote<strong>in</strong>a transmembrana sono<br />
comprese tutte e tre le funzioni. Infatti non avviene una traduzione del segnale come per le<br />
prote<strong>in</strong>e-G, ma i recettori per i fattori natriuretici legano anche il nucleoti<strong>di</strong> ATP e risultano essere<br />
da questo attivate.<br />
Ora parliamo dei fattori natriuretici, e poi dei rispettivi recettori.<br />
179<br />
• = amm<strong>in</strong>oaci<strong>di</strong> identici<br />
<strong>in</strong> A, B, C<br />
ANP = Atrial Natriuretic<br />
Peptide<br />
BNP = Bra<strong>in</strong> Natriuretic<br />
Peptide<br />
CNP = Natriuretic<br />
Peptide C
S<strong>in</strong>tesi e struttura dei fattori natriuretici<br />
L’uro<strong>di</strong>lat<strong>in</strong>a (ANF) è il fattore natriuretici descritto per primo. È un piccolo peptide formato da 28<br />
AA, che deriva da un precursore <strong>in</strong>attivo formato da <strong>12</strong>6 AA (pro-ANF), che, a sua volta, deriva dal<br />
pre-pro-ANF:<br />
Il pro-ANF è la forma d’immagazz<strong>in</strong>amento nei granuli atriali. Dietro a<strong>pp</strong>ropriati stimoli il pro-ANF<br />
perde l’amm<strong>in</strong>o-term<strong>in</strong>ale 1-98 ed è secreto l’ANF attivo, che è formato da 28 AA. È detto anche<br />
fattore natriuretico <strong>di</strong> tipo A. Esiste poi il tipo b (BNF; B da bra<strong>in</strong> perché identificato <strong>in</strong>izialmente nel<br />
cervello <strong>di</strong> maiale), ed il tipo C (CNF, pure esso purificato dal cervello <strong>di</strong> maiale), con spiccate<br />
omologie strutturali tra essi.<br />
Nei tre fattori natriuretici ritroviamo il caratteristico anello formato da 17 AA, che è “saldato” per la<br />
presenza <strong>di</strong> due ciste<strong>in</strong>e <strong>in</strong>varianti che formano un ponte <strong>di</strong>solfuro. Sono sopra illustrate le strutture<br />
dei tre fattori natriuretici, dove sono tratteggiati gli AA identici nei tre pepti<strong>di</strong>. Le <strong>di</strong>fferenze più<br />
marcate sono fuori dell’anello e una delle due ciste<strong>in</strong>e che formano il ponte <strong>di</strong>solfuro, <strong>in</strong> pratica,<br />
risulta essere l’amm<strong>in</strong>oacido C-term<strong>in</strong>ale.<br />
Il tipo B è stato identificato nei granuli cromaff<strong>in</strong>i della ghiandola surrenale.<br />
Cenni sulle funzioni fisiologiche dei fattori natriuretici<br />
Recettori per i fattori natriuretici<br />
I fattori natriuretici si legano a specifiche prote<strong>in</strong>e recettoriali transmembrana, che sono più <strong>di</strong> una,<br />
che non rispondono necessariamente ad un solo tipo <strong>di</strong> fattore natriuretici.<br />
Sono contrad<strong>di</strong>st<strong>in</strong>ti dalla presenza <strong>di</strong> c<strong>in</strong>que dom<strong>in</strong>i:<br />
- Dom<strong>in</strong>io extracellulare (all’N-term<strong>in</strong>ale) che lega<br />
il fattore natriuretico.<br />
- Dom<strong>in</strong>io idrofobico transmembrana<br />
- Dom<strong>in</strong>io citoplasmatico che lega ATP e con<br />
omologia <strong>di</strong> sequenza con le prote<strong>in</strong>e c<strong>in</strong>asi<br />
- Dom<strong>in</strong>io citoplasmatico con attività guanilato<br />
ciclasica<br />
- Zona C-term<strong>in</strong>ale con 10-20 siti <strong>di</strong> fosforilazione.<br />
180
S<strong>in</strong>o ad oggi sono stati descritti 3 recettori per fattori natriuretici e sono stati contrad<strong>di</strong>st<strong>in</strong>ti dalle<br />
sigle:<br />
ANFR – A<br />
ANFR –B<br />
ANFR – C<br />
Occorre ricordare che le sigle A, B, C, non sono necessariamente legate al tipo <strong>di</strong> fattore<br />
natriuretico legato dal recettore. Infatti, per esempio, un ANF può reagire con un recettore <strong>di</strong> tipo A,<br />
ma anche con un recettore <strong>di</strong> tipo C.<br />
I fattori natriuretici <strong>di</strong> tipo A, si legano a:<br />
ANPR – A ed ANPR – B<br />
I fattori natriuretici <strong>di</strong> tipo B, si legano a:<br />
ANPR – C ed ANPR – A (modestamente)<br />
I fattori natriuretici <strong>di</strong> tipo C, si legano a:<br />
ANPR – C ed ANPR – B<br />
Nello schema sopra riportato sono evidenziati i dom<strong>in</strong>i. Sia il recettore <strong>di</strong> tipo A, che quello <strong>di</strong> tipo<br />
B, sono formati da poco più <strong>di</strong> 1000 AA. Il recettore <strong>di</strong> tipo C è <strong>in</strong>vece formato da solo 496 AA, con<br />
una zona citoplasmatica formata da soli 37 AA. Tale ANPR – C non possiede ovviamente attività<br />
guanilato cilclasica, e qu<strong>in</strong><strong>di</strong> è una presenza un po’ misteriosa nelle membrane plasmatiche. Si<br />
ritiene che abbia funzione <strong>di</strong> “tampone”o “clearance” per i fattori natriuretici, cioè ne legherebbe<br />
l’eccesso, rimuovendoli dalla circolazione. Tuttavia è anche <strong>in</strong> grado <strong>di</strong> <strong>in</strong>teragire con prote<strong>in</strong>e-G<br />
<strong>in</strong>ibendo l’adenilato ciclasi e con l’attivazione del ciclo dei fosfo<strong>in</strong>ositi<strong>di</strong>.<br />
Le <strong>in</strong>terazioni tra fattori natriuretici e recettori sono state ben documentate da Koller & Coll.<br />
(Science, 252, <strong>12</strong>0, 1991), che hanno utilizzato cellule <strong>in</strong> coltura Cos-7, che sono versatili per<br />
proce<strong>di</strong>menti <strong>di</strong> trasfezione. È stato possibile <strong>in</strong>serire il gene per i recettori <strong>di</strong> tipo A, o<strong>pp</strong>ure B,<br />
o<strong>pp</strong>ure C, <strong>in</strong> <strong>di</strong>st<strong>in</strong>te cellule per fare esprimere a tali cellule quantità superiori alla norma dei<br />
rispettivi recettori. Qu<strong>in</strong><strong>di</strong> Koller & Coll. <strong>di</strong>sponevano <strong>di</strong> tre l<strong>in</strong>ee cellulari arricchite nei tre tipi <strong>di</strong><br />
recettori. Esponevano tali cellule ai tre fattori natriuretici ed osservavano la risposta ai fattori<br />
natriuretici, misurando il GMPC prodotto.<br />
181
Il fattore hANP (h = human) <strong>in</strong>nalzava la<br />
produzione <strong>di</strong> GMPC nelle cellule con recettori<br />
<strong>di</strong> tipo A ed un po’ nelle cellule con recettori <strong>di</strong><br />
tipo B.<br />
Il pBNP (p = porc<strong>in</strong>e) <strong>in</strong>crementava la<br />
produzione <strong>di</strong> GMPC sia <strong>in</strong> cellule con recettori<br />
<strong>di</strong> tipo A che B.<br />
L’hCNP (h = human) <strong>in</strong>duceva la produzione <strong>di</strong><br />
GMPC solo <strong>in</strong> cellule arricchite <strong>in</strong> recettori <strong>di</strong><br />
tipo B.<br />
Si può verificare che, comunque, i recettori <strong>di</strong><br />
tipo C non rispondono a nessun fattore<br />
natriuretico come ipotizzato, perché mancanti,<br />
<strong>in</strong> pratica, del dom<strong>in</strong>io citoplasmatico ∗ .<br />
Produzione <strong>di</strong> GMPC<br />
Il recettore <strong>di</strong> tipo A è normalmente fosforilato, ed <strong>in</strong> tale stato risponde bene al fattore <strong>di</strong> tipo A,<br />
producendo GMPC. È stato osservato (J. Biol. Chem., 267, -21-15431, 1992) che la<br />
defosforilazione è associata a de-sensibilizzazione. Infatti, l’acido okadaico (ve<strong>di</strong> pag.163, che è un<br />
noto e potente <strong>in</strong>ibitore delle prote<strong>in</strong>e <strong>fosfatasi</strong> <strong>di</strong> tipo 2A, <strong>in</strong>ibisce la INH, che defosforila la Cdc-25,<br />
ve<strong>di</strong> pag.132) blocca sia la desensibilizzazione del recettore <strong>di</strong> tipo A che la sua defosforilazione.<br />
Qu<strong>in</strong><strong>di</strong> tutto lascia <strong>in</strong>tendere che se un recettore è nello stato fosforilato è attivo, mentre è <strong>di</strong>sattivo<br />
nello stato de-fosforilato.<br />
La fosforilazione dei recettori è un fenomeno che si ripresenta. Infatti anche il recettore βadrenergico<br />
è estesamente fosforilato da una specifica c<strong>in</strong>asi, con conseguente <strong>di</strong>sattivazione.<br />
Anche la rodops<strong>in</strong>a (che è il recettore della luce) è <strong>di</strong>sattivata da un’estesa fosforilazione al Cterm<strong>in</strong>ale.<br />
Per i recettori dei fattori natriuretici troviamo che la fosforilazione del recettore provoca una<br />
risposta <strong>di</strong> segno o<strong>pp</strong>osto a quella provocata nei due esempi prima citati.<br />
Infatti la fosforilazione del recettore per il fattore natriuretico attiva la funzionalità del recettore<br />
stesso, mentre per il β-adrenergico e la rodops<strong>in</strong>a accade il contrario.<br />
Nelle uova <strong>di</strong> riccio <strong>di</strong> mare la GC contiene s<strong>in</strong>o a 17 ser<strong>in</strong>e fosforilate. Il trattamento con resact<br />
(ve<strong>di</strong> più avanti) fa <strong>di</strong>m<strong>in</strong>uire a circa 2 tali residui.<br />
Per i recettori dei fattori natriuretici resta ancora da def<strong>in</strong>ire quale prote<strong>in</strong>a c<strong>in</strong>asi è implicata nel<br />
processo <strong>di</strong> fosforilazione.<br />
∗ I risultati riportati <strong>in</strong> figura (produzione <strong>di</strong> cGMP) sono <strong>in</strong> accordo con quanto è schematizzato nella figura <strong>di</strong><br />
pag.181.<br />
182
Legame con ATP dei recettori per i fattori natriuretici<br />
È <strong>in</strong>teressante analizzare la struttura<br />
primaria del dom<strong>in</strong>io citoplasmatico, che,<br />
per primo, segue imme<strong>di</strong>atamente il<br />
dom<strong>in</strong>io transmembrana, per ritrovare <strong>in</strong><br />
esso molti degli elementi strutturali delle<br />
prote<strong>in</strong>e c<strong>in</strong>asi, secondo la classificazione<br />
<strong>di</strong> Hanks, Qu<strong>in</strong>n e Hunter (ve<strong>di</strong> pagg.83-<br />
85). Qui <strong>di</strong> seguito è riportata una figura<br />
tratta da J. Biol. Chem., 268 (8), 5997,<br />
1993, con la struttura primaria del dom<strong>in</strong>io<br />
con omologia per c<strong>in</strong>asi (K<strong>in</strong>ase Doma<strong>in</strong>)<br />
del recettore per l’EGF (EGFR-KD).<br />
E’ stata confrontata con il recettore per l’EGF perché esiste, come si può constatare, un’elevata<br />
omologia <strong>di</strong> sequenza tra questo e l’NPRA – KHD (dom<strong>in</strong>io con omologia per la c<strong>in</strong>asi – K<strong>in</strong>ase<br />
Homology Doma<strong>in</strong> – del recettore A per il fattore natriuretico NPRA). In numeri romani sono<br />
riportati i subdom<strong>in</strong>i HOH.<br />
È possibile riconoscere il consueto Rossmann motiv nel subdom<strong>in</strong>io I. La lis<strong>in</strong>a “72” (<strong>in</strong> riferimento<br />
alla PKA), il Glu “91”. La sequenza APE nell’VIII, preceduta nove residui prima dalla treon<strong>in</strong>a “197”<br />
(assente nell’EGFR – KD) autofosforilabile nella PKA e l’Arg (R) 280 della PKA.<br />
Inoltre sono stati prodotti recettori del tipo A con sostituzioni <strong>di</strong> alcuni degli amm<strong>in</strong>oaci<strong>di</strong> <strong>in</strong>varianti<br />
con l’AA alan<strong>in</strong>a <strong>in</strong> quasi tutti i subdom<strong>in</strong>i (le sostituzioni sono <strong>in</strong><strong>di</strong>cate con frecce verso il basso<br />
<strong>in</strong><strong>di</strong>canti A). Sono stati preparati 8 recettori mutanti con Alan<strong>in</strong>a che sostituisce altri AA come<br />
<strong>in</strong><strong>di</strong>cato, e nell’istogramma B è riportato il GMPC prodotto per stimolazione da ANP. La prima barra<br />
verticale <strong>in</strong><strong>di</strong>ca, con un tratto nero, l’attività guanilato ciclasica del recettore non mo<strong>di</strong>ficato trattato<br />
con 0.5 micromolare <strong>di</strong> ANP, accanto al controllo (barra vuota), cioè alle cellule (si tratta sempre <strong>di</strong><br />
Cos-7) controllo, cioè non trattate con ANP.<br />
Si può concludere che i subdom<strong>in</strong>i I e II non compromettono l’attività guanilato ciclasica. Invece<br />
tutti gli altri dom<strong>in</strong>i sono s<strong>in</strong>golarmente <strong>in</strong><strong>di</strong>spensabili per l’attività guanilato ciclasica del recettore.<br />
Possiamo <strong>in</strong>terpretare questi risultati affermando che il dom<strong>in</strong>io “c<strong>in</strong>asico” non è affatto deputato<br />
ad attività c<strong>in</strong>asica, perché non è <strong>in</strong><strong>di</strong>spensabile orientare con Rossmann motiv l’ATP e, d’altra<br />
parte, mancano alcuni dei residui essenziali nel subdom<strong>in</strong>io VI (l’Arg-R-165 è essenziale per il<br />
trasferimento del fosfato e nel NPRA tale R manca). D’altra parte gli stessi autori hanno verificato,<br />
su membrane delle cellule COS, che l’ATP è <strong>in</strong><strong>di</strong>spensabile per la produzione <strong>di</strong> GMPC.<br />
183
Qu<strong>in</strong><strong>di</strong> l’ATP si lega al dom<strong>in</strong>io c<strong>in</strong>asico, ma non è il substrato <strong>di</strong> alcuna attività c<strong>in</strong>asica. Serve a<br />
regolare l’attività guanilato ciclasica.<br />
Fertilizzazione<br />
È noto che specifici pepti<strong>di</strong> prodotti dalle cellule uovo attraggono gli spermatozoi. Stu<strong>di</strong> a<strong>pp</strong>rofon<strong>di</strong>ti<br />
sono stati eseguiti con il riccio <strong>di</strong> mare. Sono noti due pepti<strong>di</strong>:<br />
speract: Gly – Phe – Asp – Leu – Asn – Gly – Gly – Gly – Val – Gly<br />
10 AA<br />
resact: Cys – Val – Thr – Gly – Ala – Pro – Gly – Lys – Val – Gly – Gly – Gly – Arg – Leu<br />
14 AA<br />
Questi pepti<strong>di</strong>, prodotti dalla cellula uovo, determ<strong>in</strong>ano chemiotassi negli spermatozoi. Si è visto<br />
che nello spermatozoo provocano un aumento <strong>di</strong> AMPC, GMPC e calcio. Questa risposta<br />
biochimica è dovuta ad un recettore degli spermatozoi per speract o resact, con forte omologia con<br />
i noti recettori per i fattori natriuretici <strong>di</strong> tipo A o B (ANPR – A e ANPR – B).<br />
Anche per tali recettori degli spermatozoi, la defosforilazione de-sensibilizza la cellula all’azione dei<br />
pepti<strong>di</strong> speract e resact.<br />
L’aumento <strong>di</strong> GMPC controlla la motilità delle code degli spermatozoi.<br />
Guanilato ciclasi delle cilia dei protozoi<br />
Nelle membrane ciliari <strong>di</strong> Tetrhymena e Paramecium è stata identificata una guanilato ciclasi<br />
legata a membrana che è attivata da Calcio + Calmodul<strong>in</strong>a, <strong>di</strong>versa, presumibilmente, dalla G.C. <strong>di</strong><br />
bastoncelli, che, <strong>in</strong>vece, è <strong>in</strong>ibita da Calcio, essendo il processo (nei bastoncelli) me<strong>di</strong>ato dalla<br />
recover<strong>in</strong>a. La G.C. dei flagelli dei protozoi è attivata (e non <strong>in</strong>ibita) da Calcio + Calmodul<strong>in</strong>a.<br />
Prima <strong>di</strong> occuparci della guanilato ciclasi comunemente detta solubile, accenniamo all’esistenza <strong>di</strong><br />
un altro importante secondo messaggero, l’ossido <strong>di</strong> azoto (NO), perché è stato <strong>di</strong>mostrato che<br />
l’ossido <strong>di</strong> azoto può essere prodotto da specifici sistemi enzimatici, alquanto complessi (ce ne<br />
occuperemo dopo). L’NO <strong>di</strong>ffonde alle cellule imme<strong>di</strong>atamente vic<strong>in</strong>e e stimola la Guanilato Ciclasi<br />
cosiddetta solubile, che contiene l’importante gru<strong>pp</strong>o prostetico eme, che <strong>in</strong>teragisce <strong>di</strong>rettamente<br />
con l’NO.<br />
Ci occuperemo dopo dei sistemi cellulari produttori <strong>di</strong> NO. Per il momento ricapitoliamo i 4 tipi <strong>di</strong><br />
guanilato ciclasi da noi stu<strong>di</strong>ate:<br />
• Guanilato ciclasi dei fotorecettori dei vertebrati (<strong>in</strong>ibita da calcio-recover<strong>in</strong>a)<br />
• Guanilato ciclasi presente su recettori per fattori natriuretici o per pepti<strong>di</strong> chemiotattici degli<br />
spermatozoi<br />
• Guanilato ciclasi dei flagelli dei protozoi (attivata da calcio-calmodul<strong>in</strong>a)<br />
• Guanilato ciclasi “solubile” attivata da NO, dalle seguenti proprietà:<br />
Guanilato ciclasi “solubile”<br />
Tale G.C. è attivata da NO, ed è composta <strong>di</strong> due subunità:<br />
- Subunità P.M. 70000 Da, che lega NO; denom<strong>in</strong>ata presunta “regolatrice”<br />
- Subunità P.M. 82000, denom<strong>in</strong>ata presunta “catalitica”.<br />
È la 82 KDa che è deputata alla s<strong>in</strong>tesi <strong>di</strong> GMPC, perché presenta omologia <strong>di</strong> sequenza con G.C.<br />
dei recettori per fattori natriuretici (FEBS Lett., 239, 29, 1988).<br />
Probabilmente è la subunità 70 KDa che lega l’NO e che qu<strong>in</strong><strong>di</strong> dovrebbe contenere il gru<strong>pp</strong>o eme.<br />
184
185
L’Ossido <strong>di</strong> Azoto<br />
L’ossido <strong>di</strong> azoto è un importante secondo messaggero <strong>in</strong><strong>di</strong>viduato <strong>in</strong> anni recenti (1989).<br />
Da tempo si sapeva che certi derivati azotati possono <strong>in</strong>durre rilassamento sui vasi sanguigni. Per<br />
esempio, la nitroglicer<strong>in</strong>a ed il nitroprussiato so<strong>di</strong>co sono calmanti <strong>di</strong> spasmi del muscolo car<strong>di</strong>aco.<br />
Da tempo era stata ipotizzata l’esistenza <strong>di</strong> un Fattore Rilassante Derivante dall’Endotelio<br />
(Endothelium Derived Relax<strong>in</strong>g Factor – EDRF), ma, nonostante <strong>in</strong>numerevoli tentativi, non era<br />
mai stato isolato. Oggi è unanimemente riconosciuto che l’EDRF è il semplice ossido <strong>di</strong> azoto<br />
(NO). È proprio la natura gassosa <strong>di</strong> tale NO che ha impe<strong>di</strong>to <strong>di</strong> fatto il suo isolamento.<br />
Si pervenne tuttavia all’identificazione dell’NO nei sistemi biologici, <strong>in</strong> seguito ad osservazioni a<br />
carico delle cellule macrofagi, che lo producono perché citotossico, qu<strong>in</strong><strong>di</strong> senza legame alcuno<br />
con eventuali proprietà <strong>di</strong> me<strong>di</strong>azione chimica.<br />
L’NO è un ra<strong>di</strong>cale (possiede un elettrone spaiato) e, come tale, è citotossico, come tutte le<br />
sostanze ra<strong>di</strong>caliche (si pensi all’anione superossido). Può essere correttamente <strong>in</strong><strong>di</strong>cato con tale<br />
elettrone spaiato: • NO. Lo svilu<strong>pp</strong>o <strong>di</strong> NO è sempre accompagnato dalla produzione <strong>di</strong> nitriti e <strong>di</strong><br />
nitrati, <strong>in</strong> quanto l’NO, a contatto con l’ossigeno, da’ luogo alla seguente importante reazione:<br />
2 • NO + O2 —————→ N2O4 —————→ - NO2 + - NO3<br />
ipoazotide nitriti nitrati<br />
Cioè lo svilu<strong>pp</strong>o <strong>di</strong> NO <strong>in</strong> ambiente ossigenato da’ luogo alla produzione <strong>di</strong> nitriti e <strong>di</strong> nitrati. In<br />
generale, la produzione <strong>di</strong> nitrati può derivare dallo svilu<strong>pp</strong>o <strong>di</strong> NO.<br />
Già nel 1981 era stato osservato che le <strong>in</strong>fezioni batteriche, nell’uomo, sono accompagnate dalla<br />
produzione <strong>di</strong> nitrati. Si accertò poi che il donatore <strong>di</strong> azoto era l’azoto guani<strong>di</strong>nico del noto<br />
amm<strong>in</strong>oacido standard arg<strong>in</strong><strong>in</strong>a e che tale reazione sull’arg<strong>in</strong><strong>in</strong>a era portata avanti dai macrofagi,<br />
che sono cellule <strong>di</strong> tipo leucocitario, e qu<strong>in</strong><strong>di</strong> <strong>di</strong> orig<strong>in</strong>e eritroide, che sono <strong>di</strong>stribuite ampiamente<br />
nei tessuti e che sono presenti anche nel sangue; tali macrofagi (anche neutrofili) portano avanti la<br />
fagocitosi, con la <strong>di</strong>struzione <strong>di</strong> cellule estranee all’organismo.<br />
Si accertò che l’arg<strong>in</strong><strong>in</strong>a veniva convertita <strong>in</strong> citrull<strong>in</strong>a, durante la fagocitosi e, soltanto nel 1989, fu<br />
<strong>di</strong>mostrato che l’ossido <strong>di</strong> azoto è prodotto per conversione dell’arg<strong>in</strong><strong>in</strong>a <strong>in</strong> citrull<strong>in</strong>a. La successiva<br />
conversione a nitriti e nitrati avviene per reazione dell’NO con l’ossigeno, come sopra specificato.<br />
Nei macrofagi l’NO svolge funzioni citotossiche perché un ra<strong>di</strong>cale. D’altra parte <strong>in</strong> tale specifica<br />
sede è prodotto <strong>in</strong> quantità relativamente elevate.<br />
Qu<strong>in</strong><strong>di</strong> <strong>in</strong> s<strong>in</strong>tesi, nei MACROFAGI:<br />
Per quanto riguarda l’identificazione della funzione me<strong>di</strong>atrice chimica (secondo messaggero)<br />
dell’NO, furono importanti le proprietà note da tempo dei vaso-rilassanti nitroglicer<strong>in</strong>a e<br />
nitroprussiato so<strong>di</strong>co, che sono, <strong>in</strong> realtà, produttori <strong>in</strong> loco <strong>di</strong> ossido <strong>di</strong> azoto, che <strong>di</strong>ffonde alle<br />
cellule vic<strong>in</strong>e e stimola il noto enzima Guanilato Ciclasi, la forma “solubile”, che è dotata <strong>di</strong> gru<strong>pp</strong>o<br />
eme. L’ossido <strong>di</strong> azoto stimola la guanilato ciclasi, e l’aumento locale <strong>di</strong> GMPC porta, con modalità<br />
ancora da def<strong>in</strong>ire, al rilassamento del muscolo liscio. È stato ipotizzato che l’aumento del GMPC<br />
porti all’attivazione della Prote<strong>in</strong>a C<strong>in</strong>asi <strong>di</strong>pendente da GMPC (PKG) che, a sua volta, fosforila le<br />
catene leggere della mios<strong>in</strong>a, competendo con la nota fosforilazione da parte della c<strong>in</strong>asi specifica<br />
per le catene leggere della mios<strong>in</strong>a (ve<strong>di</strong> pag.93-94), che, secondo lo schema già a<strong>pp</strong>rofon<strong>di</strong>to, va<br />
verso la contrazione del muscolo liscio. Però questa parte del meccanismo è ancora da<br />
<strong>di</strong>mostrare. È certo che il GMPC prodotto porta al rilassamento del muscolo liscio.<br />
Qu<strong>in</strong><strong>di</strong> per l’NO sono stati identificati due ruoli <strong>in</strong><strong>di</strong>pendenti (a<strong>pp</strong>arentemente):<br />
- svolge funzioni citotossiche nei macrofagi<br />
- ha un ruolo <strong>di</strong> Secondo messaggero <strong>in</strong> un ampio spettro <strong>di</strong> tipi cellulari.<br />
186
Occorre ricordare che l’NO è un gas. Come tale <strong>di</strong>ffonde rapidamente, ignorando qualsiasi “filtro”,<br />
cioè canale, <strong>di</strong> membrana. Interessa qu<strong>in</strong><strong>di</strong> tutte le cellule nei <strong>di</strong>ntorni del sito <strong>di</strong> produzione<br />
dell’ossido <strong>di</strong> azoto stesso. È tra l’altro l’unico secondo messaggero <strong>di</strong> natura gassosa s<strong>in</strong>o ad<br />
oggi identificato.<br />
Sa<strong>pp</strong>iamo che tutti i messaggi chimici devono avere carattere transitorio. Per esempio l’AMPC è<br />
s<strong>in</strong>tetizzato dall’adenilato ciclasi, ma esiste la fosfo<strong>di</strong>esterasi che lo rimuove. Anche il GMPC ha 4<br />
enzimi ciclasici (a<strong>pp</strong>ena trattati) e una specifica fosfo<strong>di</strong>esterasi (importantissima nel processo <strong>di</strong><br />
fototrasduzione): è <strong>in</strong>fatti attivata dalla prote<strong>in</strong>a-G specifica dei fotorecettori, cioè la trasduc<strong>in</strong>a.<br />
Perché l’NO è un ra<strong>di</strong>cale, questo reagirà a-specificamente con molti <strong>di</strong>versi tipi <strong>di</strong> sostanze,<br />
<strong>in</strong>nescando reazioni ra<strong>di</strong>caliche, o<strong>pp</strong>ure può essere “spento” con le modalità che <strong>in</strong> parte abbiamo<br />
già detto (produzione <strong>di</strong> nitriti e nitrati). Comunque resta stabilito che l’NO non necessita <strong>di</strong><br />
specifici processi enzimatici per la sua rimozione. Infatti si “spegne” spontaneamente,<br />
<strong>in</strong>teressando, nell’arco della sua breve vita, un ristretto ambiente che circonda il sito stesso <strong>di</strong><br />
produzione (dell’NO). È stato calcolato che:<br />
- l’NO “vive” circa 5 secon<strong>di</strong><br />
- l’NO non può <strong>di</strong>ffondere a più <strong>di</strong> 0.2-0.6 mm dal sito <strong>di</strong> produzione.<br />
Meccanismo <strong>di</strong> rimozione dell’ossido <strong>di</strong> azoto<br />
Tra le più importanti reazioni alle quali partecipa l’NO ricor<strong>di</strong>amo le seguenti (oltre alla reazione<br />
con O2, ve<strong>di</strong> pag.186):<br />
▪ reazione con l’ossiemoglob<strong>in</strong>a (nel sangue arterioso), con produzione <strong>di</strong> nitrato e<br />
metaemoglob<strong>in</strong>a:<br />
• NO + Hb (Fe ++ ) O2 —————→ - NO3 + Hb (Fe +++ )<br />
▪ reazione con metaemoglob<strong>in</strong>a (nel sangue venoso):<br />
• NO + Hb (Fe +++ ) —————→ NO3 · Hb (Fe +++ )<br />
Enzimi produttori <strong>di</strong> ossido <strong>di</strong> azoto<br />
Esistono più forme dell’enzima che produce ossido <strong>di</strong> azoto. È denom<strong>in</strong>ato NO S<strong>in</strong>tasi (NOS).<br />
Presenta una notevole complessità, e <strong>di</strong>pende da <strong>di</strong>versi fattori. Tra l’altro è attivato da calcio +<br />
calmodul<strong>in</strong>a (qui ritroviamo una caratteristica che si ripete per enzimi produttori <strong>di</strong> secon<strong>di</strong><br />
messaggeri: anche l’adenilato ciclasi, una forma <strong>di</strong> guanilato ciclasi e vari altri enzimi produttori <strong>di</strong><br />
secon<strong>di</strong> messaggeri <strong>di</strong>pendono, a loro volta, dalla calmodul<strong>in</strong>a). Questo aspetto è anche<br />
importante per la purificazione della NO S<strong>in</strong>tasi stessa. Infatti la CaM può scomparire<br />
progressivamente durante le varie ta<strong>pp</strong>e della purificazione e, parallelamente, si osserva una<br />
progressiva scomparsa <strong>di</strong> attività enzimatica NOS. In realtà deve essere sempre presente la CaM<br />
per registrare l’attività enzimatica NOS.<br />
La reazione No S<strong>in</strong>tasica è ossidoriduttiva e <strong>di</strong>pende dal NADPH. Per la purificazione dell’NO<br />
S<strong>in</strong>tasi è <strong>in</strong>teressante riportare le osservazioni <strong>di</strong> Brendt & Snyder, che, per la purificazione ad<br />
omogeneità <strong>di</strong> NOS da cervello, hanno impiegato una prelim<strong>in</strong>are cromatografia a scambio ionico<br />
(DEAE cellulosa), seguita da una cromatografia per aff<strong>in</strong>ità. Infatti, la NOS specificamente si lega,<br />
come altri enzimi NADP <strong>di</strong>pendenti, ad una res<strong>in</strong>a che porta covalentemente legato Adenos<strong>in</strong> 2’-5’<br />
<strong>di</strong> fosfato (che corrisponde circa a ½ NADPH o NADP).<br />
Ci si accorse, stu<strong>di</strong>ando la struttura primaria dell’NOS, che ha molte analogie con l’enzima<br />
Citocromo P-450 reduttasi.<br />
Infatti anche la NOS lega Flav<strong>in</strong> Aden<strong>in</strong> D<strong>in</strong>ucleotide (FAD), Flav<strong>in</strong> Mononucleotide (FMN) e<br />
<strong>di</strong>pende da tetraidrobiopter<strong>in</strong>a (BH4), che è precursore dell’acido folico (è il cofattore della<br />
fenilalan<strong>in</strong>a idrossilasi). Qu<strong>in</strong><strong>di</strong> riassumiamo i fattori da cui <strong>di</strong>pende:<br />
Calmodul<strong>in</strong>a – NADPH – FAD – FMN - BH4<br />
Inoltre si tenga presente che contiene un gru<strong>pp</strong>o eme con un atomo <strong>di</strong> ferro. Qu<strong>in</strong><strong>di</strong> la reazione<br />
<strong>di</strong>pende da ben 6 cofattori, oltre il substrato.<br />
187
Per entrare nel merito del meccanismo <strong>di</strong> reazione, si tenga presente che avviene un trasferimento<br />
bielettronico come <strong>in</strong> una monossigenasi a funzione mista, della quale ricor<strong>di</strong>amo lo schema:<br />
R – H + NADPH + H + + O2 —————→ R – OH + NADP + + H2O<br />
Simile a questo schema è la prima parte della reazione catalizzata dall’NOS. Il substrato è<br />
l’arg<strong>in</strong><strong>in</strong>a, che riceve un ossigeno nell’azoto omega del gru<strong>pp</strong>o guani<strong>di</strong>lico e che <strong>di</strong>venta perciò<br />
idrossi-arg<strong>in</strong><strong>in</strong>a. Tale composto però è solo <strong>in</strong>terme<strong>di</strong>o, perché NOS utilizza ancora ½<br />
equivalente <strong>di</strong> NADPH ed 1 equivalente <strong>di</strong> ossigeno molecolare per convertire l’idrossi-arg<strong>in</strong><strong>in</strong>a <strong>in</strong><br />
citrull<strong>in</strong>a, con formazione <strong>di</strong> NO secondo lo schema:<br />
Osserviamo subito quali sono gli utili <strong>in</strong>ibitori specifici <strong>di</strong> questa reazione: <strong>in</strong> genere sono analoghi<br />
dell’<strong>in</strong>terme<strong>di</strong>o N-idrossi-arg<strong>in</strong><strong>in</strong>a, per esempio l’N-metil-arg<strong>in</strong><strong>in</strong>a (NMA). È o<strong>pp</strong>ortuno ricordare<br />
che un notevole ostacolo al rilevamento <strong>di</strong> questo enzima nei sistemi biologici è costituito dal<br />
semplice dosaggio dell’enzima stesso: <strong>in</strong>fatti, producendo una sostanza gassosa (l’NO), non è<br />
possibile rilevarlo con metodologie semplici. Oltre a tutto, l’NO reagisce subito e si usa pertanto<br />
misurare la formazione <strong>di</strong> citrull<strong>in</strong>a dall’arg<strong>in</strong><strong>in</strong>a, anche se occorre porre attenzione a non dosare<br />
enzimi del ciclo dell’urea! Qu<strong>in</strong><strong>di</strong>, <strong>in</strong> pratica, la citrull<strong>in</strong>a che si accumula rispecchia l’NO prodotto,<br />
adottando le dovute precauzioni per una corretta <strong>in</strong>terpretazione.<br />
Isoenzimi dell’NO s<strong>in</strong>tasi<br />
In seguito al lavoro notevole svilu<strong>pp</strong>ato <strong>in</strong> questi ultimi tempi, è possibile confrontare le strutture <strong>di</strong><br />
NOS proprie <strong>di</strong> <strong>di</strong>versi tessuti. È riprodotto, a tal f<strong>in</strong>e, lo schema seguente, <strong>in</strong>cluso nella<br />
monografia <strong>di</strong> Bredt & Snyder (Ann. Rev. Biochem., 63, 175-195,1994).<br />
188
E’ qui confrontata la struttura <strong>di</strong> NOS da cervello (bra<strong>in</strong> = bNOS); da endotelio (eNOS); da<br />
macrofagi (macNOS) e da fegato (hepNOS). Viene <strong>in</strong>oltre riportata, per confronto, la struttura<br />
della citocromo P-450 reduttasi (CPR).<br />
Si può, <strong>in</strong> generale, rilevare che le NOS s<strong>in</strong>tasi possiedono due dom<strong>in</strong>i pr<strong>in</strong>cipali:<br />
- all’N-term<strong>in</strong>ale esiste il dom<strong>in</strong>io <strong>di</strong> legame con il gru<strong>pp</strong>o eme<br />
- al C-term<strong>in</strong>ale abbiamo la serie <strong>di</strong> subdom<strong>in</strong>i, leganti CaM, FMN, FAD e NADP che, sommati<br />
assieme, costituiscono il dom<strong>in</strong>io riduttasico.<br />
Ora commentiamo brevemente le proprietà <strong>di</strong> queste 4 NOS.<br />
Ossido <strong>di</strong> azoto s<strong>in</strong>tasi neuronale (bNOS)<br />
Esistono più forme <strong>di</strong> bNOS dovute a splic<strong>in</strong>g alternativo. Nella zona <strong>di</strong> legame per l’eme è stato<br />
<strong>in</strong><strong>di</strong>viduato, nella Ser-372, un sito <strong>di</strong> fosforilazione da parte <strong>di</strong> PKA. Può <strong>in</strong>oltre essere fosforilata<br />
da PKG e PKC. La fosforilazione porta ad un calo <strong>di</strong> attività sia della bNOS che della eNOS; tale<br />
fenomeno potrebbe costituire un’<strong>in</strong>ibizione tipo feed-back della NOS. Infatti, l’NO prodotto dalla<br />
NOS determ<strong>in</strong>a l’attivazione della guanilato ciclasi. Il GMPC attiva la PKG che, con la fosforilazione<br />
e <strong>in</strong> attivazione della NOS, <strong>in</strong>staura un meccanismo <strong>di</strong> <strong>in</strong>ibizione retroattivo.<br />
È stato <strong>di</strong>mostrato che l’NO svolge importanti funzioni <strong>di</strong> neurotrasmettitori nel sistema nervoso.<br />
Da “Le Scienze” 287, 28, 1992.<br />
Nelle congiunzioni s<strong>in</strong>aptiche, i term<strong>in</strong>ali pres<strong>in</strong>aptici fondono con la membrana le vescicole<br />
contenenti glutammato, che è liberato nella giunzione e che, qu<strong>in</strong><strong>di</strong>, <strong>di</strong>ffonde. Occorre ricordare<br />
che esistono gli importanti recettori NMDA, che rispondono al glutammato e riversano calcio nella<br />
post-s<strong>in</strong>apsi. Infatti tali recettori NMDA (cosiddetti perché rispondono ad un analogo del<br />
glutammato, cioè l’acido N-Metil-D-Aspartato), <strong>in</strong> presenza <strong>di</strong> glutammato, si aprono e lasciano<br />
entrare lo ione calcio. L’aumento <strong>di</strong> calcio determ<strong>in</strong>a un legame <strong>di</strong> tale ione alla CaM, che cambia<br />
conformazione e si lega alla bNOS attivandola, con consumo <strong>di</strong> arg<strong>in</strong><strong>in</strong>a e produzione <strong>di</strong> citrull<strong>in</strong>a e<br />
dell’importante NO.<br />
189
Nei grafici è ben riportato che l’aumento <strong>di</strong> NMDA (<strong>in</strong> ascisse, grafico a s<strong>in</strong>istra) determ<strong>in</strong>a un<br />
contemporaneo aumento <strong>di</strong> citrull<strong>in</strong>a ed anche <strong>di</strong> GMP ciclico. D’altra parte (grafico a destra), se i<br />
processi avvengono <strong>in</strong> presenza dell’importante <strong>in</strong>ibitore dell’NO s<strong>in</strong>tasi (cioè della N-Metil-<br />
Arg<strong>in</strong><strong>in</strong>a, NMA), si ha progressivo calo <strong>di</strong> formazione <strong>di</strong> citrull<strong>in</strong>a e <strong>di</strong> GMP ciclico. Da queste prove<br />
si può concludere che la produzione <strong>di</strong> NO è correlata alla produzione <strong>di</strong> GMP ciclico.<br />
L’NO è anche neurotossico, se prodotto <strong>in</strong> eccesso<br />
Interessante è lo schema seguente, per spiegare la neurotossicità dell’NO (da Bredt & Snyder,<br />
Ann. Rev. Biochem. 63, 175-195, 1994). L’NO, come altri ra<strong>di</strong>cali, può danneggiare il DNA,<br />
deam<strong>in</strong>andolo. Tale danno stimola l’attivazione della Poli ADP Ribosio S<strong>in</strong>tetasi (PARS, ve<strong>di</strong><br />
pag.193), che utilizza NAD come substrato depletando la cellula <strong>di</strong> NAD e, <strong>di</strong> conseguenza, <strong>di</strong> ATP<br />
utilizzato per la sua s<strong>in</strong>tesi: la conseguenza è la morte della cellula. Si tenga presente che la PARS<br />
può utilizzare anche 50 NAD per una s<strong>in</strong>gola ADP-ribosilazione degli istoni.<br />
NO s<strong>in</strong>tasi <strong>di</strong> endotelio (eNOS)<br />
È l’enzima che spiega la vaso<strong>di</strong>latazione, ed è comunemente accettato che l’NO è il più importante<br />
vaso<strong>di</strong>latatore.<br />
190
Uno stimolo esterno, per esempio Acetil Col<strong>in</strong>a, provoca un <strong>in</strong>flusso <strong>di</strong> calcio nelle cellule<br />
dell’endotelio (che rifasciano i vasi sanguigni). Tale aumento determ<strong>in</strong>a un’attivazione della eNOS<br />
con produzione <strong>di</strong> NO, il quale <strong>di</strong>ffonde nelle vic<strong>in</strong>e cellule del tessuto muscolare liscio che riveste i<br />
vasi sanguigni, dove <strong>in</strong>contra il gru<strong>pp</strong>o eme della Guanilato S<strong>in</strong>tetasi “solubile”. La GS viene<br />
attivata da NO, ed il GMP ciclico rilassa il muscolo. Si tenga presente che la GS è attivata <strong>di</strong><br />
almeno 50 volte da parte dell’NO!!!<br />
La eNOS è caratterizzata da una sequenza consenso per la miristoilazione (ve<strong>di</strong> tabella pag.6), e<br />
ciò le consente <strong>di</strong> essere “ancorata” alla membrana plasmatica. Anche l’eNOS può essere<br />
fosforilata come bNOS.<br />
NO s<strong>in</strong>tasi dei macrofagi (macNOS)<br />
Questo isoenzima è caratterizzato dall’<strong>in</strong>ducibilità. Ovvero è <strong>in</strong> pratica assente nel macrofago non<br />
stimolato. È solo l’attivazione <strong>in</strong>nescata da specifici componenti della membrana dei batteri che<br />
consente livelli elevati <strong>di</strong> NOS nei macrofagi. Infatti nei macrofagi attivati è evidenziabile un<br />
<strong>in</strong>cremento dello Shunt dei pentosi fosfato, proprio per il NADPH consumato dall’NO s<strong>in</strong>tasi<br />
(comunque <strong>in</strong> macrofagi e neutrofili si attiva anche la NADPH ossidasi – che produce superossido<br />
– e che consuma anch’essa NADPH).Ve<strong>di</strong> pag.192.<br />
L’NO ed il superossido si uniscono <strong>in</strong> una reazione non enzimatica, generando peross<strong>in</strong>itrito, che è<br />
più tossico delle due specie, NO e superossido, prese s<strong>in</strong>golarmente. Avviene la seguente<br />
reazione tra le due specie ra<strong>di</strong>caliche:<br />
Il peross<strong>in</strong>itrito si decompone <strong>in</strong> ra<strong>di</strong>cale idrossile (sembra, <strong>in</strong> effetti, che la tossicità del<br />
peross<strong>in</strong>itrito sia dovuta alla sua capacità <strong>di</strong> generare tale specie ra<strong>di</strong>calica altamente tossica).<br />
È stato <strong>in</strong><strong>di</strong>viduato il componente del batterio che determ<strong>in</strong>a “attivazione” del macrofago: si tratta<br />
dell’endotoss<strong>in</strong>a, dalla struttura molto complessa – contenente l’importante lipide A – che è stata<br />
già illustrata (ve<strong>di</strong> pag.175). Si tratta <strong>di</strong> un lipopolisaccaride (LPS).<br />
A<strong>pp</strong>arentemente la macNOS purificata non è stimolata da calmodul<strong>in</strong>a. In realtà ha una fortissima<br />
aff<strong>in</strong>ità per essa e, <strong>in</strong> pratica, la macNOS la lega sempre, per cui non è possibile rilevare <strong>in</strong><br />
laboratorio la stimolazione da CaM aggiunta, <strong>in</strong> quanto è già presente prima dell’eventuale<br />
aggiunta. L’endotoss<strong>in</strong>a da sola da’ una risposta forte, ma con l’<strong>in</strong>terferone-γ si ha un notevole<br />
potenziamento.<br />
NO s<strong>in</strong>tasi <strong>di</strong> epatociti (hepNOS)<br />
La NOS <strong>di</strong> macrofagi non è l’unico esempio <strong>di</strong> NO s<strong>in</strong>tasi <strong>in</strong>ducibile. Anche nel fegato (privo <strong>di</strong><br />
macrofagi) può essere <strong>in</strong>dotta una NO s<strong>in</strong>tasi con una varietà <strong>di</strong> stimoli, oltre al LPS e<br />
all’<strong>in</strong>terferone-γ. Anche Tumor Necrosis Factor-α ed <strong>in</strong>terleuch<strong>in</strong>a-1 β <strong>in</strong>ducono la s<strong>in</strong>tesi <strong>di</strong> NO<br />
s<strong>in</strong>tasi nel fegato. Poiché una risposta simile a quella del fegato è fornita da una certa varietà <strong>di</strong><br />
tessuti, è stato ipotizzato che l’NO s<strong>in</strong>tasi costituisca un “primor<strong>di</strong>ale” elemento <strong>di</strong> <strong>di</strong>fesa dei<br />
tessuti, prima dello svilu<strong>pp</strong>o, nel corso dell’evoluzione, del sistema immunitario.<br />
Analogie tra NO e CO<br />
L’ossido <strong>di</strong> Carbonio (che non è un ra<strong>di</strong>cale) ha una struttura chimica alquanto simile all’NO (che<br />
<strong>in</strong>vece è un ra<strong>di</strong>cale) e tutti e due sono composti gassosi.<br />
L’ossido <strong>di</strong> carbonio può attivare la Guanilato Ciclasi “solubile”, come l’NO. L’ossido <strong>di</strong> carbonio è<br />
prodotto <strong>in</strong> vivo dall’eme ossigenasi, che sc<strong>in</strong>de il gru<strong>pp</strong>o eme formando biliver<strong>di</strong>na e CO. Se <strong>in</strong><br />
vivo l’eme ossigenasi è <strong>in</strong>ibita dal forte suo <strong>in</strong>ibitore Z<strong>in</strong>co-Protoporfir<strong>in</strong>a IX (un analogo del gru<strong>pp</strong>o<br />
eme), si osserva una contemporanea <strong>di</strong>m<strong>in</strong>uzione del GMP ciclico: ovvero si ipotizza che parte del<br />
GMP ciclico sia prodotto dalla guanilato ciclasi per stimolo da CO; quando è <strong>in</strong>ibito l’enzima che<br />
produce CO si ha, per conseguenza, la <strong>di</strong>m<strong>in</strong>uita produzione <strong>di</strong> GMPC. La forte tossicità del CO<br />
potrebbe essere dovuta a questa sua proprietà vicariante dell’ossido <strong>di</strong> azoto.<br />
191
192
ADP Ribosilazioni e Poli-ADP Ribosilazioni<br />
Il NAD, classico coenzima ossidoriduttivo, funziona anche da donatore <strong>di</strong> residui Adenos<strong>in</strong> Di<br />
fosfato-ribosio. Esempi noti: Toss<strong>in</strong>a colerica subunità A e B (1 subunità A + 5 B). La B riconosce il<br />
GM1 sulla superficie della cellula e A (subunità ADP ribosilante) entra nella cellula e ADP ribosila Gi<br />
(<strong>in</strong> corrispondenza <strong>di</strong> un residuo <strong>di</strong> arg<strong>in</strong><strong>in</strong>a = blocco attività GTPasica della G-prote<strong>in</strong> = GTPasi<br />
<strong>in</strong>attiva = G-Prote<strong>in</strong> sempre attiva).<br />
Toss<strong>in</strong>a <strong>di</strong>fterica: ADP ribosila EF2 (traslocasi) = blocco della s<strong>in</strong>tesi proteica.<br />
La poli ADP ribosilazione è esclusivamente nucleare. Sembra sia implicata nell’evidenziazione <strong>di</strong><br />
danni al DNA.<br />
193
Ciclo dei fosfo<strong>in</strong>ositi<strong>di</strong><br />
mio-<strong>in</strong>ositolo: è un polialcol. È classificato come vitam<strong>in</strong>a. Se manca nella <strong>di</strong>eta <strong>di</strong> animali da<br />
esperimento si hanno <strong>di</strong>sor<strong>di</strong>ni <strong>di</strong> varia natura. Si forma, nei vegetali, dal Glucosio-6P.<br />
Nelle piante è largamente <strong>di</strong>ffuso come galact<strong>in</strong>olo (galattosio + myo-<strong>in</strong>ositolo).<br />
Nel 1984, Berridge & Irv<strong>in</strong>e (Nature, 3<strong>12</strong>, 315) stabilirono che IP3 (ve<strong>di</strong> più avanti) è un secondo<br />
messaggero implicato nella mobilizzazione del calcio endocellulare.<br />
Ma già nel 1953, Hok<strong>in</strong>g & Hok<strong>in</strong>g videro che sotto stimolo da Acetilcol<strong>in</strong>a le cellule pancreatiche<br />
determ<strong>in</strong>avano l’<strong>in</strong>corporazione del 32 P nell’<strong>in</strong>ositolo.<br />
Negli animali è presente <strong>in</strong> un fosfolipide (fosfati<strong>di</strong>l <strong>in</strong>ositolo, PI).<br />
194
Ve<strong>di</strong>amo la bios<strong>in</strong>tesi <strong>di</strong> questo fosfolipide.<br />
L’acido fosfati<strong>di</strong>co reagisce con il CTP:<br />
195
Esiste un enzima (anzi più enzimi; ve<strong>di</strong> pag.232) che presentano attività fosfolipasica C:<br />
⇒ IP3:<br />
Ha vita breve. Nell’ambito <strong>di</strong> pochi secon<strong>di</strong> viene idrolizzato progressivamente a <strong>in</strong>ositolo. Trova un<br />
recettore specifico R2 sulla membrana del reticolo endoplasmatico e si ha liberazione <strong>di</strong> calcio da<br />
una riserva endocellulare <strong>di</strong> calcio (il reticolo endoplasmatico).<br />
⇒ Digliceride (DG):<br />
Diffonde lateralmente <strong>in</strong> membrana. È un forte attivatore della PKC (ve<strong>di</strong> pag.101). Tale PKC è<br />
però attivata anche da calcio (e fosfolipi<strong>di</strong> aci<strong>di</strong> tipo PS, fosfati<strong>di</strong>lser<strong>in</strong>a).<br />
Qu<strong>in</strong><strong>di</strong> l’attività fosfolipasica C genera 2 secon<strong>di</strong> messaggeri che convergono ambedue su PKC.<br />
Infatti IP3 fa <strong>in</strong>nalzare il calcio endocellulare.<br />
Si ricor<strong>di</strong> che la PKC è attivata anche da proteolisi da calpa<strong>in</strong>a (e si forma una PKC <strong>in</strong><strong>di</strong>pendente<br />
da Ca ++ ).<br />
In a<strong>pp</strong>arenza si <strong>in</strong>staura un ciclo autoattivante: il Ca ++ attiva la Fosfolipasi C (ve<strong>di</strong> più avanti<br />
pag.231), si libera IP3 e DG; IP3 libera Ca ++ che, <strong>in</strong>sieme ad altri fattori, attiva la fosfolipasi C.<br />
Rilascio <strong>di</strong> calcio da parte <strong>di</strong> microsomi<br />
I microsomi sono ottenuti <strong>in</strong> vitro per<br />
vescicolazione del reticolo endoplasmatico.<br />
Se questi sono sospesi <strong>in</strong> un me<strong>di</strong>um<br />
contenente 2 µM Ca ++ , si ha, <strong>in</strong> circa 5<br />
m<strong>in</strong>uti, un calo considerevole del Ca ++ libero<br />
(circa 0.25 µM Ca ++ f<strong>in</strong>ale). Se si aggiunge<br />
tapsigarg<strong>in</strong>a (un sesquiterpene, estratto<br />
dall’Ombrellifera Thapsia garganica,<br />
promotore <strong>di</strong> tumori sulla pelle <strong>di</strong> topi), si ha<br />
un aumento considerevole del calcio.<br />
IP3 conferma l’aumento (ve<strong>di</strong> fig.C).<br />
In D si vede che 1µM IP3 determ<strong>in</strong>a un<br />
istantaneo rilascio <strong>di</strong> calcio da parte dei<br />
microsomi, confermato dalla Tg.<br />
Si ritiene che Tg <strong>in</strong>ibisca le SERCA ATPasi<br />
(ve<strong>di</strong> pag.97). Poiché molto probabilmente<br />
esiste uno stato stazionario, tra Ca ++ che<br />
entra per azione della pompa del calcio e<br />
Ca ++ che esce, bloccando l’<strong>in</strong>gresso, si<br />
osserva solo il rilascio (riserve <strong>di</strong><br />
Ca ++ endocellulari, ve<strong>di</strong> anche pag.231).<br />
196<br />
From:<br />
Thastrup e coll. Proc. Note. Acad. Sci. 87,<br />
2466, 1990
Diversi ormoni stimolano l’attività fosfolipasica C<br />
(tra cui la seroton<strong>in</strong>a). Anche analoghi del GTP<br />
non idrolizzabili (che stimolano<br />
permanentemente G-prote<strong>in</strong>) determ<strong>in</strong>ano<br />
attivazione <strong>di</strong> fosfolipasi C. Si pensa che la<br />
fosfolipasi C sia attivata per me<strong>di</strong>azione da parte<br />
<strong>di</strong> G-prote<strong>in</strong>s. La toss<strong>in</strong>a della pertosse (che<br />
ADP ribosila le Gi) <strong>in</strong>ibisce la fosfolipasi C.<br />
M = microsomi Tg = tapsigarg<strong>in</strong>a<br />
Metabolismo dell’IP3<br />
Sicuro bersaglio dell’IP3 sono i recettori (R2) sull’ER. Ma, come si è detto, è un segnale transiente<br />
(come tutti i secon<strong>di</strong> messaggeri) e viene degradato rapidamente da <strong>fosfatasi</strong> a <strong>in</strong>ositolo libero:<br />
197
Con la reazione 2 (ve<strong>di</strong> pag.199), l’<strong>in</strong>ositolo può reagire <strong>di</strong>rettamente con CDP <strong>di</strong>acilglicerolo e il<br />
ciclo riprende con la formazione <strong>di</strong> fosfati<strong>di</strong>l <strong>in</strong>ositolo ed, eventualmente, due fosforilazioni con<br />
riprist<strong>in</strong>o del PIP2. I sali <strong>di</strong> litio bloccano la <strong>fosfatasi</strong> che catalizza il <strong>di</strong>stacco dell’ultimo fosfato. Tali<br />
sali sono utilizzati <strong>in</strong> me<strong>di</strong>c<strong>in</strong>a, <strong>in</strong> quanto esercitano azione tranquillante. Tuttavia l’IP3 non viene<br />
soltanto degradato (<strong>in</strong>serto: ve<strong>di</strong> pag.200). Può essere ulteriormente fosforilato <strong>in</strong> 3 a Inositolo 1, 3,<br />
4, 5 P4 da una <strong>in</strong>ositol c<strong>in</strong>asi (ve<strong>di</strong> ta<strong>pp</strong>a 1 a pag.197 e 1 a pag.200). È anch’esso un secondo<br />
messaggero e sembra che promuova l’<strong>in</strong>gresso <strong>di</strong> calcio dalla membrana plasmatica. L’Inositolo 1,<br />
3, 4, 5 P4 è defosforilati <strong>in</strong> 5 a Inositolo 1, 3, 4 P3 (<strong>di</strong>verso dall’IP3 “classico”), che, a sua volta, può<br />
essere fosforilato <strong>in</strong> 6 a Inositolo 1, 3, 4, 6 P4, che sembra <strong>in</strong>attivo (ve<strong>di</strong> ta<strong>pp</strong>a 2 a pag.200 e ta<strong>pp</strong>a<br />
2 a pag.197).<br />
Comunque l’Inositolo 1, 3, 4 P3 è defosforilati prima <strong>in</strong> posizione 3 a IP2 e subisce successivi<br />
passaggi <strong>di</strong> defosforilazione.<br />
I tempi <strong>di</strong> risposta all’IP3 variano: da 1 sec negli astrociti a 5-10 m<strong>in</strong>uti <strong>in</strong> oociti. Nelle cellule sono<br />
stati identificati anche IP5 e IP6 (anche 1 mM!! Sono i fosfo<strong>in</strong>ositoli più abbondanti <strong>in</strong> cellule HL60:<br />
IP5 = 35 µM e IP6 = 50µM; 100 volte superiori a IP3), la cui concentrazione endocellulare non<br />
sembra variare <strong>in</strong> seguito a stimoli esterni. Questi composti vengono secreti ed hanno azione<br />
extracellulare. Presentano un limitato turnover. Micro<strong>in</strong>iezioni <strong>di</strong> IP5 e IP6 <strong>in</strong>ducono rapide<br />
alterazioni del battito car<strong>di</strong>aco. Sono 10 – 100 volte più potenti dell’acido glutammico. IP4 non ha<br />
effetto.<br />
Il fosfati<strong>di</strong>l<strong>in</strong>ositolo (PI) può costituire ancore per<br />
prote<strong>in</strong>e esterne alle cellule.<br />
A pag.203 e riportato l’<strong>in</strong>sieme dei processi prima esam<strong>in</strong>ati. Si osservi che la PLC libera DG, che<br />
verrà riciclato ad acido fosfati<strong>di</strong>co (ve<strong>di</strong> DGK), CDP-DG, etc. e IP3 che ritornerà <strong>in</strong>ositolo.<br />
198
199
Inserto: Metabolismo dell’Inositol Trifosfato (IP3)<br />
Formazione dell’isomero dell’IP3 (analisi dei processi riassunti a pag.197)<br />
Con queste due reazioni è spiegata la formazione dell’isomero dell’IP3 (la posizione 3 è fosforilata<br />
anziché la 5). Tale isomero è effettivamente presente e può accompagnare la produzione <strong>di</strong> IP3. In<br />
certi casi questo IP3 può essere presente a concentrazioni maggiori rispetto a quelle dell’IP3<br />
“classico”. L’IP3 isomero può essere fosforilato <strong>in</strong> 6 e si ha un nuovo tetrafosfato.<br />
Bombes<strong>in</strong>a:<br />
Neuropeptide <strong>di</strong> 14 AA, prodotto da neuroni del<br />
sistema nervoso centrale e periferico.<br />
Regola la concentrazione del Ca ++ nel muscolo<br />
liscio.<br />
200
La fosforilazione <strong>in</strong> posizione 3 dei fosfati<strong>di</strong>l<strong>in</strong>ositi<strong>di</strong><br />
Nei paragrafi precedenti sono state analizzate le vie che sc<strong>in</strong>dono il fosfolipide acido Fosfati<strong>di</strong>l<br />
Inositolo 4, 5 – bis fosfato (ad opera della fosfolipasi C) e i processi che rielaborano il suo prodotto<br />
IP3. Ci siamo cioè occupati soprattutto <strong>di</strong> processi degradativi degli <strong>in</strong>ositolo. Circa la s<strong>in</strong>tesi dei<br />
fosfati<strong>di</strong>l<strong>in</strong>ositi<strong>di</strong> è stato ben caratterizzato un nuovo enzima ubiquitario che fosforila <strong>in</strong> una<br />
posizione un po’ <strong>in</strong>solita del fosfati<strong>di</strong>l<strong>in</strong>ositolo: <strong>in</strong>fatti la nuova c<strong>in</strong>asi <strong>in</strong> questione è <strong>in</strong> grado <strong>di</strong><br />
fosforilate specificamente la posizione 3 dell’anello del myo-<strong>in</strong>ositolo del fosfati<strong>di</strong>l <strong>in</strong>ositolo. In vitro<br />
tale enzima è <strong>in</strong> grado <strong>di</strong> portare avanti le seguenti tre fosforilazioni, che <strong>di</strong>fferiscono solo per il<br />
substrato (già variamente fosforilato, ovvero sono gli <strong>in</strong>terme<strong>di</strong> che portano alla s<strong>in</strong>tesi del PIP2 –<br />
ve<strong>di</strong> via centrale <strong>di</strong> pag.199):<br />
- Fosforilazione <strong>in</strong> 3 del fosfati<strong>di</strong>l<strong>in</strong>ositolo<br />
- Fosforilazione <strong>in</strong> 3 del fosfati<strong>di</strong>l<strong>in</strong>ositolo 4-fosfato<br />
- Fosforilazione <strong>in</strong> 3 del fosfati<strong>di</strong>l<strong>in</strong>ositolo 4, 5 bis-fosfato<br />
L’enzima è denom<strong>in</strong>ato fosfati<strong>di</strong>l<strong>in</strong>ositolo 3-c<strong>in</strong>asi (PI3 c<strong>in</strong>asi), ed <strong>in</strong> vivo sembra che il suo<br />
substrato sia soltanto il PIP2, ovvero sembra che sia operativa solo la terza reazione, con<br />
formazione del fosfati<strong>di</strong>l<strong>in</strong>ositolo 3, 4, 5 tris-fosfato. Per semplicità <strong>in</strong><strong>di</strong>cheremo tale composto con<br />
la sigla PIP3.<br />
Con una reazione <strong>di</strong> questo tipo si ottiene un fosfati<strong>di</strong>l <strong>in</strong>ositolo ancora più fosforilato del PIP2<br />
“classico”. È stato <strong>di</strong>mostrato che tale fosfo<strong>in</strong>ositi<strong>di</strong> non è scisso da alcun tipo <strong>di</strong> fosfolipasi C. Ci<br />
occuperemo dopo delle importanti funzioni biologiche <strong>di</strong> tale PIP3. Ve<strong>di</strong>amo ora le reazioni a suo<br />
carico:<br />
- Il PIP3 è defosforilato <strong>in</strong> posizione 5, ottenendo il fosfati<strong>di</strong>l <strong>in</strong>ositolo 3, 4 bisfosfato, che, a sua<br />
volta, è ancora defosforilato <strong>in</strong> posizione 4, ottenendo il fosfati<strong>di</strong>l-<strong>in</strong>ositolo 3-fosfato (qu<strong>in</strong><strong>di</strong> si<br />
ha defosforilazione della posizione 5 e poi della 4, cioè è ripercorsa schematicamente a ritroso<br />
la via <strong>di</strong> s<strong>in</strong>tesi del PIP2). In conclusione la posizione 3 è resistente nei confronti delle <strong>fosfatasi</strong>.<br />
Possiamo subito constatare che il PIP2 è substrato <strong>di</strong> due enzimi:<br />
- la fosfolipasi C, che libera <strong>di</strong>gliceride ed IP3;<br />
- la PI3 c<strong>in</strong>asi, che forma PIP3.<br />
N.B.: questa c<strong>in</strong>asi, che fosforila <strong>in</strong> posizione 3 il fosfolipide, non va confusa con la c<strong>in</strong>asi che<br />
fosforila <strong>in</strong> 3 l’<strong>in</strong>ositolo fosforilato IP3 (ta<strong>pp</strong>a 1, pag.200)<br />
Ambedue gli enzimi sono sotto il controllo <strong>di</strong> prote<strong>in</strong>e G: la PI3 c<strong>in</strong>asi è attivata da Ras (è una<br />
prote<strong>in</strong>a G <strong>di</strong> tipo monometrico) e dal recettore per PDGF (ve<strong>di</strong> paragrafo seguente). La PLC è<br />
attivata dalle prote<strong>in</strong>e G <strong>di</strong> tipo Gp.<br />
201
Circa la funzione <strong>di</strong> questo nuovo fosfati<strong>di</strong>l <strong>in</strong>ositolo tris-fosfato, <strong>di</strong>ciamo solo che avvia importanti<br />
stimoli mitogeni. Per esempio la riorganizzazione del citoscheletro <strong>in</strong> cellule PAE (ve<strong>di</strong> pag.214) è<br />
stata ben delucidata (ve<strong>di</strong> Curr. Biology, 4, 385, 1994). In realtà il suo meccanismo d’azione non è<br />
ancora noto nei dettagli. Meglio conosciuta è la via d’attivazione della PI3K (ma dal 1997 la PI3K è<br />
legata all’attività della PKB; ve<strong>di</strong> pagg.205-207):<br />
Attivazione della PI3 c<strong>in</strong>asi<br />
La PI3 c<strong>in</strong>asi (PI3K) è formata da due subunità:<br />
▪ una subunità p85 <strong>di</strong> PM 85000 Da, con funzioni regolatorie. Esiste una p85-α ed una p85-β<br />
con elevata omologia <strong>di</strong> sequenza fra <strong>di</strong> loro. Sono note le proprietà della α. Tale p85 presenta<br />
due dom<strong>in</strong>i SH2 ed un dom<strong>in</strong>io SH3.<br />
▪ una subunità p110 <strong>di</strong> PM 110000 Da, con funzioni catalitiche, che è attivata quando i dom<strong>in</strong>i<br />
SH2 della p85 si legano alle tiros<strong>in</strong>e nello stato fosforilato del recettore per il PDGF.<br />
È qui sotto riportato lo schema del recettore per il PDGF. Tale schema, <strong>in</strong>sieme a quello<br />
dell’EGFR, è riportato anche a pag.117. Qui è più dettagliato: per esempio è messa <strong>in</strong> risalto la<br />
struttura etero-<strong>di</strong>merica della PI3K; <strong>in</strong>oltre è chiaramente specificato che l’autofosforilazione delle<br />
tiros<strong>in</strong>e avviene per <strong>di</strong>merizzazione del recettore sotto stimolo del PDGF. Inoltre la parte<br />
extracellulare del recettore contiene 5 dom<strong>in</strong>i “tipo immunoglobul<strong>in</strong>a”.<br />
From Current Biology 4, 385 (1994)<br />
Le tiros<strong>in</strong>e autofosforilabile sono 7. Non sono equivalenti tra loro, ai f<strong>in</strong>i dell’<strong>in</strong>terazione con i<br />
dom<strong>in</strong>i SH2 delle varie prote<strong>in</strong>e che ad essi si legano. Infatti sono giustamente <strong>in</strong><strong>di</strong>cati con segni<br />
convenzionali <strong>di</strong>versi tra loro. Ricor<strong>di</strong>amo che sono i 3 AA che imme<strong>di</strong>atamente seguono la tiros<strong>in</strong>a<br />
a conferire specificità per il tipo <strong>di</strong> SH2 e qu<strong>in</strong><strong>di</strong> per la prote<strong>in</strong>a che ad essi si lega. Sono <strong>in</strong><strong>di</strong>cate le<br />
prote<strong>in</strong>e: p60-src; PI3K; Ras-GAP (prote<strong>in</strong>a che aumenta la capacità <strong>di</strong> idrolizzare il GTP della<br />
prote<strong>in</strong>a-G p21-Ras); la fosfolipasi-C <strong>di</strong> tipo γ (la sua attivazione è descritta <strong>in</strong> dettaglio a pag.232).<br />
202
Per quanto riguarda l’<strong>in</strong>terazione PI3K e PDGFR, si può osservare che le tiros<strong>in</strong>e autofosforilabili<br />
implicate sono:<br />
- Tyr 740, <strong>in</strong>serita nella sequenza YMDM<br />
- Tyr 751, <strong>in</strong>serita nella sequenza YVPM.<br />
Nel paragrafo seguente vedremo meglio i dom<strong>in</strong>i <strong>di</strong> tipo SH2 ed SH3.<br />
Possiamo ricostruire la catena <strong>di</strong> eventi che porta all’attivazione della PI3K:<br />
Fattore <strong>di</strong> crescita piastr<strong>in</strong>ico Recettore per il PDGF<br />
⇓<br />
complesso PDGF-<strong>di</strong>mero del recettore<br />
⇓<br />
autofosforilazione delle tiros<strong>in</strong>e<br />
⇓<br />
legame della PI3K (ed altre prote<strong>in</strong>e)<br />
a specifiche tiros<strong>in</strong>e fosforilate tramite<br />
il dom<strong>in</strong>io (o i dom<strong>in</strong>i) SH2<br />
⇓<br />
attivazione della PI3K<br />
Sull’importanza della PI3K abbiamo un preciso riscontro con il virus a DNA del Polioma, che è<br />
molto simile all’SV 40 (ve<strong>di</strong> prima struttura c-Src; pag.211). Questi sono virus oncogeni a DNA.<br />
La trascrizione avviene <strong>in</strong> corrispondenza <strong>di</strong><br />
un’orig<strong>in</strong>e (ori) e procede <strong>in</strong> senso antiorario e<br />
orario nello schema a lato. È prodotto, per<br />
splic<strong>in</strong>g alternativo, un mRNA per antigene Tpiccolo,<br />
T-me<strong>di</strong>o e T-grande. In senso orario<br />
sono trascritti i geni per prote<strong>in</strong>e virali (VP), ma<br />
ciò avviene tar<strong>di</strong>vamente.<br />
(T = tumorali)<br />
La prote<strong>in</strong>a T-me<strong>di</strong>a (PM 58000 Da) forma un<br />
complesso 1:1 con prote<strong>in</strong>e <strong>di</strong> tipo src, attivando<br />
generalmente la capacità tiros<strong>in</strong>-c<strong>in</strong>asica <strong>di</strong><br />
queste. Le T-me<strong>di</strong>a fosforilate si associano, via<br />
SH2 (<strong>di</strong> p85 della PI3K), con PI3K. La T-me<strong>di</strong>a<br />
impe<strong>di</strong>sce la fosforilazione <strong>di</strong> Tyr 527 <strong>di</strong> src.<br />
È stato <strong>di</strong>mostrato che tutte le mutazioni del Tme<strong>di</strong>o<br />
che annullano l’<strong>in</strong>terazione con PI3K<br />
sono accompagnate da scomparsa dell’azione<br />
trasformante del polioma <strong>in</strong> cellule 3T3<br />
(fibroblasti) <strong>in</strong> coltura.<br />
Le l<strong>in</strong>ee nello schema <strong>in</strong><strong>di</strong>cano le parti<br />
dell’mRNA tradotte.<br />
T-piccolo <strong>in</strong>ibisce la defosforilazione <strong>di</strong> MEK da parte <strong>di</strong> Prote<strong>in</strong>a Fosfatasi 2A (PP2A); ve<strong>di</strong><br />
pag.159.<br />
203
1) T me<strong>di</strong>o forma un<br />
complesso 1:1 con<br />
prote<strong>in</strong>e src, attivando<br />
l’attività tiros<strong>in</strong> c<strong>in</strong>asica <strong>di</strong><br />
<strong>pp</strong>60. E’ promossa la<br />
defosforilazione <strong>di</strong> Tyr-<br />
527 e, qu<strong>in</strong><strong>di</strong>, l’attivazione<br />
<strong>di</strong> src.<br />
2) Quando T me<strong>di</strong>o è<br />
fosforilato su Tyr-315 si<br />
associa con PI3K.<br />
3) Tutte le mutazioni del T<br />
me<strong>di</strong>o che annullano<br />
<strong>in</strong>terazioni con PI3K =<br />
polioma non trasformante.<br />
4) T me<strong>di</strong>o si associa a csrc<br />
(che possiede Tyr-<br />
527) attivandola, ma non<br />
a v-src, che non ha Tyr-<br />
527.<br />
204
Correlazioni tra la Leucemia Acuta Trasformante (AKT) e la Prote<strong>in</strong>a C<strong>in</strong>asi B<br />
[TIBS 22(261)pag. 355, sett. 1997- TIBS 22(259)pag.267, luglio 1997]<br />
L’enzima PI3-C<strong>in</strong>asi è responsabile dell’attività <strong>di</strong> altri enzimi. Tra questi è importante una nuova<br />
Prote<strong>in</strong>a C<strong>in</strong>asi, denom<strong>in</strong>ata Prote<strong>in</strong>a C<strong>in</strong>asi B (PKB), che pertanto andrà aggiunta al nutrito<br />
numero <strong>di</strong> prote<strong>in</strong>e c<strong>in</strong>asi che sono già state descritte. Tale PKB è una Ser<strong>in</strong>/Treon<strong>in</strong> C<strong>in</strong>asi.<br />
In breve è stato <strong>di</strong>mostrato che il Fosfatil Inositolo 3,4,5 tris-fosfato (PIP3) “arruola” su membrana<br />
la PKB, che per essere completamente attiva richiede anche alcune fosforilazioni su se stessa da<br />
parte <strong>di</strong> altre prote<strong>in</strong>e c<strong>in</strong>asi (ve<strong>di</strong> oltre , sono le PDK1 e PDK2, ovvero P-<strong>in</strong>ositol Dipendent<br />
K<strong>in</strong>ase). La PKB attiva determ<strong>in</strong>a la fosforilazione <strong>di</strong> una serie <strong>di</strong> substrati (ve<strong>di</strong> più avanti) che<br />
generano una risposta complessiva <strong>di</strong> tipo anabolico, tipo quella scatenata dall’<strong>in</strong>sul<strong>in</strong>a; <strong>in</strong>fatti per<br />
tale PKB è stato ipotizzato un ruolo importante nel processo a cascata generato dall’<strong>in</strong>sul<strong>in</strong>a<br />
stessa. E’ molto <strong>in</strong>teressante, <strong>in</strong>oltre, che si ottenga anche una risposta <strong>di</strong> so<strong>pp</strong>ressione<br />
dell’apoptosi, che sotto il profilo logico è del tutto congruente. Ovvero, se <strong>in</strong> una cellula è promosso<br />
un processo <strong>di</strong> svilu<strong>pp</strong>o (più <strong>in</strong> generale anabolico), è doveroso che contemporaneamente sia<br />
annullato il processo <strong>di</strong> morte cellulare programmata, perché assolutamente <strong>in</strong>compatibili.<br />
Tale PKB è stata <strong>in</strong><strong>di</strong>viduata grazie all’attività enzimatica co<strong>di</strong>ficata dall’RNA <strong>di</strong> un virus (<strong>di</strong> tipo<br />
retrovirus come moltri altri virus oncogeni, primo fra tutti il virus del sarcoma <strong>di</strong> Rous che co<strong>di</strong>fica<br />
per v-src). Tale virus è denom<strong>in</strong>ato AKT (AKute Trasform<strong>in</strong>g), identificato nei l<strong>in</strong>fomi <strong>di</strong> cellule T <strong>in</strong><br />
ro<strong>di</strong>tori. Il gene trasmesso dal virus co<strong>di</strong>fica per una prote<strong>in</strong>a, la cui controparte cellulare fu presto<br />
identificata nell’uomo: si tratta della PKB.<br />
Proprietà della Prote<strong>in</strong>a C<strong>in</strong>asi B<br />
Le proprietà funzionali sono leggibili attraverso la struttura modulare della PKB stessa. Nell’uomo<br />
sono state descritte 3 PKB (PKB-α, PKB-β1 e PKB-β2). Ci riferiamo, per semplicità alla PKB-α<br />
umana. Le altre presentano, comunque, un’elevata omologia <strong>di</strong> sequenza.<br />
1) La PKB-α presenta, all’Nterm<strong>in</strong>ale<br />
(dall’amm<strong>in</strong>oacido 1 al<br />
106), un dom<strong>in</strong>io <strong>di</strong> tipo<br />
Plekstr<strong>in</strong>a, denom<strong>in</strong>ato PH<br />
(Pleckstr<strong>in</strong>-Homology).<br />
Thr 308 Ser473<br />
PH Dom<strong>in</strong>io c<strong>in</strong>asico Coda<br />
1 106 148 4<strong>12</strong> 480<br />
I dom<strong>in</strong>i PH sono riscontrabili <strong>in</strong> molte altre prote<strong>in</strong>e. La plekstr<strong>in</strong>a è una prote<strong>in</strong>a, contenente tali<br />
dom<strong>in</strong>i PH, che è il pr<strong>in</strong>cipale substrato della fosforilazione della PKC nelle piastr<strong>in</strong>e (ve<strong>di</strong><br />
pag.107). Il ruolo <strong>di</strong> tali dom<strong>in</strong>i non era ben def<strong>in</strong>ito. In generale, per essi è stato ipotizzato un ruolo<br />
<strong>di</strong> zip-code, cioè un dom<strong>in</strong>io che <strong>in</strong><strong>di</strong>rizza la prote<strong>in</strong>a che lo contiene verso determ<strong>in</strong>ati bersagli. Gli<br />
stessi SH2 ed SH3 sono, <strong>di</strong> fatto, dei zip-code (tipici dom<strong>in</strong>i zip-code sono quelli che <strong>in</strong><strong>di</strong>rizzano<br />
alcune PTP-Prote<strong>in</strong> Tiros<strong>in</strong>-Phosphatases- ve<strong>di</strong> pag.167).<br />
I dom<strong>in</strong>i PH sono assai <strong>di</strong>ffusi tra le GEP, cioè le prote<strong>in</strong>e che attivano le G-prote<strong>in</strong> <strong>di</strong> tipo Ras<br />
(SOS è una GEP). Recentemente sono state identificate una <strong>in</strong>tera famiglia <strong>di</strong> GEP, che<br />
contengono tutte un dom<strong>in</strong>io PH (si tratta della Dbl-Diffuse B cell Limphoma, che sono le GEP <strong>di</strong><br />
Rho; quest’ultima a<strong>pp</strong>artiene alla superfamiglia delle prote<strong>in</strong>a Ras). S’ipotizzava che tali PH<br />
<strong>in</strong><strong>di</strong>rizzassero le prote<strong>in</strong>e che li contengono verso determ<strong>in</strong>ati elementi presenti sulla membrana.<br />
Con la scoperta della PKB tale ipotesi è stata verificata.<br />
⇒ Infatti il dom<strong>in</strong>io PH della PKB <strong>in</strong><strong>di</strong>rizza la PKB stessa verso il Fosfati<strong>di</strong>l-<br />
Inositolo 3,4,5-tris fosfato (PIP3)<br />
Questo processo è <strong>di</strong> fondamentale importanza, anche per comprendere il ruolo della PI3-c<strong>in</strong>asi<br />
stessa. Infatti la PI3K produce un composto, il PIP3, per il quale non era stato identificato un<br />
enzima che lo elabora, come per esempio avviene per il PIP2 (<strong>in</strong>fatti la fosfolipasi C idrolizza il<br />
PIP2, con produzione <strong>di</strong> <strong>di</strong>gliceride ed IP3). La funzione della PI3K è quella <strong>di</strong> produrre il PIP3 che,<br />
<strong>in</strong> quanto tale, attira la PKB. Infatti il processo è transiente, perché esiste una PIP3-<strong>fosfatasi</strong>, che<br />
rimuove il fosfato dalla posizione 5, annullando il possibile “arruolamento” della PKB. Infatti il<br />
prodotto <strong>di</strong> defosforilazione <strong>in</strong> posizione 5 del PIP3 non arruola la PKB attraverso il dom<strong>in</strong>io PH.<br />
205<br />
⇐
2) In posizione centrale la PKB presenta il “classico” dom<strong>in</strong>io prote<strong>in</strong>a-c<strong>in</strong>asico, omologo a quello<br />
<strong>di</strong> altre prote<strong>in</strong>e c<strong>in</strong>asi, con struttura riconducibile a quella illustrata a pag.91.<br />
Per presentare completa attività occorre anche che la Treon<strong>in</strong>a-308 sia fosforilata. E’ stato<br />
ipotizzato che tale fosforilazione avvenga ad opera <strong>di</strong> una P-<strong>in</strong>ositol Dipendent K<strong>in</strong>ase, cioè una<br />
prote<strong>in</strong>a c<strong>in</strong>asi che è attivata dal Fosfati<strong>di</strong>l-Inositolo 3,4-bis-fosfato.<br />
3) Nella parte C-term<strong>in</strong>ale esiste una cosidetta “tail” (coda) dove una ser<strong>in</strong>a 473 deve essere<br />
fosforilata da una PDK2.<br />
La seguente figura (riprodotta da TIBS sett.’97 pag.357) riassume questi processi.<br />
206
Processi up-stream alla PKB:<br />
(fare riferimento allo schema della pag<strong>in</strong>a precedente).<br />
Un fattore <strong>di</strong> crescita, per esempio l’<strong>in</strong>sul<strong>in</strong>a, si lega al suo recettore. Si ha autofosforilazione <strong>di</strong><br />
alcune tiros<strong>in</strong>e, che richiamano la subunità regolatoria (p85) della PI3K<strong>in</strong>ase attraverso i dom<strong>in</strong>i<br />
SH2. La p85 tiene a sé legata anche la subunità catalitica della PI3K, ovvero la p110. (Per<br />
l’attivazione della PI3K è possibile anche seguire la via che co<strong>in</strong>volge Ras- ve<strong>di</strong> pag.216).<br />
Comunque sia, via recettore per fattore <strong>di</strong> crescita, o via Ras, si ottiene l’attivazione della<br />
PI3K<strong>in</strong>ase, che s<strong>in</strong>tetizza PtdIns (3,4,5) P3; quest’ultimo composto richiama sulla membrana la<br />
prote<strong>in</strong>a PKB.<br />
Con l’azione accessoria delle PDK1 e PDK2 si ottiene anche la fosforilazione della Treon<strong>in</strong>a-308 e<br />
della Ser<strong>in</strong>a-473, con piena attività della PKB.<br />
Processi down-stream alla PKB:<br />
Il seguito <strong>di</strong> questo processo a cascata è decifrabile attraverso l’<strong>in</strong><strong>di</strong>viduazione dei substrati della<br />
PKB stessa.<br />
Come osservazione <strong>di</strong> carattere generale, ricor<strong>di</strong>amo che la PKB è una Ser<strong>in</strong>-Treon<strong>in</strong> c<strong>in</strong>asi. E’<br />
stata def<strong>in</strong>ita la sua sequenza consenso <strong>di</strong> fosforilazione:<br />
sito <strong>di</strong> fosforilazione<br />
↓<br />
- Arg- x -Arg- y - z -S/T - h - y -<br />
La Ser<strong>in</strong>a, o treon<strong>in</strong>a, fosforilabile da PKB è preceduta dai 2 residui fortemente basici <strong>di</strong> Arg<strong>in</strong><strong>in</strong>a,<br />
dove x può essere qualsiasi amm<strong>in</strong>oacido, y e z devono essere amm<strong>in</strong>oaci<strong>di</strong> <strong>di</strong> basso <strong>in</strong>gombro<br />
(per esempio glic<strong>in</strong>a) ed h-y ra<strong>pp</strong>resenta un nucleo idrofobico.<br />
→ Ricercando sulla banca dati i possibili substrati della PKB, è stata <strong>in</strong><strong>di</strong>viduata la Glicogeno<br />
S<strong>in</strong>tasi C<strong>in</strong>asi 3 (GSK3), che nella forma fosforilata è meno attiva, e qu<strong>in</strong><strong>di</strong> fosforila meno<br />
<strong>in</strong>tensamente la Glicogeno S<strong>in</strong>tasi, che esisterà più facilmente <strong>in</strong> forma de-fosforilata, cioè attiva.<br />
(Questa GSK3 è stata scoperta recentemente, e si pensava che la GS fosse <strong>di</strong>rettamente<br />
substrato della PKA. Possono essere operativi ambedue i fenomeni. Comunque la GS può essere<br />
fosforilata, e <strong>di</strong>sattivata, <strong>in</strong> una molteplicità <strong>di</strong> mo<strong>di</strong>, <strong>di</strong>versamente dalla Glicogeno Fosforilasi, che<br />
è fosforilata, e qu<strong>in</strong><strong>di</strong> attivata, solo sulla Ser<strong>in</strong>a-14).<br />
→ La PKB fosforila, e attiva, la S6c<strong>in</strong>asi (S6K), ovvero la prote<strong>in</strong>a c<strong>in</strong>asi specifica per le subunità<br />
S-6 dei ribosomi, con <strong>in</strong>cremento dalla s<strong>in</strong>tesi proteica.<br />
→ La PKB rende attivo E2F, regolando il ciclo cellulare. Si ricorderà che il fattore <strong>di</strong> trascrizione<br />
E2F è <strong>di</strong> norma legato alla prote<strong>in</strong>a ret<strong>in</strong>oblastoma (Rb), risultando da questa bloccato. Quando<br />
Rb è fosforilata, si ha rilascio <strong>di</strong> E2F (ve<strong>di</strong> pag.137). E’ stato ipotizzato che PKB fosforili Rb.<br />
E’ stato <strong>di</strong>mostrato che l’attivazione <strong>di</strong> PKB determ<strong>in</strong>a un blocco dell’apoptosi. Infatti cellule<br />
esposte a raggi UV e contemporaneamente attivate <strong>in</strong> PKB non entrano <strong>in</strong> apoptosi.<br />
Da ultimo (ve<strong>di</strong> figura <strong>di</strong> pag<strong>in</strong>a precedente), stress cellulari <strong>di</strong> varia natura attivano una particolare<br />
prote<strong>in</strong>a c<strong>in</strong>asi attivata da MAPK (MAPKAP2) che fosforila la Ser 473, contribuendo ad attivare la<br />
PKB.<br />
207
<strong>Prote<strong>in</strong>e</strong> con attività Tiros<strong>in</strong> C<strong>in</strong>asica non recettoriali<br />
Esistono numerose prote<strong>in</strong>e con attività tiros<strong>in</strong> c<strong>in</strong>asica non legata a recettori (cioè non-RTK). Le<br />
più note sono le Src-PTK (ve<strong>di</strong> paragrafo seguente). Ma ne esistono altre. La struttura <strong>di</strong> alcune <strong>di</strong><br />
queste è illustrata nella figura seguente, tratta da Thomas & Brugge, Ann. Rev. of Cell and<br />
Developmental Biology, 13, 515, 1997):<br />
La Csk è una PTK cellulare che ha una struttura assi simile alla Src, mancante però<br />
dell’ancoraggio alla membrana plasmatica (<strong>in</strong>fatti non presenta il dom<strong>in</strong>io SH4), pur presentando<br />
una struttura assai simile a quella della Src (a partire dall’N-term<strong>in</strong>ale esiste, <strong>in</strong>fatti, un dom<strong>in</strong>io SH-<br />
3, un dom<strong>in</strong>io SH-2 ed il dom<strong>in</strong>io prote<strong>in</strong>a-tiros<strong>in</strong>-c<strong>in</strong>asico). Csk deriva da Cellular src k<strong>in</strong>ase, e<br />
tale denom<strong>in</strong>azione riflette molto bene la sua reale funzione. Infatti fosforila la tiros<strong>in</strong>a 527 della<br />
stessa Src (rendendola non-attiva, ve<strong>di</strong> alla pag<strong>in</strong>a seguente il meccanismo molecolare <strong>di</strong> tale<br />
<strong>in</strong>ibizione). Tale enzima si rende necessario anche perché la stessa Src non è <strong>in</strong> grado <strong>di</strong><br />
autofosforilarsi sulla tiros<strong>in</strong>a 527. La Csk è, d’altronde, versatile per questo ruolo (fosforilazione <strong>di</strong><br />
un’altra PTK), <strong>in</strong> quanto non contiene una tiros<strong>in</strong>a equivalente alla tiros<strong>in</strong>a-527 della Src.<br />
La Tec è una PTK non associata a recettori che presenta forti omologie strutturali con Csk, con<br />
qualche dom<strong>in</strong>io accessorio <strong>in</strong> più. Infatti, come Csk (ve<strong>di</strong> figura sopra) ha i dom<strong>in</strong>i SH3, SH2 e il<br />
catalitico con, <strong>in</strong> più all’N-term<strong>in</strong>ale, un dom<strong>in</strong>io PH (Plekstr<strong>in</strong> Homology, ve<strong>di</strong> pag.205). Qu<strong>in</strong><strong>di</strong> ha<br />
qualche analogia con la PKB, solo che PKB è una S/T c<strong>in</strong>asi, mentre Tec è una Tiros<strong>in</strong> c<strong>in</strong>asi.<br />
Le Syk/ZAP possono essere substrati della stessa Src. Il dom<strong>in</strong>io catalitico è preceduto da due<br />
dom<strong>in</strong>i SH2. Syk e ZAP sono due prote<strong>in</strong>e <strong>di</strong>st<strong>in</strong>te, anche se altamente omologhe. Syk è attivata<br />
da o<strong>pp</strong>ortune lect<strong>in</strong>e sia <strong>in</strong> piastr<strong>in</strong>e che <strong>in</strong> cellule B, mentre ZAP svolge un ruolo critico<br />
nell’attivazione delle cellule T.<br />
Fak (Focal adesion k<strong>in</strong>ase) è una PTK non associata a recettori che è fosforilata ed attivata <strong>in</strong><br />
seguito all’associazione a molte <strong>in</strong>tegr<strong>in</strong>e. Infatti, all’N-term<strong>in</strong>ale, possiede l’importante dom<strong>in</strong>io <strong>di</strong><br />
legame alle <strong>in</strong>tegr<strong>in</strong>e. Possiede poi altri dom<strong>in</strong>i accessori al C-term<strong>in</strong>ale che controllano il legame<br />
alle placche <strong>di</strong> adesione, <strong>in</strong> particolare alla prote<strong>in</strong>a tal<strong>in</strong>a <strong>in</strong> esse presente.<br />
208
<strong>Prote<strong>in</strong>e</strong> c<strong>in</strong>asi della famiglia Src (da S.A. Courtneidge, “Prote<strong>in</strong> K<strong>in</strong>ase”, pag.213)<br />
L’importante prote<strong>in</strong>a tiros<strong>in</strong>-c<strong>in</strong>asi Src a<strong>pp</strong>artiene ad una famiglia che comprende numerose altre<br />
prote<strong>in</strong>e: si tratta della Famiglia della Src-c<strong>in</strong>asi (Src-PTK). Nella Tabella seguente sono elencate<br />
le pr<strong>in</strong>cipali Src-PTK:<br />
Src è riportata per prima; può essere considerata Src-PTK prototipo. Contiene anche un dom<strong>in</strong>io<br />
SH4 (all’N-term<strong>in</strong>ale), che governa la reazione <strong>di</strong> miristoilazione, dove la glic<strong>in</strong>a <strong>in</strong> posizione 2 è<br />
essenziale.<br />
La prote<strong>in</strong>a Yes deriva dai virus Y73 che genera il sarcoma <strong>di</strong> Esh (Yes = Y73 and Esh sarcoma).<br />
Le prote<strong>in</strong>e della famiglia Src sono assai <strong>di</strong>stribuite (Xenopus, Drosophila, Hydra, spugne, ecc.).<br />
Non si trovano nel lievito, per cui si pensa che siano associate ad organismi pluricellulari.<br />
Struttura terziaria della prote<strong>in</strong>a Src [da Current Biology 7 (5) R295 (1997)]<br />
E’ stata def<strong>in</strong>ita <strong>in</strong> dettaglio la struttura terziaria della prote<strong>in</strong>a c-Src. Nella parte destra della figura<br />
della pag<strong>in</strong>a seguente è riconoscibile il noto dom<strong>in</strong>io bi-lobato della <strong>Prote<strong>in</strong>e</strong> C<strong>in</strong>asi (ve<strong>di</strong> pag.87).<br />
E’ evidenziato l’Activation segment, che corrisponde alla nota ansa catalitica con l’importante<br />
Treon<strong>in</strong>a-197 (riferita alla PKA) che, <strong>di</strong> norma, deve essere fosforilata per consentire l’accesso al<br />
peptide substrato. Infatti una importante Src-PTK (la Lck) è fosforilata proprio <strong>in</strong> tale posizione per<br />
essere attivata. L’elica C contiene il Glutammico-91 (numerazione riferita alla PKA).<br />
La Y527, se fosforilata, s’<strong>in</strong>nesta nella fessura presente nel dom<strong>in</strong>io SH2, e la Src risulta<br />
quiescente (non attiva), come è già stato esposto a pag.117. Ne deriva che il dom<strong>in</strong>io SH2<br />
accoglie il “retro” del dom<strong>in</strong>io catalitico.<br />
Anche il dom<strong>in</strong>io SH3 si lega al segmento proteico che unisce l’SH2 al dom<strong>in</strong>io catalitico. Infatti<br />
tale segmento, che contiene uno o due residui <strong>di</strong> prol<strong>in</strong>e, forma un’elica s<strong>in</strong>istrorsa (è possibile<br />
constatarlo me<strong>di</strong>ante attenta osservazione della figura) <strong>di</strong> tipo PP-II. Vedremo che i dom<strong>in</strong>i SH3 <strong>di</strong><br />
alcune prote<strong>in</strong>e presentano tale proprietà, ovvero <strong>di</strong> legare eliche s<strong>in</strong>istrorse contenenti prol<strong>in</strong>a<br />
presenti <strong>in</strong> altre prote<strong>in</strong>e. Qui, <strong>in</strong> Src, l’<strong>in</strong>terazione è realizzata nell’ambito della stessa<br />
macromolecola.<br />
L’<strong>in</strong>terazione della ”coda” C-term<strong>in</strong>ale contenente Y527-fosforilata con SH2 è <strong>di</strong> natura debole.<br />
Altre <strong>in</strong>terazioni SH2 con tiros<strong>in</strong>e fosforlate sono, al contrario, ben più <strong>in</strong>tense.<br />
Anche l’<strong>in</strong>terazione SH3 ⎯→ elica PP-2 è <strong>di</strong> natura debole. Al riguardo è <strong>in</strong>teressante che nel<br />
cosiddetto RT loop del dom<strong>in</strong>io SH3 <strong>di</strong> Src-virale esistono delle sostituzioni amm<strong>in</strong>oaci<strong>di</strong>che, che<br />
<strong>in</strong>deboliscono tale <strong>in</strong>terazione e rendono la prote<strong>in</strong>a v-Src più attiva della controparte protooncogenica.<br />
Qu<strong>in</strong><strong>di</strong> la prote<strong>in</strong>a v-Src è do<strong>pp</strong>iamente <strong>in</strong>debolita nelle sue funzioni quiescenti:<br />
1. manca della Tiros<strong>in</strong>a 527<br />
2. ha il loop RT del dom<strong>in</strong>io SH3 mo<strong>di</strong>ficato, con conseguente m<strong>in</strong>or attrazione per la parte<br />
catalitica.<br />
209
Qu<strong>in</strong><strong>di</strong> la struttura <strong>di</strong> Src-quiescente è stata paragonata a quella <strong>di</strong> un arma<strong>di</strong>llo arrotolato su sé<br />
stesso. In tale conformazione la C helix, che contiene il glutammico-91, è esposta al solvente e<br />
non può <strong>in</strong>teragire con la lis<strong>in</strong>a-72, che trasferirebbe il fosfato dell’ATP sulla prote<strong>in</strong>a substrato. E’<br />
<strong>in</strong>teressante che un cambio analogo <strong>di</strong> orientazione dell’elica C è realizzato nel processo <strong>di</strong><br />
attivazione della Cdk2 per legame alla cicl<strong>in</strong>a.<br />
210
Dom<strong>in</strong>i SH2 e SH3<br />
Sono dom<strong>in</strong>i con funzione caratteristica presenti nel prodotto <strong>di</strong> espressione dell’oncogene src,<br />
cioè nella prote<strong>in</strong>a <strong>pp</strong>60 src , dotata <strong>di</strong> attività tiros<strong>in</strong>-c<strong>in</strong>asica (ve<strong>di</strong> pag.72 e pag.110-113). Sono<br />
denom<strong>in</strong>ati SH perché Src Homology. Esistono dom<strong>in</strong>i <strong>di</strong> tipo:<br />
⇒ SH1<br />
Ne è presente soltanto uno, verso il C-term<strong>in</strong>ale della<br />
60-Src, e possiede attività tiros<strong>in</strong>-c<strong>in</strong>asica. È seguito<br />
dalla caratteristica Tyr-527, autofosforilabile =<br />
<strong>in</strong>ibizione dell’attività tiros<strong>in</strong>-c<strong>in</strong>asica. (classificazione<br />
H.Q.H.; ve<strong>di</strong> pag.83, etc.).<br />
⇒ SH2<br />
È formato da circa 110 residui ed è presente <strong>in</strong> una<br />
copia nella 60-Src. Tali dom<strong>in</strong>i sono presenti nella<br />
zona centrale della 60-Src. Possiedono l’importante<br />
proprietà <strong>di</strong> riconoscere tiros<strong>in</strong>e fosforilate presenti <strong>in</strong><br />
prote<strong>in</strong>e (ve<strong>di</strong> pag.117), anche nella Src stessa.<br />
Infatti, nella forma “quiescente”, la Src è fosforilata <strong>in</strong><br />
Tyr-527, che porta all’associazione <strong>di</strong> tale Tyr con<br />
l’SH2 della stessa Src, con ripiegamento su se stessa<br />
della catena polipepti<strong>di</strong>ca e scomparsa dell’attività<br />
tiros<strong>in</strong> c<strong>in</strong>asica. La Src virale non possiede tale tyr-<br />
527 e manca <strong>di</strong> tale meccanismo auto<strong>in</strong>ibitorio. I<br />
dom<strong>in</strong>i SH2 sono largamente <strong>di</strong>stribuiti tra prote<strong>in</strong>e: la<br />
PI3K ne contiene 2. Anche la PLC-γ ne contiene 2.<br />
Grb-2, un’importante prote<strong>in</strong>a “adattatrice”, ne<br />
contiene uno solo (ma contiene 2 dom<strong>in</strong>i SH3).<br />
Un dom<strong>in</strong>io SH2 è specifico per determ<strong>in</strong>ate tiros<strong>in</strong>e<br />
fosforilate. Come si è detto, il legame avviene <strong>in</strong> base<br />
ai tre AA che seguono la tiros<strong>in</strong>a fosforilata.<br />
2 dom<strong>in</strong>i SH2 sono presenti nella Prote<strong>in</strong> Tiros<strong>in</strong><br />
Fosfatasi PTP 1C (ve<strong>di</strong> pag.163). In tale caso la<br />
<strong>fosfatasi</strong> è “pilotata” sui suoi substrati da tali dom<strong>in</strong>i<br />
SH2.<br />
⇒ SH3<br />
Formato <strong>in</strong> me<strong>di</strong>a da circa 60 AA, è presente nella<br />
porzione N-term<strong>in</strong>ale della 60-Src. Ciascun SH3 ha<br />
aff<strong>in</strong>ità per tratti ricchi <strong>di</strong> prol<strong>in</strong>a <strong>di</strong> altre prote<strong>in</strong>e (ve<strong>di</strong><br />
più avanti).<br />
Vedremo <strong>in</strong> dettaglio gli SH3 presenti nella subunità 85-α della PI3K, nella spettr<strong>in</strong>a e nella<br />
prote<strong>in</strong>a Src. La prote<strong>in</strong>a c-Abl (è una tiros<strong>in</strong> c<strong>in</strong>asi ed è trasmessa, nella forma virale, dal virus<br />
della leucemia mur<strong>in</strong>a <strong>di</strong> Abelson; ve<strong>di</strong> pag.113) è associata con filamenti <strong>di</strong> act<strong>in</strong>a e la delezione<br />
<strong>in</strong> suoi dom<strong>in</strong>i SH3 elim<strong>in</strong>a l’associazione ai filamenti <strong>di</strong> act<strong>in</strong>a e determ<strong>in</strong>a trasformazione<br />
cellulare. In generale si ritiene che i dom<strong>in</strong>i SH3 consentano il legame al citoscheletro. Tuttavia<br />
hanno una funzione più ampia.<br />
All’N-term<strong>in</strong>ale la Src è miristoilata (ve<strong>di</strong> pagg.23-24) per poter essere ancorata alla membrana<br />
plasmatica.<br />
Nell’importante “prote<strong>in</strong>a adattatrice” Grb-2 (ve<strong>di</strong> più avanti) sono contenuti 2 dom<strong>in</strong>i SH3 (qu<strong>in</strong><strong>di</strong><br />
la Grb-2 possiede 1 dom<strong>in</strong>io SH2 e 2 dom<strong>in</strong>i SH3).<br />
In conclusione, nella prote<strong>in</strong>a Src troviamo l’SH1, che conferisce alla Src la proprietà <strong>di</strong> fosforilate<br />
le tiros<strong>in</strong>e <strong>di</strong> vari substrati.<br />
211
L’SH3 potrebbe essere <strong>in</strong>teso come dom<strong>in</strong>io <strong>di</strong> posizionamento, perché può “pilotare” la Src<br />
stessa sul citoscheletro, e l’SH2 garantisce l’<strong>in</strong>ibizione dell’attività tiros<strong>in</strong> c<strong>in</strong>asica della stessa Src,<br />
ma anche l’<strong>in</strong>terazione con altre prote<strong>in</strong>e perché si associa a tiros<strong>in</strong>e fosforilate.<br />
Circa i dom<strong>in</strong>i SH2 (che, ripetiamo, sono largamente <strong>di</strong>stribuiti tra le prote<strong>in</strong>e implicate nel<br />
metabolismo regolatorio), occorre sottol<strong>in</strong>eare che consentono <strong>di</strong> spiegare la f<strong>in</strong>alità del processo<br />
multiplo <strong>di</strong> autofosforilazione dei recettori per fattori <strong>di</strong> crescita (per esempio PDGFR ed EGFR;<br />
ve<strong>di</strong> pag.117, etc.), processo che era rimasto enigmatico s<strong>in</strong>o alla scoperta degli SH2.<br />
È <strong>in</strong>teressante che <strong>di</strong>verse prote<strong>in</strong>e implicate nel metabolismo regolatorio contengono sia dom<strong>in</strong>i<br />
SH2 che SH3 (per esempio PI3K e Grb-2), per cui può potenzialmente stabilirsi una rete<br />
estremamente complessa <strong>di</strong> <strong>in</strong>terazioni multiple (vedremo alcuni esempi che sono stati<br />
completamente ricostruiti).<br />
Proprietà strutturali dei dom<strong>in</strong>i SH2<br />
La costante <strong>di</strong> <strong>di</strong>ssociazione tra SH2 e pepti<strong>di</strong> s<strong>in</strong>tetici formati da soli 5 AA con tiros<strong>in</strong>a fosforilata<br />
e o<strong>pp</strong>ortune sequenze verso il C-term<strong>in</strong>ale è dell’or<strong>di</strong>ne del nanomolare: si tratta qu<strong>in</strong><strong>di</strong> <strong>di</strong><br />
<strong>in</strong>terazioni molto forti.<br />
Waksman e coll. (Nature, 358, 646, 1992) hanno risolto ai raggi-X la struttura <strong>di</strong> un SH2 <strong>di</strong> v-src<br />
complessato a pepti<strong>di</strong> con tiros<strong>in</strong>a fosforilata. Al <strong>di</strong> là dei dettagli strutturali, occorre rilevare che:<br />
- L’N- ed il C-term<strong>in</strong>ale <strong>di</strong> tale dom<strong>in</strong>io sono spazialmente contigui (questo avviene anche negli<br />
SH3). Pertanto tale dom<strong>in</strong>io è, a tutti gli effetti, un modulo, perché è teoricamente <strong>in</strong>seribile <strong>in</strong><br />
qualsiasi prote<strong>in</strong>a senza scompag<strong>in</strong>are eccessivamente la sua struttura e senza <strong>di</strong>m<strong>in</strong>uire la sua<br />
capacità <strong>di</strong> ripiegarsi nella struttura solita funzionale.<br />
Qui sopra è riportato lo schema della struttura. I rettangoli <strong>in</strong><strong>di</strong>cano α-eliche e le frecce <strong>in</strong><strong>di</strong>cano<br />
strutture β. Si può osservare che l’AA N-term<strong>in</strong>ale 144 ed il C-term<strong>in</strong>ale 249 sono contigui e<br />
partecipano ad una β struttura. Il foglio A <strong>in</strong><strong>di</strong>ca 4 tratti a struttura β, con le catene 2, 3 e 4<br />
antiparallele. Il C-term<strong>in</strong>ale del tratto 4 partecipa alla formazione del foglio B, dove esistono anche i<br />
due tratti antiparalleli 5 e 6. Qu<strong>in</strong><strong>di</strong> parte del 4, il 5 ed il 6 sono su <strong>di</strong> un piano (foglio B). I due piani<br />
A e B hanno qu<strong>in</strong><strong>di</strong> <strong>in</strong> comune l’asse 4. Esistono poi due α-eliche ai lati. Grosso modo l’<strong>in</strong>tera<br />
struttura è “a calice”, con le due α-eliche ai lati, ed al centro c’è la “tasca”, dove avviene<br />
l’<strong>in</strong>terazione con la fosfo-tiros<strong>in</strong>a, mentre parte dei filamenti β 4, 5 e 6 legano gli AA generalmente<br />
idrofobici collocati nel fosfo-tiros<strong>in</strong> peptide a valle della tiros<strong>in</strong>a fosforilata. Tre amm<strong>in</strong>oaci<strong>di</strong> basici<br />
<strong>in</strong>teragiscono con il residuo nettamente acido del fosfato: sono l’Arg-155 (sull’α-elica 1), l’Arg-175<br />
(sul filamento β numero 2) e la Lys-203 (sul filamento β numero 4).<br />
Waksman e coll. hanno confrontato le sequenze <strong>di</strong> 30 dom<strong>in</strong>i SH2, <strong>in</strong><strong>di</strong>viduati <strong>in</strong> 30 <strong>di</strong>verse<br />
prote<strong>in</strong>e. Se tali sequenze vengono all<strong>in</strong>eate si può constatare che i residui che legano<br />
fosfotiros<strong>in</strong>a sono <strong>in</strong>varianti, mentre esiste un gru<strong>pp</strong>o <strong>di</strong> amm<strong>in</strong>oaci<strong>di</strong> che formano una seconda<br />
zona dove alloggiano gli AA del fosfo-tiros<strong>in</strong> peptide che sono <strong>in</strong> posizione +1 e +3, mentre <strong>in</strong><br />
posizione zero compare la fosfotiros<strong>in</strong>a.<br />
2<strong>12</strong>
Si tratta del filamento 4, 5 e 6 dove (ve<strong>di</strong> area qui sottotratteggiata) esiste alta varianza<br />
amm<strong>in</strong>oaci<strong>di</strong>ca. Ciò è <strong>in</strong> l<strong>in</strong>ea con la necessità che <strong>di</strong>versi dom<strong>in</strong>i SH2 riconoscano specifiche (e<br />
qu<strong>in</strong><strong>di</strong> <strong>di</strong>verse tra loro) sequenze “a valle” della fosfo-tiros<strong>in</strong>a.<br />
Stu<strong>di</strong> cristallografici hanno <strong>di</strong>mostrato che, per esempio, Y (P) – M – D – M (AA n° 0 +1 +2 +3)<br />
lega la struttura SH2 della PI3K.<br />
Struttura e funzione dei dom<strong>in</strong>i SH3<br />
Anche la struttura dei dom<strong>in</strong>i SH3 è stata risolta completamente (ve<strong>di</strong> Morton & Campbell, Curr.<br />
Biology, 1994, 615).<br />
Quale controparte riconoscono i dom<strong>in</strong>i SH3? È stato accertato che <strong>in</strong><strong>di</strong>viduano i cosiddetti “pepti<strong>di</strong><br />
ricchi <strong>in</strong> prol<strong>in</strong>a” presenti <strong>in</strong> altre prote<strong>in</strong>e. Una <strong>di</strong> queste prote<strong>in</strong>e, con i dom<strong>in</strong>i ricchi <strong>in</strong> prol<strong>in</strong>a, è la<br />
Sos (Son of Sevenless), identificata <strong>in</strong>izialmente con uno screen genetico nella Drosophila. La<br />
prote<strong>in</strong>a Sos ha due dom<strong>in</strong>i ricchi <strong>in</strong> prol<strong>in</strong>a che si legano a due dom<strong>in</strong>i SH3 presenti nella prote<strong>in</strong>a<br />
adattatrice Grb-2. La Sos ha la proprietà <strong>di</strong> legarsi alla prote<strong>in</strong>a-G p21-Ras, attivandola, cioè<br />
<strong>in</strong>crementando lo scambio tra GDP (uscente dalla Ras) e GTP (entrante nella Ras). La Sos è una<br />
GEP (GTP Exchange Prote<strong>in</strong>) o GEF (GTP Exchange Factor).<br />
Un peptide s<strong>in</strong>tetico che è stato usato negli stu<strong>di</strong> <strong>di</strong> legame con dom<strong>in</strong>i SH3 è qui riportato:<br />
peptide s<strong>in</strong>tetico R K L P P R P S K<br />
Si è visto che il tratto ricco <strong>in</strong> prol<strong>in</strong>a forma un’elica s<strong>in</strong>istrorsa, che s’<strong>in</strong>serisce perfettamente <strong>in</strong><br />
una “nicchia” formata dalla catena polipepti<strong>di</strong>ca del dom<strong>in</strong>io SH3. Sono qui <strong>di</strong> seguito riportati gli<br />
schemi delle strutture <strong>di</strong> tre dom<strong>in</strong>i SH3 presenti nelle tre prote<strong>in</strong>e p85-α (subunità regolatoria della<br />
PI3K), spettr<strong>in</strong>a e la prote<strong>in</strong>a Src. Si può rilevare la stretta somiglianza delle tre strutture: un<br />
“foglio” con due catene β antiparallele (c, d e anche b, spezzata, <strong>in</strong> spettr<strong>in</strong>a e Src) ed un foglio,<br />
<strong>in</strong>feriore nell’illustrazione, contenente tre catene β antiparallele (e, a, b).<br />
Anche per i dom<strong>in</strong>i SH3 (come per gli SH2) si riscontra la contiguità del C-term<strong>in</strong>ale e dell’Nterm<strong>in</strong>ale,<br />
<strong>in</strong><strong>di</strong>cando che i dom<strong>in</strong>i SH3 sono moduli strutturali <strong>in</strong><strong>di</strong>pendenti, che possono<br />
virtualmente essere <strong>in</strong>seriti <strong>in</strong> qualsiasi localizzazione <strong>in</strong> una prote<strong>in</strong>a.<br />
Il dom<strong>in</strong>io SH3 si <strong>di</strong>spone con una struttura “a calice”, che lega, al centro, il dom<strong>in</strong>io ricco <strong>in</strong> prol<strong>in</strong>a<br />
ed anche nell’SH3 esiste una varianza <strong>in</strong> certe zone, il che potrebbe spiegare una specificità <strong>di</strong><br />
<strong>in</strong>terazione tra s<strong>in</strong>goli SH3 e s<strong>in</strong>goli dom<strong>in</strong>i ricchi <strong>in</strong> prol<strong>in</strong>a. Ritorneremo sulla funzione biologica <strong>di</strong><br />
tali dom<strong>in</strong>i.<br />
213
Un dom<strong>in</strong>io SH3 è formato, <strong>in</strong> me<strong>di</strong>a, da circa 60 AA.<br />
Increspatura <strong>di</strong> cellule endoteliali e PDGF<br />
È stato <strong>di</strong>mostrato il <strong>di</strong>retto co<strong>in</strong>volgimento della PI3 c<strong>in</strong>asi nel cambiamento <strong>di</strong> cellule endoteliali <strong>di</strong><br />
aorta <strong>di</strong> maiale, siglate PAE (Porc<strong>in</strong>e Aortic Endothelial). Sotto stimolo da PDGF tali cellule danno<br />
un significativo “ruffl<strong>in</strong>g” (<strong>in</strong>crespatura) ben evidenziabile al microscopio, se le cellule sono trattate<br />
con falloi<strong>di</strong>na fluorescente, che visualizza i filamenti <strong>di</strong> act<strong>in</strong>a. Infatti con PDGF si osserva nelle<br />
cellule la comparsa <strong>di</strong> ruffl<strong>in</strong>g <strong>in</strong>sieme ad una <strong>di</strong>sarticolazione dei filamenti <strong>di</strong> act<strong>in</strong>a. Cont<strong>in</strong>ua a<br />
restare enigmatico l’ipotetico ruolo del PIP3 s<strong>in</strong>tetizzato dalla PI3K, ma gli effetti dell’”arruolamento”<br />
da parte del recettore della PI3K sono ben documentati.<br />
Wennstrom & Coll. (Current Biology, 4, 385, 1994) hanno condotto una serie <strong>di</strong> importanti<br />
osservazioni, che possiamo commentare riferendoci <strong>di</strong>rettamente ai pr<strong>in</strong>cipali risultati dei loro<br />
esperimenti:<br />
Materiale estratto con anticorpo anti PDGFR ed<br />
esposte ad ATP-γ- 32 P<br />
Materiale estratto con anticorpo anti p85-α<br />
Materiale estratto con anticorpo anti p110<br />
In (a) è illustrato il tracciato <strong>di</strong> membrane <strong>di</strong> cellule PAE trattate senza (-) e con (+) PDGF, che<br />
hanno subito i seguenti trattamenti: dopo una breve <strong>in</strong>cubazione con anticorpo anti recettore per<br />
PDGF è stato estratto il recettore (con prote<strong>in</strong>e eventualmente ad esso attaccate) ed è stato<br />
esposto ad ATP-γ- 32 P, che marcava le tiros<strong>in</strong>e autofosforilate.<br />
214
Poi è stata eseguita l’elettroforesi su cellule Wild Type (WT), o<strong>pp</strong>ure WT + wortmann<strong>in</strong>a (un<br />
<strong>in</strong>ibitore specifico della PI3K, estratto dal Penicillum fumiculosum), o<strong>pp</strong>ure cellule<br />
bio<strong>in</strong>gegnerizzate, il cui recettore per il PDGF aveva l’amm<strong>in</strong>oacido fenilalan<strong>in</strong>a al posto <strong>di</strong> tiros<strong>in</strong>a<br />
nelle posizioni 740 e 751 (Y740/751F; ve<strong>di</strong> pag.202). Inoltre, nello stesso modo sono state anche<br />
trattate delle cellule WT che esprimevano transitoriamente un forte arricchimento <strong>in</strong> p85 (WT ∆<br />
p85).<br />
Si può osservare che sempre l’autofosforilazione è scatenata dalla presenza del PDGF (<strong>in</strong><br />
co<strong>in</strong>cidenza con il Peso Molecolare 200 KDa). Le cellule Y740/751F non danno, <strong>in</strong> pratica,<br />
autofosforilazione, mentre è ben evidente che, quando c’è arricchimento della p85, si ottiene<br />
anche la sua fosforilazione.Si può <strong>in</strong>oltre osservare che (<strong>in</strong> aggiunta <strong>di</strong> wortmann<strong>in</strong>a, <strong>in</strong>ibitore della<br />
PI3K), non si altera il quadro.<br />
In (b) è illustrato che si ha fosforilazione della p85 perché è stata estratta specificamente tale<br />
prote<strong>in</strong>a con antisiero <strong>di</strong>retto contro <strong>di</strong> essa.<br />
In (c) è illustrato che, con antisiero anti p110, si vede anche la subunità 110, che è la subunità<br />
catalitica della PI3K.<br />
Particolarmente <strong>in</strong>teressanti sono i risultati <strong>in</strong> (b) e (c), dove le Wild Type danno la fosforilazione<br />
della p110 e p85. Ma le cellule Y740/751F non fosforilano nessuna delle due. Qu<strong>in</strong><strong>di</strong> è sufficiente<br />
non avere le due tiros<strong>in</strong>e autofosforilate che specificamente “arruolano” la p85 della PI3K (ve<strong>di</strong><br />
pag.202), che viene meno l’adesione della PI3K e la conseguente sua fosforilazione.<strong>in</strong> questo<br />
caso la fosforilazione probabilmente non ha effetti specifici a<strong>pp</strong>arenti sull’attività della PI3K: è una<br />
conseguenza dell’associazione al recettore.<br />
Nell’istogramma riportato a lato, sono<br />
illustrati i risultati ottenuti (espressi come<br />
PIP3 prodotto) con le stesse cellule già<br />
utilizzate per le prove analizzate <strong>in</strong><br />
elettroforesi. Nelle cellule Wild Type (WT) è<br />
evidente il forte aumento <strong>di</strong> PIP3 prodotto,<br />
e la sua produzione è completamente<br />
bloccata dalla wortmann<strong>in</strong>a.<br />
Si può <strong>in</strong>oltre constatare che, nelle cellule<br />
Y740/751F, la produzione <strong>di</strong> PIP3 è già a<br />
buoni livelli e non risente dello stimolo da<br />
PDGF, anche se resta a livelli più bassi<br />
delle cellule Wild Type. Qu<strong>in</strong><strong>di</strong> p85 e p110<br />
sono arruolate e fosforilate (ve<strong>di</strong> (b) e (c),<br />
pag.214) e questi processi non sono <strong>in</strong>ibiti<br />
da wortmann<strong>in</strong>a, che <strong>in</strong>ibisce, <strong>in</strong>vece, la<br />
produzione <strong>di</strong> PIP3.<br />
215
Con questa premessa, da alcuni autori, è stata ipotizzata una via complementare <strong>di</strong> stimolazione<br />
della PI3K, anche se quella legata alla traslocazione sul recettore autofosforilata sembra la<br />
predom<strong>in</strong>ante. Il seguente schema è tratto da Kodkai & coll. (Current Biology, 4, 798, 1994):<br />
Il recettore per il fattore <strong>di</strong> crescita ha tiros<strong>in</strong>e autofosforilata che legano specificamente il dom<strong>in</strong>io<br />
SH2 della prote<strong>in</strong>a “adattatrice” Grb-2, che, a sua volta, lega con due dom<strong>in</strong>i SH3 altrettanti dom<strong>in</strong>i<br />
ricchi <strong>in</strong> prol<strong>in</strong>a <strong>di</strong> un’altra prote<strong>in</strong>a adattatrice Sos che, come è stato ampiamente documentato,<br />
<strong>in</strong>crementa l’<strong>in</strong>corporazione <strong>di</strong> GTP dalla p21-Ras (una prote<strong>in</strong>a G-monomerica), venendo da<br />
questa attivata. La Ras “attivata” attiva, a sua volta, la subunità catalitica (p110) della PI3 c<strong>in</strong>asi.<br />
Questa capacità da parte della p21-Ras <strong>di</strong> attivare <strong>di</strong>rettamente la PI3K è stata <strong>di</strong>mostrata<br />
recentemente. Anche la prote<strong>in</strong>a Rac sembrerebbe co<strong>in</strong>volta <strong>in</strong> tale processo (Rac e Rho sono<br />
due prote<strong>in</strong>e simili alla Ras, implicate nella riorganizzazione del citoscheletro).<br />
In tale schema è riportata, nella parte destra, anche la via <strong>di</strong> attivazione della MAP-c<strong>in</strong>asi (ve<strong>di</strong><br />
pag.151).<br />
Qu<strong>in</strong><strong>di</strong> da uno stesso recettore esistono due vie <strong>in</strong><strong>di</strong>pendenti e convergenti sulla PI3K (riportate<br />
ambedue nella parte s<strong>in</strong>istra della figura).<br />
Che esista un collegamento tra la PI3 c<strong>in</strong>asi e la Rac è anche su<strong>pp</strong>ortato dalla ricerca <strong>di</strong> omologie<br />
<strong>di</strong> sequenze alla banca dati: <strong>in</strong>fatti la p85 contiene un dom<strong>in</strong>io simile a quello delle “prote<strong>in</strong>e<br />
attivanti l’attività GTP-asica” <strong>di</strong> Rac e Rho. Come esiste la prote<strong>in</strong>a GAP (prote<strong>in</strong>a attivante<br />
l’attività GTP-asica della Ras), così esistono specifiche prote<strong>in</strong>e attivanti l’attività GTP-asica <strong>di</strong> altre<br />
prote<strong>in</strong>e-G a<strong>pp</strong>artenenti alla famiglia Ras (come le Rac e le Rho). È utile ricordare che la GAP, <strong>di</strong><br />
fatto, <strong>in</strong>attiva la Ras, perché <strong>in</strong>crementa la velocità d’idrolisi del GTP legato, e, come è noto, se la<br />
Ras lega GTP è attiva, mentre è <strong>in</strong>attiva quando lega GDP.<br />
Rho (Ras Homology) e Rac a<strong>pp</strong>artengono alla subfamiglia Rho. Rho e Rac sono me<strong>di</strong>atori delle<br />
funzioni delle <strong>in</strong>tegr<strong>in</strong>e.<br />
216
In questa pag<strong>in</strong>a sono riportate le sequenze del lato N-term<strong>in</strong>ale <strong>di</strong> 11 prote<strong>in</strong>e che presentano<br />
una <strong>di</strong>screta omologia <strong>di</strong> sequenza. La qu<strong>in</strong>ta prote<strong>in</strong>a è la RACGAP, cioè la prote<strong>in</strong>a attivante<br />
l’attività GTP-asica della Rac; la P190 è una Rho-GAP; la 3BP1 è una prote<strong>in</strong>a che lega i dom<strong>in</strong>i<br />
SH3 dell’oncoprote<strong>in</strong>a c-Abl.<br />
La seconda prote<strong>in</strong>a (INP5P) è l’importante <strong>in</strong>ositol-polifosfato 5-<strong>fosfatasi</strong>; tale enzima rimuove con<br />
meccanismo idrolitico il fosfato dalla posizione 5 <strong>di</strong> un <strong>in</strong>ositolo polifosforilato (si presti attenzione<br />
al fatto che il substrato è un <strong>in</strong>ositolo polifosforilato e non un fosfolipide fosforilato dell’<strong>in</strong>ositolo).<br />
Tale enzima catalizza la ta<strong>pp</strong>a 2 <strong>di</strong> pag.200, che porta alla formazione dell’<strong>in</strong>ositolo 1, 3, 4<br />
trisfosfato <strong>di</strong>verso dal “classico” <strong>in</strong>ositolo 1, 4, 5 trisfosfato, che, comunque, è pure esso<br />
defosforilati <strong>in</strong> posizione 5 per dare l’<strong>in</strong>ositolo 1, 4 bis-fosfato (ve<strong>di</strong> prima ta<strong>pp</strong>a <strong>di</strong> pag.197 <strong>in</strong><br />
basso). È un enzima che comunque rimuove <strong>in</strong>ositi<strong>di</strong> polifosfati con funzione specifica(l’IP3<br />
“classico” e il tetra-kis-fosfato, che presentano funzioni più conosciute <strong>di</strong> altri derivati dell’<strong>in</strong>ositolo):<br />
è qu<strong>in</strong><strong>di</strong> un enzima che rimuove un messaggio.<br />
Per l’uomo è stata descritta la S<strong>in</strong>drome Oculo Cerebro Renale <strong>di</strong> Lowe (OCRL, ve<strong>di</strong> prima riga<br />
della figura), che è una malattia ere<strong>di</strong>taria legata alla mutazione <strong>di</strong> un gene che co<strong>di</strong>fica una<br />
prote<strong>in</strong>a che ha una stretta omologia con la <strong>in</strong>ositolpolifosfato-5-<strong>fosfatasi</strong> (INS5P, seconda riga<br />
della figura). L’OCRL ha profon<strong>di</strong> effetti sul cristall<strong>in</strong>o, sul cervello e sul rene, e si ritiene pertanto<br />
che la prote<strong>in</strong>a co<strong>di</strong>ficata dal gene mutato sia particolarmente importante <strong>in</strong> tali organi. L’omologia<br />
<strong>di</strong> sequenza con la INP5P porta a ipotizzare a ragion veduta che proprio tale enzima, implicato nel<br />
turnover dei fosfo<strong>in</strong>ositi<strong>di</strong>, sia alterato nella OCRL.<br />
In particolare, le omologie tra tutte le prote<strong>in</strong>e della figura sono tra l’AA-50 e l’AA-147. Non è nota<br />
la specifica funzione <strong>di</strong> tale dom<strong>in</strong>io.<br />
In conclusione, le omologie <strong>di</strong> sequenze rilevate tra INP5P (idrolisi <strong>di</strong> <strong>in</strong>ositol-polifosfati), p85<br />
(subunità regolatoria della PI3K) e prote<strong>in</strong>e del tipo GAP sono un’importante <strong>in</strong><strong>di</strong>cazione che<br />
prote<strong>in</strong>e legate <strong>di</strong>rettamente o <strong>in</strong><strong>di</strong>rettamente al ciclo dei fosfo<strong>in</strong>ositi<strong>di</strong> sono tra esse<br />
strutturalmente collegate e qu<strong>in</strong><strong>di</strong>, <strong>in</strong> qualche modo, una è derivata dall’altra nel corso<br />
dell’evoluzione.<br />
D’altra parte viene r<strong>in</strong>forzata l’ipotesi che la Ras, o altre prote<strong>in</strong>e <strong>di</strong> tale famiglia, possano<br />
<strong>in</strong>teragire con la PI3K (ve<strong>di</strong> schema <strong>di</strong> pag.216).<br />
217
218