Sommario delle reazioni degli acidi carbossilici - PianetaChimica.it
Sommario delle reazioni degli acidi carbossilici - PianetaChimica.it
Sommario delle reazioni degli acidi carbossilici - PianetaChimica.it
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
www.pianetachimica.<strong>it</strong><br />
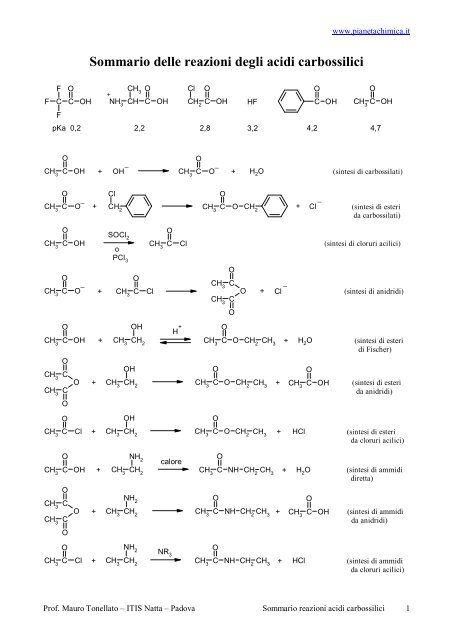
<strong>Sommario</strong> <strong>delle</strong> <strong>reazioni</strong> <strong>degli</strong> <strong>acidi</strong> <strong>carbossilici</strong><br />
F O<br />
F C C OH<br />
F<br />
CH 3<br />
O Cl O<br />
NH 3<br />
CH C OH CH 2<br />
C OH<br />
+<br />
O<br />
O<br />
HF<br />
C OH CH 3<br />
C OH<br />
pKa 0,2 2,2 2,8 3,2 4,2 4,7<br />
O<br />
CH 3<br />
C OH<br />
+<br />
O<br />
−<br />
OH CH 3<br />
C<br />
−<br />
O +<br />
H 2 O<br />
(sintesi di carbossilati)<br />
CH 3<br />
O<br />
C<br />
Cl<br />
O<br />
−<br />
O + CH 2<br />
CH 3<br />
C O CH 2<br />
+<br />
− Cl (sintesi di esteri<br />
da carbossilati)<br />
O<br />
CH 3<br />
C OH<br />
O<br />
CH 3<br />
C<br />
CH 3<br />
CH 3<br />
CH 3<br />
CH 3<br />
O<br />
−<br />
O<br />
C OH<br />
O<br />
C<br />
C<br />
O<br />
O<br />
C<br />
O<br />
SOCl 2<br />
o<br />
CH 3<br />
O<br />
C Cl<br />
(sintesi di cloruri acilici)<br />
PCl 3<br />
O<br />
+<br />
O<br />
CH 3<br />
C<br />
CH 3<br />
C Cl<br />
CH 3<br />
C<br />
O + Cl −<br />
(sintesi di anidridi)<br />
O<br />
OH<br />
H +<br />
O<br />
+ CH 3<br />
CH 2<br />
CH 3<br />
C O CH 2<br />
CH 3<br />
+ H 2<br />
O<br />
(sintesi di esteri<br />
di Fischer)<br />
OH<br />
O<br />
+ CH 3<br />
CH 2<br />
CH 3<br />
C O CH 2<br />
CH 3<br />
+ CH 3<br />
C OH (sintesi di esteri<br />
da anidridi)<br />
OH<br />
O<br />
Cl + CH 3<br />
CH 2<br />
CH 3<br />
C O CH 2<br />
CH 3<br />
+ HCl<br />
(sintesi di esteri<br />
da cloruri acilici)<br />
O<br />
CH 3<br />
CH 3<br />
CH 3<br />
O<br />
C OH<br />
O<br />
C<br />
O<br />
C<br />
O<br />
NH 2<br />
O<br />
calore<br />
+ CH 3<br />
CH 2<br />
CH 3<br />
C NH CH 2<br />
CH 3<br />
+ H 2<br />
O (sintesi di ammidi<br />
diretta)<br />
NH 2<br />
O<br />
O<br />
+ CH 3<br />
CH 2<br />
CH 3<br />
C NH CH 2<br />
CH 3<br />
+ CH 3<br />
C OH (sintesi di ammidi<br />
da anidridi)<br />
O<br />
CH 3<br />
C<br />
NH 2 NR 3<br />
O<br />
Cl + CH 3<br />
CH 2<br />
CH 3<br />
C NH CH 2<br />
CH 3<br />
+ HCl<br />
(sintesi di ammidi<br />
da cloruri acilici)<br />
Prof. Mauro Tonellato – ITIS Natta – Padova <strong>Sommario</strong> <strong>reazioni</strong> <strong>acidi</strong> <strong>carbossilici</strong> 1
www.pianetachimica.<strong>it</strong><br />
O<br />
CH 3<br />
C NH<br />
O<br />
NH<br />
H2 O / OH −<br />
2<br />
CH 2<br />
CH 3<br />
CH 3<br />
C OH + CH 3<br />
CH<br />
o<br />
2<br />
(idrolisi dei derivati)<br />
H 2<br />
O / H +<br />
O<br />
LiAlH 4<br />
OH<br />
OH<br />
CH 3<br />
CH 2<br />
C O CH 2<br />
CH 3<br />
(e poi H 2<br />
O)<br />
CH 3<br />
CH 2<br />
CH 2<br />
+ CH 3<br />
CH 2<br />
O<br />
LiAlH 4<br />
OH<br />
CH 3<br />
CH 2<br />
C Cl<br />
(e poi H 2<br />
O)<br />
CH 3<br />
CH 2<br />
CH 2<br />
(riduzione <strong>degli</strong> esteri)<br />
(riduzione dei cloruri)<br />
O<br />
O<br />
LiAl(tBuO) 3 H<br />
CH 3<br />
CH 2<br />
C Cl<br />
CH 3<br />
CH 2<br />
C<br />
-78 °C<br />
H<br />
(oppure H 2<br />
e Pd/BaSO 4<br />
)<br />
(riduzione dei cloruri<br />
ad aldeidi)<br />
LiAlH 4<br />
NH 2<br />
CH 3<br />
CH 2<br />
C N<br />
(e poi H 2<br />
O)<br />
CH 3<br />
CH 2<br />
CH 2<br />
(riduzione dei n<strong>it</strong>rili)<br />
O<br />
CH 3<br />
CH 2<br />
C NH<br />
LiAlH 4<br />
CH 3<br />
(e poi H 2<br />
O)<br />
CH 3<br />
CH 2<br />
CH 2<br />
NH CH 3<br />
(riduzione <strong>delle</strong> ammidi)<br />
O<br />
OH<br />
CH 3<br />
MgBr<br />
CH 3<br />
CH 2<br />
C O CH 2<br />
CH 3<br />
CH 3<br />
CH 2<br />
C CH 3<br />
(e poi H 2<br />
O)<br />
CH 3<br />
O<br />
O<br />
CH 3<br />
MgBr<br />
CH 3<br />
CH 2<br />
C N CH 3<br />
CH 3<br />
CH 2<br />
C CH 3<br />
(e poi H<br />
CH 2<br />
O)<br />
3<br />
(esteri coi reattivi di Grignard)<br />
(ammidi N,N disost<strong>it</strong>u<strong>it</strong>e<br />
con reattivi di Grignard)<br />
O<br />
CH 3<br />
CH 2<br />
C OH<br />
CH 3<br />
Li<br />
(e poi H 2<br />
O)<br />
O<br />
CH 3<br />
CH 2<br />
C CH 3<br />
(<strong>acidi</strong> con reattivi l<strong>it</strong>io-organici)<br />
O<br />
O<br />
AlCl 3<br />
CH 3<br />
CH 2<br />
C Cl + CH 3<br />
CH 2<br />
C<br />
+ HCl<br />
(acilazione di Friedel Crafts)<br />
O<br />
CH 3<br />
C CH 2<br />
O<br />
C OH<br />
100 °C<br />
O<br />
CH 3<br />
C CH 3<br />
+ CO 2<br />
(decarbossilazione dei β cheto<strong>acidi</strong>)<br />
O<br />
CH 3<br />
CH 2<br />
CH 2<br />
C OH<br />
Cl 2<br />
P (tracce)<br />
Cl<br />
CH 3<br />
CH 2<br />
CH<br />
O<br />
C OH<br />
(α alogenaziome di<br />
Hell, Wohlhard, Zelinsky)<br />
O<br />
Cl<br />
O<br />
CH 2<br />
C OH<br />
O<br />
+ CN − H 2<br />
O<br />
CH 2<br />
C OH<br />
OH −<br />
C N<br />
C<br />
CH 2<br />
C<br />
O<br />
OH<br />
OH<br />
(sintesi di acido malonico)<br />
Prof. Mauro Tonellato – ITIS Natta – Padova <strong>Sommario</strong> <strong>reazioni</strong> <strong>acidi</strong> <strong>carbossilici</strong> 2
www.pianetachimica.<strong>it</strong><br />
O<br />
C<br />
CH 2<br />
C<br />
O<br />
OEt<br />
OEt<br />
−<br />
EtO<br />
EtOH<br />
O<br />
C<br />
: CH<br />
C<br />
O<br />
OEt<br />
OEt<br />
R<br />
Cl<br />
R<br />
O<br />
C<br />
CH<br />
C<br />
O<br />
OEt<br />
OEt<br />
O<br />
H 2 O / H + R CH 2<br />
C OH + CO 2<br />
(sintesi malonica)<br />
2<br />
CH 3<br />
O<br />
C<br />
− O<br />
EtO<br />
OEt CH 3<br />
C<br />
EtOH<br />
CH 2<br />
O<br />
C<br />
OEt<br />
+ EtOH (condensazione di Claisen)<br />
O<br />
C<br />
CH 2<br />
C<br />
O<br />
OEt<br />
CH 3<br />
−<br />
EtO<br />
EtOH<br />
O<br />
C<br />
: CH<br />
C<br />
O<br />
OEt<br />
CH 3<br />
R Cl<br />
R<br />
O<br />
C<br />
CH<br />
C<br />
O<br />
OEt<br />
O<br />
H 2 O / H + R CH 2<br />
C CH 3<br />
+ CO 2<br />
CH 3<br />
(sintesi acetacetica)<br />
MgBr<br />
CH 3<br />
CH 2<br />
+ CO 2<br />
etere<br />
(e poi H 2<br />
O)<br />
O<br />
CH 3<br />
CH 2<br />
C OH<br />
(carbonatazione)<br />
COOH<br />
−<br />
O + CO2<br />
(e poi H 2<br />
O)<br />
OH<br />
(sintesi di Kolbe dell'acido salicilico)<br />
OH<br />
CH 3<br />
CH 2<br />
O<br />
−<br />
H<br />
C O + 2 SO 4<br />
+ CH 3<br />
CH 2<br />
C OH<br />
(carbonilazione)<br />
(e poi H 2<br />
O)<br />
CH 3<br />
O<br />
C<br />
OH<br />
H + HCN<br />
CH 3<br />
CH<br />
OH<br />
H 2<br />
O / H +<br />
C N CH 3<br />
CH<br />
O<br />
C<br />
OH<br />
(sintesi di α idrossi<strong>acidi</strong>)<br />
CH 3<br />
O<br />
C<br />
NH 2<br />
NH 2<br />
O<br />
NH H 2<br />
O / H +<br />
3<br />
H + HCN<br />
CH 3<br />
CH C N CH 3<br />
CH C OH<br />
(sintesi di α ammino<strong>acidi</strong>)<br />
CH 3<br />
O<br />
C<br />
O<br />
Cl + HCN<br />
CH 3<br />
C<br />
O<br />
H 2<br />
O / H +<br />
C N CH 3<br />
C<br />
O<br />
C<br />
OH<br />
(sintesi di α cheto<strong>acidi</strong>)<br />
Prof. Mauro Tonellato – ITIS Natta – Padova <strong>Sommario</strong> <strong>reazioni</strong> <strong>acidi</strong> <strong>carbossilici</strong> 3