You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
ISOMERIA<br />
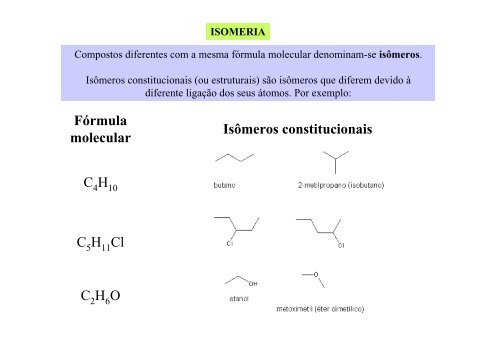
Compostos diferentes com a mesma fórmula molecular denominam-se isômeros.<br />
Isômeros constitucionais (ou estruturais) são isômeros que diferem devido à<br />
diferente ligação dos seus átomos. Por exemplo:<br />
Fórmula<br />
molecular<br />
C 4 H 10<br />
C 5 H 11 Cl<br />
C 2 H 6 O<br />
Isômeros constitucionais
ISOMERIA<br />
Os isômeros constitucionais podem ser subdivididos em:<br />
a) Isomeria de Função;<br />
b) Isomeria de Cadeia;<br />
c) Isomeria de posição;<br />
d) Isomeria de Compensação ou Metameria;<br />
e) Isomeria Dinâmica ou Tautomeria.<br />
-Nem todos os grupos estão unidos ao mesmo centro<br />
-São moléculas muito diferentes tanto em suas propriedades físicas como<br />
químicas.
a) Isomeria de Função<br />
A diferença entre os<br />
isômeros está no<br />
grupo funcional.<br />
ISOMERIA
ISOMERIA<br />
b) Isomeria de Cadeia<br />
A diferença entre os<br />
isômeros está no tipo<br />
de cadeia carbônica.
ISOMERIA<br />
c) Isomeria de<br />
Posição<br />
A diferença entre os<br />
isômeros está na<br />
posição de um grupo<br />
funcional, de<br />
uma insaturação ou<br />
de um substituinte.
ISOMERIA<br />
d) Isomeria de<br />
Compensação ou<br />
Metameria<br />
A diferença entre os<br />
isômeros está apenas<br />
na posição de um<br />
heteroátomo.
ISOMERIA e) Tautomeria<br />
Este tipo de isomeria ocorre quando dois compostos de mesma<br />
fórmula molecular e grupos funcionais diferentes coexistem em<br />
equilíbrio dinâmico no qual um deles está continuamente se<br />
transformando no outro e vice-versa.<br />
A tautomeria ocorre somente na fase líquida, em compostos cuja molécula possui um<br />
elemento muito eletronegativo, como o oxigênio ou nitrogênio, ligado ao mesmo<br />
tempo ao hidrogênio e a um carbono insaturado (que possui ligação π).
ESTEREOQUÍMICA<br />
QUÍMICA NOVA, 20(6) (1997) OS FÁRMACOS E A QUIRALIDADE: UMA BREVE ABORDAGEM
TALIDOMIDA<br />
ESTEREOQUÍMICA
E COM OS ALIMENTOS ?<br />
DOCE<br />
ESTEREOQUÍMICA<br />
AMARGO
ESTEREOQUÍMICA<br />
MOLÉCULA AQUIRAL<br />
É aquela que é superponível com sua imagem no espelho<br />
Têm elementos de simetria
ESTEREOQUÍMICA<br />
MOLÉCULA QUIRAL<br />
É aquela que não é superponível com sua imagem no espelho
ESTEREOQUÍMICA<br />
Estuda as estruturas moleculares em três dimensões;<br />
Estereoisômeros<br />
Enantiômeros (enantion, grego oposto)<br />
Diastereoisômeros<br />
São produtos<br />
diferentes?
ESTEREOQUÍMICA<br />
ISÔMEROS<br />
CONSTITUCIONAL ESTEREOISÔMEROS<br />
Imagem da molécula em um espelho<br />
plano não é sobreponível a ela<br />
mesmo<br />
Todo enantiômero deve possuir um<br />
centro quiral<br />
Espelho<br />
ENANTIÔMEROS DIASTEREOISÔMEROS<br />
Imagem da molécula, em um<br />
espelho plano é sobreponível a ela<br />
mesmo
CENTRO QUIRAL<br />
ESTEREOQUÍMICA<br />
Carbono com quatro grupos diferentes ligados a ele<br />
Carbono QUIRAL Também chamado de centro quiral;<br />
Características deste carbono:<br />
Assimétrico;<br />
Geometria tetraédrica;<br />
Hibridação sp 3 ;
ESTEREOQUÍMICA<br />
COMO IDENTIFICAR UMA MOLÉCULA QUIRAL<br />
1. Ao avaliar a sobreposição não devemos “romper ou formar” ligações;<br />
2. Para ser uma molécula quiral basta uma única região do molécula não coincidir com a<br />
outra imagem;<br />
Espelho<br />
III e IV Não são superponíveis ENANTIÔMEROS
ESTEREOQUÍMICA<br />
COMO IDENTIFICAR UMA MOLÉCULA QUIRAL<br />
3. Moléculas quirais não possuem plano de simetria;<br />
Plano de simetria<br />
Esta molécula é AQUIRAL Possui plano de simetria<br />
Esta molécula também possui plano de simetria AQUIRAL
2-cloropropano<br />
ESTEREOQUÍMICA<br />
COMO IDENTIFICAR UMA MOLÉCULA QUIRAL<br />
2-clorobutano
CENTRO QUIRAL<br />
ESTEREOQUÍMICA<br />
Outros átomos que também podem fazem quatro ligações pode ser um centro quiral;<br />
1. Devido a geometria tetraédrica o centro quiral do carbono pode existir em ambos os<br />
arranjos tridimensionais que não são imagens superponíveis;<br />
Estereoisômeros as<br />
imagens não são<br />
superponíveis<br />
2-butanol
Propriedades de moléculas quirais<br />
ESTEREOQUÍMICA<br />
• Os ENANTIÔMEROS possuem as mesmas propriedades FÍSICAS (P.F; P.E; Espectro<br />
IV; UV; RMN se medidos em solventes aquirais) EXCETO O SENTIDO DE<br />
ROTAÇÃO DO PLANO DE POLARIZAÇÃO DA LUZ.<br />
• Os ENANTIÔMEROS possuem as mesmas propriedades QUÍMICAS EXCETO AS<br />
REAÇÕES COM OUTROS COMPOSTOS OPTICAMENTE ATIVOS.<br />
ATIVIDADE ÓTICA DE MOLÉCULAS QUIRAIS<br />
DEXTROROTATÓRIAS (d, +) Gira a luz polarizada para a direita<br />
LEVOROTATÓRIAS (l,-) Gira a luz polarizada para a esquerda
ESTEREOQUÍMICA<br />
COMPOSTO OPTICAMENTE ATIVO<br />
São capazes de modificar a rotação da luz polarizada;<br />
COMPOSTOS QUIRAIS SÃO OPTICAMENTE ATIVOS<br />
MISTURA RACÊMICA<br />
Mistura de partes iguais dos enantiômeros (+) e (-).<br />
IMPORTÂNCIA DA QUIRALIDADE<br />
1. A quiralidade está difundida em todo o universo;<br />
2. O corpo humano é estruturalmente QUIRAL;<br />
3. A maioria das moléculas dos seres vivos são quirais e, geralmente, somente um tipo<br />
é encontrado;<br />
4. Quase todos os aminoácidos que formam as proteínas são quirais e todos desviam a<br />
luz para a esquerda (levorotatórios);
ESTEREOQUÍMICA
ESTEREOQUÍMICA<br />
Os enantiômeros giram o plano da luz polarizada em iguais quantidades mas em direções<br />
opostas;<br />
Ou seja, enantiômeros resolvidos (separados) apresentam atividade ótica;<br />
Onda eletromagnética<br />
ATIVIDADE ÓTICA<br />
Descoberto pelo físico João-Baptista Biot – 1815;<br />
1848 Luis Pasteur princípio da <strong>estereoquímica</strong><br />
As oscilações do campo elétrico e magnético podem ocorrer em todos os possíveis<br />
planos perpendiculares a direção de propagação.
ATIVIDADE ÓTICA<br />
ESTEREOQUÍMICA<br />
Onda eletromagnética polarizada<br />
Quando um feixe de luz comum passa através de um polarizador;<br />
O polarizador interage com o campo elétrico da luz;<br />
Após a interação a luz emerge do polarizador oscilando apenas em um plano;<br />
POLARÍMETRO<br />
Equipamento capaz de polarizar a luz;<br />
A lente geralmente é constituída de CaCO 3 em determinada forma cristalina <br />
Chamado de polaróide PRISMA DE NICOL;
ATIVIDADE ÓTICA<br />
ESTEREOQUÍMICA<br />
POLARÍMETRO
ATIVIDADE ÓTICA<br />
A) Polarímetro sem amostra;<br />
ESTEREOQUÍMICA<br />
POLARÍMETRO<br />
B) Observação de uma amostra que não é opticamente ativa;<br />
C) Observação de uma amostra que é opticamente ativa;<br />
Rotação da luz polarizada;
ATIVIDADE ÓTICA<br />
Medições realizadas em graus;<br />
ESTEREOQUÍMICA<br />
MEDIÇÃO<br />
A rotação pode ocorrer para duas direções:<br />
DIREITA (SENTIDO DO RELÓGIO) Assume-se valor POSITIVO <br />
dextrorotatório (d, +)<br />
ESQUERDA (SENTIDO CONTRÁRIO DO RELÓGIO) Assume-se valor<br />
NEGATIVO Levorotatória (l, -);<br />
FATORES QUE INFLUENCIAM:<br />
Concentração da solução;<br />
Comprimento de onda utilizado na fonte de luz;<br />
Comprimento do tubo de amostra;<br />
Temperatura;<br />
Natureza do solvente.
ATIVIDADE ÓTICA<br />
D = raia D do sódio (589,6 nm);<br />
T = temperatura, 0 C;<br />
α= rotação observada, graus<br />
L = comprimento do tubo de amostra, cm<br />
C = concentração da solução, g.mL -1<br />
ESTEREOQUÍMICA<br />
ROTAÇÃO ESPECÍFICA<br />
OBS: NO SI a m = Poder rotatório ótico específico (rad m 2 kg -1 )
ATIVIDADE ÓTICA<br />
ESTEREOQUÍMICA
ESTEREOQUÍMICA<br />
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)<br />
1. Não existe correlação entre a configuração do enantiômero e a direção da rotação<br />
ótica;<br />
2. Não existe correlação entre a designação R e S e a direção de rotação ótica;<br />
R Do latin rectus (direito – a favor do relógio)<br />
S Do latin sinister (esquerdo – contra o relógio)<br />
COMO DETERMINAR A PRIORIDADE DOS GRUPOS?
ESTEREOQUÍMICA<br />
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)<br />
BASES (regras de precedência):<br />
1. Número atômico do elemento ligado ao centro quiral<br />
• Menor número atômico menor prioridade (4)<br />
• Maior número atômico maior prioridade (1)<br />
OBS: No caso de isótopos o de maior massa atômica tem maior prioridade<br />
2. Quando os átomos ligados ao centro quiral forem iguais passa-se a determinar a<br />
prioridade pelo próximo átomo;<br />
3. Deve-se posicionar o grupo de menor precedência (4) na posição contrária ao<br />
observador (atrás do plano);<br />
Visão da molécula com o grupo de menor prioridade apontando para fora do plano
ESTEREOQUÍMICA<br />
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)
BASES:<br />
ESTEREOQUÍMICA<br />
3. Quando houver ligações duplas ou triplas deve-se duplicar ou triplicar ambos os<br />
átomos;<br />
(S)-Alanina<br />
[(S)-(+)-2-ácido<br />
aminopropionico]<br />
[α]D = +8.5°<br />
(S)-Gliceraldeído<br />
[(S)-(–)-2,3-dihidroxipropanal], [α]D = –8.7°
ESTEREOQUÍMICA<br />
(R)-(+)-2-Metil-1-butanol (S)-(–)-2-Metil-1-butanol<br />
(R)-(–)-1-Cloro-2-metilbutano S)-(+)-1-Cloro-2-metilbutano
ESTEREOQUÍMICA<br />
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)<br />
PROJEÇÕES DE FISCHER<br />
1. As linhas verticais representam ligações que se projetam para trás do plano do papel (ou<br />
que estão no plano do papel);<br />
2. As linhas horizontais representam ligações que se projetam para fora do plano do papel;<br />
3. As intersecções das linhas horizontais e verticais representa um átomo de carbono,<br />
normalmente um carbono quiral;<br />
4. Quando usamos as projeções de Fischer para testar a superponibilidade de duas<br />
estruturas é permitido girá-las de 180 0 no plano do papel;<br />
5. Não podemos girar as estruturas de nenhum outro ângulo;<br />
6. Deve-se manter as estruturas no plano do papel;<br />
7. Não é permitido virar as estruturas Fischer
MISTURA RACÊMICA<br />
Mistura de partes iguais de enantiômeros;<br />
São opticamente inativos;<br />
Podem ser separados:<br />
ESTEREOQUÍMICA<br />
Solventes quirais; Cromatografia com coluna quiral;<br />
Reações que envolvam substâncias também quirais;<br />
Butanona<br />
Aquiral<br />
hidrogênio<br />
Aquiral (±)-2-butanol<br />
quiral
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS<br />
São estereoisômeros cujas moléculas não são imagens especulares superponíveis;<br />
São moléculas que apresentam dois ou mais centros quirais (exceto para isômeros cis,<br />
trans onde as moléculas não apresentam centros quirais);<br />
Para compostos cujos centros quirais são tetraédricos (sp 3 ) o número total de<br />
estereoisômeros não excederá 2 n , onde n é o número de centros quirais tetraédricos (regra<br />
de van’t Hoff);<br />
Os diasteroisômeros apresentam propriedades físicas diferentes (P.F; P.E; solubilidades,<br />
etc.);
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS<br />
Exemplos de diasteroisômeros sem carbono quiral<br />
DIASTEROISÔMEROS
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS<br />
Exemplos de diasteroisômeros com dois carbonos quirais<br />
DIFERENTES PROPRIEDADES FÍSICAS<br />
ENANTIÔMEROS<br />
DISTEROISÔMEROS<br />
MESMAS PROPRIEDADES FÍSICAS E QUÍMICAS<br />
ENANTIÔMEROS
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS<br />
Exemplos de diasteroisômeros com DOIS carbonos quirais<br />
Exemplos de diasteroisômeros com UM carbono quiral<br />
Diasteroisômeros
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS<br />
Treonina<br />
Enantiômeros Enantiômeros
MESOESTRUTURAS<br />
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS<br />
Estruturas com dois carbonos quirais nem sempre possuem 4 estereoisômeros;<br />
Ocorre com moléculas que mesmo contendo centros quirais elas são aquirais.
MESOESTRUTURAS<br />
ESTEREOQUÍMICA<br />
DIASTEREOISÔMEROS
CLASSIFICAÇÃO DAS RELAÇÕES ENTRE MOLÉCULAS<br />
São superponíveis?<br />
SIM<br />
São a mesma<br />
molécula<br />
NÃO<br />
Tem a mesma fórmula molecular?<br />
OU<br />
São iguais em seus pesos moleculares e<br />
suas composições elementares?<br />
SIM NÃO Não são isômeros<br />
São isômeros<br />
É um deles superponível<br />
com a imagem no espelho do outro?<br />
SIM<br />
São enântiômeros<br />
São quirais<br />
NÃO<br />
São diasteroisômeros<br />
Diferem unicamente pelo<br />
arranjo de seus átomos no espaço? NÃO<br />
SIM<br />
São estereoisômeros<br />
NÃO<br />
São estereoisômeros<br />
conformacionais<br />
São isômeros<br />
estruturais<br />
São intercambiáveis a<br />
temperatura ambiente?<br />
SIM<br />
São estereoisômeros<br />
figuracionais<br />
NÃO São superponíveis com suas<br />
SIM São aquirais<br />
respectivas imagens no espelho?