Processos termicos.pdf - Unidade Acadêmica de Física - UFCG
Processos termicos.pdf - Unidade Acadêmica de Física - UFCG
Processos termicos.pdf - Unidade Acadêmica de Física - UFCG
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
<strong>Física</strong> II – Profs Ricardo e Amauri 4<br />
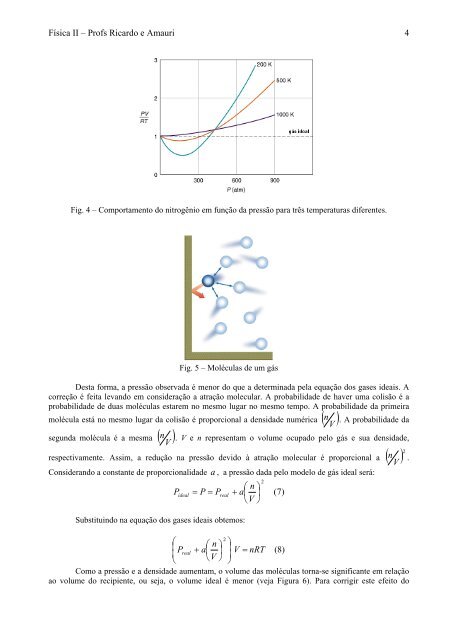
Fig. 4 – Comportamento do nitrogênio em função da pressão para três temperaturas diferentes.<br />
Fig. 5 – Moléculas <strong>de</strong> um gás<br />
Desta forma, a pressão observada é menor do que a <strong>de</strong>terminada pela equação dos gases i<strong>de</strong>ais. A<br />
correção é feita levando em consi<strong>de</strong>ração a atração molecular. A probabilida<strong>de</strong> <strong>de</strong> haver uma colisão é a<br />
probabilida<strong>de</strong> <strong>de</strong> duas moléculas estarem no mesmo lugar no mesmo tempo. A probabilida<strong>de</strong> da primeira<br />
molécula está no mesmo lugar da colisão é proporcional a <strong>de</strong>nsida<strong>de</strong> numérica ( )<br />
n . A probabilida<strong>de</strong> da<br />
V<br />
n . V e n representam o volume ocupado pelo gás e sua <strong>de</strong>nsida<strong>de</strong>,<br />
segunda molécula é a mesma ( ) V<br />
respectivamente. Assim, a redução na pressão <strong>de</strong>vido à atração molecular é proporcional a ( ) 2<br />
Consi<strong>de</strong>rando a constante <strong>de</strong> proporcionalida<strong>de</strong> a , a pressão dada pelo mo<strong>de</strong>lo <strong>de</strong> gás i<strong>de</strong>al será:<br />
⎛ n ⎞<br />
Pi<strong>de</strong>al = P = Preal<br />
+ a⎜<br />
⎟<br />
⎝V<br />
⎠<br />
Substituindo na equação dos gases i<strong>de</strong>ais obtemos:<br />
2<br />
( 7)<br />
n .<br />
V<br />
2<br />
⎛ n ⎞<br />
⎜ ⎛ ⎞<br />
Preal + a ⎟ V = nRT ( 8)<br />
⎜<br />
⎜ ⎟<br />
V ⎟<br />
⎝ ⎝ ⎠ ⎠<br />
Como a pressão e a <strong>de</strong>nsida<strong>de</strong> aumentam, o volume das moléculas torna-se significante em relação<br />
ao volume do recipiente, ou seja, o volume i<strong>de</strong>al é menor (veja Figura 6). Para corrigir este efeito do