Protocol clinic naÅ£ional: âAdenomul de prostatÄâ - Ministerul SÄnÄtÄÅ£ii
Protocol clinic naÅ£ional: âAdenomul de prostatÄâ - Ministerul SÄnÄtÄÅ£ii
Protocol clinic naÅ£ional: âAdenomul de prostatÄâ - Ministerul SÄnÄtÄÅ£ii
- No tags were found...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009D. RESURSELE UMANE ŞI MATERIALELE NECESARE PENTRU RESPECTAREAPREVEDERILOR DIN PROTOCOL.......................................................................................................................30D.1. Instituţiile <strong>de</strong> asistenţă medicală primară..........................................................................................................30D.2. Serviciul <strong>de</strong> asistenţă medicală urgentă şa etapa prespitalicească....................................................................30D.3. Instituţiile secţiile <strong>de</strong> asistenţă medicală specializată <strong>de</strong> ambulatoriu..............................................................30D.4. Instituţiile <strong>de</strong> asistenţă medicală spitalicească: secţii specializate (urologie) sau <strong>de</strong> profil general.................31E. INDICATORII DE MONITORIZARE A IMPLEMENTĂRII PROTOCOLULUI........................................34ANEXE.........................................................................................................................................................................35Anexa 1. Ghidul pacientului cu AP..........................................................................................................................35Anexa 2. Formular pentru obţinerea <strong>de</strong> acord al pacientului....................................................................................37Anexa 3. Fişa <strong>de</strong> monitorizare a pacienţilor – formular <strong>de</strong> înregistrare a acţiunilor ulterioare referitoarela pacienţi, efectuate în baza protocolului................................................................................................39Anexa 4. Sala <strong>de</strong> operaţii şi instrumentele chirurgicale............................................................................................40Anexa 5. Scorurile <strong>de</strong> aprecierea a severităţii în a<strong>de</strong>nomul <strong>de</strong> prostată...................................................................41BIBLIOGRAFIE.........................................................................................................................................................424
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009ABREVIERILE FOLOSITE ÎN DOCUMENTAMT asociaţie medicală teritorialăAP a<strong>de</strong>nom <strong>de</strong> prostatăAgHBs antigen superficial (s) al virusului hepatitic Banti-HBc anticorpi către antigenul HBc (IgM+IgG sau „total”)anti-VHC anticorpi către spectrul <strong>de</strong> proteine ale virusului hepatic CBCR boală cronică <strong>de</strong> rinichiDZ diabet zaharatFCC frecvenţă a contracţiilor cardiaceFG filtraţie glomerularăNPP nume, prenume, patronimicHTA hipertensiune arterialăIPSS Scorul internaţional al simptomelor provocate <strong>de</strong> a<strong>de</strong>nomul <strong>de</strong> prostată(International prostate symptom score)IRA insuficienţă renală acutăIRC insuficienţă renală cronicăIRM imagistică prin rezonanţă magneticăITU infecţie a tractului urinari.m. intramusculari.v. intravenosi.r. intrarectalLUTS simptome din partea tractului urinar inferior (lower urinary tract symptoms)MS <strong>Ministerul</strong> SănătăţiiQoL calitate <strong>de</strong> viaţăPSA antigenul specific <strong>de</strong> prostată (prostate specific antigen)RM Republica MoldovaSATI secţie <strong>de</strong> anesteziologie şi terapie intensivăSIRS Sindromul <strong>de</strong> răspuns inflamator sistemic (systemic inflammatory responsesyndrome), actualmente este preferat faţă <strong>de</strong> termenul „sepsis”.s.c. subcutanatTA tensiune arterialăTC tomografie computerizatăTUIP rezecţie transuretrală (endoscopică) a a<strong>de</strong>nomului <strong>de</strong> prostatăTURP incizie transuretrală (endoscopică) a prostateiUR urină rezidualăUSG ultrasonografieUSMF Universitatea <strong>de</strong> Stat <strong>de</strong> Medicină şi FarmacieVSC volum al sîngelui circulant5
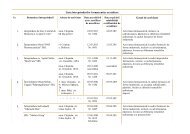
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009A.4. Scopurile protocolului• Depistarea activă a pacienţilor cu LUTS la niveluri <strong>de</strong> asistenţă medicală primară şi <strong>de</strong>ambulatoriu specializată.• Ameliorarea diagnosticării AP.• Micşorarea ratei <strong>de</strong> complicaţii acute la pacienţii cu AP.• Sporirea eficienţei tratamentului în AP.• Sporirea <strong>de</strong> calitate în supravegherea pacienţilor cu AP.A.5. Data elaborării protocolului: mai 2009A.6. Data următoarei revizuiri: mai 2011A.7. Lista şi informaţiile <strong>de</strong> contact ale autorilor şi ale persoanelor care auparticipat la elaborarea protocoluluiNumeleDr. Adrian Tănase,doctor habilitat în medicină,profesor universitarDr. Vitalie Ghicavîi,doctor în medicină, conferenţiaruniversitarDr. Petru Cepoida,doctor în medicinăDr. Elena Maximenco, MPHFuncţia <strong>de</strong>ţinutăşef catedră Urologie şi Nefrologie Chirurgicală a USMF„Nicolae Testemiţanu”; specialist principal în urologie,hemodializă şi transplant renal al MS RMconferenţiar universitar, catedra Urologie şi NefrologieChirurgicală a USMF „Nicolae Testemiţanu”nefrolog, Centrul <strong>de</strong> Dializă şi Transplant Renal, SpitalulClinic Republicanexpert local în sănătate publică, Programul Preliminar <strong>de</strong>Ţară al „Fondului Provocările Mileniului” pentru BunaGuvernare7
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009B. PARTEA GENERALĂDescriere(măsuri)B.1. Nivel <strong>de</strong> asistenţă medicală primarăMotive(repere)Paşi(modalităţi şi condiţii <strong>de</strong> realizare)I II III1. Profilaxia secundarăC.2.2, C.2.3Ameliorarea manifestărilor <strong>clinic</strong>e ale AP. Prevenirea<strong>de</strong>zvoltării complicaţiilor în AP.• Recomandarea consultaţiei la urologului (algoritmulC.1.1).2. Screening-ulC.2.4, algoritmul C.1.13. Spitalizarea pacientuluiC.2.5.5I<strong>de</strong>ntificarea AP în grupurile <strong>de</strong> risc cu simptome LUTS(IPSS > 7).• Efectuarea screening-ului în grupurile <strong>de</strong> risc cusimptomatologia LUTS, prepon<strong>de</strong>rent la vîrsta > 45<strong>de</strong> ani, prin aplicarea chestionarului IPSS (IPSS>7),inclusiv şi prin forma <strong>de</strong> autotestare (anexa 5; caseta9) şi îndreptarea la urolog.Asigurarea la timp a spitalizării, la necesitate. • Criteriile <strong>de</strong> spitalizare <strong>de</strong> urgenţă (tabelul 3).Descriere(măsuri)B.2. Nivel <strong>de</strong> asistenţă medicală urgentă la etapa prespitalicească (echipe AMU generale)Motive(repere)Paşi(modalităţi şi condiţii <strong>de</strong> realizare)I II III1. DiagnosticulC.2.52. TratamentulC.2.5.63. Transportare în staţionarC. 2.5.5Depistarea stărilor <strong>de</strong> urgenţă şi a complicaţiilor acute înAP.Prevenirea agravării complicaţiilor acute ale AP.Ameliorarea simptomatică a stării pacientului.• Anamneza (caseta 9).• Examenul <strong>clinic</strong> (caseta 10).• Acordarea primului ajutor şi a tratamentului <strong>de</strong> urgenţăla etapa prespitalicească (la necesitate) (tabelul7; antişoc – D.1).Transferul în instituţii medico-sanitară <strong>de</strong> profil. • Aprecierea posibilităţilor <strong>de</strong> transportare a pacientuluiconform criteriilor <strong>de</strong> spitalizare <strong>de</strong> urgenţă(tabelul 3).9
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009I II III6. SupraveghereaC.2.5.8Algoritmul C.1.17. RecuperareaC. 2.5.6.1, C.2.5.9Prevenirea complicaţiilor acute şi cronice ale AP.Asigurarea la timp a consultaţiei la medicii specialişti.Sporirea calităţii <strong>de</strong> viaţă a pacientului.Prevenirea <strong>de</strong>zvoltării complicaţiilor postoperatorii.• Supravegherea se efectuează conform algoritmilorspecial (algoritmul C.1.1; caseta 30; tabelul 9).• Consultaţia medicilor specialişti (la necesitate).• Implementarea modificărilor în stilul <strong>de</strong> viaţă (caseta7).• Tratamentul ambulatoriu (casetele 12-20), inclusivmanagementul maladiilor asociate (la necesitate),în perioada postoperatorie.Descriere(măsuri)B.4. Nivel <strong>de</strong> staţionar (raional, municipal, republican)Motive(repere)Paşi(modalităţi şi condiţii <strong>de</strong> realizare)I II III1. Profilaxia secundarăC.2.2, C.2.32. Spitalizarea şi transferulC.2.5.5, C.2.5.73. DiagnosticulC.2.5, C.2.7Algoritmul C.1.1Ameliorarea manifestărilor <strong>clinic</strong>e ale AP.Prevenirea <strong>de</strong>zvoltării complicaţiilor în AP.Precizarea diagnostică, efectuarea diagnosticului diferenţial.Optimizarea terapiei şi asigurarea volumului a<strong>de</strong>cvat <strong>de</strong>tratament, inclusiv al celui chirurgical.Confirmarea prezenţei <strong>de</strong> AP.Depistarea severităţii şi a caracteristicilor în AP.Stabilirea prezenţei <strong>de</strong> complicaţii acute şi cronice ale AP(tabelul 10), precum şi <strong>de</strong> maladii asociate, care pot influenţamanagementul AP.• Respectarea unui set <strong>de</strong> măsuri <strong>de</strong> diagnostic pozitivşi diferenţial (caseta 11).• Acordarea tratamentelor conservator şi chirurgicala<strong>de</strong>cvate (casetele 12-27; tabelele 5-8).• Necesitatea şi direcţia spitalizării urgente şi <strong>de</strong> planse efectuează conform criteriilor <strong>de</strong> spitalizare (tabelele3).• Evaluarea criteriilor <strong>de</strong> transfer în SATI (tabelul 4).• Evaluarea criteriilor <strong>de</strong> transfer în alte secţii (caseta28).• Anamneza (caseta 9).• Examenul <strong>clinic</strong> (caseta 10; anexa 5).• Investigaţiile para<strong>clinic</strong>e obligatorii şi recomandabile(tabelul 2).• Evaluarea diagnosticului pozitiv şi al severităţii AP(caseta 11) şi a complicaţiilor lui (tabelul 10).11
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 20094. TratamentulC 2.5.6Algoritmul C.1.15. SupraveghereaC.2.5.8Algoritmul C.1.16. Externarea sau transferulC.2.5.7Prevenirea <strong>de</strong>zvoltării sau agravării complicaţiilor acuteşi cronice.Ameliorarea stării pacientului.Prevenirea complicaţiilor intra- şi postoperatorii.Asigurarea la timp a consultaţiei la medicii specialişti.Revenirea pacientului în cîmpul <strong>de</strong> muncă.Asigurarea condiţiilor <strong>de</strong> recuperare eficientă în continuare.• Continuarea tratamentului <strong>de</strong> urgenţă iniţiat la etapaprespitalicească (la necesitate) (tabelul 7; antişoc- D.1.).• Modificarea <strong>de</strong> regim (tabelul 6) şi tratamentul nemedicamentos(tabelul 5).• Tratamentul medicamentos (casetele 12-20).• Tratamentul chirurgical (casetele 21-27; tabelul 8).• Supravegherea în staţionar (caseta 29).• Consultaţia medicilor specialişti (la necesitate).• Evaluarea criteriilor <strong>de</strong> externare şi <strong>de</strong> transfer (caseta28).12
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Antece<strong>de</strong>ntele:• Prezenţa factorilor <strong>de</strong> risc pentru <strong>de</strong>zvoltarea AP şi a complicaţiilor lui (casetele 2-4).• Evoluţia în timp a acuzelor pacientului, cu AP suspectat sau diagnosticat.C.2.5.2. Examenul <strong>clinic</strong>Caseta 10. Examenul <strong>clinic</strong> la pacienţii cu AP [5, 12, 30]• Picături „scăpate” <strong>de</strong> urină pe lenjerie/ pantaloni;• Glob vezical (<strong>de</strong>terminat la inspecţie, la percuţie şi/ sau la palpaţie): evaluarea este obligatoriepentru exclu<strong>de</strong>rea retenţiei acute <strong>de</strong> urină.• Tuşeul rectal: <strong>de</strong>terminarea aproximativă a dimensiunilor a<strong>de</strong>nomului <strong>de</strong> prostată, a consistenţeiei, a numărului şi a dimensiunilor nodulilor şi diagnosticul diferenţial orientativ cucancerul prostatei;• Prezenţa semnelor SIRS: febră, frisoane, transpiraţii, prezenţa focarului <strong>de</strong> infecţie la nivelulsistemului uropoietic, fatigabilitate sporită, slăbiciune generală (anexa 5).• Aprecierea stării altor organe şi sisteme cu evi<strong>de</strong>nţierea manifestărilor patologice,caracteristice pentru maladiile asociate şi disfuncţia acestor organe şi sisteme. Maladiileasociate şi complicaţiile lor.17
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009• Dezavantajele: diminuarea libido şi a potenţei, micşorarea volumului <strong>de</strong> ejaculat. În trialuriau fost înregistrate la 5-10% dintre pacienţi. Aceste efecte adverse sunt maxime în primul an<strong>de</strong> tratament. Astfel, administrarea la pacienţii tineri, pînă la 40 <strong>de</strong> ani, este restrînsă.• Particularităţi: micşorează nivelul PSA total cu ≈ 50% după tratament timp <strong>de</strong> un an, darnu creează dificultăţi în diagnosticul diferenţial cu a<strong>de</strong>nocarcinomul <strong>de</strong> prostată (studiiprospective în cohortă, inclusiv confirmate histologic). Nivelul PSA, fracţiei libere, sca<strong>de</strong> saurămîne neschimbat conform datelor diferitelor cercetări ştiinţifice.• Reprezentanţi şi posologie: Finasteridă: 5 mg/zi. Prepon<strong>de</strong>rent suprimă activitatea 5-α reductazei <strong>de</strong> tipul I. Dutasteridă 0,5 mg/zi. Suprimă activitatea atît 5-α reductazei, tipul I şi tipul II.• Asocierea inhibitorilor 5-α reductazei cu antagoniştii receptorilor α-adrenergici este benefică,iar ultimii după realizarea efectului iniţial pozitiv pot fi suspendaţi la distanţă <strong>de</strong> 9-12 luni,fără nicio înrăutăţire a simptomatologiei LUTS.Caseta 14. Antagoniştii receptorilor α-adrenergici [6, 11, 25]• Eficienţa în ameliorarea simptomatologiei este comparabilă sau superioară inhibitorilor 5-αreductazei. Efectul pozitiv se realizează net mai rapid (timp <strong>de</strong> 48 <strong>de</strong> ore), în comparaţie cuinhibitorii 5-α reductazei. La distanţă <strong>de</strong> o lună se recomandă verificarea eficienţei (IPSS).• În special sunt eficienţi la pacienţii cu participarea unei componente funcţionale maipronunţate, care participă în manifestarea LUTS (ex., persoane cu a<strong>de</strong>nomul relativ mic,volum rezidual redus <strong>de</strong> urină în caz <strong>de</strong> IPSS şi QoL relativ înalte, fără complicaţii cronice).• Avantajele suplimentare: ameliorare rapidă a simptomatologiei LUTS. Poate ajuta larezolvarea retenţiei acute <strong>de</strong> urină, fără cateterizare. Însă la majoritatea pacienţilor episodulretenţiei acute <strong>de</strong> urină se repetă pe parcursul ultimelor 2 luni.• Dezavantajele: efectele adverse cuprind diferite <strong>de</strong>reglări ale sistemului nervos vegetativ.Datele <strong>clinic</strong>e publicate <strong>de</strong>monstrează că eficienţa <strong>clinic</strong>ă se păstrează la distanţă > 6-12 luni<strong>de</strong> administrare permanentă, dar la moment nu există trialuri dublu-oarbe în această privinţă.Preparatele „hiperselective” (ex., Tamsulosină sau Afluzozină) sunt mai bine suportate <strong>de</strong>către pacienţi în şedinţe lungi <strong>de</strong> tratament.• Particularităţi: Preparatele mai vechi, cu selectivitatea redusă, (ex., Prazosin şi Doxazosin) au un efectantihipertensiv semnificativ. Administrarea lor este recomandată în caz <strong>de</strong> asociere a APşi a HTA. Aceste preparate iniţial se administrează în doza terapeutică minimă (1 mg)seară înainte <strong>de</strong> somn din cauza riscului sporit <strong>de</strong> hipotensiune la prima administrare. La pacienţii normotensivi, în special cu DZ, există risc sporit <strong>de</strong> <strong>de</strong>zvoltare a hipotensiuniiortostatice. Astfel, la normotensivi şi la diabetici sunt recomandate preparatele mai noi,cu selectivitate sporită (ex., Tamsulosină sau Afluzozină).• Reprezentanţii şi posologie: Inhibitorii receptorilor α-adrenergici neselectivi:- Fenoxibezamină. Practic nu se utilizează datorită efectelor adverse pronunţate. Inhibitorii receptorilor α-1-adrenergici selectivi:- Tamsulosină: o capsulă <strong>de</strong> 0,4 mg dimineaţă.- Afluzozină: 1-3 comprimate (5-15 mg) o dată pe zi.- Terazosină: 1 mg x 2 ori/zi cu majorarea treptată pînă la 10 mg/zi (2 prize).- Doxazosin: 1 mg/zi cu majorare treptată pînă la 4-8 mg/zi (2 prize).- Prazosin: 3-4 mg/zi cu majorare treptată a dozei pînă la 15-20 mg/zi (3-4 prize).22
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Caseta 15. Preparate fitoterapeutice cu acţiune asupra AP [15, 30, 49, 50]• Unele trialuri şi metaanalize <strong>de</strong>monstrează eficienţa similară a preparatelor fitoterapeutice cuinhibitorii 5-α reductazei şi antagoniştii receptorilor α1-adrenergici. Însă aceste date necesităo dovadă ştiinţifică mai bine argumentată.• Avantajele suplimentare: pot fi administrate în monoterapie sau în tratament combinat alAP, uşor sau mediu, administrarea în<strong>de</strong>lungată nu se asociază cu reducerea eficienţei sau cuapariţia efectelor adverse. În acelaşi timp, inhibitorii 5-α reductazei şi antagoniştii receptorilorα-adrenergici sunt mai bine studiaţi şi reprezintă medicamentele <strong>de</strong> prima linie.• Dezavantajele: standardizarea preparatelor halenice este tot<strong>de</strong>auna dificilă. Efectele adverseprincipale includ reacţii alergice şi <strong>de</strong>reglările gastrointestinale.• Particularităţi: mecanismul <strong>de</strong> acţiune rămîne incert şi necesită cercetare în continuare.• Reprezentanţi şi posologie: Extract din Serenoa repens (ex., Prostamol uno): 160-320 mg o dată/zi. Scoarţa Pygeum africanum (ex., Ta<strong>de</strong>nan): 50 mg x 2 ori/zi. A<strong>de</strong>noprosin, 1 sup. (250 mg) i.r. 1-2 ori/ zi.Caseta 16. Profilaxia sindromului tromboembolic pulmonar la pacienţii cu AP în perioadapostoperatorie [5, 12, 30]• Se administrează anticoagulantele directe (Heparină şi heparinele cu masa moleculară mică).• Administrarea heparinelor <strong>de</strong> masă moleculară mică este mai avantajoasă din punct <strong>de</strong> ve<strong>de</strong>reeconomic, secundar implicaţiei reduse a personalului medical în administrare, precum şi rateinet reduse <strong>de</strong> efectele adverse (reacţii alergice, hemoragii, trombocitopenie).• Se administrează în ziua intervenţiei chirurgicale + 5-7 zile (pînă la mobilizarea completă apacientului).• Posologie recomandată: Heparină: 2500 – 5000 UI x 4 ori/zi, s.c. (în funcţie <strong>de</strong> masa pacientului). Nadroparină <strong>de</strong> calciu (2850 UI/ 0,3 ml), s.c., o dată / zi. Dalteparină <strong>de</strong> sodiu (5,000 – 10,000 UI anti-Xa/0,2 ml – 0,4 ml), s.c., o dată / zi.Caseta 17. Terapia antibacteriană în AP: medicaţie empirică [5, 12]• Tratamentul antibacterian este iniţial empiric, iar în continuare este guvernat conformantibioticosensibilităţii germenului bacterian <strong>de</strong>pistat.• AP cu scop profilactic (risc relativ redus – tabelul 1), durata 5-7 zile: Monoterapia cu formele soli<strong>de</strong>: Ciprofloxacină (250 mg sau 500 mg) x 2 ori sau Cefalexină(250 mg) x 3 ori/zi, sau Amoxicilină (500 mg) x 3 ori/zi.• AP cu scop profilactic după intervenţie chirurgicală (risc relativ redus – tabelul 1), duratatratamentului, durata 7-10 zile (în special după cateterizarea vezicii urinare): Monoterapie cu formule parenterale, eventual biterapie (al 2-lea preparat poate fi subformă <strong>de</strong> comprimate anterior citate): Ampicilină (1,0) x 4 ori/zi sau Cefazolină (1,0) x 4ori/zi sau Amoxicilină (1,0) x 4 ori/zi sau Ciprofloxacină (200 mg dizolvate per 200 mlsol. Clorură <strong>de</strong> sodiu 0,9%) sau Ceftriaxon (1,0) x 2 ori/zi ± formele soli<strong>de</strong> sus-enumerate.• Infecţie urinară postoperatorie sau infectarea plăgii (risc relativ mediu – tabelul 1),durata tratamentului ≥ 14 zile: Biterapie parenterală: Ampicilină (2,0) x 3-4 ori/zi sau Cefazolină (1,0) x 4 ori/zi, sauAmoxicilină (1,0) x 4 ori/zi, sau Ceftriaxon (1,0) x 2 ori/zi, sau Ceftazidim (1,0) x 2ori/zi + Ciprofloxacină (200 mg dizolvate per 200 ml sol. Clorură <strong>de</strong> sodiu 0,9%), sauAmikacină (0,25 – 10 ml x 3 ori/zi).23
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Caseta 19. Tratament hemostatic în AP [5, 12]• Hematuria refractară la tratament cu inhibitorii 5-α reductazei reprezintă una dintreindicaţiile absolute în tratamentul chirurgical al a<strong>de</strong>nomului <strong>de</strong> prostată.• În macrohematurie pot fi recomandate instalarea son<strong>de</strong>i uretrale şi lavajul vezicii urinare.• Hemoragia postoperatorie (inclusiv, macrohematuria) poate servi drept indicaţie pentruintervenţia chirurgicală repetată.• În hemoragia apreciată ≥ 0,5 l se iniţiază suplinirea volemică cu soluţii coloi<strong>de</strong> şicristaloi<strong>de</strong> (<strong>de</strong>xtranii şi Hidroxietilamidon sunt contraindicaţi).• În hemoragia apreciată ≥ 1,0 l este solicitată administrarea sîngelui sau a masei eritrocitare.• Plasma proaspăt congelată este obligatoriu administrată la pacienţii cu semnelesindromului coagulării intravasculare diseminate.• Cu scop hemostatic se utilizează pînă la micşorarea hematuriei şi/ sau a hemoragiei + 2-3 zile: Gluconat <strong>de</strong> calciu sol. 10% – 5 sau 10 ml) sau Clorură <strong>de</strong> calciu (sol. 5% – 5 sau 10 ml)x 2-3 ori/zi, i.v. Etamzilat sol. 12,5% – 2 ml x 3 ori/zi, i.v., i.m. Acid aminocapronic sol. 5% – 100 ml x 1-2 ori/zi, i.v. Trombină* (local).• La pacienţii cu microhematurie pot fi administrate antioxidantele cu efect vasoprotector(Acid ascorbic, comprimate cîte 0,5 x 3 ori/zi, per os, sau sol. 5%-5 ml, i.v., şi Tocoferolacetat, capsule – cîte 400 UI x 1-2 ori/zi, per os).Caseta 20. Fitoterapia şi uroantiseptice în ITU asociate ale sistemului uropoietic [15]• Se administrează în cure în<strong>de</strong>lungate cu scop profilactic.• Se recomandă schimbarea preparatului vegetal fiecare 10-14 zile.• Infuzia sau, mai rar, maceratul apos reprezintă formele farmacologice principale.• Preparatele vegetale posedă proprietăţile antiinflamatoare, emoliente, spasmolitice, diuretice,antibacteriene.• Preparatele vegetale tabletate: Cyston**, Kanefron** H etc.• Preparatele vegetale cu acţiune prepon<strong>de</strong>rent antiinflamatorie: muguri <strong>de</strong> Ppn (TurionesPini), muguri <strong>de</strong> plop (Gemmae Populi), frunze şi rădăcini <strong>de</strong> nalbă mare (Folium et RadixAlthaea), nalbă <strong>de</strong> grădină (Althaea rosea), mugur <strong>de</strong> mesteacăn (Gemmae Betulae).• Uroantiseptice: ex., Nitroxolină 1-3 comprimate – cîte 50 mg x 3-4 ori/zi sau Nitrofurantoină1-2 comprimate – cîte 100 mg x 3 -4 ori/zi.C.2.5.6.3. Tratamentul chirurgicalCaseta 21. Tratamentul chirugical în AP [5, 12, 17, 20, 22, 24, 27, 29, 32]• Radicale clasice: Rezecţie transuretrală a a<strong>de</strong>nomului <strong>de</strong> prostată (endoscopică) (TURP). Incizie transuretrală a prostatei (endoscopică) (TUIP). A<strong>de</strong>nomectomie <strong>de</strong>schisă.• Radicale miniinvazive Vaporizare transuretrală (TUVP, alternativă TURP/TUIP la pacienţi cu AP < 20 cm 3 ). Enucleare cu laser: Nd:YAG, KTP:YAG, cu diodă, Holmium:YAG, energia este transmisăprin fibră simplă, interstiţială sau cu unghiul drept.Notă: *preparatul nu este înregistrat în RM**preparat compus25
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009 Meto<strong>de</strong>le electrochirurgicale (electrocoagulare bipolară, rezecţie prin coagulare intermitentă,rotorezecţie). Rezultatele aplicării acestor tehnici sunt promiţătoare, dar necesită afi confirmate în trialuri.• Laparatomie cu rezolvarea peritonitei şi suturarea/ plastia vezicii urinare în caz <strong>de</strong>ruptură a vezicii urinare.• Paliative: instalarea cateterului uretral Foley sau Nelaton, efectuarea cistostomei, aplicareacistofixului, nefrostomie (în obstrucţie infrarenală <strong>clinic</strong> semnificativă), stent uretral.Caseta 22. Indicaţii pentru tratamentul chirurgical în AP [5, 12, 17, 24, 27, 29]• Indicaţii absolute: Retenţie acută <strong>de</strong> urină, refractară la tratamentul aplicat. Retenţie acută recidivantă <strong>de</strong> urină. Hematurie recurentă, refractară la tratament cu inhibitorii 5-α reductazei. Insuficienţă renală secundară AP. Calculi în vezica urinară.• Manifestările <strong>clinic</strong>e, care reduc semnificativ calitatea vieţii (IPSS ≥ 20, QoL ≥ 4, în special5-6) reprezintă indicaţiile cele mai frecvente pentru intervenţia chirurgicală <strong>de</strong> plan.• Volumul rezidual mare <strong>de</strong> urină în vezica urinară, <strong>de</strong> asemenea, poate servi drept indicaţiepentru intervenţia chirurgicală. Însă varietăţile lui şi lipsa corelaţiei directe cu riscul retenţieiacute <strong>de</strong> urină şi severitatea LUTS nu permit obiectivizarea cantitativă a acestei indicaţii.• Indicaţii pentru a<strong>de</strong>nomectomie <strong>de</strong>schisă: AP mare <strong>de</strong> prostată (> 80-100 cm 3 , diverticululvezicii urinare sau calculi mari ai vezicii urinare).• Indicaţii pentru meto<strong>de</strong>le laser: administrarea anticoagulanţilor, reducerea riscului <strong>de</strong> afectarea procesului <strong>de</strong> ejaculare, în loc <strong>de</strong> prostatectomie <strong>de</strong>schisă (Holmium: YAG).• Notă: Meto<strong>de</strong>le paliative se utilizează nu numai la pacienţii cu contraindicaţii pentrutratamentul chirurgical radical al a<strong>de</strong>nomului <strong>de</strong> prostată, ci şi la pacienţii internaţi pe urgenţă,ex., cu retenţie acută <strong>de</strong> urină. Tratamentul radical este efectuat în astfel <strong>de</strong> cazuri „la rece”.Tabelul 8. Analiza comparativă a TUIP şi a TURP [27, 43]TUIP Indice TURPMai rare Complicaţii Mai frecventeEgală Eficienţa la prostate cu V < 30 cm 3 EgalăInferioară Eficienţa la prostate cu V > 30 cm 3 SuperioarăRedusRiscul hemoragieiSporitşi al necesităţii transfuziei <strong>de</strong> sîngeRedus Riscul <strong>de</strong>zvoltării ejaculării retrogra<strong>de</strong> SporitMicşorată Durata spitalizării MajoratăMicşorată Durata intervenţiei chirurgicale MajoratăInferioară Eficienţa la distanţă SuperioarăNotă: Riscul <strong>de</strong>zvoltării complicaţiilor postoperatorii corelează direct cu volumul prostatei şi cudurata intervenţiei chirurgicale.Caseta 23. Meto<strong>de</strong>le alternative <strong>de</strong> tratament [5, 12]• Aplicarea transrectală a ultrasunetului focalizat <strong>de</strong> înaltă intensitate (HIFU).• Ablaţiune cu un<strong>de</strong> radio <strong>de</strong> frecvenţă înaltă (TUNA).• Termoterapia cu microun<strong>de</strong> (TUMT).26
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Caseta 24. Aplicarea transrectală a ultrasunetului focalizat <strong>de</strong> înaltă intensitate (HIFU)[26, 28]• Unică metodă <strong>de</strong> ablaţiune complet noninvazivă a ţesutului a<strong>de</strong>nomatos, semnificativameliorează LUTS şi Q max.• Lipsesc trialuri randomizate, rată <strong>de</strong> recidivă 10% per an.• Este necesară anestezie generală sau cel puţin o sedare importantă.• Criterii <strong>de</strong> exclu<strong>de</strong>re pentru HIFU: calcificările prostatei, distanţa rectul – colul vezical > 4cm, volumul prostatei > 75 cm 3 , lobul mediu mare, lipsa indicaţiilor absolute.Caseta 25. Ablaţiune cu un<strong>de</strong>le radio <strong>de</strong> frecvenţă înaltă (TUNA) [34, 51]• Ablaţiunea ţesutului a<strong>de</strong>nomatos cu ajutorul un<strong>de</strong>lor radio <strong>de</strong> frecvenţă înaltă, cu ajutorulacelor speciale introduse transuretral.• Semnificativ ameliorează Q max şi LUTS, nu influenţează volumul prostatei.• Este necesară numai anestezie locală.• Numai un trial randomizat, care confirmă eficienţa proce<strong>de</strong>ului. Rezultatele <strong>de</strong> distanţă nuau fost apreciate în trialuri.• Necesitate în tratament chirurgical consecutiv (TURP) este ≈ 20% timp <strong>de</strong> 3 ani.Caseta 26. Termoterapia cu microun<strong>de</strong> (TUMT) [10, 37]• Există protocoale cu doză redusă şi sporită <strong>de</strong> iradiere a prostatei. Cel cu doza sporită oferăameliorare mai evi<strong>de</strong>ntă a simptomatologiei AP şi rezultate mai durabile a tratamentului, <strong>de</strong>şieste asociat cu rata sporită a complicaţiilor.• Ameliorează semnificativ LUTS şi Q max, micşorează volumul prostatei. Poate necesitainstalarea cateterului uretral din cauza retenţiei <strong>de</strong> urină în perioada precoce postoperatorie.• Numărul limitat <strong>de</strong> trialuri randomizate, predomină studii <strong>de</strong>schise.• Poate fi efectuată fără anestezie, ceea ce permite aplicarea acestei meto<strong>de</strong> la pacienţi cupatologii asociate severe.• Rată <strong>de</strong> succes este 72% la distanţă <strong>de</strong> 6 luni.• Nu se recomandă pacienţilor cu lobul mediu mare şi cu dimensiunile reduse ale segmentuluiintraprostatic al uretrei.Caseta 27. Rezultatele aşteptate ale intervenţiei chirurgicale [5, 12]• Ameliorarea LUTS (obiectivizare prin IPSS).• Creşterea vitezei fluxului urinar în timpul micţiunii (Q max <strong>de</strong>terminată cu ajutorul uroflowmetriei).• Diminuarea volumului rezidual <strong>de</strong> urină (obiectivizat cu ajutorul USG transrectale.)C.2.5.7. Criteriile <strong>de</strong> externare şi <strong>de</strong> transferCaseta 28. Criterii <strong>de</strong> externare în AP (după intervenţie chirurgicală) [5, 12, 30]• Dispariţia semnelor <strong>de</strong> inflamaţie, locală şi generală (anexa 5), apreciate <strong>clinic</strong> şi para<strong>clinic</strong>.• Local: cicatrizarea primară sau secundară.• Absenţa hematuriei.• Stabilizarea funcţiei <strong>de</strong> urinare <strong>de</strong> sine stătător, apreciate <strong>clinic</strong> şi para<strong>clinic</strong> (cu excepţiasituaţiilor după efectuarea operaţiilor paliative (casetele 21-22; algoritmul C.1.1).27
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009• Agravarea evoluţiei altor maladii – după controlul complicaţiilor AP sau tratamentul luichirurgical sau după severitatea patologiei asociate pacientul poate fi transferat în secţiilespecializate corespunzătoare pentru continuarea tratamentului respectiv.• Dezvoltarea şocului (infecţios, hemoragic) – transfer în SATI, după controlul şocului (+ 1zi) – transfer în secţie.C.2.5.8. Supravegherea pacienţilorTabelul 9. Monitorizare minimă a pacientului cu AP în funcţie <strong>de</strong> tratamentul aplicat [12, 35]Modalitatea<strong>de</strong> tratamentAşteptarevigilentăInhibitori ai5α-reductazeiadrenoblocanteIntervenţiechirurgicalăMeto<strong>de</strong>alternativePeriodicitateasupravegherii6 lunianual12 săptămîni6 lunianual6 săptămîni3 lunianual6 săptămîni3 lunianual6 săptămîni3 luni; 6 lunianualIPSSşi QoLUSG transrectală cu<strong>de</strong>terminarea volumuluirezidual <strong>de</strong> urinăUroflowmetrieHistologieDa Da Da NuDa Da Da NuDa Da Da NuDa Da Da DaDa Da Da DaNotă: În caz <strong>de</strong> tratament chirurgical sau <strong>de</strong> aplicare a meto<strong>de</strong>lor alternative (TUNA, HIFU,TUMT), este recomandată şi efectuarea uroculturii, în special în grupurile <strong>de</strong> risc sporit al ITU.Caseta 29. Supravegherea pacienţilor cu AP în spital [12, 30]• Conduita generală a pacientului cu AP (algoritmul C.1.1).• Conduita pacientului după externare din spital (caseta 30).• Abordarea complexă în timpul tratamentului în staţionar şi după externare (algoritmul C.1.1;casetele 7, 12-27; tabelele 5-8). Reglementarea comportamentului pacientului, particularităţilor dietetice (tabelul 5). Evaluarea necesităţii transferului în SATI, a continuării tratamentului în SATI sau atransferului din SATI în secţie (tabelele 4 şi 7). Stabilirea volumului şi a caracterului măsurilor terapeutice (casetele 12-20) şi diagnosticela etapele consecutive <strong>de</strong> management (tabelul 2). Tratamentul chirurgical al AP (algoritmul C.1.1; casetele 21-27).Caseta 30. Evaluarea pacienţilor cu AP, externaţi după tratament chirurgical [12, 30]• Evaluarea este efectuată iniţial <strong>de</strong> urolog la distanţă <strong>de</strong> 1, 3 şi <strong>de</strong> 12 luni postoperatoriu. Dacăpacientul rămîne stabil în continuare el este supravegheat <strong>de</strong> medicul <strong>de</strong> familie.• Agravarea vădită a stării pacientului sau <strong>de</strong>zvoltarea complicaţiilor acute solicită reevaluareurgentă la urolog.28
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009• Profilul diagnostic cuprin<strong>de</strong>: Evoluţia AP (caseta 31). Evaluarea diagnostică a maladiilor asociate sistemului uropoietic conform protocoalelor<strong>clinic</strong>e naţionale sau ghidurilor existente în domeniu. Acuzele, în special, persistenţa disuriei şi a <strong>de</strong>reglărilor <strong>de</strong> micţiune (LUTS) în perioadapostoperatorie. Aprecierea dinamică este importantă pentru exclu<strong>de</strong>rea altor cauze LUTS<strong>de</strong>cît AP, precum şi diagnosticarea timpurie a recidivei AP. Examenul fizic: TA, FCC, status volemic, per rectum (la necesitate). Investigaţiile <strong>de</strong> laborator: creatinină cu calcularea FG, uree, analiză generală <strong>de</strong> sînge,analiză generală <strong>de</strong> urină. Investigaţiile instrumentale: Uroflowmetrie.C.2.5.9. Evoluţia a<strong>de</strong>nomului <strong>de</strong> prostatăCaseta 31. Variantele <strong>de</strong> evoluţie a AP [12, 30]• Evoluţie sub<strong>clinic</strong>ă, fără <strong>de</strong>zvoltare a complicaţiilor <strong>clinic</strong> manifeste.• Evoluţie sub<strong>clinic</strong>ă, cu <strong>de</strong>zvoltarea complicaţiilor, care nu afectează semnificativ calitateavieţii.• Dezvoltare a complicaţiilor cronice, care solicită tratament chirurgical.• Evoluţie clasică cu complicaţii acute, eventual cu necesitatea intervenţiei chirurgicale urgente<strong>de</strong> corecţie.• Cazuri <strong>de</strong>păşite, cu acordarea tratamentului chirurgical paliativ.C.2.6. ComplicaţiileTabelul 10. Complicaţiile AP [5, 12, 30, 38]ComplicaţiiDescriereAcute • Retenţie acută <strong>de</strong> urină• ITU acută: cistită acută, pielonefrită acută• Insuficienţă renală acută prin obstrucţie infrarenală• Ruptură a vezicii urinareIntraoperatorii • Sindromul TUR (risc sporit la fumători, hemoragii masive şi AP mare)şi • Hemoragie din loja a<strong>de</strong>nomului operat, eventual cu şoc hemoragicpostoperatorii • Infecţie la nivelul plăgii postoperatorii, eventual cu şoc toxicoinfecţios• Sindromul tromboembolic pulmonar• Incontinenţă <strong>de</strong> urină, contractura colului vezical şi strictura uretrei• Disfuncţiile sexuale• Fistule postchirurgicale• Reoperaţie: 1-2% per an• Infecţiile cronice ale căilor <strong>de</strong> drenaj urinar (ex., cateter uretral)Cronice • Cistită cronică şi ITU repetate• Calcul al vezicii urinare• Diverticulul vezicii urinare• Boală cronică <strong>de</strong> rinichi: reflux vezicoureteral, hidrocalicoză şihidronefroză, pielonefrită cronică• Insuficienţă renală cronică, HTA secundară nefrogenă (rar)29
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009D. RESURSELE UMANE ŞI MATERIALELE NECESARE PENTRURESPECTAREA PREVEDERILOR DIN PROTOCOL30D.1. Instituţiile<strong>de</strong> asistenţămedicalăprimarăD.2. Serviciul<strong>de</strong> asistenţămedicalăurgentă şa etapaprespitaliceascăD.3. Instituţiile/ secţiile <strong>de</strong>asistenţămedicalăspecializată <strong>de</strong>ambulatoriuPersonal:• Medic <strong>de</strong> familie.• Asistentă a medicului <strong>de</strong> familie.• Laborant cu studii medii.Aparataj, utilaj:• Tonometru şi fonendoscop.• Laborator <strong>clinic</strong>, capabil să efectueze analiză generală <strong>de</strong> sînge,analiză generală <strong>de</strong> urină, creatinină în sînge.Medicamente, instrumentar:• Set antişoc: glucocorticosteroizi (ex., Prednisolon 30 mg în fiole,nr.10); vasoconstrictoare (ex., Norepinefrină 0,1% – 1 ml, în fiole,nr. 2), antihistaminice (ex., Difenhidramină 1% – 1ml, în fiole, nr. 5),analgezice (ex., Diclofenac 75 mg – 3 ml, în fiole, nr. 5), suport volemic(sol. Clorură <strong>de</strong> sodiu 0,9% sau sol. Glucoză 5%, flacoane cîte 500 ml,nr. 2), seringe, ace, set pentru perfuzie (<strong>de</strong> unică folosinţă).• Mănuşi.Personal:• Medic <strong>de</strong> urgenţă/felcer.• Asistenta medicală <strong>de</strong> urgenţă.Aparataj, utilaj:• Tonometru şi fonendoscop.Medicamente, instrumentar:• Set antişoc: vezi D.1.Personal:• Urologi, chirurgi.• Asistentele medicale.• Medic <strong>de</strong> laborator şi laborant cu studii medii.Aparataj, utilaj:• Tonometru şi fonendoscop.• Electrocardiograf.• Ultrasonograf.• Laborator <strong>clinic</strong> pentru <strong>de</strong>terminare <strong>de</strong>: capabil să efectueze analizăgenerală <strong>de</strong> sînge şi urină; creatinină, uree, glicemie, potasiu în sînge,PSA şi PSA, fracţie liberă (recomandabil); Rh-factorul şi grupulsangvinic, AgHbs, anti-VHC, analiza SIDA, reacţia MRS.Medicamente, instrumentar:• Set antişoc: vezi D.1.• Mănuşi.• Medicaţia antibacteriană: vezi D.4 (secţiile nespecializate).• Medicaţiile antispastică şi analgezică: vezi D.4.• Medicamentele cu acţiune patogenetică asupra AP: vezi D.4.• Fitoterapia AP: vezi D.4.• Fitoterapia ITU: vezi D.4.
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009D.4. Instituţiile<strong>de</strong> asistenţămedicalăspitalicească:secţii specializate(urologie) sau <strong>de</strong>profil generalPersonal:• Medici specialişti (urolog, chirurg).• Alţi specialişti (funcţionalist, imagist).• Asistentele medicale.• Medici laboranţi şi laboranţi cu studii medii.• Specialiştii serviciului morfologic.Aparataj, utilaj:• Tonometru şi fonendoscop.• Electrocardiograf (se preferă portabil).• Ultrasonograf (pentru secţii specializate suplimentar pentruexaminarea organele interne în regimul Doppler color).• Aparat radiografic (se preferă mobil).• Laborator <strong>clinic</strong> pentru <strong>de</strong>terminarea următorilor parametri: biologici – analiză generală <strong>de</strong> sînge, analiză generală <strong>de</strong> urină; biochimici (în sînge) – creatinină, uree, glicemie, potasiu, sodiu;în secţiile specializate (urologie) suplimentar: calciu (total şiionizat), bilirubină, ALT, amilază, fosfatază alcalină; imunologici – PSA şi PSA, fracţiei libere; Rh şi grupul sangvinic,AgHbs, anti-HbcIg total, anti-VHC, analiza SIDA, reacţia MRS; culturali: urocultură, hemocultură; în secţiile specializate(urologie) suplimentar: însămînţare din alte ţesuturi şilichi<strong>de</strong> biologice normale şi patologice, cu <strong>de</strong>terminareaantibioticosensibilităţii; coagulogramă – protrombină, fibrinogen; în secţiile specializate(urologie) suplimentar: activitatea fibrinolitică, timpultrombinic, timpul <strong>de</strong> tromboplastină parţial activat, testul cuo-fenantrolină, D-dimerii pentru <strong>de</strong>terminarea produselor <strong>de</strong><strong>de</strong>gradare a fibrinogenului. în secţiile specializate (urologie) suplimentar:- proba Reberg (probele renale funcţionale);- proba Neciporenko.În secţiile specializate (urologie, nefrologie) suplimentar:• Posibilitate <strong>de</strong> efectuare a cistoscopiei.• Laborator <strong>de</strong> medicină nucleară care să efectueze scintigrafia renalădinamică.• Posibilitate <strong>de</strong> efectuare <strong>de</strong>: TC (obligatoriu), angiografie şi IRM.Medicamente, instrumentar:• Set antişoc: vezi D.1.• Mănuşi.• Cistoscop.• Catetere uretrale: Foley. Nelaton.• Inhibitorii 5-α reductazei: Finasteridă (comprimate cîte 5 mg). Dutasteridă (capsule cîte 0,5 mg).31
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009• Antagoniştii receptorilor α-adrenergici: Tamsulosină (capsule – cîte 0,4 mg). Afluzozină (comprimate – cîte 5 şi 10 mg). Terazosin (comprimate – cîte 1 şi 5 mg). Doxazosin (comprimate – cîte 1 şi 2 mg). Prazosin (comprimate – cîte 1 şi 5 mg).• Preparatele fitoterapeutice cu acţiune la AP: Extract din Serenoa repens (ex., Prostamol) (capsule – cîte 160 sau320 mg). Extract din scoarţa Pygeum africanum (ex., Ta<strong>de</strong>nan) (capsule 50mg). A<strong>de</strong>noprosin, supozitoare rectale – cîte 250 mg.• Anticoagulanţii: Nadroparină <strong>de</strong> calciu (2850 UI/ 0,3 ml). Dalteparină <strong>de</strong> sodiu (10,000 UI anti-Xa/0,4 ml). Heparină (5000 UI/ ml).• Medicaţia antibacteriană: Cefalosporinele: Cefazolină (pulbere 1,0 în flacon) şi Ceftriaxon(pulbere 1,0 în flacon). Aminopenicline: Ampicilină (comprimate/capsule – 0,5 şi pulbere1,0 în flacon) sau Amoxicilină (comprimate/capsule – 0,5 şipulbere 1,0 în flacon). Fluorchinolone: Ciprofloxacină (comprimate/capsule – 500 mg şisol. 200 mg – 100 ml). Metronidazol (comprimate – 500 mg). Ketoconazol (comprimate/capsule – 200 mg) sau Fluconazol(comprimate/capsule – 100 mg). Preparatele medicamentoase accesibile numai la nivel <strong>de</strong> secţiispecializate (Urologie):- Amoxicilină + Acid clavulanic (pulbere 500 mg + 100 mg sau1000 mg + 200 mg).- Ceftazidim (pulbere 1,0 în flacon).- Metronidazol (sol. 500 mg – 100 ml).- Vancomicină (pulbere liofilizată pentru infuzii 0,5 sau 1,0).- Amikacină (pulbere liofilizată 0,25 – 10 ml).- Imipenem + Cilastină (0,5 + 0,5 – soluţie pentru infuzii).• Medicaţia hemostatică: Preparatele sîngelui (masă eritrocitară, plasmă proaspăt congelată) Calciu gluconat (sol. 10% – 5 sau 10 ml) sau Calciu clorid (sol.5% – 5 sau 10 ml). Etamzilat sol. 12,5% – 2 ml. Acid aminocapronic sol. 5% – 100 ml. Trombină* (pentru aplicare locală).Notă: *preparatul nu este înregistrat în RM32
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009• Medicaţia analgezică: Nimesulid (suspensie pentru administrare per os, cîte 100 mg înplic) sau Paracetamol (comprimate cîte 500 mg). Ketorolac (comprimate cîte 10 mg şi pulbere 30 mg – 1 ml) sauDiclofenac (comprimate cîte 50 mg, supozitorii rectale cîte 50 mgşi pulbere 75 mg – 3 ml) sau Metamizol <strong>de</strong> Natriu (sol. 50% - 2ml). Tramadol (sol. 50 mg – 1 ml şi capsule cîte 100 mg). Preparatele medicamentoase accesibile numai la nivel <strong>de</strong> secţiispecializate (Urologie):- Morfină clorhidrat (sol. 1% – 1 ml).- Promedol (sol. 2% – 1 ml).• Terapia <strong>de</strong> <strong>de</strong>zintoxicare: Sol. Natriu clorid 0,9% – 200 sau 500 ml. Sol. Glucoză 5% – 200 sau 500 ml şi 40% – 10 sau 20 ml.• Medicaţia antispastică: Drotaverină (comprimate – cîte 40 sau 80 mg şi sol. 2% – 2 ml). Platifilină (sol. 0,2% – 1ml).• Medicaţia antioxidantă: Acid ascorbic (comprimate – cîte 0,5 şi sol. 5% – 5 ml). Tocoferol acetat (capsule – cîte 400 UI).• Fitoterapeutice pentru ITU: Cyston. Kanefron H. Ceai renal.• Uroantiseptice pentru ITU: Nitroxalin, comprimate – cîte 50 mg. Nitrofurantoină, comprimate – cîte 100 mg.• Antihipotensive: Benzoat <strong>de</strong> cafeină sol. 20% – 1ml şi Niketamidăsol. 25% –1 ml.• Ace, seringi (2, 5, 10, 20 ml), set pentru perfuzii (<strong>de</strong> unică folosinţă).• Faşă, bint, tamponaşe.• Antiseptice (ex., Betadină).• Dezinfectante.• Sală <strong>de</strong> operaţii şi instrumente chirurgicale (anexa 4).• Sală chirurgicală <strong>de</strong> pansamente.33
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009E. INDICATORII DE MONITORIZARE A IMPLEMENTĂRII PROTOCOLULUINr. Scopul Indicatorul1. Depistarea activăa pacienţilor cuLUTS la niveluri <strong>de</strong>asistenţă medicalăprimară şi <strong>de</strong> ambulatoriuspecializată2. Ameliorarea diagnosticăriiAP3. Micşorarea ratei <strong>de</strong>complicaţii acute lapacienţi cu AP4. Sporirea eficienţeitratamentului în AP5. Sporirea <strong>de</strong> calitateîn supraveghereapacienţilor cu APPon<strong>de</strong>rea persoanelor/ pacienţilor cuLUTS, cărora în mod documentat, li s-aoferit informaţii sub formă <strong>de</strong> discuţii/ghid al pacientului etc. <strong>de</strong>spre AP <strong>de</strong> cătremedicul specialist (urolog), pe parcursulunui anPon<strong>de</strong>rea pacienţilor cu LUTS cu IPSS ≥8 în vîrstă <strong>de</strong> peste 40 <strong>de</strong> ani, care s-auadresat la medicul specialist (urolog) şicărora li s-a efectuat tuşeul rectal, PSA,USG transrectală a prostatei şi uroflowmetriaPon<strong>de</strong>rea pacienţilor cu AP, asociat cucomplicaţii acute, spitalizaţi în instituţiamedico-sanitară, pe parcursul anuluiPon<strong>de</strong>rea pacienţilor cu AP trataţi conformprotocolului <strong>clinic</strong> naţional A<strong>de</strong>nomul<strong>de</strong> prostată în IMSP, pe parcursulanuluiPon<strong>de</strong>rea pacienţilor cu AP, monitorizaţiconform protocolului <strong>clinic</strong> naţional A<strong>de</strong>nomul<strong>de</strong> prostată, <strong>de</strong> medicul specialist(urolog), pe parcursul anuluiMetoda <strong>de</strong> calculare a indicatoruluiNumărător NumitorNumărul <strong>de</strong> persoane/ pacienţi cu LUTS,cărora <strong>de</strong> către medicul specialist (urolog),în mod documentat, li s-a oferit informaţiisub formă <strong>de</strong> discuţii/ ghid al pacientuluietc. <strong>de</strong>spre AP, pe parcursul ultimului an x100Numărul <strong>de</strong> pacienţi cu LUTS cu IPSS ≥ 8în vîrstă <strong>de</strong> peste 40 <strong>de</strong> ani, care s-au adresatla medicul specialist (urolog) şi cărora lis-a efectuat tuşeul rectal, PSA, USG transrectalăa prostatei şi uroflowmetria, pe parcursulultimului an x 100Numărul <strong>de</strong> pacienţi cu AP, asociat cu complicaţiiacute, spitalizaţi în instituţia instituţiamedico-sanitară, pe parcursul ultimuluian x 100Numărul <strong>de</strong> pacienţi cu AP, trataţi conformprotocolului <strong>clinic</strong> naţional A<strong>de</strong>nomul <strong>de</strong>prostată în IMSP, pe parcursul ultimului anx 100Numărul <strong>de</strong> pacienţi cu AP, monitorizaţiconform protocolului <strong>clinic</strong> naţional A<strong>de</strong>nomul<strong>de</strong> prostată, <strong>de</strong> medicul specialist(urolog), pe parcursul ultimului an x 100Numărul <strong>de</strong> pacienţi cu LUTS,care se află sub supraveghereamedicului specialist (urolog),pe parcursul ultimului anNumărul <strong>de</strong> pacienţi cu LUTScu IPSS ≥ 8, în vîrstă <strong>de</strong> peste40 <strong>de</strong> ani, care se află sub supraveghereamedicului specialist(urolog), pe parcursul ultimuluianNumărul <strong>de</strong> pacienţi cu AP, spitalizaţiîn instituţia medico-sanitară,pe parcursul ultimuluianNumărul total <strong>de</strong> pacienţi cuAP, spitalizaţi în instituţia medico-sanitară,pe parcursul ultimuluianNumărul total <strong>de</strong> pacienţi cu APcare se află sub supraveghereamedicului specialist (urolog),pe parcursul ultimului an34
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009La momentul actual nu există meto<strong>de</strong> <strong>de</strong> profilaxie primară a a<strong>de</strong>nomului <strong>de</strong> prostată.Tehnicile existente pot ameliora simptomatologia din partea tractului urinar inferior. Modificărilerecomandate ale stilului <strong>de</strong> viaţă cuprind: limitarea aportului <strong>de</strong> lichid la nivel <strong>de</strong> 1,5 l, cu micşorareaconsumului înainte <strong>de</strong> somn sau în timpul activităţilor publice; limitarea sau evitarea consumului<strong>de</strong> alcool şi cafeinei, care au un efect diuretic şi iritant; aplicarea meto<strong>de</strong>i <strong>de</strong> urinare dublă pînăla evacuarea mai completă a urinei din vezica urinară; tehnici distractive (ex., respiraţie profundăetc.) pentru a controla mai bine simptomele iritative; suspendarea sau înlocuirea medicamentelorcu efect potenţial negativ asupra simptomatologiei a<strong>de</strong>nomului <strong>de</strong> prostată (ex., diuretice, antihistaminice);tratamentul condiţiilor, care agravează suplimentar evoluţia a<strong>de</strong>nomului <strong>de</strong> prostată:diabet zaharat, hipertensiune arterială, insuficienţă cardiacă congestivă, constipaţii.36
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Anexa 2. Formular pentru obţinerea <strong>de</strong> accord al pacientuluiN.P.P.AdresaPersoana şi telefonul <strong>de</strong>contactNr. poliţei <strong>de</strong> asigurareNr. buletinului <strong>de</strong>i<strong>de</strong>ntitateVîrstă/ sex/ invaliditateAcord privind aplicarea măsurilor diagnostice, terapeutice,anestezice, <strong>de</strong> reanimare şi a intervenţiei chirurgicale1. Autorizez medicul curant şi medicii din instituţia medicală să execute asupra mea procedurilediagnostice şi <strong>de</strong> tratament medical sau chirurgical, consi<strong>de</strong>rate necesare.2. Am fost informat privind etiologia, patogeneza, evoluţia, prognosticul şi complicaţiile posibileale traumatismului renal, cu specificarea particularităţilor cazului meu, necesitatea aplicăriimăsurilor diagnostice şi <strong>de</strong> tratament la fiecare etapă <strong>de</strong> acordare a ajutorului medical.Am primit răspuns la întrebările adresate.3. Am fost informat asupra naturii şi scopului procedurilor diagnostice şi terapeutice, a intervenţieichirurgicale, asupra beneficiilor şi prejudiciilor posibile privind complicaţiile şi riscurileposibile. Mi s-a răspuns la întrebările adresate.4. Sunt conştient că, în <strong>de</strong>cursul intervenţiei diagnostice, chirurgicale sau al unui act terapeuticpot apărea situaţii imprevizibile, care necesită proceduri diferite <strong>de</strong> cele preconizate. Consimtefectuarea intervenţiilor chirurgicale şi a procedurilor diagnostice, pe care medicii le consi<strong>de</strong>rănecesare.5. Privind intervenţia programată, <strong>de</strong>clar că am fost informat <strong>de</strong>spre tipul <strong>de</strong> anestezie, la carevoi fi supus şi <strong>de</strong>spre tehnicile <strong>de</strong> monitorizare a funcţiilor vitale. Mi s-a explicat că existăun risc în anumite complicaţii. Accept ca anesteziologul să modifice tratamentul anestezicprogramat.6. Rezultatele examinărilor, lichi<strong>de</strong>lor biologice, ţesuturilor sau al părţilor <strong>de</strong> organe, obţinute înurma intervenţiei chirurgicale sau a procedurii diagnostice, pot fi folosite în scopuri medicaleşi ştiinţifice.7. Fiind conştient <strong>de</strong> beneficiile şi <strong>de</strong> riscurile măsurilor diagnostice, terapeutice, anestezice, <strong>de</strong>reanimare, chirurgicale, le accept fără a solicita asigurări suplimentare în privinţa rezultatelor.8. Confirm că am citit şi am înţeles în întregime cele expuse mai sus.37
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009IndiceDataAcordul <strong>de</strong> obţinerea anamnezei şi<strong>de</strong> efectuare aexamenului fizicAcordul <strong>de</strong> efectuarea investigaţiilorinstrumentaleşi <strong>de</strong> laboratorAcordul <strong>de</strong> efectuarea tratamentuluinemedicamentosAcordul <strong>de</strong> efectuarea tratamentuluimedicamentosAcordul <strong>de</strong> efectuarea intervenţiilorchirurgicaleMedic<strong>de</strong> familieMedic <strong>de</strong>urgenţăNivel consultativspecializatNivel spitalicesc(inclusiv secţiispecializate)Notă: Dacă pacientul este inconştient şi la momentul implementării măsurilor diagnostice,terapeutice, anestezice, <strong>de</strong> reanimare, a intervenţiilor chirurgicale, atunci documentul este semnat<strong>de</strong> o persoană însoţitoare.38
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Anexa 3. Fişa <strong>de</strong> monitorizare a pacienţilor – formular <strong>de</strong> înregistrare aacţiunilor ulterioare referitoare la pacienţi, efectuate în baza protocoluluiN.P.P.AdresaPersoana, telefonul <strong>de</strong> contactNr. poliţei <strong>de</strong> asigurareNr. buletinului <strong>de</strong> i<strong>de</strong>ntitateVîrsta Sexul InvaliditateaÎnălţimeaIndiceNivelprespitalicescMasaNivel consultativspecializatNivel<strong>de</strong> staţionarDataSeveritatea APIPSSQoLComplicaţiiOraManifestarea <strong>clinic</strong>ăTA, PSHematuria, leucocituriaLeucocitoza, VSH-ulCreatinina, ureeaPSA, PSA fracţie liberăUSG prostateiUroflowmetriaTC (sau IRM)TratamentulconservatorTratamentul chirurgicalMedicul curantAsistenta medicală39
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Anexa 4. Sala <strong>de</strong> operaţii şi instrumentele chirurgicale• Sala <strong>de</strong> operaţii, asigurată cu apă (rece şi caldă), încălzire, sistem <strong>de</strong> ventilaţie Lampă chirurgicală Masă chirurgicală (funcţională) Lămpi UV• Instrumentele chirurgicale Coagulator Bisturii Pense Coher, Mosquit, Fiodorov Foarfece curbe şi drepte Depărtătoare Son<strong>de</strong> Seringă Janet• Material <strong>de</strong> sutură Catgut nr. 1, 2, 3, 4, 5, 6 Vikril 000 Mătase nr. 1, 2, 3, 4, 5, 6 Capron nr. 1, 2, 3, 4, 5, 6• Mijloacele <strong>de</strong> protecţie (pentru fiecare chirurg, asistentă medicală din sala <strong>de</strong> operaţie,infirmieră) Halat Costum chirurgical Mască Mănuşi Ochelarii <strong>de</strong> protecţie Bahile• Consumabile (sterile <strong>de</strong> unică folosinţă sau sterilizate) Biurete hemostatice Drenuri Seringi Ace chirurgicale Ace vasculare Sisteme <strong>de</strong> perfuzii Catetere ureterale 4, 5, 6 Catetere Foley 20, 22 Catetere Petzer 28, 30, 32 Faşă Tamponaşe Tifon Şerveţele• Instrumentar şi set <strong>de</strong> medicamente necesare pentru efectuarea anesteziei locale şigenerale (conform standar<strong>de</strong>lor naţionale corespunzătoare)• Set antişoc (vezi D.1)• Alcool etilic 96%, alcool etilic 70%• Iod, Betadină• Dezinfectante40
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009Anexa 5. Scorurile pentru aprecierea gravităţii a<strong>de</strong>nomului <strong>de</strong> prostatăTabelul 11. Evaluarea scorului IPSS (Scorul International al Simptomelor Prostatice –International Prostate Symptom Score) [5]Scorul simptomelorÎn ultima lună, cît <strong>de</strong> <strong>de</strong>s aţi avutsenzaţia că nu aţi golit completvezica după ce aţi terminat <strong>de</strong>urinat?În ultima lună, cît <strong>de</strong> <strong>de</strong>s a trebuitsă urinaţi din nou la maipuţin 2 ore după ultima urinare?În ultima lună, cît <strong>de</strong> <strong>de</strong>s s-a întîmplatcă, în timp ce urinaţi, săse oprească jetul pentru că apoisă se reia?În ultima lună, cît <strong>de</strong> <strong>de</strong>s vi s-apărut dificil să amînaţi urinatul?În ultima lună, cît <strong>de</strong> <strong>de</strong>s aţi avutun jet urinar slab?În ultima lună, cît <strong>de</strong> <strong>de</strong>s a trebuitsă împingeţi sau să forţaţiînceputul urinatului?Deloc Mai puţin<strong>de</strong> o datăpe ziMai puţin<strong>de</strong> ½ dintimpAproximativ½din timpMai mult<strong>de</strong> ½ dintimpAproapeîntot<strong>de</strong>auna0 1 2 3 4 50 1 2 3 4 50 1 2 3 4 50 1 2 3 4 50 1 2 3 4 50 1 2 3 4 5În ultima lună, <strong>de</strong> cîte ori v-aţitrezit să urinaţi noaptea? <strong>de</strong>loc 1 dată <strong>de</strong> 2 ori <strong>de</strong> 3 ori <strong>de</strong> 4 oriScorul total IPSS =Tabelul 12 In<strong>de</strong>x <strong>de</strong> evaluare a calităţii vieţii [5]Calitatea vieţii înfuncţie <strong>de</strong> simptomelorurinareDacă ar fi să vă petreceţitot restul vieţiiîn situaţia actualăScorul total QoL =ÎncîntatSatisfăcutMai multsatisfăcătorSatisfăcut şinesatisfăcut înegală măsură<strong>de</strong> 5sau maimulte oriMai multnesatisfăcutNefericitÎngrozitor0 1 2 3 4 5 6Clasificarea AP conform severităţii (American Association of Urology 2003/2006):• Uşoară (gradul I): IPSS = 0-7, QoL = 0-2. Absenţa complicaţiilor APPacientul cu IPSS > 7 sau Qol > 2 este îndreptat la urolog pentru evaluarea AP• Medie (gradul II): IPSS = 8-19, QoL = 3-4. Eventual, prezenţa complicaţiilor cronice ale AP;• Severă (gradul III): IPSS = 20-35, QoL = 5-6. Prezenţa complicaţiilor cronice ale AP.Eventual, prezenţa complicaţiilor acute.41
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 2009BIBLIOGRAFIE1. Aarnink R., Beerlage H., <strong>de</strong> la Rosette J. et al. Transrectal ultrasound of the prostate:innovations and future applications // J. Urol., 1998; 159(5): 1568-1579.2. An<strong>de</strong>rson J., Roehrborn C., Schalken J. et al. The progression of benign prostatic hyperplasia:examining the evi<strong>de</strong>nce and <strong>de</strong>termining the risk // Eur. Urol., 2001; 39(4): 390-399.3. Andriole G., Guess H., Epstein J. et al. Treatment with finasteri<strong>de</strong> preserves usefulness ofprostate specific antigen in the <strong>de</strong>tection of prostate cancer: results of a randomized, doubleblind,placebo-controlled <strong>clinic</strong>al trial // Urology, 1998; 52(2): 195-201.4. Andriole G., Kirby R. Safety and tolerability of the Dual 5 alpha-Reductase Inhibitordutasteri<strong>de</strong> in the treatment of benign prostatic hyperplasia // Eur. Urol., 2003; 44(1): 82-88.5. AUA practice gui<strong>de</strong>line committee. AUA gui<strong>de</strong>lines on management of benign prostatichyperplasia // American Urological Association Education and Research, Inc., J. Urol., 2003;170(2 Pt 1): 530-547 / Updated 2006.6. Barkin J., Guimaraes M., Jacobi G. et al. Alpha-blocker therapy can be withdrawn in themajority of men following initial combination therapy with the dual 5-alphareductase inhibitordutasteri<strong>de</strong> // Eur. Urol., 2003; 44(4): 461-466.7. Barry M., Fowler F., O’Leary M. et al. The American Urological Association Symptom In<strong>de</strong>xfor benign prostatic hyperplasia // J. Urol., 1992; 148: 1549-1557.8. Boyle P. Epi<strong>de</strong>miology of benign prostatic hyperplasia: risk factors and concomitance withhypertension // Br. J. Clin. Pract. Suppl., 1994; 74: 18-22.9. Chute C., Panser L., Girman C. et al. The prevalence of prostatism: a population based surveyof urinary symptoms //. J. Urol., 1993; 150(1): 85-89.10. Dahlstrand C., Wal<strong>de</strong>n M., Deirsson G. et al. Transurethral microwave thermotherapy versustransurethral resection for symptomatic benign prostatic obstruction: a prospective randomizedstudy with a 2-year follow-up // Br. J. Urol., 1995; 76(5): 614-618.11. Debruyne F. Alpha blockers: are all created equal? // Urology. 2000; 56(5 Suppl 1): 20-2.12. <strong>de</strong> la Rosette J., Alivizatos G., Ma<strong>de</strong>rsbacher S. et al. Gui<strong>de</strong>lines on Benign ProstaticHyperplasia // European Association of Urology, 2008, 60 pp.13. El Din K., <strong>de</strong> Wildt M., Rosier P. et al. The correlation between urodynamic and cystoscopicfindings in el<strong>de</strong>rly men with voiding complaints // J. Urol., 1996; 155(3): 1018-1022.14. Epstein R., Lydick E., <strong>de</strong> Labry L. et al. Age-related differences in risk factors for prostatectomyfor benign prostatic hyperplasia: the VA Normative Aging Study // Urology 1991; 38(Suppl.1): 9-12.15. Fagelman E., Lowe F. Herbal medications in the treatment of benign prostatic hyperplasia(BPH) // Urol. Clin. North. Am., 2002; 29(1): 23-239.16. Flanigan R., Reda D., Wasson J. et al. 5-year outcome of surgical resection and watchful waitingfor men with mo<strong>de</strong>rately symptomatic BPH: a <strong>de</strong>partment of Veterans Affairs cooperative study// J. Urol., 1998; 160(1): 12-1.17. Gallucci M., Puppo P., Perachino M. et al. Transurethral electrovaporization of the prostate vs.transurethral resection. Resection of a multicentric, randomised <strong>clinic</strong>al study on 150 patients// Eur. Urol., 1998; 33(4): 359-364.18. Girman C., Jacobsen S., Guess H. et al. Natural history of prostatism: relationship amongsymptoms, prostate volume and peak urinary flow // J. Urol., 1995; 153(5): 1510-1515.19. Grino P., Bruskewitz R., Blaivas J. et al. Maximum urinary flow rate by uroflowmetry: automaticor visual interpretation // J. Urol., 1993; 149(2): 339-341.20. Hartung R., Leyh H., Liapi C. et al. Coagulating intermittent cutting. Improved highfrequencysurgery in transurethral prostatectomy, Eur. Urol., 2001; 39(6): 676-681.42
<strong>Protocol</strong> <strong>clinic</strong> naţional „A<strong>de</strong>nomul <strong>de</strong> prostată”, Chişinău 200941. Roehrborn C., Boyle P., Bergner D. et al. PLESS Study Group Serum prostate-specific antigenand prostate volume predict long-term changes in symptoms and flow rate: results of a fouryear,randomized trial comparing finasteri<strong>de</strong> versus placebo // Urology, 1999; 54(4): 662-669.42. Scheckowitz E., Resnick M. Imaging of the prostate. Benign prostatic hyperplasia // Urol.Clin. North. Am., 1995; 22(2): 321-332.43. Tkocz M., Prajsner A. Comparison of long-term results of transurethral incision of the prostatewith transurethral resection of the prostate, in patients with benign prostatic hypertrophy //Urol., 2002; 21(2): 112-116.44. Van Venrooij G., Eckhardt M., Gisholf K. et al. Data from frequency-volume charts versussymptom scores and quality of life score in men with lower urinary tract symptoms due tobenign prostatic hyperplasia // Eur. Urol., 2001; 39(1): 42-47.45. Vaughan D., Imperato-McGinley J., McConnell J. et al. Long-term (7 to 8-year) experiencewith finasteri<strong>de</strong> in men with benign prostatic hyperplasia // Urology, 2002, 60(6): 1040-1044.46. Vesely S., Knutson T., Damber J. et al. Relationship between age, prostate volume, prostatespecificantigen, symptom score and uroflowmetry in men with lower urinary tract symptoms //Scand. J. Urol. Nephrol., 2003; 37(4): 322-328.47. Wilkinson A., Wild S. Is pre-operative imaging of the urinary tract worthwhile in the assessmentof prostatism? Br. J. Urol., 1992; 70(1): 53-57.48. Wilkinson A., Wild S. Survey of urological centres and review of current practice in the preoperativeassessment of prostatism // Br. J. Urol., 1992; 70(1): 43-45.49. Wilt T., Ishani A., Mac Donald R. et al. Pygeum africanum for benign prostatic hyperplasia //Cochrane Database Syst. Rev., 2002; (1): CD001044.50. Wilt T., Ishani A., Stark G. et al. Serenoa repens for benign prostatic hyperplasia // CochraneDatabase Syst. Rev., 2000; (2): CD001423.51. Zlotta A., Giannakopoulos X., Maehlum O. et al. Long-term evaluation of transurethral needleablation of the prostate (TUNA) for treatment of symptomatic benign prostatic hyperplasia:<strong>clinic</strong>al outcome up to five years from three centers // Eur. Urol., 2003; 44(1): 89-93.44