Anorganische Nomenklatur nach IUPAC – Vergleichende ...
Anorganische Nomenklatur nach IUPAC – Vergleichende ...
Anorganische Nomenklatur nach IUPAC – Vergleichende ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
fertig<br />
Spezielle Ligand-<br />
Kenntzeichungen:<br />
verbrückend: !<br />
mehrfach: "<br />
Benutze den<br />
vollen Elementnamen<br />
des ZA<br />
ohne Endung<br />
Benutze den<br />
Elementstamm<br />
des ZA und die<br />
Endung -id<br />
Benutze den<br />
Elementstamm<br />
des ZA und die<br />
Endung -at<br />
fertig<br />
Mehr als ein Ligand<br />
gleicher Art<br />
erhält einen MP<br />
Alle Ligandnamen<br />
ohne MP<br />
werden alphabetisch<br />
geordnet<br />
Ausgewählte<br />
Trivialnamen<br />
für Liganden:<br />
H2O: aqua<br />
OH!: hydroxido<br />
CN !: cyanido<br />
NH3 : ammin<br />
CO: carbonyl<br />
NO: nitrosyl<br />
SCN!: thiocyanato<br />
SCN!: isothiocyanato<br />
ja<br />
ja<br />
Ist der Ligand<br />
neutral oder positiv geladen<br />
und das ZA<br />
ein Metall?<br />
nein<br />
Hänge ein -o<br />
an den<br />
Ligandnamen<br />
Besteht das<br />
Ion aus einer Sorte<br />
Element?<br />
nein<br />
nein<br />
ja<br />
Ist die<br />
Verbindung<br />
radikalisch?<br />
ja<br />
Setze die Anz.<br />
ungepaarter e!<br />
in die Klammer<br />
Finde den<br />
Ligandnamen<br />
analog zum ZA<br />
oder als<br />
Trivialnamen<br />
nein<br />
Ist die<br />
Verbindung negativ<br />
geladen?<br />
Setze die<br />
Ladung der Verb.<br />
in die Klammer<br />
nein<br />
nein<br />
Mehr als ein ZA<br />
erhält einen<br />
MP<br />
Behandle jeden<br />
Ligand-Typ<br />
einzeln<br />
ja<br />
Gibt es mehrere<br />
verschiedene<br />
Liganden?<br />
Ist die<br />
Verbindung ein<br />
neutraler oder anionischer<br />
Metallkomplex?<br />
Setze keine<br />
Klammer<br />
ja<br />
ja<br />
Das Atom (ausser<br />
Wasserstoff) mit<br />
der kleinsten EN<br />
ist das ZA<br />
Ausgewählte<br />
Stammnamen:<br />
H: Hydr-<br />
B: Bor-<br />
C: Carbid / Carbonat<br />
N: Nitr-<br />
O: Oxid(o) / Oxigenat<br />
F: Fluor-<br />
Al: Alumin-<br />
Si: Silic-<br />
P: Phosph-<br />
S: Sulf-<br />
Cl: Chlor-<br />
Fe: Ferr-<br />
Cu: Cupr-<br />
Zn: Zinc-<br />
Mo: Molybd-<br />
Ag: Argent-<br />
Sn: Stann-<br />
Sb: Stib-<br />
Ir: Irid-<br />
Au: Aur-<br />
Hg: Mercur-<br />
Pb: Plumb-<br />
nein<br />
fertig<br />
Setze keine<br />
Klammer<br />
nein<br />
Gibt es Liganden?<br />
(andere Elemente<br />
als das ZA)<br />
Ist die<br />
Verbindung<br />
ungeladen?<br />
ja<br />
EN: Elektronegativität<br />
(siehe Periodensystem)<br />
MP: Multiplikationspräfix<br />
bi-, tri-, tetra-, … bei<br />
Zweideutigkeit auch<br />
bis-, tris-, tetrakis, …<br />
ZA: Zentralatom oder -ion<br />
2. LIGANDENNAMEN: 1. STAMM: 3. KLAMMER:<br />
Ligandnamenstamm()<br />
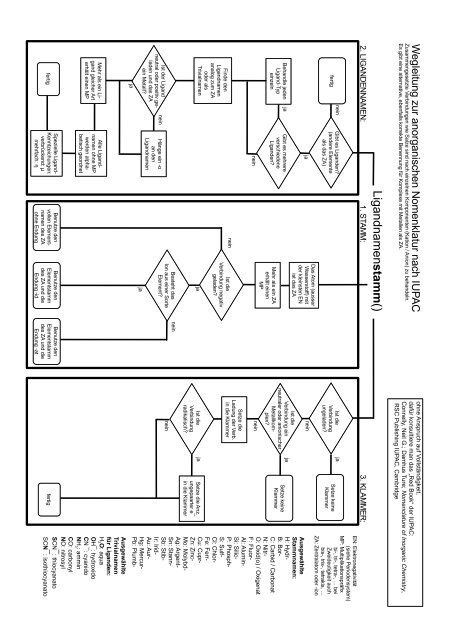
Zusammengesetzte Verbindungen wie Salze sind <strong>nach</strong> einzelnen Komponenten (Kation / Anion) zu behandeln.<br />
Es gibt eine alternative, ebenfalls korrekte Benennung für Komplexe mit Metallen als ZA.<br />
Wegleitung zur anorganischen <strong>Nomenklatur</strong> <strong>nach</strong> <strong>IUPAC</strong><br />
ohne Anspruch auf Vollständigkeit,<br />
dafür konsultiere man das „Red Book“ der <strong>IUPAC</strong>:<br />
Connelly, Neil G.; Damhus Ture; Nomenclature of Inorganic Chemistry,<br />
RSC Publishing <strong>IUPAC</strong>, Cambridge