(十) 恆溫控制器: 美國Eppendorf 公司(十一) 恆溫水浴加熱器: Hotech ...
(十) 恆溫控制器: 美國Eppendorf 公司(十一) 恆溫水浴加熱器: Hotech ...
(十) 恆溫控制器: 美國Eppendorf 公司(十一) 恆溫水浴加熱器: Hotech ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
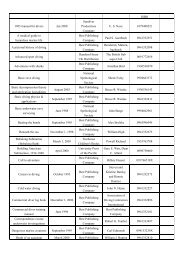
(<strong>十</strong>) <strong>恆溫控制器</strong>: 美國 Eppendorf <strong>公司</strong><br />
(<strong>十</strong>一) <strong>恆溫水浴加熱器</strong>: <strong>Hotech</strong> <strong>公司</strong><br />
(<strong>十</strong>二) SDS-PAGE 電泳槽:Bio-Rad <strong>公司</strong><br />
(<strong>十</strong>三) Protein wet transfer tank: 英國 Amersham <strong>公司</strong><br />
(<strong>十</strong>四) 組織均質機(PT-2100): 瑞典 POLYTRON <strong>公司</strong><br />
(<strong>十</strong>五) Tubes for reporter assay: 德國 SARSETEDT <strong>公司</strong><br />
(<strong>十</strong>六) 培養皿、離心管:NUNC <strong>公司</strong><br />
第二節 實驗方法<br />
壹、細胞培養:<br />
H1299 與 Saos-2 細胞從液態氮保存筒中取出解凍後,均<br />
培養在細胞培養專用的培養皿中,H1299 細胞以含高葡萄糖的<br />
Dulbecco modified eagle medium(DMEM),加入 10% 胎牛血<br />
清(fetal bovine serum)、2 mM L-Glutamine 培養之,同時<br />
每毫升培養液中加入 100 units penicillin 及 100 units<br />
streptomycin。Saos-2 細胞以 McCoy's 5A medium modified,<br />
加入 15% 胎牛血清、2 mM L-Glutamine 培養之,同時每毫升<br />
的培養液中加入 100 units penicillin 及 100 units<br />
streptomycin。兩種細胞皆置於 37℃、5% CO2、濕度為 95%的<br />
培養箱中進行培養,並每隔 2~3 天更換一次培養液。待細胞長<br />
滿培養皿後,以胰蛋白酶(Trypsin/EDTA)將細胞分盤繼代培養<br />
或供給實驗之使用。細胞形態的觀察以光學顯微鏡為之。<br />
- 10 -
貳、細胞轉染(transfection)<br />
10 5<br />
在轉染細胞之前 24 小時,將細胞以每個培養皿約有 1~3×<br />
細胞的數目(滿度約為 50~80%)分至 35 mm 細胞培養皿中進<br />
行培養。隔日,進行轉染前先取 97 μl 不含胎牛血清的 DMEM<br />
置於微量離心管內,再取 3 μl FuGENE 6 transfection<br />
reagent 一滴滴加入 DMEM 中並輕輕混和均勻,之後於室溫下<br />
靜置 5 分鐘。5 分鐘後,把 Fugene 6 與 DMEM 的混合液一滴滴<br />
緩緩加入含有 1μg,濃度約為 0.1~2 μg/μl 之待轉染的 DNA<br />
溶液中混和均勻,並於室溫中靜至 20 分鐘。靜置時間到後,<br />
將 DNA、Fugene 6 與 DMEM 的混合液一滴一滴緩緩加入至之前<br />
已分盤之待轉染細胞的細胞培養液中。均勻混合後,將培養皿<br />
放入 37℃,5% CO2的培養箱中培養至所需的時間。<br />
參、腺病毒感染細胞傳遞 DNA<br />
利用腺病毒(adenovirus)感染(infect)細胞之前 24 小<br />
時,先將每盤預備感染之細胞的滿度調整至培養皿面積的<br />
50~60 %。進行感染時,先將培養皿中的細胞培養液抽乾,加<br />
入原本體積<strong>十</strong>分之二量的新鮮細胞培養液至培養皿內,之後再<br />
加入實驗設計所需數量的腺病毒至細胞培養液中並混合均<br />
勻。此後,每半個小時搖晃混合培養液一次,並於搖晃四次(即<br />
兩個小時)後加入原本體積<strong>十</strong>分之三量的新鮮細胞培養液至培<br />
養皿內。此時,培養皿內的細胞培養液約為原本體積的二分之<br />
一,以此量的細胞培養液持續培養同時感染細胞 8 小時,期間<br />
不需搖晃培養皿。直至 8 小時後(感染後第 10 個小時)補充細<br />
- 11 -
胞培養液(二分之一)至原本培養細胞所需的體積,並培養細胞<br />
到實驗設計所需的時間。<br />
肆、西方點墨法(Western blot analysis)<br />
將養在培養皿內的細胞以 PBS 清洗二次後,取適量事前先<br />
加入蛋白酶抑制劑(protease inhibitors)的 RIPA 緩衝液溶解<br />
細胞 5~10 分鐘。之後,將溶解完全的細胞溶液吸取至微量離<br />
心管中置於冰上。利用超音波震碎機震盪之前收集到的細胞溶<br />
液約 5 分鐘,以達到完全萃取蛋白質的目的。震盪過後,以<br />
13,200 rpm 的速度離心細胞溶液 5 分鐘,於離心後吸取出上<br />
清液置於新的微量離心管內,並按照一定的比例加入聚丙烯醯<br />
胺蛋白質電泳染劑(SDS-PAGE loading dye),均勻混合後於<br />
95℃下加熱 5 分鐘。取適量已製備完成的蛋白質樣品以適當濃<br />
度的凝膠進行聚丙烯醯胺蛋白質電泳分析(SDS-PAGE)。電泳結<br />
束後,利用濕式轉印裝置(wet-transfering aparatus)將該凝<br />
膠上的蛋白質轉印(transfer)到硝化纖維膜(nitrocellulose<br />
membrane)上。轉印結束,在室溫下將轉印膜泡在 5 %脫脂奶<br />
粉溶於 PBS/Tween 20 緩衝液的阻隔緩衝液(blocking buffer)<br />
中 1 小時。阻隔(blocking)結束後,以阻隔緩衝液稀釋一級抗<br />
體(primary antibody)到適用的比例,並將阻隔後的轉印膜浸<br />
泡在該稀釋過的一級抗體緩衝液中,於 4℃下放置隔夜。隔日,<br />
取出轉印膜並以 PBS/Tween 20 緩衝液清洗三次。之後,以阻<br />
隔緩衝液稀釋二級抗體(secondary antibody)到適用的比<br />
例,並將轉印膜浸泡在該稀釋過的二級抗體緩衝液中,於室溫<br />
下放置 1 小時。時間到後,取出轉印膜並以 PBS/Tween 20 緩<br />
- 12 -
衝液清洗三次。最後,將轉印膜以 ECL 西方點墨偵測試劑(ECL<br />
western blotting detection reagent)浸泡 1 分鐘,並移至<br />
暗房中以 X 光底片感光適當的時間後沖片顯像。<br />
伍、純化 PIP 蛋白質與胺基酸定序前置工作<br />
取 4 隻出生後 5~7 週大的小鼠解剖後取出心臟,並將心臟<br />
切開泡在 PBS 中洗去殘留的血液。之後,把心臟切碎集中放置<br />
到試管內並加入取適量事前先加入蛋白酶抑制劑的冰的組織<br />
均質緩衝液(homogenization buffer)中。接著置於冰上,並<br />
利用組織均質機以 15 秒為間隔打碎心臟樣品 4 次使之均質<br />
化。均質後,加入與組織均質緩衝液等量並且已加入蛋白酶抑<br />
制劑的 RIPA 緩衝液,混合後靜置於冰上 5~10 分鐘。之後,利<br />
用超音波震碎機震盪心臟樣品溶液約 5 分鐘,以達到完全萃取<br />
蛋白質的目的。震盪過後,以 15,000 rpm 的速度離心心臟樣<br />
品溶液 30 分鐘,於離心後吸取出上清液置於新的離心試管<br />
內。取適量 PIP 抗體加入收集到的心臟上清液中,於 4℃下,<br />
旋轉混合 1 小時。一小時後,加入適量的免疫沉澱小球<br />
(protein A/G plus-agarose/Santa Cruz)並於 4℃下旋轉混<br />
合 3 小時。時間結束後,離心沉澱免疫沉澱小球同時吸去上清<br />
液。之後,按照 PBS、RIPA、RIPA、PBS 的順序清洗小球 4 次,<br />
在最後一次離心後吸去上清液並加入適量聚丙烯醯胺蛋白質<br />
電泳染劑,均勻混合後於 95℃下加熱 10 分鐘。加熱完畢後,<br />
離心沉澱小球並取適量已製備完成的蛋白質樣品以適當濃度<br />
的凝膠進行聚丙烯醯胺蛋白質電泳分析。電泳結束後,利用濕<br />
式轉印裝置將該凝膠上的蛋白質轉印到 PVDF 膜(PVDF<br />
- 13 -
membrane)上。轉印結束,利用考馬斯亮藍 R-250(Coomassie<br />
Blue R-250)染 PVDF 膜使膜上蛋白呈色,並以甲醇(methanol)<br />
及醋酸(acetic acid)退染之。最後,以純水洗去多餘的退染<br />
液並剪下欲送交定序的蛋白質區塊置於微量離心管中保存在<br />
4℃下,即可送交定序。<br />
陸、細胞週期分析(Cell cycle analysis)<br />
以培養皿培養細胞至適當的時間並到達可供分析的滿<br />
度。吸取出培養皿中培養液置於 15 ml 離心管中,並以 PBS 清<br />
洗細胞一次。之後,加入適量的胰蛋白脢處理細胞 2~5 分鐘,<br />
把細胞從培養皿上分離下來並盡量將細胞沖吸成單一細胞。接<br />
著把單一細胞懸浮液吸出培養皿加到之前取出培養液的 15 ml<br />
離心管中,以 1,000 rpm 的速度離心細胞 5 分鐘。離心結束後,<br />
吸出不要的培養液並以 PBS 清洗及離心沉澱細胞兩次。最後,<br />
將細胞懸浮於 5 ml 冰的 70%酒精中,於 4℃下放置隔夜。隔<br />
日,以 2,000 rpm 的速度離心 10 分鐘沉澱細胞,接著吸去不<br />
要的酒精,並以含有 0.1%牛血清(bovine calf serum)的冰<br />
PBS 清洗及離心沉澱細胞兩次。之後,將細胞懸浮於以 PBS 稀<br />
釋成 50%的 DNA 析出緩衝液(DNA extraction buffer)中,並<br />
於室溫下靜置 5 分鐘後離心沉澱細胞。最後,吸去 DNA 析出緩<br />
衝液並將細胞懸浮於適量的 PI 溶液(propidium iodide<br />
solution)中,在室溫下避光 30 分鐘後置於冰上等待分析。時<br />
間到後,將細胞懸浮液通過濾網除去過大的顆粒雜質,並以流<br />
式細胞儀(FACS Calibur/Becton Dickinson)分析細胞周期分<br />
佈(cell cycle profiles)狀況。<br />
- 14 -
柒、螢光素酶報導基因分析( luciferase reporter gene assay)<br />
將欲使用的細胞分盤培養至 50~80%的滿度,之後利用腺<br />
病毒按照實驗設計分別感染細胞將 PIP 或 p53 基因送入細胞中<br />
表達。在腺病毒感染細胞 4 小時後,利用 Fugene 6 轉染細胞<br />
送進螢光素酶報導基因(luciferase reporter gene)與半乳糖<br />
苷酶基因(β-galactosidase gene),接著繼續培養細胞 24 小<br />
時。24 小時後,吸去培養皿中的培養液並以 PBS 清洗細胞兩<br />
次後加入蟲螢光素酶報導基因分析配件組(Luciferase<br />
reporter gene assay kit/Roche)中的細胞溶解緩衝液(lysis<br />
buffer)溶解細胞五分鐘。之後,將溶解完全的細胞溶液吸取<br />
至微量離心管中以 13,200 rpm 的速度離心細胞溶液 2 分鐘,<br />
並於離心後吸取出上清液置於新的微量離心管內放在冰上保<br />
存等待分析。分析蟲螢光素酶活性時,取一冷光分析專用的試<br />
管 (SARSETEDT) 先 加 入 35 μl 的螢光素酶分析試劑<br />
(luciferase assay reagent),接著加入 15 μl 的待測細胞<br />
上清液並於快速混合後插入冷光分析儀(BERTHOLD)中分析樣<br />
品的發光量,即為螢光素酶的活性。同一細胞上清液可利用<br />
ONPG(o-nitrophenyl-β-D-galactopyranoside)當作半乳糖苷<br />
酶的受質,測其在波長 420 nm 下的吸光值,即為半乳糖苷酶<br />
的活性。半乳糖苷酶的活性可用來當作評估細胞轉染效率的指<br />
標,並用來校正不同細胞溶液樣品間蟲螢光素酶的活性大小。<br />
- 15 -