B II - 1 - Überführungszahlen und Wanderungsgeschwindigkeit
B II - 1 - Überführungszahlen und Wanderungsgeschwindigkeit
B II - 1 - Überführungszahlen und Wanderungsgeschwindigkeit
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
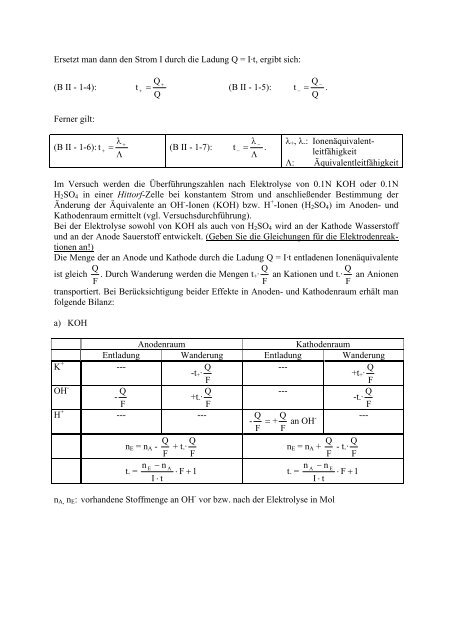
Ersetzt man dann den Strom I durch die Ladung Q = I·t, ergibt sich:<br />
(B <strong>II</strong> - 1-4):<br />
Ferner gilt:<br />
Q +<br />
t + = (B <strong>II</strong> - 1-5):<br />
Q<br />
λ<br />
(B <strong>II</strong> - 1-6): =<br />
Λ<br />
+<br />
t +<br />
(B <strong>II</strong> - 1-7):<br />
λ<br />
=<br />
Λ<br />
−<br />
t − .<br />
Q −<br />
t − = .<br />
Q<br />
λ+, λ-: Ionenäquivalentleitfähigkeit<br />
Λ: Äquivalentleitfähigkeit<br />
Im Versuch werden die <strong>Überführungszahlen</strong> nach Elektrolyse von 0.1N KOH oder 0.1N<br />
H2SO4 in einer Hittorf-Zelle bei konstantem Strom <strong>und</strong> anschließender Bestimmung der<br />
Änderung der Äquivalente an OH - -Ionen (KOH) bzw. H + -Ionen (H2SO4) im Anoden- <strong>und</strong><br />
Kathodenraum ermittelt (vgl. Versuchsdurchführung).<br />
Bei der Elektrolyse sowohl von KOH als auch von H2SO4 wird an der Kathode Wasserstoff<br />
<strong>und</strong> an der Anode Sauerstoff entwickelt. (Geben Sie die Gleichungen für die Elektrodenreaktionen<br />
an!)<br />
Die Menge der an Anode <strong>und</strong> Kathode durch die Ladung Q = I·t entladenen Ionenäquivalente<br />
Q Q Q<br />
ist gleich . Durch Wanderung werden die Mengen t+· an Kationen <strong>und</strong> t-· an Anionen<br />
F<br />
F<br />
F<br />
transportiert. Bei Berücksichtigung beider Effekte in Anoden- <strong>und</strong> Kathodenraum erhält man<br />
folgende Bilanz:<br />
a) KOH<br />
K +<br />
OH -<br />
H +<br />
Anodenraum Kathodenraum<br />
Entladung Wanderung Entladung Wanderung<br />
---<br />
Q<br />
-t+·<br />
F<br />
---<br />
Q<br />
+t+·<br />
F<br />
Q<br />
-<br />
F<br />
Q<br />
+t-·<br />
F<br />
---<br />
Q<br />
-t-·<br />
F<br />
--- ---<br />
---<br />
Q Q -<br />
- = + an OH<br />
F F<br />
Q Q<br />
nE = nA - + t-·<br />
F F<br />
Q Q<br />
nE = nA + - t-·<br />
F F<br />
n E − n A<br />
t- = ⋅ F + 1<br />
I ⋅ t<br />
n A − n E<br />
t- = ⋅ F + 1<br />
I ⋅ t<br />
nA, nE: vorhandene Stoffmenge an OH - vor bzw. nach der Elektrolyse in Mol