Nafest + ½ Cl2 NaClKristall 1 5 NaGas + ClGas _ _ 3 _ + _ _ 4 _ _ _ 2
Nafest + ½ Cl2 NaClKristall 1 5 NaGas + ClGas _ _ 3 _ + _ _ 4 _ _ _ 2
Nafest + ½ Cl2 NaClKristall 1 5 NaGas + ClGas _ _ 3 _ + _ _ 4 _ _ _ 2
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
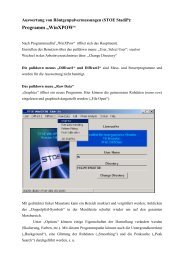
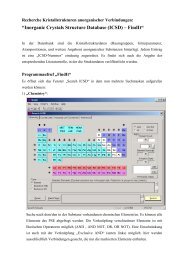
Aufgabe 1: Geben Sie den Born-Haber-Kreisprozess für die Bildung von NaCl wieder und stellen Sie die<br />
Gleichung zur Bestimmung der Gitterenergie auf.<br />
max. Punktzahl: 5<br />
Bildungsenthalpie<br />
BH<br />
<strong>Nafest</strong> + <strong>½</strong> <strong>Cl2</strong><br />
<strong>NaClKristall</strong><br />
Sublimationsenthalpie SH(Na)<br />
1<br />
5<br />
<strong>NaGas</strong> + <strong>ClGas</strong><br />
_ _ 3 _ + _ _ 4 _ _ _<br />
Elektronenaffinität<br />
EA<br />
b) Wie heißt der in a) angegebene Kreislauf.<br />
c) Berechnen Sie die Gitterenergie von NaCl in kJ/mol.<br />
SH(Na) = + 109 kJ/mol; I(Na) = + 496 kJ/mol; <strong>½</strong> Hdiss(<strong>Cl2</strong>): + 122 kJ/mol;<br />
EA: – 348 kJ/mol; BH = – 411 kJ/mol.<br />
max. Punktzahl: 4<br />
Aufgabe 2: Zeigen Sie anhand eines MO-Diagramms der Valenzelektronen, welchen Magnetismus Sauerstoff<br />
hat (Beschriftung der AO’s und MO’s) und geben Sie die Bindungsordnung molekularen<br />
Sauerstoffs an.<br />
max. Punktzahl: 4<br />
Aufgabe 3: a) Geben Sie die Valenzstrichformeln nach Lewis folgender Anionen an: Sulfit, Thiosulfat und<br />
Nitrit und geben Sie die Oxidationszahlen sämtlicher Atome an.<br />
b) IF3 ist nicht trigonal-planar aufgebaut. Geben Sie die nach der VSEPR-Theorie maßgeblichen<br />
Gründe dafür an. Bestimmen Sie mit Hilfe dieser Theorie die wahre Gestalt des Moleküls.<br />
max. Punktzahl: 5<br />
Aufgabe 4: Erklären Sie mit Hilfe der Quantenzahlen den Aufbau des Periodensystems. Beantworten Sie dazu<br />
folgende Fragen: Warum stehen in der ersten obersten Zeile nur zwei Elemente, in der<br />
zweitobersten 8?<br />
Wieso werden in der 4. Zeile zehn weitere Elemente eingebaut? Warum gibt es exakt 14<br />
Lanthanoid-Elemente und nicht 13 oder 15?<br />
max. Punktzahl: 3<br />
Aufgabe 5: a) Erklären Sie, warum Fe(III)-Salz-Lösungen sauer reagieren? (Reaktionsgleichung)<br />
b) Warum ist Borsäure eine Säure? Geben Sie die Reaktionsgleichung dazu an!<br />
max. Punktzahl: 2<br />
Aufgabe 6: a) Zur Darstellung von chemischen Elementen benutzt man in der Technik in Abhängigkeit von<br />
der zu reduzierenden Verbindung unterschiedliche Reduktionsmittel. Womit reduziert man<br />
1) SiO2, 2) SiCl4, 3) KCl bzw. 4) NaCl. Formulieren Sie jeweils die entsprechenden<br />
Reaktionsgleichungen mit Angabe der sich ändernden Oxidationszahlen.<br />
b) Beschreiben Sie anhand von Reaktionsgleichungen die Darstellung von Pb nach dem Röst-<br />
Reaktions- bzw. Röst-Reduktionsverfahren (ein Verfahren reicht).<br />
max. Punktzahl: 7<br />
Aufgabe 7: a) Ordnen Sie den Brandklassen A, B, C, D die zu löschenden Stoffklassen zu.<br />
b) Geben Sie für die folgenden Gefahrensymbole die jeweils rechtsgültige Beschreibung an: F+, E,<br />
N, Xn.<br />
max. Punktzahl: 4<br />
Aufgabe 8: a) Geben Sie die Reaktionsgleichung zur Entstehung von Schwefelwasserstoff aus Thioacetamid an<br />
(Lewis-Formel) und erläutern Sie die pH-Abhängigkeit der Sulfidfällung.<br />
b) Erläutern Sie anhand von Reaktionsgleichungen, weshalb bei der Urotropin-Fällung Hydroxide<br />
ausfallen.<br />
max. Punktzahl: 4<br />
Aufgabe 9: a) Formulieren Sie das Chromat-Dichromat-Gleichgewicht.<br />
b) Geben Sie die Reaktionsgleichung für die Reaktion von Chromat mit Ethanol an.<br />
c) Erläutern Sie anhand des Chromations die pH-Abhängigkeit von Redoxpotenzialen.<br />
max. Punktzahl: 4<br />
Aufgabe 10: Salpetersäure ist eine im Labor sowie in der Großindustrie häufig eingesetzte Säure.<br />
a) Geben Sie den Namen und, in Teilschritten, die Reaktionsgleichungen des industriellen<br />
Herstellungsverfahrens an.<br />
2
) Erläutern Sie das Verfahren zur Herstellung des stickstoffhaltigen Eduktes. Geben Sie ebenfalls<br />
den Namen dieses Verfahrens an.<br />
max. Punktzahl: 5<br />
Aufgabe 11: Erläutern Sie anhand von Reaktionsgleichungen die technische Darstellung von Schwefelsäure nach<br />
dem Kontaktverfahren. Warum wird ein Katalysator verwendet?<br />
max. Punktzahl: 3<br />
Aufgabe 12: Bei der Aufbereitung von metallhaltigen, wässrigen Lösungen wird häufig die Schwerlöslichkeit<br />
der entsprechenden Sulfide, Hydroxide oder Carbonate ausgenutzt.<br />
a) Al(OH)3 und Fe(OH)3 haben vergleichbare pKL-Werte von > 30. Trotzdem können Sie nur Eisen<br />
im stark basischen Milieu quantitativ ausfällen. Warum?<br />
b) In welchem technisch wichtigen Prozess (Name und Ziel des Prozesses) wird die in Teil a)<br />
angesprochene Reaktion ausgenutzt.<br />
max. Punktzahl: 3<br />
Aufgabe 13: a) Nennen Sie ein Phosphormineral und beschreiben Sie einen praktikablen Reaktionsweg zur<br />
Darstellung von elementarem Phosphor aus diesem Mineral (mit Reaktionsgleichung).<br />
b) Skizzieren Sie die räumliche Anordnung der Atome im weißen Phosphor und geben Sie den<br />
Bindungswinkel an den Phosphoratomen an.<br />
max. Punktzahl: 4<br />
Aufgabe 14: a) Was versteht man unter „temporärer“ und „permanenter“ Wasserhärte? Geben Sie Beispiele.<br />
b) Beschreiben Sie anhand einer Reaktionsgleichung die Auflösung von Carbonatgestein durch<br />
CO2-haltiges Wasser.<br />
max. Punktzahl: 3<br />
Aufgabe 15: Geben Sie die Gleichungen für die Reaktion eines Alkalimetalls mit H2O sowie für die Reaktionen<br />
der Alkalimetalle Li, Na und K mit O2 (Verbrennung an Luft) unter Angabe der Oxidationszahlen<br />
an.<br />
max. Punktzahl: 4<br />
Aufgabe 16: a) Tragen Sie direkt in das Diagramm den prinzipiellen Verlauf der Siedepunkte der<br />
Chalkogenwasserstoffe und der Halogenwasserstoffe ein (bezeichnen Sie die Punkte mit den<br />
Formeln).<br />
b) Falls Sie eine Unstetigkeit in den Kurven der Reihen der Chalkogen(Halogen)verbindungen<br />
haben, begründen Sie diese (Stichworte genügen).<br />
max. Punktzahl: 5<br />
Aufgabe 17: FeS hat einen KL-Wert von 10 -18 mol 2 ·l -2 . Geben Sie unter Angabe des Rechenweges den minimalen<br />
pH-Wert an, bei dem in einer gesättigten wässrigen H2S-Lösung noch eine vollständige Fällung von<br />
FeS erfolgt.<br />
c(gesättigte wässrige H2S-Lösung) = 0,1 mol/l<br />
vollständige Fällung: c(Fe 2+ nach der Fällung) = 10 -5 mol/l<br />
KS1(H2S) = 10 –7 mol/l<br />
KS2(H2S) = 10 –13 mol/l<br />
max. Punktzahl: 3<br />
Aufgabe 18: Ein Beispiel für ein galvanisches Element ist das System Sn/Pb. Wir betrachten ein System, in dem<br />
ein Zinnblech in eine Lösung getaucht ist, die 1 mol/L Sn2+ enthält sowie ein Bleiblech, das in eine<br />
Lösung taucht, die 0,001 mol/L Pb2+ enthält. Außerdem sind die beiden Halbzellen durch eine<br />
poröse Fritte verbunden. Wie ist die Spannung zwischen beiden Elektroden bei 25 °C?<br />
(E 0 Sn = -0,136 V; E 0 Pb = -0,126 V)<br />
max. Punktzahl: 3<br />
Aufgabe 19: Das Löslichkeitsprodukt von Lithiumcarbonat beträgt 8,15·10 -4 (298 K). Wie groß ist die<br />
Löslichkeit von Lithiumcarbonat in a) mol/L, b) in g pro 100 g Wasser (Dichte = 1,00)<br />
max. Punktzahl: 2<br />
Aufgabe 20: a) Welches Volumen einer 2,5 M Blei(II)nitrat-Lösung enthält 0,05 mol Pb 2+ ?<br />
b) Wie viel Milliliter einer 5,0 M K2Cr2O7-Lösung müssen verdünnt werden, um 250 ml einer 0,1<br />
M Lösung zu erhalten?<br />
c) Welche Konzentration hat eine Lösung, die man bei Verdünnung von 10 ml einer 10 M NaOH-<br />
Stammlösung auf 250 ml erhält?<br />
max. Punktzahl: 3<br />
Aufgabe 21: Der pH-Wert einer 0,0475 M Phosphorigensäure ist 1,59. Berechnen Sie den prozentualen<br />
Dissoziationsgrad und die Konstante KS1. (KS1>>KS2).<br />
max. Punktzahl: 2<br />
Aufgabe 22: 2,0 g eines Gemisches aus KCl und KBr werden mit Schwefelsäure abgeraucht, wobei 1,982 g<br />
K2SO4 entstehen. Welche Zusammensetzung (Masseprozent) hat das Gemisch?<br />
max. Punktzahl: 2