Lösungen - emuki
Lösungen - emuki
Lösungen - emuki
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Lösungen</strong><br />
Grundwissen Chemie 10<br />
KLENZE-GYMNASIUM MÜNCHEN<br />
Naturwissenschaftlich-technologisches Gymnasium<br />
Fakten, Kompetenzen, Aufgaben Leitenberger, v1.0<br />
H<br />
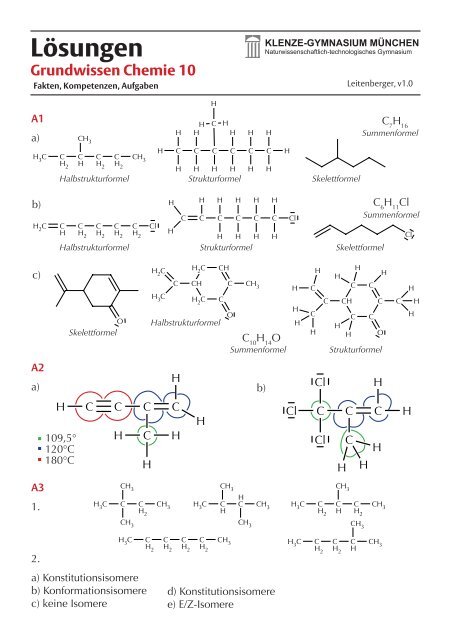
A1<br />
a)<br />
H 3 C<br />
C<br />
H 2<br />
CH 3<br />
C C<br />
H H 2<br />
Halbstrukturformel<br />
C<br />
H 2<br />
CH 3<br />
H<br />
H C H<br />
H H H H H<br />
C C C C C C<br />
H H H H H H<br />
Strukturformel<br />
H<br />
Skelettformel<br />
C 7<br />
H 16<br />
Summenformel<br />
b)<br />
H 2 C<br />
H H H H H H<br />
C 6<br />
H 11<br />
Cl<br />
C C C C C C Cl<br />
Summenformel<br />
C C C C C Cl<br />
H H 2 H 2 H 2 H H<br />
2<br />
H H H H<br />
Cl<br />
Halbstrukturformel Strukturformel Skelettformel<br />
c)<br />
A2<br />
a)<br />
A3<br />
1.<br />
O<br />
Skelettformel<br />
H 2 C<br />
H 3 C<br />
C<br />
H 2 C<br />
CH<br />
H 2 C<br />
Halbstrukturformel<br />
H<br />
CH<br />
C<br />
C<br />
O<br />
CH 3<br />
C 10<br />
H 14<br />
O<br />
Summenformel<br />
b)<br />
H<br />
H<br />
H<br />
C<br />
C<br />
H<br />
H<br />
Cl<br />
C<br />
H<br />
H<br />
CH<br />
H<br />
C<br />
C<br />
H<br />
C<br />
C<br />
C<br />
O<br />
Strukturformel<br />
H C C C C<br />
H<br />
109,5° H C H<br />
120°C<br />
Cl C Cl<br />
C<br />
C<br />
C<br />
H<br />
180°C<br />
H<br />
H H<br />
CH 3<br />
H 3 C C C CH 3 H 3 C C<br />
H 2 H<br />
CH 3<br />
CH 3<br />
CH 3<br />
H<br />
C CH 3<br />
H 3 C<br />
C<br />
H 2<br />
CH 3<br />
C<br />
H<br />
H<br />
H<br />
C<br />
H 2<br />
CH 3<br />
CH 3<br />
H<br />
C H<br />
H<br />
H<br />
2.<br />
H 3 C<br />
C<br />
H 2<br />
C<br />
H 2<br />
C<br />
H 2<br />
C<br />
H 2<br />
CH 3 H 3 C C<br />
H 2<br />
C<br />
H 2<br />
C<br />
H<br />
CH 3<br />
a) Konstitutionsisomere<br />
b) Konformationsisomere<br />
c) keine Isomere<br />
d) Konstitutionsisomere<br />
e) E/Z-Isomere
A4<br />
1.a)<br />
H 3 C<br />
2. a) 3,3-Dichlorprop-1-en b) 2-Brom-1-chlor-3-ethyl-4,5-dimethylhexan<br />
c) 2,6,8-Trimethyl-4-propyldecan<br />
A5<br />
A6<br />
Butan: vdWK (4 C-Atome, unverzweigt) → -0,5°C<br />
2,2-Dimethylbutan: vdWK (6 C-Atome, verzweigt) → -50°C<br />
Hexan: vdWK (6 C-Atome, unverzweigt) → -69°C<br />
1-Chlorhexan: vdWK (6 C-Atome, unverzweigt), Dipol-Dipol-Kräfte → -135°C<br />
Hexansäure: vdWK (6 C-Atome, unverzweigt), H-Brücken → -206°C<br />
In der Antwort sollte außerdem vorkommen: Anlagerungsfläche, zwischenmolekulare Kräfte, Vergleich<br />
der Stärken der Kräfte.<br />
A7<br />
Glycerin: weitgehend polar, H-Brücken möglich, vdWK kaum möglich<br />
Hexan: vollkommen unpolar, nur vdWK<br />
Diethylether: etwas polar, aber geringer EN-Unterschied, vdWK möglich<br />
Wasser: vollkommen polar<br />
Ähnliches löst sich in Ähnlichem. Glycerin und Wasser sind beide polar, deshalb lösen sie sich gut.<br />
A8<br />
CH 3<br />
C<br />
H<br />
C<br />
H 2<br />
C<br />
H 2<br />
H 2 C<br />
C<br />
H<br />
CH 3<br />
C<br />
H 2<br />
CH 3<br />
d) e) Cl f) g)<br />
H 2 C C C<br />
H<br />
h)<br />
H 3 C<br />
H<br />
O<br />
C<br />
C 18<br />
H 36<br />
O 2<br />
+ 26 O 2<br />
→ 18 CO 2<br />
+ 18 H 2<br />
O<br />
i)<br />
b)<br />
CH 3<br />
C C CH 2 Cl C C<br />
H<br />
CH 3<br />
C<br />
H 2<br />
C<br />
HC<br />
C<br />
H 2<br />
H<br />
C<br />
C<br />
Cl<br />
O<br />
C<br />
C<br />
C<br />
HO<br />
C<br />
C<br />
O<br />
H 3 C<br />
O CH 3<br />
H<br />
CH<br />
C<br />
H 2<br />
C<br />
C<br />
OH<br />
CH<br />
CH<br />
C<br />
H 2<br />
Cl<br />
C<br />
H 2<br />
H 3 C<br />
O<br />
C<br />
H 2<br />
H<br />
OH<br />
O O CH 3<br />
C<br />
CH<br />
C<br />
O<br />
C<br />
C<br />
OH<br />
C<br />
O<br />
C<br />
C<br />
H 2<br />
OH<br />
H 3 C<br />
C<br />
C<br />
H 2<br />
CH 3<br />
H<br />
C<br />
H 2<br />
C<br />
H 2<br />
c)<br />
CH 3 CH 3<br />
H 3 C C C<br />
H 2<br />
C CH 3<br />
Br<br />
CH 3 O<br />
O<br />
C C<br />
H<br />
H<br />
H 3 C C C<br />
CH H 2<br />
3<br />
j)<br />
C C C OH<br />
H H 2 H 2 H 2 C C<br />
H<br />
Halogen<br />
Doppelbindung<br />
Hydroxygruppe<br />
Ketogruppe<br />
Aldehydgruppe<br />
Estergruppe<br />
Carboxygruppe<br />
F<br />
C<br />
H 2<br />
CH 3<br />
C<br />
H<br />
CH 2<br />
A9<br />
a)<br />
H<br />
H<br />
H<br />
C C C C<br />
Cl<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
C C C C<br />
H<br />
H<br />
Cl<br />
1-Chlorbutan 2-Chlorbutan 1,1-Dichlorbutan<br />
H<br />
C C C C<br />
Cl<br />
H<br />
Cl<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
C C C C<br />
H<br />
Cl<br />
Cl<br />
H<br />
H<br />
H<br />
H<br />
1,2-Dichlorbutan<br />
2,2-Dichlorbutan<br />
b) funktioniert wie auf Seite 9 mit Methan abgebildet. Das gesuchte Nebenprodukt<br />
entsteht bei der Vereinigung zweier Butylradikale (Abbruchreaktion).<br />
A11<br />
Butansäure ist schon eine Säure und kann nicht mehr weiter oxidiert werden.<br />
2-Methylbutan-2-ol ist ein tertiärer Alkohol und kann ebenfalls nicht oxidiert werden.<br />
Ethanal ist ein Aldehyd und kann zur Carbonsäure oxidiert werden:<br />
A12<br />
Die Säurestärke hängt von der Polarisierung der OH-Bindung und von der<br />
Stabilisierung des entstehenden Anions ab. Beim Alkohol ist das Anion schlecht<br />
stabilisiert, bei den Carbonsäuren gut. Ameisensäure hat eine kürzere C-Kette als<br />
Essig säure und ist deshalb etwas stärker (weniger Störung des Elektronensoges).<br />
H<br />
H<br />
H<br />
Cl<br />
C C C C<br />
Cl<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
H<br />
Es gibt noch<br />
weitere Möglichkeiten,<br />
z.B. mit drei<br />
Chloratomen<br />
oder mehr.<br />
c) Es handelt sich um eine Kettenreaktion, d.h. jedes eingesetzte Chlorradikal lässt<br />
wieder ein neues entstehen (vorausgesetzt die Abbruchreaktionen kommen nicht<br />
zu häufig vor).<br />
A10<br />
a) Funktioniert wie auf Seite 10 mit Ethen abgebildet. Beim nucleophilen Rückseitenangriff<br />
am Bromoniumion kann nur 1,2-Dibrompropan entstehen.<br />
b) Statt Bromidion greift beim nucleophilen Rückseitenangriff ein Hydroxidion an.<br />
Ox:<br />
Red:<br />
H 3 C<br />
H<br />
C<br />
H<br />
H<br />
C<br />
+I<br />
C<br />
O<br />
+ 2 OH — →<br />
H<br />
H<br />
+II +I<br />
H<br />
H<br />
+III<br />
C C<br />
2 Cu 2+ + 2 e — + 2 OH — → Cu 2<br />
O + H 2<br />
O<br />
C OH + H<br />
H 2<br />
O<br />
2<br />
O<br />
OH<br />
+ H 2<br />
O<br />
→<br />
→<br />
H 3 C<br />
H<br />
– C O<br />
H 2<br />
C<br />
O<br />
O<br />
–<br />
H<br />
+<br />
+ H 3<br />
O<br />
+<br />
+ H 3<br />
O<br />
O<br />
OH<br />
+ 2 e — + H 2<br />
O<br />
Essigsäure analog.
A13<br />
a)<br />
H<br />
H<br />
H<br />
N<br />
H<br />
∂ + ∂ –<br />
+ C O<br />
H<br />
H<br />
H<br />
H<br />
H<br />
+ –<br />
N C O<br />
H<br />
H 2 N<br />
H<br />
C<br />
H<br />
OH<br />
b)<br />
H 3 C<br />
C<br />
H 2<br />
O<br />
H H 3 C<br />
+<br />
H 3 C<br />
∂ +<br />
C<br />
H CH 3<br />
∂ –<br />
+ –<br />
O H 3 C C O C O<br />
H 2<br />
CH 3<br />
H 3 C<br />
CH 3<br />
C O C OH<br />
H 2<br />
CH 3<br />
Halbketal<br />
CH 3<br />
+<br />
H<br />
H 2<br />
O +<br />
H 3 C C O C OH HO C H<br />
H<br />
H 3 C C O C O C CH 3<br />
2<br />
H 2<br />
H 2<br />
CH 3<br />
H<br />
CH 3<br />
Vollketal<br />
CH 3<br />
A14<br />
HC<br />
HC<br />
O<br />
C<br />
C<br />
C<br />
H<br />
OH<br />
C<br />
CH<br />
OH<br />
+<br />
HO<br />
C<br />
O<br />
CH 3<br />
Kondensation<br />
Hydrolyse<br />
Entfernt man Wasser aus dem Reaktionsgemisch, wird die Wahrscheinlichkeit für<br />
die Hydrolyse (Rückreaktion) verringert.<br />
HC<br />
HC<br />
O<br />
C<br />
C<br />
C<br />
H<br />
OH<br />
C<br />
CH<br />
O<br />
C<br />
O<br />
CH 3<br />
+ H 2<br />
O<br />
A15<br />
H<br />
H<br />
H<br />
H<br />
C<br />
C<br />
C<br />
H<br />
O<br />
O<br />
O<br />
O<br />
C<br />
O<br />
C<br />
O<br />
C<br />
H 2<br />
C<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
C<br />
H 2<br />
C<br />
H<br />
H<br />
C<br />
H 2<br />
C<br />
C<br />
H 2<br />
H<br />
C<br />
C<br />
H<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
H 2<br />
C<br />
C<br />
H 2<br />
C<br />
H<br />
H 2<br />
C<br />
C<br />
H 2<br />
H<br />
C<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
C<br />
H 2<br />
H 2<br />
C<br />
C<br />
H 2<br />
CH 3<br />
CH 3<br />
CH 3<br />
A16<br />
Die häufigste Form ist die<br />
Ringform (Seite 13). Fehling-Probe<br />
ist trotzdem posititv,<br />
weil ein Teil in Kettenform<br />
vorliegt. Diese hat eine<br />
oxidierbare Aldehydgruppe.<br />
H 2 N<br />
A17<br />
H<br />
C<br />
O<br />
C<br />
N<br />
CH H<br />
H 3 C CH 3<br />
H<br />
C<br />
H<br />
O<br />
C<br />
N<br />
H<br />
H O<br />
C C<br />
CH 2<br />
OH<br />
N<br />
H<br />
H<br />
C C<br />
CH 3<br />
O<br />
OH