Vorlesung 25 - Elsa
Vorlesung 25 - Elsa
Vorlesung 25 - Elsa
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
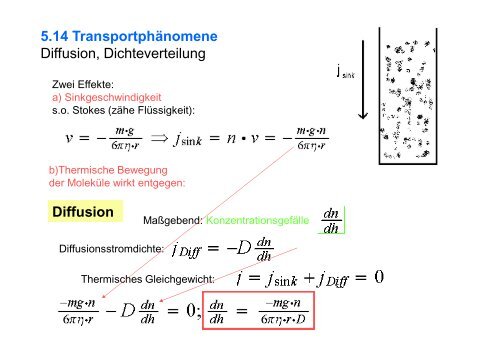
5.14 Transportphänomene<br />
Diffusion, Dichteverteilung<br />
Zwei Effekte:<br />
a) Sinkgeschwindigkeit<br />
s.o. Stokes (zähe Flüssigkeit):<br />
b)Thermische Bewegung<br />
der Moleküle wirkt entgegen:<br />
Diffusion<br />
Maßgebend: Konzentrationsgefälle<br />
Diffusionsstromdichte:<br />
Thermisches Gleichgewicht:
oder<br />
h<br />
''Barometrische Höhenformel''<br />
für die Teilchenzahldichte<br />
s.o.:<br />
die Einsteinsche Beziehung:<br />
Bei Gasen<br />
η ~√ T<br />
Diffusion eines Gases in ein anderes:<br />
T=konst. mit<br />
Gas 1<br />
Gas 2<br />
P 1 =n 1 kT<br />
P 2 =n 2 kT
Annahme<br />
P1=P2 àn1=n2<br />
Thermische Bewegung:<br />
Gase vermischen,<br />
keine zusätzliche Energie!<br />
Thermische Molekularbewegung ''sorgt'' für Mischung: ''Diffusion''<br />
Teilchendichte des i- ten Gases<br />
Gesamtdruck P (Summe aller Partialdrucke):<br />
Partialdruck
Daltonsche Regel<br />
Diffusion von Gasen durch poröse Trennwände<br />
stetiger Molekülstrom: In<br />
Molekülstrom<br />
1.Ficksche Gesetz<br />
Bisher stationär: Konstantes Konzentrationsgefälle
Wie<br />
fließt bei x1 in V rein<br />
fließt bei x2 aus V raus<br />
mit dem 1.Fickschen Gesetz<br />
2.Ficksche Gesetz<br />
Diffusionsgleichung!
Die Diffusionskonstante hängt ab von der mittleren (thermischen)<br />
Geschwindigkeit vt hund der freien Weglänge Λ<br />
Λ : mittlere Strecke zwischen zwei Stößen<br />
D~vth* Λ<br />
Vergleich zweier Gase:<br />
dabei wurde angenommen,<br />
leichtere Gase diffundieren schneller als schwerere!<br />
siehe Exp: Tonzylinder<br />
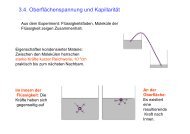
Osmose<br />
Exp.:Pfeffersche Zelle<br />
z.B.:H2O -Moleküle diffundieren<br />
durch eine semipermeable<br />
Membran in die Zuckerlösung<br />
àhöherer Druck in der Zelle<br />
àOsmotischer Druck<br />
Semipermeable Membran
Gesetz van t'Hoff:<br />
M:Masse des im Volumen V gelösten Stoffes<br />
experimenteller Befund! C=M/V=Massenkonzentration<br />
z.B:C=0.1Mol/Liter,T=0°<br />
Große Bedeutung in der Biologie:<br />
z.B:Erbsen quellen in<br />
Erbsen schrumpfen in konzentrier Kochsalzlösung<br />
Wärmetransport<br />
a) Wärmeleitung<br />
b) Wärmeströmung<br />
c) Wärmestrahlung (3.Sem.)
Beispiele: λ<br />
Temperaturgefälle:<br />
Silber 423<br />
Kupfer 394<br />
Aluminium 201<br />
Eisen 71<br />
Porzellan 1<br />
Wasser 0.6<br />
Luft 0.023<br />
oder mit der Wärmeleitfähigkeit λ<br />
Metalle: Leitfähigkeit ~<br />
Elektrischen<br />
Leitfähigkeit
Wärmeströmung<br />
Durch Dichtevariation
Addendum: Maxwellsche Geschwindigkeitsverteilung<br />
Die Anzahl der Teilchen<br />
in dem Geschwindigkeits<br />
-volumenelement<br />
(Boltzmann-Verteilung s.o.)<br />
mit C als Normierungskonstante<br />
bestimmt durch Teilchenzahl
y1.5e+7<br />
300K<br />
1.<strong>25</strong>e+7<br />
1e+7<br />
O 16<br />
7.5e+6<br />
1000K<br />
5e+6<br />
2.5e+6<br />
H<br />
300K<br />
0<br />
0<br />
1<strong>25</strong>0<br />
<strong>25</strong>00<br />
3750<br />
5000<br />
Kelvin<br />
x