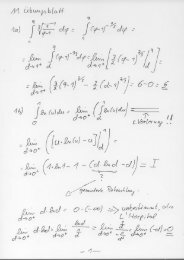Heterogene Katalyse
Heterogene Katalyse
Heterogene Katalyse
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
<strong>Katalyse</strong><br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Als <strong>Katalyse</strong> (griech. κατάλυσις, katálysis - die Auflösung, Abschaffung,<br />
Aufhebung) wird die Veränderung (Beschleunigung, Veränderung der<br />
Selektivität) einer chemischen Reaktion durch Beteiligung eines Katalysators<br />
bezeichnet. Der Katalysator geht aus der Gesamtreaktion wieder hervor und<br />
kann somit mehrere <strong>Katalyse</strong>zyklen durchlaufen.<br />
Bei der homogenen <strong>Katalyse</strong> gehört der Katalysator der gleichen Phase an<br />
wie das Reaktionssystem (z. B. flüssiger Katalysator in flüssiger<br />
Reaktionsmischung gelöst).<br />
Bei der heterogenen <strong>Katalyse</strong> liegt der Katalysator im allgemeinen als Feststoff<br />
vor, d.h. die Reaktanden (flüssig oder gasförmig) und der Katalysator sind<br />
einander berührende, jedoch verschiedene Phasen.
<strong>Heterogene</strong> <strong>Katalyse</strong><br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
potentielle<br />
Energie<br />
E Kat.<br />
Adsorption<br />
(Het.)<br />
<strong>Katalyse</strong><br />
E ReakẸAkt.<br />
Reaktionsweg<br />
Desorption
Teilschritte der heterogenen <strong>Katalyse</strong><br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
• Äußere und innere Diffusion<br />
der Reaktanden zur<br />
Oberfläche (1,2)<br />
• Adsorption an der<br />
Oberfläche (3)<br />
• Diffusion auf der Oberfläche<br />
• Reaktion (4)<br />
• Desorption von der<br />
Oberfläche (5)<br />
• Innere und äußere Diffusion<br />
der Produkte von der<br />
Oberfläche weg (6,7)
Eigenschaften des Katalysator<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Aktivität (Verringerung der Aktivierungsenergie, Beschleunigung der<br />
Reaktionsgeschwindigkeit)<br />
Stabilität (Der Katalysator sollte unbeschadet aus der Reaktion hervorgehen<br />
sowie eine hohe chemische, thermische und mechanische Beständigkeit<br />
aufweisen.)<br />
Selektivität (Für unterschiedliche Reaktionen<br />
müssen unterschiedliche Katalysatoren eingesetzt<br />
werden.)<br />
Ni<br />
CH 4 + H 2 O<br />
Methanisierung<br />
CO / H 2<br />
Cu/Cr/Zn-<br />
Oxid<br />
CH 3 OH<br />
Methanolsynthese<br />
Fe, Co<br />
C n H 2n+m + H 2 O<br />
Fischer-<br />
Tropsch-<br />
Synthese
Mechanismen der heterogenen <strong>Katalyse</strong><br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
• Langmuir-Hinshelwood (Reaktion zwischen<br />
adsorbierten Molekülen/Atomen)<br />
• Eley-Rideal (Reaktion zwischen adsorbiertem und<br />
ankommenden Molekül/Atom)
Langmuir-Hinshelwood-Mechanismus für<br />
unimolekuare Reaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
A<br />
(g)<br />
⇔<br />
A (ads)<br />
⎯→<br />
B<br />
Der Abbau erfolgt gleichmäßig entlang der Oberfläche. Die Produkte<br />
sind nur schwach gebunden und desorbieren rasch von der<br />
Oberfläche.<br />
Der geschwindigkeitsbestimmende Schritt ist die Abbaureaktion an der<br />
Oberfläche.<br />
Reaktionsrate = k kat θ A<br />
A<br />
p A<br />
B<br />
Für Langmuir-Adsorption<br />
kbp<br />
Rate =<br />
1+<br />
bp<br />
mit b =k ads<br />
/k des<br />
Θ Α<br />
schnell<br />
k het<br />
schnell
Langmuir-Hinshelwood-Mechanismus für<br />
unimolekuare Reaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Niedrieger Druck<br />
bzw. schwache<br />
Bindung<br />
bp1<br />
Rate ≈ k<br />
Reaktionsrate ist<br />
unabhängig vom<br />
Gaspartialdruck.<br />
Reaktion nullter<br />
Ordnung.<br />
Bedeckungsgrad<br />
der Oberfläche<br />
annähernd eins.
Langmuir-Hinshelwood-Mechanismus für<br />
bimolekuare Reaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Langmuir-Hinshelwood-Reaktion mit Oberflächenreaktion als<br />
geschwindigkeitsbestimmenden Schritt:<br />
A (ads)<br />
+<br />
B (ads)<br />
A (g)<br />
B (g)<br />
rds<br />
⎯⎯→<br />
⇔ A (ads)<br />
⇔ B (ads)<br />
AB (ads)<br />
fast<br />
⎯⎯→<br />
AB (g)<br />
p A<br />
Reaktionsrate = A<br />
schnell<br />
k θ A θ B<br />
Θ Α<br />
B<br />
p B<br />
Θ Β<br />
k het<br />
AB<br />
schnell
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
{ }<br />
{ }<br />
B<br />
d<br />
B<br />
B<br />
A<br />
B<br />
a<br />
B<br />
A<br />
d<br />
A<br />
B<br />
A<br />
A<br />
a<br />
A<br />
surface<br />
d<br />
a<br />
surface<br />
g<br />
surface<br />
d<br />
a<br />
surface<br />
g<br />
k<br />
dt<br />
d<br />
p<br />
k<br />
dt<br />
d<br />
k<br />
dt<br />
d<br />
p<br />
k<br />
dt<br />
d<br />
S<br />
B<br />
k<br />
k<br />
S<br />
B<br />
S<br />
A<br />
k<br />
k<br />
S<br />
A<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
=<br />
=<br />
+<br />
−<br />
=<br />
=<br />
=<br />
=<br />
+<br />
−<br />
=<br />
=<br />
−<br />
+<br />
−<br />
+<br />
Desorptionsrate<br />
)<br />
(1<br />
für B<br />
Adsorptionsrate<br />
Desorptionsrate<br />
)<br />
(1<br />
für A<br />
Adsorptionsrate<br />
Langmuir-Hinshelwood-Mechanismus für<br />
bimolekuare Reaktionen
Langmuir-Hinshelwood-Mechanismus für<br />
bimolekuare Reaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Im Gleichgewicht:<br />
θ<br />
A<br />
=<br />
k<br />
b<br />
a A<br />
p<br />
p<br />
A<br />
θ<br />
θ<br />
S<br />
=<br />
k<br />
mit<br />
d<br />
A<br />
θ<br />
A A S<br />
b A<br />
A<br />
=<br />
k<br />
k<br />
a A<br />
d<br />
A<br />
θ<br />
B<br />
=<br />
k<br />
b<br />
a B<br />
p<br />
p<br />
B<br />
θ<br />
θ<br />
S<br />
=<br />
k<br />
mit<br />
d B<br />
θ<br />
B B S<br />
b B<br />
B<br />
=<br />
k<br />
k<br />
a B<br />
d B<br />
Für den Bedeckungsgrad gilt:<br />
θ<br />
S<br />
θ<br />
=<br />
S<br />
( 1−<br />
{ θ + θ })<br />
+ θ<br />
A<br />
A<br />
+ θ<br />
B<br />
B<br />
= 1
Langmuir-Hinshelwood-Mechanismus für<br />
bimolekuare Reaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Mit der Reaktionsrate<br />
θ<br />
θ<br />
θ<br />
θ<br />
θ<br />
S<br />
S<br />
S<br />
A<br />
B<br />
+ b<br />
A<br />
( 1+<br />
b p + b p )<br />
=<br />
=<br />
=<br />
p<br />
A<br />
A<br />
θ<br />
A<br />
( 1+<br />
b p + b p )<br />
A<br />
( 1+<br />
b p + b p )<br />
A<br />
( 1+<br />
b p + b p )<br />
A<br />
S<br />
b<br />
b<br />
+ b<br />
A<br />
B<br />
1<br />
A<br />
A<br />
A<br />
p<br />
p<br />
B<br />
B<br />
A<br />
B<br />
p<br />
B<br />
B<br />
B<br />
B<br />
Rate<br />
B<br />
θ<br />
S<br />
= 1<br />
B<br />
B<br />
B<br />
= 1<br />
= k θ A θ B<br />
( ) 2<br />
=<br />
kb<br />
1+<br />
b<br />
A<br />
A<br />
p<br />
p<br />
A<br />
A<br />
b<br />
+<br />
B<br />
b<br />
p<br />
B<br />
B<br />
p<br />
B
Langmuir-Hinshelwood-Mechanismus für<br />
bimolekuare Reaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Reaktionsrate<br />
Für konstanten Partialdruck p B<br />
Reaktionsrate begrenzt durch die<br />
Oberflächenkonzentration von A<br />
Θ Β >> Θ Α<br />
p A<br />
Reaktionsrate begrenzt durch die<br />
Oberflächenkonzentration von B<br />
Θ Β
Eley-Rideal-Mechanismus für<br />
bimolekulare Oberflächenreaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Ein adsorbiertes Molekül kann<br />
direkt mit einem auftreffenden<br />
Gasmolekül reagieren.<br />
B<br />
p A<br />
Θ Α<br />
A<br />
p B<br />
k het<br />
schnell<br />
AB
Eley-Rideal-Mechanismus für<br />
bimolekulare Oberflächenreaktionen<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Reaktionsrate = k Θ Α p B = k b A p A p B / (1+b A p A )<br />
Θ Α = 1<br />
Bemerke: Für<br />
konstanten p A , ist die<br />
Rate immer erster<br />
Ordnung in p B<br />
Rate<br />
Für konstanten p B<br />
Niedriger Druck bzw.<br />
schwache Bindung<br />
b A p A > 1<br />
Rate = k p B …….. nullter Ordnung in A<br />
k exp<br />
k exp
Vergleich<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Wenn mann die Reaktionsrate als Funktion des Bedeckungsgrades<br />
durch die Komponente A misst, steigt sie zu Beginn für beide<br />
Mechanismen an.<br />
Eley-Rideal: Die Reaktionsrate wächst bis zum Bedeckungsgrad<br />
Θ A = 1 an.<br />
Langmuir-Hinshelwood: Die Reaktionsrate durchläuft ein<br />
Maximum und endet bei Θ A = 1 bei Null.<br />
Die Reaktion B + S B-S kann nicht<br />
erfolgen wenn die gesamte Oberfläche<br />
durch A blockiert ist.
Energetische Betrachtung<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Übergangszustand<br />
# hom<br />
Langmuir-Hinshelwood Kinetics<br />
Adsorption der Reaktanden und Desorption der<br />
Produkte laufen sehr schnell ab. ΔE ads und<br />
ΔE des sind sehr klein.<br />
potentielle Energie<br />
ΔE hom<br />
ΔE ads<br />
Reaktanden<br />
# het<br />
ΔE het<br />
Die Oberflächenreaktion mit ΔE het ist<br />
geschwindigkeitsbestimmend.<br />
adsorbierte Reaktanden<br />
ΔE des<br />
Produkte<br />
adsorbierte Produkte<br />
Reaktionskoordinate
Prinzip von Sabatier<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Wenn unterschiedliche Metalle als Katalysatoren ein und derselben Reaktion<br />
benutzt werden, kann eine allgemeine Korrelation zwischen der Reaktionsrate und<br />
der Position des Metalls im Periodensystem der Elmente beobachtete werden:<br />
Vulkankurve
Beispiele für katalytische Prozesse<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
• Die katalytische Aufspaltung (Cracking) von Erdöl zu<br />
Benzinprodukten in Erdölraffinerien.<br />
• Reduktion von Stickoxiden aus den Motorabgasen im Platin-<br />
Katalysator von Kraftfahrzeugen<br />
• Ammoniaksynthese (Haber-Bosch-Verfahren)<br />
• Oxidation von Wasserstoff und Sauerstoff zu Wasser in<br />
Brennstoffzellen<br />
• Nahezu alle biochemischen Vorgänge werden durch Enzyme<br />
katalysiert.
Ammoniaksynthese nach dem Haber-<br />
Bosch-Verfahren<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Wissenschaftliche Leistungen:<br />
• Untersuchung der zugrunde liegenden chemischen Reaktion (Fritz Haber, Walther<br />
Nernst)<br />
• Systematische Suche nach geeigneten Katalysatoren (Alwin Mittasch)<br />
• Technische Realisierung im großen Maßstab, wobei zum Teil vollkommen neue<br />
Lösungen entwickelt werden mussten (Carl Bosch, Fritz Haber)<br />
• Patentanmeldung des Haber-Bosch-Verfahrens durch die BASF 1910<br />
• Nobelpreise für Chemie für Fritz Haber (1918) und Carl Bosch (1931)<br />
1 3 Fe, 200 bar, 500°<br />
C<br />
0<br />
N2 + H<br />
2<br />
←⎯⎯⎯⎯<br />
→2NH<br />
3<br />
ΔHB<br />
=<br />
2 2<br />
- 46 kJ/mol<br />
Ökonomische Bedeutung:<br />
• Weltweite, jährliche Ammoniakproduktion beträgt ca. 97·10 6 t (im Jahr 1997)<br />
• 90% der weltweiten Ammoniaksynthese wird durch das Haber-Bosch-Verfahren<br />
realisiert.<br />
• NH3-Synthese einzig technisch bedeutsame Verfahren, bei dem der reaktionsträge<br />
Stickstoff der Luft in chemische Verbindungen überführt wird.<br />
• Ammoniak Vorläufersubstanz für z. B. Düngemittel und Sprengstoffe<br />
• Ca. 3% des Weltenergieverbrauches wird zur Synthese von Ammoniak nach dem<br />
Haber-Bosch-Verfahren verwendet.
Bedeutung/Verwendung von Ammoniak<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Ammoniak<br />
NH 3<br />
Nitrate<br />
Salpetersäure<br />
HNO 3<br />
Harnstoff<br />
(NH 2<br />
) 2<br />
CO<br />
weitere<br />
organische und<br />
anorganische<br />
Stickstoffverbindungen<br />
Nitroaromaten<br />
(z. B. Anilin)<br />
Düngemittel<br />
Kunstharze<br />
Hydroxylamin<br />
Nitrile<br />
Sprengstoffe<br />
Adipinsäure<br />
HOOC-(CH 2<br />
) 4<br />
-<br />
COOH<br />
Amine<br />
Hydrazin
Ammoniaksynthese nach dem Haber-<br />
Bosch-Verfahren<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Fe-Katalysator
Mechanismus der Ammoniaksynthese<br />
Grenzflächenchemie<br />
SS 2006<br />
Dr. R. Tuckermann<br />
Fe<br />
N2 ←⎯→<br />
2Nads<br />
Fe<br />
H<br />
2<br />
←⎯→<br />
2H<br />
ads<br />
Fe<br />
Nads<br />
+ H<br />
ads<br />
←⎯→( NH ) ads<br />
Fe<br />
( NH )<br />
ads<br />
+ H<br />
ads<br />
←⎯→( NH<br />
2<br />
) ads<br />
Fe<br />
( NH<br />
2<br />
) + H<br />
ads<br />
←⎯→( NH )<br />
ads<br />
3 ads<br />
( NH<br />
3<br />
) ads<br />
←⎯→<br />
NH<br />
3