21-24 Richtlinien Tumormarker - SGKC/SSCC
21-24 Richtlinien Tumormarker - SGKC/SSCC
21-24 Richtlinien Tumormarker - SGKC/SSCC
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
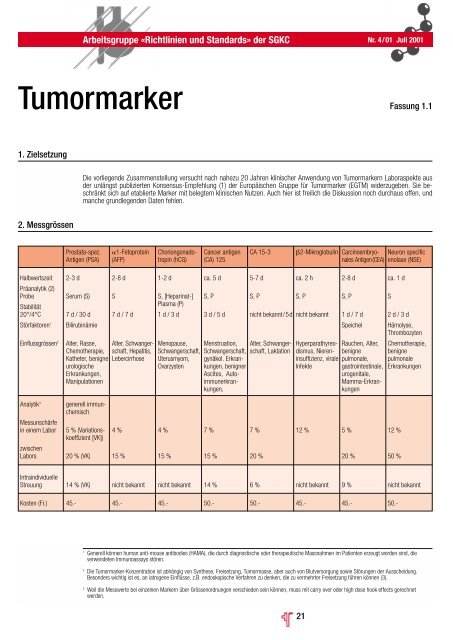
Arbeitsgruppe «<strong>Richtlinien</strong> und Standards» der <strong>SGKC</strong> Nr. 4/01 Juli 2001<br />
<strong>Tumormarker</strong> Fassung 1.1<br />
1. Zielsetzung<br />
Die vorliegende Zusammenstellung versucht nach nahezu 20 Jahren klinischer Anwendung von <strong>Tumormarker</strong>n Laboraspekte aus<br />
der unlängst publizierten Konsensus-Empfehlung (1) der Europäischen Gruppe für <strong>Tumormarker</strong> (EGTM) widerzugeben. Sie beschränkt<br />
sich auf etablierte Marker mit belegtem klinischen Nutzen. Auch hier ist freilich die Diskussion noch durchaus offen, und<br />
manche grundlegenden Daten fehlen.<br />
2. Messgrössen<br />
Prostata-spez.<br />
Antigen (PSA)<br />
1-Fetoprotein<br />
(AFP)<br />
Choriongonadotropin<br />
(hCG)<br />
Cancer antigen<br />
(CA) 125<br />
CA 15-3<br />
2-Mikroglobulin<br />
Carcinoembryonales<br />
Antigen(CEA)<br />
Neuron specific<br />
enolase (NSE)<br />
Halbwertszeit<br />
Präanalytik (2)<br />
Probe<br />
Stabilität<br />
20°/4°C<br />
Störfaktoren 1<br />
Einflussgrössen 2<br />
2-3 d<br />
Serum (S)<br />
7 d / 30 d<br />
Bilirubinämie<br />
Alter, Rasse,<br />
Chemotherapie,<br />
Katheter, benigne<br />
urologische<br />
Erkrankungen,<br />
Manipulationen<br />
2-8 d<br />
S<br />
7 d / 7 d<br />
Alter, Schwangerschaft,<br />
Hepatitis,<br />
Lebercirrhose<br />
1-2 d<br />
S, [Heparinat-]<br />
Plasma (P)<br />
1 d / 3 d<br />
Menopause,<br />
Schwangerschaft,<br />
Uterusmyom,<br />
Ovarzysten<br />
ca. 5 d<br />
S, P<br />
3 d / 5 d<br />
Menstruation,<br />
Schwangerschaft,<br />
gynäkol. Erkrankungen,<br />
benigner<br />
Ascites, Autoimmunerkrankungen,<br />
5-7 d<br />
S, P<br />
nicht bekannt/5d nicht bekannt<br />
Alter, Schwangerschaft,<br />
Laktation<br />
ca. 2 h<br />
S, P<br />
Hyperparathyreodismus,<br />
Niereninsuffizienz,<br />
virale<br />
Infekte<br />
2-8 d<br />
S, P<br />
1 d / 7 d<br />
Speichel<br />
Rauchen, Alter,<br />
benigne<br />
pulmonale,<br />
gastrointestinale,<br />
urogenitale,<br />
Mamma-Erkrankungen<br />
ca. 1 d<br />
S<br />
2 d / 3 d<br />
Hämolyse,<br />
Thrombozyten<br />
Chemotherapie,<br />
benigne<br />
pulmonale<br />
Erkrankungen<br />
Analytik 3<br />
Messunschärfe<br />
in einem Labor<br />
zwischen<br />
Labors<br />
generell immunchemisch<br />
5 % (Variationskoeffizient<br />
[VK])<br />
20 % (VK)<br />
4 %<br />
15 %<br />
4 %<br />
15 %<br />
7 %<br />
15 %<br />
7 %<br />
20 %<br />
12 %<br />
5 %<br />
20 %<br />
12 %<br />
50 %<br />
Intraindividuelle<br />
Streuung<br />
14 % (VK)<br />
nicht bekannt<br />
nicht bekannt<br />
14 %<br />
6 %<br />
nicht bekannt<br />
9 %<br />
nicht bekannt<br />
Kosten (Fr.)<br />
45.-<br />
45.-<br />
45.-<br />
50.-<br />
50.-<br />
45.-<br />
45.-<br />
50.-<br />
1<br />
Generell können human anti-mouse antibodies (HAMA), die durch diagnostische oder therapeutische Massnahmen im Patienten erzeugt worden sind, die<br />
verwendeten Immunoassays stören.<br />
2<br />
Die <strong>Tumormarker</strong>-Konzentration ist abhängig von Synthese, Freisetzung, Tumormasse, aber auch von Blutversorgung sowie Störungen der Ausscheidung.<br />
Besonders wichtig ist es, an iatrogene Einflüsse, z.B. endoskopische Verfahren zu denken, die zu vermehrter Freisetzung führen können (3).<br />
3<br />
Weil die Messwerte bei einzelnen Markern über Grössenordnungen verschieden sein können, muss mit carry over oder high dose hook effects gerechnet<br />
werden.<br />
<strong>21</strong>
Groupe de travail «Directives et normes» de la <strong>SSCC</strong><br />
LABOLIFE<br />
3. Diagnostik<br />
Alle Autoren betonen für alle Marker den Mangel an Sensitivität für die Früherkennung sowie den Mangel an Spezifität für Malignität.<br />
Eine Diagnose ist in jedem Fall histologisch/cytologisch abzusichern.<br />
3.1.Screening<br />
Die Bestimmung von <strong>Tumormarker</strong>n gilt mit folgenden Ausnahmen für Screeningzwecke als nicht geeignet:<br />
• PSA bei Männern > 50 Jahren, zusätzlich zur manuellen Prostata-Untersuchung.<br />
• AFP bei Personen mit erhöhtem Risiko für hepatozelluläres Ca.<br />
• AFP und hCG bei Personen mit erhöhtem Risiko für Keimzelltumoren.<br />
3.2.Differenzialdiagnose<br />
• PSA kann bei urologischen Beschwerden zur Abgrenzung eines Prostata-Ca von einer benignen Hyperplasie beitragen. Besonders<br />
aussagekräftig ist der Quotient Gesamt/freies PSA, wobei ein Wert von ≥ 0,27 ein Karzinom mit erheblicher Sicherheit ausschliesst<br />
und eine überflüssige Biopsie vermeiden kann.<br />
• NSE erlaubt bei sehr hohen Werten die Zuordnung und Behandlung eines wenig differenzierten Bronchus-Ca als kleinzellig.<br />
• AFP legt bei stark erhöhten Werten bei Lebertumoren mit nicht eindeutiger Histologie die Behandlung wie ein hepatozelluläres<br />
Karzinom nahe.<br />
• Beim Lungen-Ca können mit Hilfe von CEA, NSE und CYFRA <strong>21</strong>-1 small (SCLC) von non small cell lung cancer (NSCLC) unterschieden<br />
werden.<br />
3.3.Prognose<br />
• ß2-Mikroglobulin ist ein wesentlicher prognostischer Faktor bei hämatologischen Malignomen, zusammen mit LDH und anderen<br />
Messgrössen (B-Symptome).<br />
• AFP und hCG erlauben eine Einteilung von metastasierenden Keimzelltumoren in prognostische Gruppen.<br />
4. Therapieüberwachung (4)<br />
CEA AFP CA 19-9 CA 72-4 CA 125 CA 15-3 NSE CYFRA hCG PSA Thyreoglobulin<br />
Kolon • •<br />
Pankreas • •<br />
Magen • • •<br />
Oesophagus<br />
•<br />
Hepatozellulär •<br />
Gallenwege<br />
•<br />
Mamma • •<br />
Ovar • •<br />
Chorion<br />
•<br />
Lunge SCLC • Lunge NSCLC • HNO-Tumoren<br />
•<br />
Keimzell • •<br />
Prostata<br />
•<br />
Schilddrüse<br />
•<br />
Kolorektale Tumoren: CEA hat für die Erfassung von Rezidiven eine Sensitivität von ca. 80 %, eine Spezifität von ca. 70 %. Besonders<br />
wertvoll ist die Messgrösse für die Erfassung von Lebermetastasen.<br />
Keimzelltumoren: AFP, in Kombination mit hCG, weist für die Erfassung von Rezidiven eine Sensitivität von > 80 % bei einer Spezifität<br />
von nahezu 100 % auf.<br />
Mamma-Ca: CEA und CA 15-3 erlauben in Kombination die Früherfassung von Metastasen in 60-80 % der Patientinnen, besonders<br />
in Knochen oder Leber.<br />
22
Arbeitsgruppe «<strong>Richtlinien</strong> und Standards» der <strong>SGKC</strong> Nr. 4/01 Juli 2001<br />
5. Zeitliche Intervalle für Wiederholungen<br />
Der Termin für Kontrolluntersuchungen ist in Abhängigkeit von der Halbwertszeit und der ursprünglichen Konzentration zu wählen:<br />
Nicht zu früh, um nicht eine inkomplette Operation vorzutäuschen, und nicht zu spät, um nicht ein Rezidiv zu verpassen. Beispiel:<br />
Bei einer präoperativen CEA-Konzentration von 100 mg/l ist eine erste Kontrolle frühestens nach ca. 40 Tagen indiziert. In jedem<br />
Fall sind Verläufe aussagekräftiger als Einzelbefunde.<br />
Vor dem Hintergrund von biologischer und analytischer Streuung wird häufig als signifikanter Unterschied zu einem Vorwert eine<br />
Veränderung um ± 25 % betrachtet (5). Zwecks Sicherung eines derartigen Unterschiedes ist in der Regel eine zweite Blutprobe zu<br />
verlangen.<br />
6. Andere Messgrössen und Verfahren<br />
6.1.Obsolete<br />
Messgrössen<br />
6.2.Weitere<br />
Messgrössen<br />
Saure Phosphatase, mit und ohne Tartrathemmung, enzymatisch wie auch als EIA<br />
• Estrogenrezeptoren (125.-), Progesteronrezeptoren (125.-) für die Abschätzung des Therapieerfolgs beim Mamma-Ca.<br />
• Tissue polypeptide antigen (TPA, 45.-) für Verlaufskontrolle von Blasen- und Lungen-Ca.<br />
• Tissue polypeptide specific antigen (TPS, nicht in Analysenliste) für die Verlaufskontrolle des metastasierenden Mamma-Ca.<br />
• Calcitonin (60.-) für die Diagnostik und Verlaufskontrolle von medullären Schilddrüsen-Ca. S, P, haltbar nur gefroren.<br />
• Freies PSA (25.-), Serum binnen 3 h abzentrifugiert, Haltbarkeit nicht bekannt. Die Bestimmung wird nur bei Gesamt-PSA<br />
zwischen 4 und 10 mg/l vorwiegend bei jüngeren Patienten empfohlen. Es ist zu beachten, dass nur ein äquimolar messender<br />
Test, der die verschiedenen Proteinformen mit gleicher Präferenz erkennt, ein unverfälschtes Bild geben kann.<br />
• CA 19-9 (50.-) hat für die Verlaufskontrolle des Pankreas-Ca eine eingeschränkte Spezifität. S, P, Haltbarkeit 20/4 °C 7 d / 30 d.<br />
• CA 72-2 (50.-) für die Verlaufskontrolle von Magen-Ca. S, P, Haltbarkeit 7 d / 30 d.<br />
• SCC (50.-) für die Verlaufskontrolle von Cervix-Ca. S, P, Haltbarkeit 7 d / 1 Monat.<br />
• CYFRA <strong>21</strong>-1 (50.-) für die Differenzialdiagnose von Lungentumoren. S, P, Haltbarkeit 7 d 1 Monat.<br />
• S-100 (nicht in Analysenliste), Serum, Haltbarkeit nicht bekannt. Verlaufskontrolle des malignen Melanoms.<br />
7. Kommentar<br />
Analytisch führt die ungenügende Standardisierung zu einer persistierenden Methodenabhängigkeit sowie fehlender Vergleichbarkeit<br />
zwischen Laboratorien (Mess- und Referenzwerte).<br />
Trotz der skizzierten Mängel geniesst die Bestimmung von <strong>Tumormarker</strong>n aktuell eine gewisse praktische Beliebtheit, die vermutlich<br />
zum Teil dem suggestiven Namen zu verdanken ist. Stamey (6) kritisierte kürzlich den undifferenzierten Einsatz von PSA angesichts<br />
der Tatsache, dass ca. 40 % der über 65-jährigen Männer ein Prostata-Karzinom aufweisen, aber nur etwa einer von 177<br />
daran stirbt.<br />
8. Referenzen<br />
1) EGTM: Consensus Recommendations. www.med.uni-muenchen.de/egtm<br />
2) Guder WG, Narayanan S, Wisser H, Zawta B. Samples: From the Patient to the Laboratory. 2. Aufl., GIT, Darmstadt 2001<br />
3) Kohse KP, Wisser H. Antibodies as a Source of Analytical Errors. J Clin Chem Clin Biochem 1990; 28: 881-892<br />
4) Stieber P. Möglicher Einsatz der <strong>Tumormarker</strong> in der Nachsorge. Der Bay Int 1996; 16: 42-54<br />
5) Soletormos G et al. Interpretations of results for tumor markers on the basis of analytical imprecision and biological variation.<br />
Clin Chem 1993; 39: 2077-2083<br />
6) Stamey TA. Preoperative Serum PSA Below 10 µg/l Predicts Neither the Presence of Prostate Cancer Nor the Rate of Postoperative<br />
Failure. Clin Chem 2001; 47: 631-634 (Opinion)<br />
Begutachtet von:<br />
Korrespondenz:<br />
U.S. Huber-Tribolet, Zürich<br />
P. Hagemann, medica, Postfach, 80<strong>24</strong> Zürich<br />
23