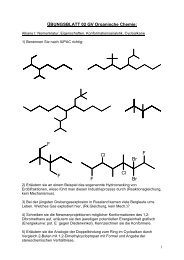
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
I. L A B O R A T O R I U M S T E C H N I K<br />
1. UN F A L L V E R H Ü T U N G<br />
<strong>NIEMALS</strong> <strong>OHNE</strong> <strong>SCHUTZBRILLE</strong> <strong>IM</strong> <strong>LABOR</strong> !!!!!<br />
1.1a Brandverhütung<br />
Viele organische Lösungsmittel (z.B. Ether, Petrolether, Schwefelkohlenstoff) besitzen<br />
einen hohen Dampfdruck und sind oft leicht entflammbar. Sie dürfen <strong>de</strong>shalb nicht in<br />
<strong>de</strong>r Nähe von offenen Flammen o<strong>de</strong>r von Wärmequellen (Gefahr <strong>de</strong>r Überdruckbildung<br />
in <strong>de</strong>n Flaschen) aufbewahrt wer<strong>de</strong>n. Lösungsmittel dürfen nur mittels eines<br />
Heizba<strong>de</strong>s (Öl- o<strong>de</strong>r Wasserbad) o<strong>de</strong>r Heizpilzes, aber nie auf offener Flamme erhitzt<br />
wer<strong>de</strong>n.<br />
Beim Kochen unter Rückfluß o<strong>de</strong>r beim Destillieren ist darauf zu achten, daß <strong>de</strong>r<br />
Kühler genügend kühlt und keine Lösungsmitteldämpfe entströmen. Lösungsmittelreste<br />
dürfen niemals in <strong>de</strong>n Ausguss gegossen wer<strong>de</strong>n.<br />
Natrium- und Kaliumreste dürfen nicht mit Wasser in Berührung kommen und erst recht<br />
nicht in <strong>de</strong>n Ausguss o<strong>de</strong>r Papierkorb geworfen wer<strong>de</strong>n (Explosionsgefahr!).<br />
Aufbewahrt wer<strong>de</strong>n diese Metalle unter Petroleum.<br />
1.1b Brandbekämpfung<br />
Lösungsmittelbrän<strong>de</strong> wer<strong>de</strong>n mit CO2-Handfeuerlöschern bekämpft.<br />
K E I N W A S S E R<br />
1
Brennen<strong>de</strong> Ölbä<strong>de</strong>r wer<strong>de</strong>n abge<strong>de</strong>ckt (Deckel o<strong>de</strong>r Lösch<strong>de</strong>cke). Falls Kleidung<br />
brennt, sofort Notdusche über <strong>de</strong>n Türen benutzen. Im Labor sollte möglichst keine<br />
Kunststoffkleidung getragen wer<strong>de</strong>n, da bei eventuellen Brän<strong>de</strong>n <strong>de</strong>r Kunststoff<br />
schmilzt und sehr schwer heilbare Brandwun<strong>de</strong>n hervorruft. Beson<strong>de</strong>rs <strong>de</strong>r Laborkittel<br />
sollte aus reiner Baumwolle bestehen.<br />
Wenn es brennt, muß sofort mit <strong>de</strong>n Löscharbeiten begonnen wer<strong>de</strong>n; kleinere Brän<strong>de</strong><br />
breiten sich sehr schnell ausl Beson<strong>de</strong>rs gefährlich sind Brän<strong>de</strong> von Benzol o<strong>de</strong>r<br />
Toluol, da sie mit sehr heißer Flamme brennen.<br />
1.2 Ätzen<strong>de</strong> Stoffe:<br />
Säuren, Laugen, Säurehalogeni<strong>de</strong> und ähnliche Stoffe verursachen schwer heilen<strong>de</strong><br />
Hautschä<strong>de</strong>n, die oft erst nach Stun<strong>de</strong>n erkennbar wer<strong>de</strong>n. Beim Umgang mit diesen<br />
Stoffen ist daher beson<strong>de</strong>re Sorgfalt angebracht. Hautstellen, die mit solchen Stoffen in<br />
Berührung kamen, sofort mit viel kaltem Wasser abspülen, Assistent benachrichtigen.<br />
Organische Stoffe (z.B. Methylierungsmittel, insbeson<strong>de</strong>re Dimethylsulfat!), dringen<br />
leicht durch die Haut ein und können nicht mit Wasser abgewaschen wer<strong>de</strong>n, daher zur<br />
Reinigung Alkohol verwen<strong>de</strong>n. Die Wirkungen zeigen sich oft nicht unmittelbar,<br />
son<strong>de</strong>rn erst nach Stun<strong>de</strong>n. Im Labor ist unbedingt eine Schutzbrille zu tragen, um<br />
Augenverletzung zu vermei<strong>de</strong>n (im an<strong>de</strong>ren Fall Verlust <strong>de</strong>s Versicherungsschutzes!).<br />
Falls Säure- und Laugenspritzer das Auge getroffen haben, Augendusche benutzen.<br />
Kleidung ist durch Tragen eines Labormantels (aus Baumwolle) zu schützen. Schon<br />
ein kleiner Spritzer Schwefelsäure durchlöchert die Kleidungl<br />
Zum Pipettieren immer Peleusball bzw. Gummihütchen o<strong>de</strong>r Schliff-(Fortuna)-Pipette<br />
verwen<strong>de</strong>n, niemals mit <strong>de</strong>m Mund.<br />
1.3 Glasbearbeitung<br />
Schwere Verletzungen treten auf, wenn man beim Überziehen eines Gummischlauches<br />
über ein Glasrohr abrutscht und sich das Glasrohr in die Hand stößt. Daher bei<br />
solchen Operationen Schutzhandschuhe verwen<strong>de</strong>n o<strong>de</strong>r die Hand mit einem Tuch<br />
schützen! Glasrohr durch Glycerin gleitend machen! Nicht mit angebrochenen<br />
Glasgeräten arbeiten.<br />
2
Beim Zerlegen von Schliffapparaten keine Gewaltanwendung, Schliffe mit einem Föhn<br />
erwärmen und nochmals versuchen, sie zu lösen. Gegebenenfalls Assistenten fragen,<br />
bzw. zum Glasbläser gehen.<br />
1.4 Arbeiten mit agressiven Verbindungen<br />
Halogenhaltige Stoffe, Nitroverbindungen, Mercaptane etc. sind oft stark giftig,<br />
gelegentlich tränenreizend o<strong>de</strong>r von üblem Geruch. Mit solchen Verbindungen sollte<br />
nur unter einem gut ziehen<strong>de</strong>n Abzug gearbeitet wer<strong>de</strong>n.<br />
Man orientiere sich vor <strong>de</strong>r Arbeit, wie etwa verschüttete Substanzproben rasch<br />
vernichtet wer<strong>de</strong>n können. Man vermei<strong>de</strong> vor allem das Einatmen von Dämpfen<br />
organischer Substanzen, beson<strong>de</strong>rs von Flüssigkeiten, die oft einen erheblichen<br />
Dampfdruck haben.<br />
Geruchsproben führe man so aus, daß man das Gefäß mit <strong>de</strong>r Substanz 20 cm von <strong>de</strong>r<br />
Nase entfernt hält und durch eine Handbewegung in Richtung Nase etwas von <strong>de</strong>m<br />
Dampf <strong>de</strong>r Verbindung in die Nase treibt. Geschmacksproben sind auf je<strong>de</strong>n Fall zu<br />
unterlassen!!! Viele Stoffe sind carcinogen, d.h. es gibt keine Toleranzgrenze. Beim<br />
Aufnehmen (Entfernen) ausgelaufener Flüssigkeiten niemals ohne Atemschutz und nur<br />
mit Handschuhen arbeiten - vorher Assistent zu Rate ziehen!<br />
Beson<strong>de</strong>rs gefährliche Verbindungen sind aus <strong>de</strong>r Tabelle (im Anhang) mit <strong>de</strong>n<br />
Maximalen Arbeitsplatz-Konzentrationen (MAK-Werten) zu erkennen. Dazu gehören<br />
u.a. Acetonitril, Anilin, Benzol, Blausäure, Chinon, Chloroform, Diazomethan,<br />
Dimethylsulfat, Hydrazin, Methylenchlorid, Methanol, nitrose Gase,<br />
Nitrosoverbindungen (beson<strong>de</strong>rs N-Nitrosoverbindungen), Phenol, Phenylhydrazin,<br />
Quecksilber, fast alle chlorierten Kohlenwasserstoffe u.v.a.<br />
Aus Sicherheitsgrün<strong>de</strong>n ist es verboten, bei <strong>de</strong>r Laborarbeit zu essen, zu trinken o<strong>de</strong>r<br />
zu rauchen !!! Das ist keine Schikane, <strong>de</strong>nken Sie an Ihre Gesundheit.<br />
Die Anordnungen <strong>de</strong>r Assistenten, die Sauberkeit und Sicherheit am Arbeitsplatz<br />
betreffen, sind unbedingt zu befolgen.<br />
3
NICHTBEACHTUNG DER VORSCHRIFTEN KANN ZUM AUSSCHLUSS AUS DEM<br />
PRAKTIKUM FÜHREN !!!<br />
Umweltbewußtes Verhalten:<br />
Es ist strengstens untersagt, die Umwelt durch fahrlässiges Hantieren und Verschütten<br />
von Chemikalien zu belasten. Versuchen Sie als Chemiker mit gutem Beispiel voran zu<br />
gehen. Nicht <strong>de</strong>r an<strong>de</strong>re - Sie sollen die Umwelt mitschützen!<br />
2. A R B E I T S V O R B E R E I T U N G<br />
Bevor eine synthetische o<strong>de</strong>r analytische organische Arbeit begonnen wer<strong>de</strong>n kann,<br />
sind folgen<strong>de</strong> Vorbereitungen zu treffen:<br />
2.1 Literatursuche:<br />
Im Regelfall liegen beim Assistenten für die im Organischen Praktikum auszuführen<strong>de</strong>n<br />
Reaktionen Arbeitsvorschriften aus. Trotz<strong>de</strong>m sollte man schon in diesem Stadium <strong>de</strong>s<br />
Studiums darüber Bescheid wissen, wie man nach Arbeitsvorschriften in <strong>de</strong>r Literatur<br />
sucht.<br />
Die gesuchte Verbindung wird zunächst als Bruttoformel aufgeschrieben und nach <strong>de</strong>r<br />
IUPAC-Nomenklatur benannt. Bei Schwierigkeiten in <strong>de</strong>r Benennung ist das Buch <strong>de</strong>r<br />
IUPAC, (International Union of Pure and Applied Chemistry) "Nomenclature of Organic<br />
Chemistry", Sections A, B und C 1 o<strong>de</strong>r das Buch von D. Hellwinkel; "Die<br />
systematische Nomenklatur <strong>de</strong>r Organischen Chemie", Springer Verlag, Hei<strong>de</strong>lberg<br />
1974, zu Rate zu ziehen.<br />
Zunächst versucht man die gesuchte Verbindung in <strong>de</strong>n gängigen Tabellenbüchern wie<br />
Chemiker-Kalen<strong>de</strong>r o<strong>de</strong>r D'Ans-Lax Handbuch zu fin<strong>de</strong>n. Bei allen hier aufgeführten<br />
Verbindungen ist die Literaturstelle im Beilstein bzw. <strong>de</strong>n Chemical Abstracts<br />
angegeben. Erst wenn diese Suche keinen Erfolg hat, benutzt man die großen<br />
Nachschlagewerke.<br />
4
Die gesamte chemische Literatur wird laufend in <strong>de</strong>n "Chemical Abstracts" und im<br />
Beilstein" so aufbereitet, daß man nach einer bereits in <strong>de</strong>r Literatur beschriebenen<br />
Verbindung sowohl unter ihrem IUPAC-Namen, als auch unter ihrem Trivialnamen (falls<br />
es so einen gibt) und nach <strong>de</strong>r Bruttoformel in <strong>de</strong>n Jahres-, 5-Jahres- o<strong>de</strong>r 10-Jahres-<br />
Registerbän<strong>de</strong>n suchen kann.<br />
In <strong>de</strong>r Regel ist die Suche unter <strong>de</strong>r Bruttoformel am sichersten, weil auch erfahrene<br />
Chemiker in <strong>de</strong>r Benennung von Verbindungen Fehler machen und dann die<br />
betreffen<strong>de</strong>n Verbindungen unter <strong>de</strong>m gegebenen Namen in <strong>de</strong>n Registerbän<strong>de</strong>n nicht<br />
zu fin<strong>de</strong>n wären.<br />
Wur<strong>de</strong> <strong>de</strong>r Name nicht richtig nach <strong>de</strong>r IUPAC-Nomenklatur gebil<strong>de</strong>t, so erhält man<br />
beim Durchsehen <strong>de</strong>r neben <strong>de</strong>r Formel stehen<strong>de</strong>n Namen <strong>de</strong>s Generalformelregisters<br />
<strong>de</strong>s "Beilsteins" o<strong>de</strong>r <strong>de</strong>s "Chemischen Zentralblattes" o<strong>de</strong>r <strong>de</strong>r "Chemical Abstracts"<br />
eine Denkhilfe: Man fin<strong>de</strong>t selbst mit beschei<strong>de</strong>nen Nomenklaturkenntnissen meist<br />
heraus, ob ein angeführter Name <strong>de</strong>r gesuchten Formel entsprechen kann. Die<br />
Formelregister sind in allen erwähnten Werken nach steigen<strong>de</strong>r Kohlenstoffzahl<br />
angeordnet, bezüglich <strong>de</strong>r Anordnung weiterer Elemente wur<strong>de</strong> aber in <strong>de</strong>n<br />
verschie<strong>de</strong>ner Formelregistern uneinheitlich verfahren. Im Beilstein und <strong>de</strong>ssen Er-<br />
gänzungswerk wer<strong>de</strong>n Verbindungen gleicher Kohlenstoffzahl in Gruppen unterteilt:<br />
(Gruppe 1 umfaßt Verbindungen, die außer Kohlenstoff nur noch ein Element<br />
enthalten, Gruppe 2 solche mit zwei Elementen, usw. Bei <strong>de</strong>r weiteren Unterteilung<br />
kommt <strong>de</strong>m Wasserstoff (häufigstes Begleitelement) die höchste Priorität zu, dann<br />
folgen Sauerstoff, Stickstoff, Chlor, Brom, Iod, Fluor, Schwefel und Phosphor (Richter-<br />
Alphabet).<br />
Es ergibt sich somit folgen<strong>de</strong> Aufeinan<strong>de</strong>rfolge <strong>de</strong>r Summenformeln:<br />
Hauptkriterium: C-Anzahl: C-1 steht vor C-2.<br />
Nebenkriterium: Anzahl <strong>de</strong>r vorhan<strong>de</strong>nen zusätzlichen Elementarten:<br />
C5H9O2N3 steht vor C5H9ONCl.<br />
5
Innerhalb <strong>de</strong>r Gruppen sind die Formeln nach steigen<strong>de</strong>r Atomzahl nach <strong>de</strong>m<br />
"Richteralphabet" angeordnet, z.B.<br />
C2-I Gruppe: C2H2, C2H4, C2H6, ....C2N2, .... C2Cl2, C2Cl4.... C2Br2 .... C2I2<br />
C2-II Gruppe:C2H2N4 ... C2H2Cl4 ... C2H3N .... C2H40, C2H402, C2H403 ... C2H4N2<br />
In <strong>de</strong>n Formelregistern <strong>de</strong>r Chemical Abstracts hat man auf die Unterteilung <strong>de</strong>r<br />
Verbindungen gleicher C-Zahl nach <strong>de</strong>r Zahl zusätzlicher Elemente verzichtet und<br />
wen<strong>de</strong>t bezüglich <strong>de</strong>r Priorität von Heteroatomen das Hill-Alphabet an: Hier besitzt<br />
zwar so wie nach <strong>de</strong>r, Richteralphabet <strong>de</strong>r Wasserstoff höchste Priorität, alle übrigen<br />
Elemente wer<strong>de</strong>n jedoch dann in alphabetischer Reihenfolge angeordnet.<br />
Die Anordnung <strong>de</strong>r obigen Bruttoformel <strong>de</strong>r C2-Gruppen ist also wie folgt vorzunehmen:<br />
C2H2, C2H2Cl4, C2H2N4, C2H3N, C2H4, C2H4N2, C2H4O, C2H4O2,<br />
C2H4O3, C2H6, C2Br2, C2Cl2, C2Cl4, C2I2,<br />
Ab <strong>de</strong>m zweiten Ergänzungswerk wur<strong>de</strong> das für die Chemical Abstracts angewandte<br />
Registerverfahren (Hill-Alphabet) auch bei <strong>de</strong>n Beilstein‘schen Sammelregistern<br />
verwen<strong>de</strong>t.<br />
Im Hauptteil <strong>de</strong>s Beilstein sind nur jene Verbindungen enthalten, die bis 1909 in <strong>de</strong>r<br />
Literatur publiziert wur<strong>de</strong>n. Das 1. Ergänzungswerk enthält Angaben über die Literatur<br />
von 1910 bis 1919, das zweite von 1920-1929 und das dritte von 1930 bis 1949. In <strong>de</strong>n<br />
Ergänzungswerken sind oben die Seitenzahlen <strong>de</strong>s Hauptwerkes und <strong>de</strong>r älteren<br />
Ergänzungswerke, auf <strong>de</strong>nen die gleiche Verbindung behan<strong>de</strong>lt wird, angegeben, so<br />
daß dadurch die Literatursuche wesentlich erleichter ist. Um die neuere Literatur zu<br />
erfassen, ist unbedingt eine Literatursuche auch in <strong>de</strong>n Registerbän<strong>de</strong>n <strong>de</strong>r Chemical<br />
Abstracts erfor<strong>de</strong>rlich. Sammelregister <strong>de</strong>r Chemical Abstracts, die die Literatur eines<br />
Zeitraumes von 5 und 10 Jahren erfassen, sind verfügbar, neuere Literaturangaben<br />
müssen <strong>de</strong>n Einzeljahresregistern entnommen wer<strong>de</strong>n.<br />
6
Am zweckmäßigsten geht man bei <strong>de</strong>r Literatursuche so vor, daß man zuerst in <strong>de</strong>n<br />
Registerbän<strong>de</strong>n neuesten Datums nach <strong>de</strong>r Verbindung sucht, weil man so gleichzeitig<br />
meist auch ältere Literatur erfasst, die in neueren Arbeiten fast immer zitiert ist.<br />
Dementsprechend beginnt man mit <strong>de</strong>r Literatursuche in <strong>de</strong>n neuesten Registerbän<strong>de</strong>n<br />
<strong>de</strong>r Chemical Abstracts und geht erst dann auf die Beilsteinbän<strong>de</strong> zurück.<br />
Wenn eine Verbindung noch nicht in <strong>de</strong>r Literatur beschrieben ist, so kann man nach<br />
Synthesebeschreibungen analoger Verbindungen suchen. Dies wird durch das<br />
Beilsteinsystem erleichtert, weil dort die Verbindungen nach Klassen geordnet sind.<br />
Beispielsweise kann man versuchen, eine Vorschrift <strong>de</strong>r beschriebenen Synthese<br />
nächst niedriger Homologer auszuführen.<br />
Wichtige Hilfe bei <strong>de</strong>r Vorplanung von Synthesen leisten Metho<strong>de</strong>nregister, <strong>de</strong>nen man<br />
entnehmen kann, welche Verfahren für bestimmte Umsetzung z.B. <strong>de</strong>n Ersatz von<br />
Halogen durch eine Hydroxylgruppe, anwendbar sind.<br />
Zu erwähnen sind hier:<br />
R.B. Wagner und H.D. Zook: "Synthetic Organic Chemistry", ausgezeichnete und<br />
übersichtliche Zusammenstellung von Metho<strong>de</strong>n zur Herstellung einfach substituierter<br />
aliphatischer Verbindungen. Lei<strong>de</strong>r sind nur jene Metho<strong>de</strong>n erfasst, die bis etwa 1954<br />
entwickelt wur<strong>de</strong>n.<br />
C. Weigand und G. Hilgetag.- "Organisch chemische Experimentierkunst". Sehr<br />
übersichtliche Zusammenstellung verschie<strong>de</strong>ner Reaktionstypen, allerdings auch nicht<br />
auf neustem Stand.<br />
I.T. Harrison und S.Harrison "Compendium of Organic Synthetic Plethods" enthält in<br />
Formelübersicht, jedoch ohne Kommentar, eine Fülle an Material, das <strong>de</strong>r neueren<br />
Literatur entnommen wur<strong>de</strong>, Geordnet nach funktionellen Gruppen. Erfor<strong>de</strong>rt doch<br />
einige Sucharbeit.<br />
C. Ä. Buehler und D. Pearson: "Survey of Organic Synthesis", ähnlich aufgebaut wie<br />
das Buch von Wagner und Zook, unter Auswertung <strong>de</strong>r Literatur bis 1970.<br />
Houben-Weyl: "Metho<strong>de</strong>n- <strong>de</strong>r organischen Chemie" : Umfangreichstes<br />
Metho<strong>de</strong>nregister mit ausführlichen Beispielen.<br />
Organic Reactions: Sehr ausführliche Behandlung häufig verwandter Metho<strong>de</strong>n (z.B.<br />
Reduktionen mit LiAlH4)- Je<strong>de</strong>s Jahr erscheint ein neuer Band.<br />
L.F. Fieser und M. Fieser: "Reagents for Organic Syntheses".<br />
7
W. Forst: "Neuere Metho<strong>de</strong>n <strong>de</strong>r Organischen Chemie", ähnliche Metho<strong>de</strong>nbehandlung<br />
wie in <strong>de</strong>n Organic Reactions, wobei beson<strong>de</strong>rer Wert auf neuere und weniger<br />
bekannte Verfahren gelegt wird.<br />
W. Theilheimer: "Synthetische Metho<strong>de</strong>n <strong>de</strong>r Organischen Chemie". Je<strong>de</strong>s Jahr<br />
erscheint ein Band, in <strong>de</strong>m in kurzer Form allgemein anwendbare neue<br />
Herstellungsverfahren <strong>de</strong>s letzten Jahres beschrieben sind.<br />
Lei<strong>de</strong>r ist die Suche nach bestimmten Metho<strong>de</strong>n durch das etwas unübersichtliche<br />
Registerverfahren (die Reaktionen sind innerhalb <strong>de</strong>r Bücher nicht nach Typen<br />
unterteilt) für <strong>de</strong>n Anfänger schwierig, doch enthalten diese Bän<strong>de</strong> eine gewaltige Fülle<br />
an Material. Beilstein und Chenical Abstracts enthalten nur zusammenfassen<strong>de</strong><br />
Referate <strong>de</strong>r Originalarbeiten.<br />
Hat man daher die betreffen<strong>de</strong> Verbindung in einem Beilstein o<strong>de</strong>r CA-Band<br />
gefun<strong>de</strong>n, so darf man sich nicht mit <strong>de</strong>n dort in Kurzform angeführten<br />
Herstellungsvorschriften zufrie<strong>de</strong>n geben, son<strong>de</strong>rn in je<strong>de</strong>m Fall ist die Originalliteratur<br />
einzusehen, die genauere Angaben über die Arbeitsbedingungen (Menge, Temperatur,<br />
Reaktionsdauer, eventuelle Schwierigkeiten, Ausbeute usw.) enthält. Unter Umstän<strong>de</strong>n<br />
ist die Herstellung ein und <strong>de</strong>rselben Verbundung in mehreren Literaturstellen<br />
beschrieben. Die Arbeitsvorschriften sind zu vergleichen, um <strong>de</strong>n rationellsten<br />
Zugangsweg ausfindig zu machen (Diskussion und Besprechung dieser<br />
Herstellungsmetho<strong>de</strong>n mit <strong>de</strong>m Assistenten).<br />
2.2 Vorbereitung <strong>de</strong>r Arbeitsmaterialien:<br />
Aus <strong>de</strong>n Arbeitsvorschriften <strong>de</strong>r Literatur kann man entnehmen, wie groß <strong>de</strong>r Ansatz zu<br />
wählen ist, um die gewünschte Menge an Produkt zu erhalten. Es ist jedoch zu<br />
beachten, daß mit Ausnahme gut überarbeiteter Laborvorschriften (Präparate aus <strong>de</strong>m<br />
„Organikum“, „Organic Synthesis“, „Vogels Textbook" etc.) in <strong>de</strong>r Originalliteratur, die<br />
Reaktionen mehrmals durchgeführt wur<strong>de</strong>n, nur die beste Ausbeute angegeben ist.<br />
Diese "Literaturausbeute" wird von Anfängern in <strong>de</strong>r Regel nicht erreicht, da kleine<br />
Fehler fast unvermeidbar sind. Aus <strong>de</strong>r Menge <strong>de</strong>r Reagentien ergibt sich die Größe<br />
<strong>de</strong>r bei <strong>de</strong>r Reaktion zu verwen<strong>de</strong>n<strong>de</strong>n Gefäße.<br />
Reagenzien vorbereiten: Auf Verunreinigung prüfen (Schmelz-Punktbestimmung (Fp)<br />
bzw. Sie<strong>de</strong>punktsbestimmung (Kp) , Brechungsin<strong>de</strong>x).<br />
8
Reagenzien abwiegen: Unbedingt darauf achten, dass die Waage exakt eben steht<br />
(durch Drehen <strong>de</strong>r Standbeine ausrichten und mit <strong>de</strong>r eingebauten 2D-Wasserwaage<br />
(„Libelle“) <strong>de</strong>n ebenen Stand überprüfen !!!)<br />
Lösungsmittel reinigen, eventuell absolutieren.<br />
Apparaturaufbau vorbereiten: Apparaturteile zusammenstellen, Schlauchverbindungen<br />
vorbereiten, Schlauchsicherungsklemmen (Ligaturen) bereitlegen.<br />
Alle diese Vorbereitungsarbeiten nehmen oft erhebliche Zeit in Anspruch (z.B.<br />
Absolutieren von Lösungsmitteln, Heranschaffen seltener Chemikalien, wenig<br />
gebrauchter Apparaturteile), daher ist es für rationelles Arbeiten unbedingt notwendig,<br />
soweit wie möglich vorzuplanen, am besten zwei Tage o<strong>de</strong>r mehr.<br />
Meist gibt es, wenn ein Ansatz einmal läuft, erhebliche Totzeit. Diese sollte unbedingt<br />
genutzt wer<strong>de</strong>n, um für das nächste und übernächste Präparat vorzuplanen.<br />
Später muß ein Chemiker imstan<strong>de</strong> sein, mehrere Ansätze gleichzeitig zu fahren und<br />
zu betreuen, das gelingt aber nur bei entsprechen<strong>de</strong>r Planung!<br />
9
2.3 Protokollführung:<br />
Hat man in <strong>de</strong>r Originalliteratur eine Arbeitsvorschrift gefun<strong>de</strong>n, so sollte man nicht<br />
damit einen Zettel beschmieren, da dieser früher o<strong>de</strong>r später verloren geht. Alle<br />
Eintragungen sind in ein Heft mit genauer Literaturangabe zu machen: Name <strong>de</strong>r<br />
Autoren (mit Vornameninitialen), Zeitschrift, Band, Seite und Erscheinungsjahr. Wenn<br />
man sich mit einem Extrakt <strong>de</strong>r Originalvorschrift begnügen muß, ist es zweckmäßig,<br />
später nochmals die Originalvorschrift zu kontrollieren, zumin<strong>de</strong>st dann, wenn man mit<br />
Schwierigkeiten zu kämpfen hat. Schon oft wur<strong>de</strong>n Randbemerkungen, die sich auf<br />
eine Arbeitsvorschrift beziehen, zunächst nicht wichtig genommen!<br />
Ein Protokoll sollte so ausgearbeitet sein, daß ein Kollege ohne weiteres danach<br />
arbeiten kann. Nach Angabe <strong>de</strong>s Namens, einer formelmäßigen Darstellung <strong>de</strong>s<br />
Reaktionsablaufes und Reaktionstyps hat das Protokoll Angaben über die Größe <strong>de</strong>s<br />
Ansatzes und <strong>de</strong>r verwen<strong>de</strong>ten Apparatur, auch Hinweise über <strong>de</strong>ren Aufbau zu<br />
enthalten. Angaben über <strong>de</strong>n Zeitbedarf für einzelne Reaktionen sind wichtig<br />
(Arbeitszeiteinteilung).<br />
Über Beobachtungen bezüglich <strong>de</strong>s Reaktionsablaufes (Temperatur- und<br />
Farbän<strong>de</strong>rungen, Schwierigkeiten (z.B. Schäumen beim Destillieren) ist während <strong>de</strong>r<br />
Arbeit Protokoll zu führen, am Tage nach <strong>de</strong>r Reaktion hat man Vieles schon wie<strong>de</strong>r<br />
vergessen! Gute Protokollführung erlaubt erst eine exakte Reproduktion und hilft Fehler<br />
aufspüren! Zum Schluß <strong>de</strong>s Protokolls sind Angaben über das Reaktionsprodukt und<br />
seine Reinheitskriterien zu machen (Schmp. , Sdp.), wobei man nicht vergessen sollte,<br />
zu schreiben, aus welchem Lösungsmittel (und mit welcher Lösungsmittelmenge)<br />
umkristallisiert wur<strong>de</strong>. Zum Schluß ist die theoretisch mögliche, die in <strong>de</strong>r Literatur<br />
erreichte und praktische Ausbeute zu berechnen.<br />
Die Protokolle müssen in einem Bericht zusammengestellt wer<strong>de</strong>n (keine losen<br />
Blätter!); neue Präparate wer<strong>de</strong>n erst nach Abgabe alten Präparate und <strong>de</strong>s<br />
Laborberichts ausgegeben.<br />
Die Protokolle sollen kurzgehalten wer<strong>de</strong>n und nur Daten und Beobachtungen<br />
enthalten, die wirklich gemessen wor<strong>de</strong>n sind.<br />
Im Folgen<strong>de</strong>n ist kurz skizziert, wie ein Laborbericht aufgebaut sein muss:<br />
10
Name <strong>de</strong>s Präparats<br />
1. Vollständige Literaturangabe (Buchtitel, Autoren, Seite, Verlag, etc.)<br />
2. Reaktionsname (z.B. Veresterung, Frie<strong>de</strong>l-Crafts-Acylierung)<br />
3. Reaktionstyp (z.B. nucleophile Substitution eines Carbonsäurechlorids)<br />
4. Vollständige Reaktionsgleichung (unter <strong>de</strong>n Formeln Angabe <strong>de</strong>s Molgewichts)<br />
5. Reaktionsverlauf (Reaktionsmechanismus)<br />
6. Geräte (Kolben, Rückflußkühler, mechanischer Rührer), keine trivialen<br />
Apparaturen abbil<strong>de</strong>n<br />
7. Eingesetzte Mengen (in mol und Gramm)<br />
8. Reaktionsbedingungen (Reaktionstemperatur, Druck, Zeitdauer ...)<br />
9. Aufarbeitung, Abtrennung, Isolierung <strong>de</strong>s gewünschten Produkts<br />
10. Reinigung u. Charakterisierung <strong>de</strong>s Präparats (Schmp., Sdp., Rf, nD, IR-Daten,<br />
eventuell NMR- und UV-Daten, zusätzlich die betreffen<strong>de</strong>n Angaben <strong>de</strong>r Literatur)<br />
11. Ausbeuteangabe: Theorie, Literatur und praktisch gefun<strong>de</strong>n jeweils in %, g und<br />
Mol.<br />
3. GERÄTE, APPARATUREN UND IHRE BENUTZUNG<br />
3.1. Reaktionsgefäße<br />
Die gebräuchlichsten Reaktionsgefäße sind Erlenmeyer- und Rundkolben die zur<br />
Erweiterung <strong>de</strong>s Anwendungsbereiches mit mehreren Hälsen versehen sind (Abb. 1):<br />
Abb. 1:<br />
300 mL<br />
300<br />
250<br />
200<br />
150<br />
100<br />
ERLENMEYER-KOLBEN<br />
Enghals Weithals<br />
300 mL<br />
300<br />
250<br />
200<br />
150<br />
100<br />
Normschliff<br />
NS29<br />
300 mL<br />
NS29<br />
300<br />
250<br />
200<br />
150<br />
100<br />
1 L<br />
Rundkolben<br />
500 mL<br />
11
Wenn nicht genügend Öffnungen zur Verfügung stehen, verwen<strong>de</strong>t man einen Claisen-<br />
Aufsatz (Abb. 2):<br />
Abb. 2:<br />
NS29<br />
Zum Zutropfen von Reaktionsflüssigkeiten wer<strong>de</strong>n Tropftrichter verwen<strong>de</strong>t, die bei<br />
geschlossenen Apparaturen einen Druckausgleich haben müssen. Abb. 3<br />
Abb. 3:<br />
mL<br />
250<br />
200<br />
150<br />
100<br />
50<br />
NS29<br />
Tropftrichter<br />
ohne mit<br />
Druckausgleich Druckausgleich<br />
3.2. Apparaturen – allgemeine Arbeitshinweise:<br />
Heutzutage wer<strong>de</strong>n die Glasteile <strong>de</strong>r Apparaturen nahezu ausschließlich mit genormten<br />
Schliffen verbun<strong>de</strong>n.<br />
3.2.1.a) Schliffe:<br />
Man unterschei<strong>de</strong>t zwischen Kegel- und Kugelschliffen. Die gebräuchlichsten sind die<br />
Kegelschliffe (Abb.4).<br />
mL<br />
250<br />
200<br />
150<br />
100<br />
50<br />
NS29<br />
75 o<br />
12
Abb. 4:<br />
Kugelschliffe haben <strong>de</strong>n Vorteil <strong>de</strong>r größeren Beweglichkeit in sich und wer<strong>de</strong>n<br />
verwen<strong>de</strong>t, wenn flexible Verbindungen erfor<strong>de</strong>rlich sind. Lei<strong>de</strong>r sind sie sehr teuer.<br />
Wenn bei einem Kegelschliff die geschliffene Fläche außen ist, so spricht man vom<br />
Kern, an<strong>de</strong>renfalls von <strong>de</strong>r Hülse. Die Bezeichnung <strong>de</strong>r Schliffgrößen sind:<br />
NS 9, NS 14,5, NS 1-01, NS 29, NS 32, .... (NS = Norm-Schliff, die Zahl bezeichnet die<br />
größte Weite - falls noch eine zweite Zahl angegeben ist) bezieht sich diese auf die<br />
Schlifflänge).<br />
Zur Verbindung von Schliffen verschie<strong>de</strong>ner Größe wer<strong>de</strong>n Übergangsstücke<br />
verwen<strong>de</strong>t. Abb. 5<br />
Abb. 5:<br />
Quickfit-<br />
Adapter<br />
29-14 14-29 NS 29 NS 14<br />
zum Einführen<br />
von Glasrohr bzw.<br />
Thermometer<br />
13
Behandlung von Schliffen:<br />
Die präzisionsgeschliffenen Flächen <strong>de</strong>r Schliffe sind äußerst empfindlich gegenüber<br />
mechanischen Verunreinigungen (Glassplitter, Staubteilchen, Sand usw.); schon<br />
kleinste Kratzer bedingen oft Undichtigkeit einer Apparatur, beson<strong>de</strong>rs beim Betrieb<br />
unter vermin<strong>de</strong>rtem Druck (Vakuum<strong>de</strong>stillation).<br />
Es ist <strong>de</strong>shalb auf peinlichste Sauberkeit <strong>de</strong>r Schliffflächen zu achten.<br />
Zur Erhöhung <strong>de</strong>r Dichtigkeit und zur Materialschonung (Reibung) wer<strong>de</strong>n die Schliffe<br />
vor <strong>de</strong>m Zusammenbau dünn mit Siliconfett bestrichen.<br />
Bei Handhabung von kleinen Substanzmengen wirkt sich die Verwendung von<br />
Schlifffett jedoch oft störend aus, da es teilweise in die Probe gelangt und diese<br />
verunreinigt. In diesen Fällen sollte man besser auf Graphit als Gleitmittel<br />
zurückgreifen.<br />
2.2.1.b)_Aufbau von_Apparaturen:<br />
Vor Aufbau einer Apparatur müssen alle dafür notwendigen Teile bereitgelegt wer<strong>de</strong>n.<br />
Kühlwasserschläuche an Kühlern sind vor <strong>de</strong>m Zusammenbau zu befestigen.<br />
Bestimmend für die Höhe <strong>de</strong>s Aufbaues und damit für die Anordnung <strong>de</strong>r Apparatur ist<br />
die Höhe <strong>de</strong>r Hebebühne mit Magnetrührer und Ölbad, Wasserbad, usw.<br />
Der Reaktionsrundkolben soll so hoch angebracht wer<strong>de</strong>n, dass durch herunterdrehen<br />
<strong>de</strong>r Hebebühne je<strong>de</strong>rzeit das Heizbad (Wasserbadtopf, Ölbadtopf) vollständig vom<br />
Reaktionskolben entfernt und entnommen wer<strong>de</strong>n kann (möglicherweise muss bei<br />
manchen Reaktionen rasch gekühlt wer<strong>de</strong>n, z.B. bei <strong>de</strong>r Grignard-Reaktion) und durch<br />
ein Kältebad ersetzt wer<strong>de</strong>n kann.<br />
Danach wird die Apparatur schrittweise vervollständigt, in<strong>de</strong>m die Schliffteile erst locker<br />
eingepaßt und dann spannungsfrei befestigt wer<strong>de</strong>n.<br />
Bei Aufbau eines Rührwerkes (KPG-Rührer, siehe unter Rühren) sollte <strong>de</strong>r schwere<br />
Motor vor Einbau <strong>de</strong>r kleineren Teile (wie Tropftrichter, Rückflußkühler usw.) am Stativ<br />
befestigt wer<strong>de</strong>n (zur Vermeidung von Glasbruch bei späterem Einbau).<br />
14
Muffen sind so anzubringen, daß jeweils die Öffnung <strong>de</strong>r Muffenhalterungen nach oben<br />
offen sind (Abb. 6).<br />
Abb .6:<br />
3.2.1.c) Allgemeine Hinweise zum Erhitzen:<br />
Organische Reaktionen, bei <strong>de</strong>nen sich durch das Erhitzen das Lösungsmittel o<strong>de</strong>r<br />
Reaktionspartner verflüchtigen könnten, dürfen nur in Rundkolben mit<br />
Rückflußkühler durchgeführt wer<strong>de</strong>n, da das Erhitzen in Bechergläsern o<strong>de</strong>r<br />
Erlenmeyerkolben auf <strong>de</strong>m Magnetrührer zum Überschäumen und in <strong>de</strong>r Folge schon<br />
oft zu gefährlichen Laborbrän<strong>de</strong>n geführt hat!!!<br />
Zur Vermeidung von Sie<strong>de</strong>verzügen müssen Sie<strong>de</strong>steine, Sie<strong>de</strong>kapillaren o<strong>de</strong>r<br />
mechanische Rührer (Magnetrührer mit Rührfisch) benutzt wer<strong>de</strong>n. Sie<strong>de</strong>steine dürfen<br />
jedoch nie in die schon heiße Flüssigkeit geworfen wer<strong>de</strong>n, da es dann zu plötzlichen<br />
Aufsie<strong>de</strong>n und Schäumen kommt. Sie<strong>de</strong>steine verlieren ihre Wirksamkeit, wenn die<br />
Sie<strong>de</strong>flüssigkeit vorübergehend abgekühlt wird, z.B. bei Zugabe von Lösungsmitteln bei<br />
<strong>de</strong>r Umkristallisation, so daß auf je<strong>de</strong>n Fall vor erneutem Anheizen neue Sie<strong>de</strong>steine<br />
zugegeben wer<strong>de</strong>n müssen. Üblicherweise wer<strong>de</strong>n heute fast ausschließlich<br />
Magnetrührer mit Rührfisch verwen<strong>de</strong>t.<br />
Bei <strong>de</strong>r Benutzung von Ölbä<strong>de</strong>rn ist strengstens darauf zu achten, dass kein<br />
Wasser in das Öl gelangt: Erhitzt man ein Ölbad, in <strong>de</strong>m sich Wasser befin<strong>de</strong>t,<br />
kann das Wasser Explosionsartig verdampfen, heisses Ölbad spritzt herum !!!<br />
Kontaminierte Ölbä<strong>de</strong>r mehrere Tage lang unterhalb 100°C halten, dann erst<br />
wie<strong>de</strong>r langsam stärker erhitzen!!!<br />
Wasserschläuche an Kühlern verlässlich mit Schlauchklemmen sichern.<br />
15
3.2.2. Reaktionsapparaturen:<br />
a) Erhitzen unter Rückfluß<br />
Reaktionen, die in sie<strong>de</strong>n<strong>de</strong>n Lösungsmitteln ablaufen, führt man im Rundkolben<br />
mit Magnetrührer und Rückflußkühler durch (Abb.8). Die aufsteigen<strong>de</strong>n<br />
Lösungsmitteldämpfe kon<strong>de</strong>nsieren im Kühler und tropfen in <strong>de</strong>n Kolben zurück.<br />
Abb. 8:<br />
Rührfisch<br />
300<br />
o C<br />
200<br />
50<br />
100<br />
AN<br />
150 AUS<br />
500 mL<br />
20 o<br />
AUS 1000<br />
20 o<br />
0 U/min<br />
1500<br />
AN<br />
250<br />
Kühlwasser<br />
Zulauf<br />
Ablauf<br />
750<br />
500<br />
Steigrohr<br />
Ölbad o<strong>de</strong>r<br />
Wasserbad<br />
Magnetrührer<br />
mit Heizung<br />
16
) Kühlen<br />
Folgen<strong>de</strong> Kühlertypen wer<strong>de</strong>n in <strong>de</strong>r Praxis verwen<strong>de</strong>t (Abb.9).<br />
Abb. 9:<br />
Liebig-<br />
Kühler<br />
20o<br />
Dimroth-<br />
Kühler<br />
20 o<br />
Rückflusskühler<br />
mit Glasolive mit Schraubolive<br />
1 2 3<br />
20 o<br />
20 o<br />
Intensiv-<br />
Kühler<br />
Dimroth-<br />
Kühler<br />
1. Liebig-Kühler: Geringe Kühlwirkung, nicht mehr in Gebrauch.<br />
2. Dimroth-Kühler: Gebräuchlichster Kühler beim Sie<strong>de</strong>n unter Rückfluß.<br />
RD14<br />
45 o<br />
RD14<br />
45 o<br />
RD14<br />
45 o<br />
RD14<br />
45 o<br />
Intensiv-<br />
Kühler<br />
3. Intensiv-Kühler: Kombination aus Liebig- und Dimroth-Kühler: Sehr gute<br />
Kühlwirkung, gut für leichtflüchtige Lösungsmittel - wie Ether - geeignet. Nachteil:<br />
Teuer.<br />
Bei stark exothermer Reaktion o<strong>de</strong>r bei Reaktionen, die bei tiefen Temperaturen<br />
durchgeführt wer<strong>de</strong>n, muß <strong>de</strong>r Reaktionskolben zusätzlich durch ein Kältebad gekühlt<br />
wer<strong>de</strong>n. Die Wahl <strong>de</strong>s Kühlmittels richtet sich nach Kühltemperatur und <strong>de</strong>r<br />
abzuführen<strong>de</strong>n Wärme.<br />
17
Ein Wasserbad ist billig und wird bei geringer notwendigen Wärmeabfuhr benutzt. Für<br />
Temperaturen um und etwas oberhalb von 0°C dient ein Gemisch aus zerstoßenem Eis<br />
und Wasser. Eine Eis-Kochsalz-Gemisch kühlt bis etwa –20°C (ca. 1/3 Salz, 2/3 Eis).<br />
Bei Verwendung von festem Kohlendioxid (Trockeneis) in Isopranol kann bis –78°C<br />
gekühlt wer<strong>de</strong>n. Diese Kältemischung bereitet man in einem Dewar-Gefäß (Abb. 10)<br />
zu.<br />
Abb. 10:<br />
hoch<br />
Dewargefäße<br />
verspiegelter Glaskörper<br />
mit Vakuum<br />
flach<br />
Mit flüssigem Stickstoff kann man bis –196°C kühlen.<br />
VORSICHT: Ein Dewargefäß, das mit Trockeneis beschickt wur<strong>de</strong>, sollte danach<br />
keinesfalls wie<strong>de</strong>r für flüssigen Stickstoff verwen<strong>de</strong>t wer<strong>de</strong>n, da durch das feste<br />
Trockeneis die innere Glaswand zerkratzt wer<strong>de</strong>n kann und bei stärkerer,<br />
schlagartiger Abkühlung auf –196°C die Gefahr einer Implosion besteht:<br />
Einmal Trockeneis – immer Trockeneis!!<br />
c) Rühren<br />
Bei verschie<strong>de</strong>nen Reaktionsansätzen, beson<strong>de</strong>rs bei solchen mit mehreren Phasen,<br />
ist gutes Rühren zur besseren Durchmischung bzw. zur Erhöhung <strong>de</strong>r<br />
Phasengrenzfläche, nötig. Dazu bieten sich verschie<strong>de</strong>ne Möglichkeiten an:<br />
1. KPG-Rührer: (KPG = Kerngeschliffenes Präzisions Glasgerät) mit verschie<strong>de</strong>nen<br />
Rührflügeltypen (Abb. 11).<br />
Abb. 11<br />
.<br />
18
Paraffin<br />
200 300 400<br />
500<br />
50 0 600<br />
1 L<br />
AN<br />
AUS<br />
KPG-Rührmotor<br />
Gummischlauch<br />
KPG-Rührwelle<br />
KPG-Rührhülse<br />
Vorteil: Sehr gutes Drehmoment und gute Durchmischung sind gewährleistet.<br />
Die Welle <strong>de</strong>s Rührers muß mit Glycerin o<strong>de</strong>r Paraffin geschmiert wer<strong>de</strong>n.<br />
2. Magnet-Rührer mit Heizung: (nur für kleinere Mengen geeignet) erlaubt in völlig<br />
abgeschlossenen Apparaturen zu rühren und gleichzeitig zu erhitzen. Er besteht aus<br />
einem mittels Motor in Rotation versetzten Magneten, <strong>de</strong>r im Reaktionsgefäß einen mit<br />
Teflon überzogenen Eisenstabmagneten (Rührfisch) bewegt.<br />
d) Gase, Dosierung und Handhabung<br />
Muß einer Reaktion Gas zugeführt wer<strong>de</strong>n (z.B. Chlorierung) ergeben sich<br />
verschie<strong>de</strong>ne Probleme (z.B. <strong>de</strong>r Trocknung, Reinigung und Dosierung).<br />
1. Gasdruckflaschen<br />
19
Gase kommen gewöhnlich in Gasdruckflaschen in <strong>de</strong>n Han<strong>de</strong>l, in <strong>de</strong>nen diese<br />
meistens auf ca. 200 atü komprimiert sind. Der schwächste Punkt dieser Gasflaschen<br />
ist das Hauptventil, das durch eine Schutzkappe beim Transport gesichert ist. Diese<br />
darf erst abgeschraubt wer<strong>de</strong>n, wenn die Gasflasche ausreichend gegen Umfallen<br />
gesichert ist, sonst besteht LEBENSGEFAHR.<br />
Gemäß aktueller Vorschriften dürfen Gasflaschen überhaupt nicht mehr in<br />
Labors freistehend aufgestellt wer<strong>de</strong>n, son<strong>de</strong>rn nur noch in dafür geeigneten<br />
Gasflaschen-Sicherheitsschränken.<br />
Die Entnahme <strong>de</strong>r Gase aus <strong>de</strong>r Bombe erfolgt über ein Reduzierventil, <strong>de</strong>ssen<br />
Funktion in Abb. 12 angegeben ist.<br />
Abb. 12:<br />
2. Bei <strong>de</strong>r Handhabung ist folgen<strong>de</strong>s zu beachten<br />
1. Flasche mit einer Kette o<strong>de</strong>r Schelle am Labortisch o<strong>de</strong>r an <strong>de</strong>r Wand sichern.<br />
2. Schutzkappe abschrauben.<br />
3. Reduzierventil anschrauben.<br />
20
4. Absperrventil und Stellschraube schließen, d.h. Stellschraube <strong>de</strong>r Gummimembrane<br />
ganz herausschrauben, Absperrventil ohne Kraftanwendung (sonst wird das<br />
Na<strong>de</strong>lventil beschädigt) zudrehen<br />
5. Hauptventil <strong>de</strong>r Bombe Öffnen, Druck wird am Manometer I angezeigt.<br />
6. An <strong>de</strong>r Stellschraube gewünschten Vordruck einstellen (Manometer II).<br />
7. Am Absperrventil Strömungsgeschwindigkeit regeln.<br />
3. Trocknen und Reinigen von Gasen<br />
Die meisten im Labor angewandten Gase sind nicht analysenrein, son<strong>de</strong>rn enthalten<br />
Beimengungen von Fremdgasen und beson<strong>de</strong>rs von Wasser.<br />
Bei einigen Reaktionen ist es unumgänglich, das Wasser vorher zu entfernen (z.B.<br />
Radikalreaktionen).<br />
Das Gas wird hierzu durch eine Waschflasche geleitet, in <strong>de</strong>r sich konzentrierte<br />
Schwefelsäure befin<strong>de</strong>t.<br />
Vor und hinter dieser Waschflasche befin<strong>de</strong>n sich Sicherheitsflaschen, die ein<br />
Rücksteigen <strong>de</strong>r Schwefelsäure, sowohl in die Bombe als auch in die Apparatur,<br />
verhin<strong>de</strong>rn (Abb.13).<br />
Abb. 14:<br />
Gase, die mit Schwefelsäure reagieren (z.B. Ammoniak), können auf diese Weise nicht<br />
getrocknet wer<strong>de</strong>n. In diesem Falle benutzt man einen sog. Trockenturm, <strong>de</strong>r je nach<br />
Anwendung mit unterschiedlichen festen Trockenmitteln (für NH3 z.B. Ca0) beschickt<br />
wird (siehe auch Kapitel: Trocknen im Labor) (Abb.14).<br />
Abb. 14:<br />
21
e) Kombinationen von Apparaturen<br />
Im Folgen<strong>de</strong>n wer<strong>de</strong>n einige <strong>de</strong>r gebräuchlichsten Anwendungsbeispiele <strong>de</strong>r<br />
Kombination von Glasapparaturen im Labor gegeben:<br />
Abb. 15:<br />
1<br />
20 o<br />
20 o<br />
2<br />
20 o<br />
20 o<br />
1. Erhitzen unter Rückfluß mit Trockenrohr<br />
2. Erhitzen unter Rückfluß und Gaseinleitung<br />
3. Reaktionskolben (Dreihals) mit KPG-Rührer, Tropftrichter und Rückflußkühler<br />
4. Reaktionskolben<br />
Tropftrichter<br />
mit KPG-Rührer, Innenthermometer, Rückflußkühler u.<br />
f) Reaktionen-unter UV-Bestrahlung<br />
250 mL<br />
200<br />
150<br />
100<br />
50<br />
200 300 400<br />
500<br />
AN<br />
50 0 600<br />
AUS<br />
1 L<br />
1 L<br />
3<br />
20 o<br />
20 o<br />
20 o<br />
20 o<br />
mL 100<br />
75<br />
50<br />
25<br />
200 300 400<br />
500<br />
50 0 600<br />
AUS<br />
1 L<br />
1 L<br />
4<br />
AN<br />
o<br />
C<br />
10 0<br />
9 0<br />
8 0<br />
7 0<br />
6 0<br />
5 0<br />
4 0<br />
3 0<br />
2 0<br />
1 0<br />
0 0<br />
1 0<br />
22
Reaktionen, bei <strong>de</strong>nen durch Bindungsbruch Radikale gebil<strong>de</strong>t wer<strong>de</strong>n müssen,<br />
benötigen eine hohe Energiezufuhr, die allein durch Heizen nicht aufgebracht wer<strong>de</strong>n<br />
kann:<br />
Cl-Cl Æ Cl • + Cl •<br />
In diesem Falle bedient man sich <strong>de</strong>r Bestrahlung mit UV-Licht, <strong>de</strong>ren Lichtquanten<br />
energiereich genug sind, Radikale zu bil<strong>de</strong>n.<br />
Abb. 16<br />
Gaseinleitung<br />
zum<br />
Netzgerät<br />
20 o<br />
20 o<br />
Tauchrohr<br />
aus Quarzglas<br />
Quecksilbertauchlampe<br />
Das Tauchrohr muß aus Quarzglas bestehen, weil normales Geräteglas die UV-<br />
Strahlung absorbiert.<br />
g) Apparatur zur azeotropen Entfernung von Reaktionswasser (Wasserabschei<strong>de</strong>r)<br />
Gleichgewichtsreaktionen, bei <strong>de</strong>nen Wasser entsteht, wie z.B. Veresterungen, wer<strong>de</strong>n<br />
so durchgeführt, dass durch Entfernung <strong>de</strong>s Reaktionswassers das Gleichgewicht<br />
„gestört“, d.h. zu Gunsten <strong>de</strong>r Produkte „verschoben“ wird. Dies kann durch azeotrope<br />
Destillation mit einem Schlepper geschehen. Ein gebräuchlicher Schlepper ist Toluol,<br />
das leichter als Wasser ist (Dichte < 1). Hierfür dient die folgen<strong>de</strong> Apparatur (Abb. 17a)<br />
Abb. 17a:<br />
23
Wasserabschei<strong>de</strong>r: links für „leichte“ LM (Dichte < 1), rechts für „schwere“ LM<br />
20 o<br />
20 o<br />
Das Azeotrop sie<strong>de</strong>t bei geringerer Temperatur als die bei<strong>de</strong>n Einzelkomponenten.<br />
Das Kon<strong>de</strong>nsat trennt sich in <strong>de</strong>r Kälte wie<strong>de</strong>r in zwei Phasen, wobei sich Wasser als<br />
schwerere Phase unten abschei<strong>de</strong>t und <strong>de</strong>r Schlepper wie<strong>de</strong>r zurück in <strong>de</strong>n Kolben<br />
gelangt.<br />
Wichtig: Den graduierten Auffangteil (Meßrohr) <strong>de</strong>s Wasserabschei<strong>de</strong>rs vor <strong>de</strong>r<br />
Reaktion auch mit Schlepper füllen, um die LM-Menge im Reaktionskolben konstant zu<br />
halten.<br />
Bei Verwendung von Lösungsmitteln, die schwerer als Wasser sind (Dichte > 1) (z.B.<br />
CH2Cl2, Dichlormethan = Methylenchlorid) verwen<strong>de</strong>t man eine an<strong>de</strong>re Apparatur, bei<br />
<strong>de</strong>r daß graduierte Meßrohr nach oben gebogen ist (Abb.17b). Wasser schei<strong>de</strong>t sich<br />
oben ab.<br />
Wichtig: Auch hier das Messrohr vor <strong>de</strong>r Reaktion (durch schräghalten) durch <strong>de</strong>n<br />
geöffneten Schliffhahn am Messrohr mit Schlepper füllen, dann <strong>de</strong>n Schliffhahn<br />
schließen und <strong>de</strong>n Wasserabschei<strong>de</strong>r auf <strong>de</strong>n Reaktionskolben setzen.<br />
Abb. 17b:<br />
24
Dieser Wasserabschei<strong>de</strong>r ist sehr empfindlich und bricht leicht!!<br />
3.2.3. Destillation:<br />
a) Destillation unter Normaldruck<br />
Die wichtigste Reinigungsmetho<strong>de</strong> für leichtflüchtige Substanzen (Flüssigkeiten) ist die<br />
Destillation. Die verunreinigte Flüssigkeit wird in einem Kolben zum Sie<strong>de</strong>n erhitzt, <strong>de</strong>r<br />
Dampf wird in einem schrägabfallen<strong>de</strong>n Kühler kon<strong>de</strong>nsiert und das "Destillat" in <strong>de</strong>r<br />
Vorlage aufgefangen. Leichter flüchtige Verbindungen (z.B. Lösungsmittel) verdampfen<br />
zuerst und wer<strong>de</strong>n verworfen. Die Hauptkomponente (z.B. Reaktionsprodukt) wird<br />
aufgefangen, wenn ein konstanter Sie<strong>de</strong>punkt abgelesen wird. Die Destillation ist<br />
been<strong>de</strong>t, wenn die Temperatur weiter ansteigt o<strong>de</strong>r abfällt (Abb. 18).<br />
Abb. 18:<br />
25
o<br />
C<br />
25 0<br />
24 0<br />
23 0<br />
22 0<br />
21 0<br />
20 0<br />
19 0<br />
18 0<br />
17 0<br />
16 0<br />
15 0<br />
14 0<br />
13 0<br />
12 0<br />
11 0<br />
10 0<br />
9 0<br />
8 0<br />
7 0<br />
6 0<br />
5 0<br />
4 0<br />
3 0<br />
2 0<br />
1 0<br />
0 0<br />
1 0<br />
Kühlwasser<br />
Vorstoß<br />
Die Destillation unter Normaldruck sollte nur bei Substanzen angewandt wer<strong>de</strong>n, die<br />
einen Sie<strong>de</strong>punkt zwischen 40-150°C besitzen. Tiefer sie<strong>de</strong>n<strong>de</strong> Komponenten wer<strong>de</strong>n<br />
nicht genügend gekühlt; <strong>de</strong>r Verlust wird zu groß (Dämpfe entweichen). In solchen<br />
Fällen muß man entwe<strong>de</strong>r die Vorlage kühlen (Eis/Kochsalz, Isopropanol/Trockeneis)<br />
o<strong>de</strong>r <strong>de</strong>n Kühler mit tiefgekühltem Methanol aus einem Kryostaten betreiben.<br />
Bei Substanzen, die höher als 150°C sie<strong>de</strong>n, ist die Gefahr <strong>de</strong>r Zersetzung bei <strong>de</strong>r<br />
Destillation unter Normaldruck sehr groß. In diesem Falle bedient man sich <strong>de</strong>r<br />
Vakuum<strong>de</strong>stillation.<br />
b) Vakuum<strong>de</strong>stillation<br />
Die Vakuum<strong>de</strong>stillation wird wie die Destiilation ohne Unterdruck meist fraktionierend<br />
durchgeführt (Abb.19):<br />
Abb.19:<br />
26
o<br />
C<br />
25 0<br />
24 0<br />
23 0<br />
22 0<br />
21 0<br />
20 0<br />
19 0<br />
18 0<br />
17 0<br />
16 0<br />
15 0<br />
14 0<br />
13 0<br />
12 0<br />
11 0<br />
10 0<br />
9 0<br />
8 0<br />
7 0<br />
6 0<br />
5 0<br />
4 0<br />
3 0<br />
2 0<br />
1 0<br />
0 0<br />
1 0<br />
Fraktionierte Vakuum<strong>de</strong>stillation<br />
zur<br />
Vakuumpumpe<br />
Bredt-Vorstoß<br />
(Spinne)<br />
Der Dampfdruck einer Flüssigkeit ist stark von <strong>de</strong>r Temperatur abhängig. Die<br />
Temperaturabhängigkeit wird durch die Gleichung von Clausius-Clapeyron<br />
beschrieben:<br />
d lnp / dT = HV / RT 2<br />
p - Dampfdruck<br />
HV<br />
molare Verdampfungsenthalpie<br />
T - absolute Temperatur (Kelvin)<br />
R - Gaskonstante<br />
in integrierter Form: ln p = -HV / RT + C<br />
ln p aufgetragen gegen 1/T sollte also eine Gera<strong>de</strong> ergeben. Dies ist nur richtig unter<br />
<strong>de</strong>r Annahme, daß HV temperaturunabhäng ist, was aber nur in kleineren<br />
Temperaturbereichen <strong>de</strong>r Fall ist (Abb. 20).<br />
Abb. 20:<br />
.<br />
27
Durch Erniedrigung <strong>de</strong>s Druckes in <strong>de</strong>r Destillationsapparatur ist es also möglich, <strong>de</strong>n<br />
Sie<strong>de</strong>punkt einer Substanz (verglichen ihrem Sie<strong>de</strong>punkt bei Normaldruck) so weit zu<br />
senken, daß eine vernünftige (40°C - 150°C) Destillationstemperatur erreicht wird.<br />
Das Vakuum wird durch eine Membranpumpe, o<strong>de</strong>r, für besseres Vakuum, durch eine<br />
Drehschieber-Ölpumpe, in speziellen Fällen <strong>de</strong>r Hochvakuum<strong>de</strong>stillation durch<br />
Quecksilber- o<strong>de</strong>r Öl-Diffusionspumpen erzeugt.<br />
Vakuum<strong>de</strong>stillationen sind so durchzufahren, daß zuerst das Vakuum angelegt wird<br />
und danach erst die Heizung angestellt wird.<br />
Zur Vermeidung eines Sie<strong>de</strong>sverzugs muss immer mit Magnetrührer und Rührfisch<br />
gerührt wer<strong>de</strong>n. Manchmal sind Sie<strong>de</strong>kapillaren günstig, beson<strong>de</strong>rs bei stark viskosen<br />
o<strong>de</strong>r schweren Flüssigkeiten. Durch die Sie<strong>de</strong>kapillare wird ständig ein geringer<br />
Gasstrom (am besten Stickstoff o<strong>de</strong>r Argon aus einem Ballon) durch die Flüssigkeit<br />
gesaugt.<br />
c) Rektifikation<br />
Zur Trennung von Gemischen mehrerer Komponenten, die nahe beieinan<strong>de</strong>rliegen<strong>de</strong><br />
Sie<strong>de</strong>punkte haben (Unterschied Kp < 50°C) genügt eine einfache Destillation zur<br />
Reinigung <strong>de</strong>r Substanzen nicht mehr. Man benutzt in solchen Fällen eine sogenannte<br />
Vigreux-Kolonne (Abb.21).<br />
Abb. 21:<br />
Vigreuxkolonne<br />
Destillationsbrücke mit<br />
Vigreuxkolonne<br />
29
Prinzip: Das Dampfgemisch steigt auf, die schwerer flüchtige Komponente kon<strong>de</strong>nsiert<br />
und fließt zurück. Der Effekt entspricht also einer Mehrfach<strong>de</strong>stillation.<br />
An <strong>de</strong>n Grenzflächen zwischen aufsteigen<strong>de</strong>m Dampf und herabfließen<strong>de</strong>m Kon<strong>de</strong>nsat<br />
erfolgt ein ständiger Stoffaustausch, so daß die Konzentration <strong>de</strong>s aufsteigen<strong>de</strong>n<br />
Dampfes an <strong>de</strong>r leichter flüchtigen Komponente immer größer wird und am<br />
Kolonnenkopf am größten ist. Die beste Anreicherung <strong>de</strong>r leichter flüchtigen<br />
Komponente wür<strong>de</strong> man dann erreichen, wenn man <strong>de</strong>n gesamten aufsteigen<strong>de</strong>n<br />
Dampf kon<strong>de</strong>nsiert und in <strong>de</strong>r Kolonne zurückfließen ließe. Man spricht dann von<br />
einem maximalen Rücklaufverhältnis; nur in diesem Falle wird überhaupt die<br />
theoretisch mögliche Gleichgewichtseinstellung erreicht.<br />
In <strong>de</strong>r Praxis will man jedoch die am Kolonnenkopf angereicherten Komponenten auch<br />
über<strong>de</strong>stillieren und in <strong>de</strong>r Vorlage sammeln. Zur Erzielung eines guten Trenneffektes<br />
muß man daher langsam <strong>de</strong>stillieren, so daß noch viel <strong>de</strong>s aufsteigen<strong>de</strong>n Dampfes<br />
kon<strong>de</strong>nsieren kann und zurückfließt, daß also das Rücklaufverhältnis noch möglichst<br />
groß ist. Es gibt auch Apparaturen, an <strong>de</strong>nen das Rücklaufverhältnis manuell<br />
eingestellt wer<strong>de</strong>n kann. (Man informiere sich zusätzlich in Lehrbüchern <strong>de</strong>r physikal.<br />
Chemie).<br />
Eine zu schnelle Destillation hat kaum eine an<strong>de</strong>re Wirkung als das Umschütten<br />
<strong>de</strong>r Substanz in einen an<strong>de</strong>ren Kolben.<br />
d) Rotationsverdampfer<br />
Da die meisten Reaktionen in Lösungsmitteln stattfin<strong>de</strong>n, muß das Lösungsmittel zur<br />
Isolierung <strong>de</strong>r Reaktionsprodukte entfernt wer<strong>de</strong>n, in <strong>de</strong>n meisten Fällen durch<br />
Destillation. Zum Ab<strong>de</strong>stillieren größerer Lösungsmittelmengen benutzt man am besten<br />
einen Rotationsverdampfer mit angelegtem Vakuum (Abb.22).<br />
30
Abb. 22:<br />
Der Destillationskolben wird schnell um seine Achse gedreht, wodurch die Oberfläche<br />
<strong>de</strong>r Flüssigkeit stark erhöht wird, was für die Dampfbildung entschei<strong>de</strong>nd ist.<br />
Außer<strong>de</strong>m wer<strong>de</strong>n durch die dauern<strong>de</strong> Bewegung <strong>de</strong>r FIüssigkeit Sie<strong>de</strong>verzüge<br />
weitgehend vermie<strong>de</strong>n. Durch Anlegen eines Vakuums wird <strong>de</strong>r Sie<strong>de</strong>punkt gesenkt,<br />
so daß die Destillation beschleunigt wird.<br />
e) Wasserdampf<strong>de</strong>stillation<br />
Der Dampfdruck eines Gemisches zweier nicht ineinan<strong>de</strong>r löslichen Substanzen ergibt<br />
sich als Summe <strong>de</strong>r Dampfdrücke <strong>de</strong>r Einzelkomponenten, d.h. <strong>de</strong>r Gesamtdampfdruck<br />
ist höher als <strong>de</strong>r <strong>de</strong>r Einzelkomponente; <strong>de</strong>r Sie<strong>de</strong>punkt <strong>de</strong>s Gemisches liegt tiefer als<br />
<strong>de</strong>r Sie<strong>de</strong>punkt <strong>de</strong>s niedrigstsie<strong>de</strong>n<strong>de</strong>n Anteils.<br />
Diese Eigenschaften nutzt man bei <strong>de</strong>r Wasserdampf<strong>de</strong>stillation aus. Ein in Wasser<br />
unlöslicher Stoff kann im Gemisch mit Wasser <strong>de</strong>stilliert bzw. durch Einleiten von<br />
Wasserdampf in die Mischung <strong>de</strong>stilliert wer<strong>de</strong>n. So können empfindliche Stoffe<br />
schonend <strong>de</strong>stilliert wer<strong>de</strong>n, <strong>de</strong>ren Sie<strong>de</strong>punkt sonst weit über 100°C liegen; z.B.<br />
etherische Öle, Phenole etc. (Abb. 23).<br />
31
Abb. 23:<br />
3.2.4. Extraktion:<br />
a) Ausschütteln<br />
Unter Ausschütteln versteht man die Extraktion eines Stoffes aus einem Lösungsmittel<br />
mit einem an<strong>de</strong>ren, nicht mischbaren Lösungsmittel (s.a. Perforation).<br />
Die auszuschütteln<strong>de</strong> Lösung wird zusammen mit <strong>de</strong>m Extraktionsmittel in einem<br />
Schütteltrichter (Schei<strong>de</strong>trichter, Abb. 24) gefüllt, dieser mit einem Stopfen<br />
verschlossen und anschließend gut durchgeschüttelt. Dabei muß man das Hahnküken<br />
und <strong>de</strong>n Stopfen gut festhalten. Der Überdruck, (beson<strong>de</strong>rs beim Ausschütteln mit<br />
Ether und auch beim Neutralisieren einer organischen Phase durch Ausschütteln mit<br />
Sodalösung) muß mehrfach abgelassen wer<strong>de</strong>n, in<strong>de</strong>m man <strong>de</strong>n Auslauf nach oben<br />
richtet und <strong>de</strong>n Hahn vorsichtig öffnet. <strong>SCHUTZBRILLE</strong> !!!<br />
32
Abb.24:<br />
VORSICHT: Das zu extrahieren<strong>de</strong> Gemisch muss selbstverständlich kälter sein<br />
als <strong>de</strong>r Sie<strong>de</strong>punkt <strong>de</strong>s zur Extraktion verwen<strong>de</strong>ten Lösungsmittels (z.B.<br />
Raumtemp. bei Extraktion mit Diethylether).<br />
An<strong>de</strong>rnfalls entsteht unkalkulierbarer und gefährlicher Überdruck !!!!!<br />
b) Perforation<br />
Mit Hilfe von Perforatoren kann man das "Ausschütteln" mit einer geringen<br />
Lösungsmittelmenge kontinuierlich durchführen. Das Lösungsmittel wird ständig<br />
verdampft, kon<strong>de</strong>nsiert im Rückflußkühler und durchströmt durch eine Fritte fein verteilt<br />
die zu extrahieren<strong>de</strong> Lösung und fließt dann in <strong>de</strong>n Sie<strong>de</strong>kolben zurück (Abb.25).<br />
Abb.25:<br />
33
c) Soxhlet und Thielepape-Aufsatz<br />
1<br />
Zur Extraktion von Feststoffen kocht man diese mit Lösungsmittel auf und <strong>de</strong>kantiert<br />
dann o<strong>de</strong>r man benutzt einen Soxhlet-Extraktor o<strong>de</strong>r einen Thielepape-Aufsatz. Bei<br />
bei<strong>de</strong>n erhitzt man das Lösungsmittel im unteren Kolben, die Dämpfe steigen auf,<br />
wer<strong>de</strong>n im Kühler kon<strong>de</strong>nsiert und das Lösungsmittel tropft auf das Extraktionsgut, das<br />
in einer Hülse eingeführt wur<strong>de</strong> (Abb.26).<br />
34
Abb.26:<br />
Heißextraktor<br />
Soxhlet-<br />
Extraktor<br />
Beim Thielepape-Aufsatz tropft <strong>de</strong>r Extrakt (das Lösungsmittel) kontinuierlich in <strong>de</strong>n<br />
Kolben zurück, beim Soxhlet-Extraktor läuft <strong>de</strong>r Extrakt erst zurück, wenn <strong>de</strong>r<br />
Flüssigkeitsspiegel die Höhe <strong>de</strong>s Heberknies erreicht hat. Bei Erhitzen über viele<br />
Stun<strong>de</strong>n erreicht man beim Soxhlet-Extraktor eine sehr gute Extraktion, weil <strong>de</strong>r obere<br />
Teil immer wie<strong>de</strong>r über das seitliche absteigen<strong>de</strong> Glasrohr automatisch geleert wird und<br />
so eine nahezu vollständige Extraktion erreicht wer<strong>de</strong>n kann.<br />
3.2.5. Sublimation<br />
Die Sublimation ist eine Reinigungsmetho<strong>de</strong> für feste Stoffe. Viele Stoffe kann man<br />
verdampfen, ohne daß sie schmelzen, und die Dämpfe direkt in fester Form<br />
kon<strong>de</strong>nsieren (auch Feststoffe besitzen einen Dampfdruck).<br />
35
Zur Reinigung eines Feststoffes wird dieser z.B. in eine Schale gefüllt, mit einem<br />
Trichter abge<strong>de</strong>ckt und langsam erhitzt. Der gereinigte Stoff schei<strong>de</strong>t sich dann<br />
kristallin auf <strong>de</strong>m kälteren Trichter ab. Für bei Normaldruck nicht zu sublimieren<strong>de</strong><br />
Stoffe benutzt man eine Sublimationsapparatur (c), an die man Vakuum anlegen kann<br />
Abb.27).<br />
Abb.27:<br />
Einfache<br />
Sublimationsapparaturen<br />
3.3. Kristallisation<br />
Kühlwasser<br />
Vakuum-<br />
Sublimille<br />
erwärmen<br />
Vakuum<br />
Kühlfinger<br />
saubere Substanz<br />
verunreinigte Substanz<br />
Eine häufig benutzte Metho<strong>de</strong> zur Reinigung fester Stoffe ist die Umkristallisation. Der<br />
zu reinigen<strong>de</strong> Stoff wird in möglichst wenig Lösungsmittel in <strong>de</strong>r Hitze gelöst, danach<br />
von unlöslichen Beimengungen filtriert und schließlich die Lösung abgekühlt, wobei die<br />
Substanz meist in reinerer Form auskristallisiert. Bei unbekannten Substanzen muß<br />
vorher ein geeignetes Lösungsmittel gefun<strong>de</strong>n wer<strong>de</strong>n, das in Vorversuchen mit einer<br />
geringen Menge <strong>de</strong>r Substanz probiert wird.<br />
Als Anhaltspunkt kann folgen<strong>de</strong> Tabelle dienen:<br />
36
Stoffklasse Gut löslich in Lösungsmittel vom Typ<br />
Kohlenwasserstoffe hydrophob Kohlenwasserstoffe, Ether,<br />
Halogenkohlenwasserstoffe<br />
Halogenkohlenwasserstoffe<br />
Ether<br />
Ester Ester<br />
Nitroverbindungen<br />
Nitrile Ethanol, Dioxan, Eisessig<br />
Ketone<br />
Al<strong>de</strong>hy<strong>de</strong><br />
Phenole Ethanol, Wasser<br />
Amine<br />
Alkohole<br />
Carbonsäuren<br />
Sulfonsäuren<br />
Salze hydrophil Wasser<br />
Auch Lösungsmittelgemische führen oft zum Ziel (z.B. Wasser/Ethanol, Aceton/<br />
Petrolether).<br />
Zur zusätzlichen Reinigung (Entfärbung) kann vor <strong>de</strong>m Aufkochen (nachträglicher<br />
Zusatz wür<strong>de</strong> zu starkem Aufschäumen und evtl. explosionsartigem Aufsie<strong>de</strong>n führen!)<br />
Aktivkohle zugesetzt wer<strong>de</strong>n, die die färben<strong>de</strong>n Verunreinigungen - meist polymere<br />
Verbindungen, die bei <strong>de</strong>r Reaktion mit entstan<strong>de</strong>n sind - absorbiert. Die Kohle wird<br />
dann heiß abfiltriert und die geklärte Lösung abgekühlt. Falls beim Abkühlen die<br />
Kristallisation nicht einsetzt, da viele organische Stoffe zur Bildung übersättigter<br />
Lösungen neigen, kann sie durch Reiben mit einem Glasstab an <strong>de</strong>r Innenwand <strong>de</strong>s<br />
Gefäßes provoziert: wer<strong>de</strong>n. Dabei bil<strong>de</strong>n sich durch Glasabrieb Kristallisationskeime,<br />
die für die Kristallisation notwendig sind. Oft kristallisiert danach die Substanz spontan<br />
aus.<br />
3.4. Trocknen im Labor (siehe auch Gase):<br />
Bei einigen Reaktionen ist es notwendig, Gase o<strong>de</strong>r flüssige Stoffe vorher zu trocknen,<br />
da die geringste Spur von Wasser zu Mißerfolg führen wer<strong>de</strong> (Claisen-Kon<strong>de</strong>nsation,<br />
Radikalreaktionen, Grignard-Reaktion). Im Folgen<strong>de</strong>n ist eine kurze Liste <strong>de</strong>r<br />
gebräuchlichsten Trockenmittel für Lösungsmittel aufgeführt:<br />
Lösungsmittel Kp [°C] Trockenmittel<br />
37
Aceton 56 CaCl2, K2CO3<br />
Anilin 184 KOH, BaO<br />
Benzol 80 Destillation, CaCl2<br />
Chloroform 61 CaCl2, P2O5<br />
Cyclohexan 81 LiAlH4<br />
Diethylether ..35 CaCl2, LiAlH4, basisches Alox<br />
Dioxan 101 CaCl2<br />
Essigsäureethylester 77 K2CO3, CaO<br />
Ethanol 78 CaO, Mg, MgO<br />
Ethylenglycol 197 Destillation<br />
Methanol 65 CaCl2, Mg, Ca0<br />
Pyridin 115 KOH, BaO<br />
Toluol 111 Destillation, CaCl2<br />
Das Trocknen unpolarer Lösungsmittel durch Einpressen von Natriumdraht wird wegen<br />
<strong>de</strong>r auftreten<strong>de</strong>n Gefahren beim Umgang mit Natriummetall und wegen <strong>de</strong>r problematischen<br />
Entsorgung grösserer Natriummengen im Grundpraktikum nicht mehr<br />
durchgeführt.<br />
Viele unpolare Lösungsmittel lassen sich sehr effektiv mit basischem Aluminiumoxid<br />
trocknen. Dazu füllt man das basische Alox in eine Chromatographiesäule aus Glas<br />
und lässt das LM durchlaufen, das eluieren<strong>de</strong> LM ist trocken (Vorsicht: bei Ether wird<br />
<strong>de</strong>r Stabilisator (BHA = 2-tButyl-4-Hydroxy-Anisol o<strong>de</strong>r BHT = di-tButyl-Hydroxy-Toluol)<br />
entfernt und muss erneut hinzugefügt wer<strong>de</strong>n.<br />
38
Trocknung von unpolaren Lösungsmitteln mit basischem Aluminiumoxid<br />
Lösungsmittel Löslichkeit von H2O im Spezifische Durchbruchs-<br />
(LM) LM bei 25°C (in Gew.%) menge (g LM pro g Al2O3)<br />
n-Hexan 0,01 1450<br />
Methylenchlorid<br />
(Dichlormethan) 0,2 55<br />
Chloroform 0,07 90<br />
Tetrachlorkohlenstoff 0,01 1150<br />
Trichlorethylen 0,025 380<br />
Tetrachlorethylen 0,02 1440<br />
Acetonitril 0,1* 20<br />
Cyclohexan 0,013 1630<br />
Benzol 0,065 170<br />
Cumol<br />
(Isopropylbenzol) 0,03 280<br />
Chlorbenzol 0,04 250<br />
Brombenzol -- 380<br />
Dekalin 0,07 1400<br />
Ether<br />
(Diethylether) 1,47 14 – 140<br />
Dioxan 0,1* 25<br />
THF<br />
(Tetrahydrofuran) 0,1* 21<br />
* Wasserlösliches LM, <strong>de</strong>ssen H2O-Gehalt auf <strong>de</strong>n angegebenen Wert eingestellt wur<strong>de</strong><br />
Über die genauen Vorschriften zur Absolutierung von Lösungsmitteln informiere man<br />
sich in entsprechen<strong>de</strong>n Lehrbüchern.<br />
Um eine Reaktion unter Wasserausschluß durchzuführen, benutzt man Trockenrohre,<br />
mit <strong>de</strong>nen die Apparatur verschlossen wird. Die Trockenrohre wer<strong>de</strong>n mit einem Glas-<br />
wollepfropfen, dann mit gekörntem Calciumchlorid und anschließend mit Glaswolle<br />
gefüllt (Abb.30).<br />
39
Abb.30:<br />
Glaswolle<br />
Trockenmittel<br />
(z.B. CaCl2) Festsubstanzen wer<strong>de</strong>n im Vakuum-Exsiccator getrocknet (Abb.31):<br />
Abb.31:<br />
Exsikkatoren<br />
150 mL<br />
zur<br />
Vakuumpumpe<br />
Substanz<br />
Trockenmittel<br />
(z.B. KOH-Plätzchen)<br />
150 mL<br />
zur<br />
Vakuumpumpe<br />
Im unteren Teil wird Trockenmittel eingefüllt (CaCl2, KOH-Plätzchen, Blaugel ..., je nach<br />
Verwendungszweck). Die zu trocknen<strong>de</strong>n Proben wer<strong>de</strong>n in Gefäßen,die durch<br />
Alufolie (gelocht) verschlossen sind, in <strong>de</strong>n Exsiccator gebracht, <strong>de</strong>r Deckel<br />
geschlossen und Vakuum angelegt (Trocknungsdauer ca. 1 Tag).<br />
3.5. Geräte zur Bestimmung physikalischer Konstanten:<br />
a) Refraktometer<br />
Eine sehr be<strong>de</strong>utsame Größe zur Charakterisierung von reinen Flüssigkeiten ist <strong>de</strong>r<br />
Brechungsin<strong>de</strong>x. Mit einem Refraktometer wird <strong>de</strong>r Grenzwinkel <strong>de</strong>r Totalreflexion<br />
gemessen, kenntlich an <strong>de</strong>r scharfen Trennungslinie zwischen hell und dunkel.<br />
40
Die Hell-Dunkel-Grenze wird am Refraktometer so eingestellt, daß sie genau im<br />
Fa<strong>de</strong>nkreuz <strong>de</strong>s rechten Meßfernrohres liegt:<br />
Durch das linke Okular kann man dann direkt <strong>de</strong>n Brechungin<strong>de</strong>x ablesen (auf 4<br />
Stellen hinter <strong>de</strong>m Komma, die letzte Ziffer geschätzt).<br />
b) Schmelzpunkt<br />
Der Schmelzpunkt ist die wichtigste physikalische Konstante zur Charakterisierung<br />
eines Feststoffes. Eine kleine Menge <strong>de</strong>r trockenen Verbindung wird fein gepulvert und<br />
in ein Schmelzpunktsröhrchen gefüllt. Dieses Röhrchen wird in das<br />
Schmelzpunktsbestimmungsgerät gestellt und langsam aufgeheizt. Durch die Lupe ist<br />
<strong>de</strong>r Verlauf zu beobachten und die Temperatur <strong>de</strong>s Beginns und En<strong>de</strong> <strong>de</strong>s Schmelzens<br />
zu notieren. Wenn <strong>de</strong>r Schmelzpunkt weit unter <strong>de</strong>m Literaturwert liegt (tiefer als 5°C),<br />
muß die Substanz nochmals gereinigt, eventuell auch besser getrocknet wer<strong>de</strong>n.<br />
Wenn <strong>de</strong>r Schmelzpunkt zu hoch liegt (größer als 2°C) wur<strong>de</strong> entwe<strong>de</strong>r zu schnell<br />
aufgeheizt (Substanz ist träger als das Thermometer) o<strong>de</strong>r es han<strong>de</strong>lt sich nicht um die<br />
gesuchte Substanz!<br />
41
c) Sie<strong>de</strong>punkt<br />
Neben <strong>de</strong>m Brechungsin<strong>de</strong>x ist für Flüssigkeiten auch immer <strong>de</strong>r Sie<strong>de</strong>punkt<br />
anzugeben. 1 ml <strong>de</strong>r Substanz wird in ein kleines Reagensglas gefüllt, ein Sie<strong>de</strong>stein<br />
hinzugefügt und das Reagensglas im Wasserbad o<strong>de</strong>r Ölbad vorsichtig erhitzt, bis die<br />
Flüssigkeit konstant sie<strong>de</strong>t. Die Sie<strong>de</strong>temperatur (Kp) wird mit einem Thermometer<br />
abgelesen, das so aufgehängt wird, daß es die Glaswän<strong>de</strong> <strong>de</strong>s Reagensglases nicht<br />
berührt und nicht in die Flüssigkeit taucht, son<strong>de</strong>rn nur von <strong>de</strong>n Dämpfen umspült wird.<br />
II. PRÄPARATIVER TEIL<br />
1. Einleitung<br />
Ein Chemiker sollte nicht nur imstan<strong>de</strong> sein, theoretische Überlegungen zur Aufklärung<br />
<strong>de</strong>r Struktur eines unbekannten Stoffes o<strong>de</strong>r zur Synthese anzustellen, son<strong>de</strong>rn muß<br />
diese Überlegungen auch in <strong>de</strong>r Praxis realisieren können.<br />
Chemie ist auch ein Handwerk und das lernt man nur durch Praxis. Diese Praxis<br />
ist aber untrennbar mit theoretischen Erwägungen über Reaktionsmechanismen,<br />
stereochemischen Fragen usw. verbun<strong>de</strong>n.<br />
42
Da es eine fast unüberschaubare Zahl von Herstellungswegen gibt, hat man versucht,<br />
diese zu ordnen. Grundlage <strong>de</strong>r Ordnung sind in <strong>de</strong>n meisten mo<strong>de</strong>rnen Lehrbüchern<br />
die Reaktionsmechanismen: Der Stu<strong>de</strong>nt soll z.B. zunächst Präparate herstellen, die im<br />
Zuge einer SN1- o<strong>de</strong>r SN2-Reaktion gebil<strong>de</strong>t wer<strong>de</strong>n, dann Eliminierungsreaktionen<br />
nach E1 und E2 ausführen, usw. Dieses System leitet zwar <strong>de</strong>n jungen Chemiker zu<br />
einem perfekten mechanistischen Denken an, lei<strong>de</strong>t aber unter <strong>de</strong>m schwerwiegen<strong>de</strong>n<br />
Mangel, daß er die Planung und Ausführung von Synthesen nur ungenügend<br />
kennenlernt.<br />
In Kenntnis dieser Tatsache wollen wir in Bayreuth, ausgehend von einfachen<br />
Verbindungen, die wichtigsten Reaktionen so behan<strong>de</strong>ln, daß wir gleichzeitig<br />
Synthesemöglichkeiten und Reaktionsmechanismen betrachten.<br />
Zunächst wer<strong>de</strong>n einfache Funktionalisierungen durchgeführt, d.h. es wer<strong>de</strong>n<br />
bestimmte funktionelle Gruppen in ein Molekül eingeführt bzw. vorhan<strong>de</strong>ne funktionelle<br />
Gruppen in an<strong>de</strong>re überführt. Auf diesem Weg sollen Sie wichtige Verbindungstypen<br />
und Reaktionen Schritt für Schritt kennenlernen.<br />
In gleicher Weise und mit gleichem Ziel wer<strong>de</strong>n dann Syntheseschritte und Reaktionen<br />
<strong>de</strong>r aromatischen Verbindungen behan<strong>de</strong>lt. Schließlich wer<strong>de</strong>n Reaktionen<br />
durchgeführt, die zum Aufbau von größeren Verbindungen (Knüpfung von Kohlenstoff-<br />
Kohlenstoff-Bindungen) geeignet sind.<br />
2. Ester organischer Säuren<br />
2.1 Be<strong>de</strong>utung als Ausgangsmaterial für die Synthese<br />
Reaktivität von Säure<strong>de</strong>rivaten:<br />
Ein leicht zugängliches und billiges Ausgangsmaterial zur Synthese einer Vielzahl<br />
aliphatischer Verbindungen sind Carbonsäuren, die beispielsweise bei <strong>de</strong>r Verseifung<br />
von Fetten anfallen:<br />
43
H 2C O<br />
HC<br />
O<br />
H 2C O<br />
O<br />
C<br />
O<br />
C<br />
O<br />
C<br />
R<br />
R<br />
R<br />
OH �<br />
H 2O<br />
H 2C<br />
HC<br />
H 2C<br />
OH<br />
OH<br />
OH<br />
Glycerin<br />
+ R C O<br />
O �<br />
Carbonsäure-Salz<br />
Carbonsäuren sind aber auch, wie wir später sehen wer<strong>de</strong>n, als<br />
Zwischenprodukte aufbauen<strong>de</strong>r Synthesen von Be<strong>de</strong>utung. Beispiele hierfür<br />
sind die „Malonestersynthese“, die „Acetessigestersynthese“ und die Hünig-<br />
Synthese.<br />
"Freie" Carbonsäuren sind relativ reaktionsträge. Will man sie für weitere<br />
synthetische Aufbaureaktionen einsetzen, so muß man sie umformen. Eine <strong>de</strong>r<br />
wichtigsten Umformungsreaktionen besteht in <strong>de</strong>r Reduktion zu primären<br />
Alkoholen, die ihrerseits wie<strong>de</strong>r in Alkylhalogeni<strong>de</strong> überführbar sind:<br />
R C<br />
O<br />
OH<br />
R CH 2 OH R CH 2 X<br />
Säuren selbst setzen <strong>de</strong>m Reduktionsschritt, <strong>de</strong>r <strong>de</strong>n Angriff eines Hydridions am<br />
Carbonylkohlenstoffatom beinhaltet, erheblichen Wi<strong>de</strong>rstand entgegen, weil in<br />
ihnen die positive Ladungsdichte am Carbonylkohlenstoffatom, verglichen mit<br />
Carbonsäure<strong>de</strong>rivaten, am geringsten ist.<br />
R C O<br />
O<br />
H R C O<br />
Eine beson<strong>de</strong>rs hohe Neigung zur Kompensation <strong>de</strong>r Ladung zeigt<br />
das Anion:<br />
O<br />
H<br />
44
R C O<br />
O<br />
�<br />
R C O<br />
Grenzstrukturen<br />
O<br />
�<br />
R C<br />
�<br />
realer<br />
Zustand<br />
In Carbonsäureami<strong>de</strong>n ist diese Neigung bereits vermin<strong>de</strong>rt, <strong>de</strong>r Stickstoff <strong>de</strong>r<br />
Amidgruppe gibt weniger bereitwillig Elektronen ab als das -O �<br />
–Atoms eines Carbonsäureanions.<br />
Noch geringer ist die Fähigkeit zur Kompensation <strong>de</strong>r positiven Ladung <strong>de</strong>s<br />
Carbonylkohlenstoffatoms in Estern, weil <strong>de</strong>r an die Alkylgruppe gebun<strong>de</strong>ne<br />
Sauerstoff noch weniger als <strong>de</strong>r Stickstoff in Carbonsäureami<strong>de</strong>n zur<br />
Elektronenabgabe bereit ist. Die geringste Neigung zur Abgabe von Elektronen<br />
haben schließlich die Halogenatome in Carbonsäurehalogeni<strong>de</strong>n. Es ergibt sich<br />
daher folgen<strong>de</strong> Reihe <strong>de</strong>r Reaktivität:<br />
hochreaktiv unreaktiv<br />
R C O<br />
X<br />
Säurehalogenid<br />
(X = Halogen)<br />
R C O<br />
Ester<br />
O<br />
R C O<br />
R NH2 Säureamid<br />
O<br />
O<br />
R C O<br />
Säureanion<br />
Nur wenige Reagenzien sind befähigt, Carbonsäuren, die am Carbonkohlenstoffatom<br />
vergleichsweise die höchste Elektronendichte und damit die geringste Carbonylaktivität<br />
aller Carbonyl-Verbindungen aufweisen, zu reduzieren. Möglich ist eine Reduktion mit<br />
komplexen Metallhydri<strong>de</strong>n, wie z.B. LiAlH4. Diese reagieren mit <strong>de</strong>r freien Carbonsäure<br />
zunächst unter Bildung eines Salzes:<br />
4<br />
R C O<br />
OH<br />
+ LiAlH 4<br />
(RCOO) 4Al � Li �<br />
O �<br />
45
Dieses Salz kann weiterreduziert wer<strong>de</strong>n (1/4 Mol LiAlH4 wird zur Salzbildung<br />
verbraucht), doch ist das entstehen<strong>de</strong> Salz in <strong>de</strong>m verwen<strong>de</strong>ten Lösungsmittel (Ether)<br />
oft zu schlecht löslich, als daß die Reaktion stattfin<strong>de</strong>n könnte.<br />
Aus diesem Grun<strong>de</strong> wer<strong>de</strong>n in <strong>de</strong>r Regel zur Reduktion nicht die freien Carbonsäuren,<br />
son<strong>de</strong>rn ihre Ester eingesetzt. Möglichkeiten, zu <strong>de</strong>ren Herstellung sollen im Folgen<strong>de</strong>n<br />
besprochen wer<strong>de</strong>n.<br />
2.2. Herstellung von Estern durch Umsatz von Säuren mit Alkoholen:<br />
R C O<br />
OH<br />
+ R'OH<br />
(H 3O �<br />
R C<br />
O<br />
OR'<br />
+ H 2O<br />
Diese Reaktion ist das Para<strong>de</strong>beispiel für eine Gleichgewichtsreaktion.<br />
Die Einstellung <strong>de</strong>s Gleichgewichtes erfolgt wegen <strong>de</strong>r geringen Carbonylaktivität <strong>de</strong>r<br />
Säuren nur sehr langsam. Sie wird durch Säurezusatz geför<strong>de</strong>rt, weil die Addition<br />
eines Protons an das Sauerstoffatom <strong>de</strong>r Carbonylgruppe unter Positivierung <strong>de</strong>s<br />
Carbonylkohlenstoffatoms dieses <strong>de</strong>m Angriff eines nukleophilen Teilchens beson<strong>de</strong>rs<br />
leicht zugänglich macht:<br />
R C O<br />
OH<br />
+ H 3O �<br />
R C + H2O OH<br />
OH<br />
Der Alkohol reagiert mit <strong>de</strong>m Carbonylkohlenstoff unter Veresterung:<br />
�<br />
46
R C<br />
R C<br />
H<br />
OH<br />
OH<br />
�<br />
�<br />
OH<br />
+R' O H R<br />
OH<br />
C<br />
�<br />
O<br />
OH<br />
OH H<br />
�<br />
OH<br />
O R' R C<br />
H<br />
O H<br />
O<br />
R'<br />
R'<br />
- H �<br />
+ H �<br />
R C O + H3O �<br />
OR'<br />
Die Lage <strong>de</strong>s Gleichgewichtes ist zugunsten <strong>de</strong>r Esterbildung verschiebbar,<br />
wenn man einen (meist <strong>de</strong>n billigeren!) Reaktionspartner im Überschuß einsetzt<br />
o<strong>de</strong>r das gebil<strong>de</strong>te Wasser aus <strong>de</strong>m Reaktionsgemisch entfernt<br />
(Massenwirkungsgesetz!). Man sollte daher von vornherein möglichst<br />
wasserfreien ("absoluten") Alkohol verwen<strong>de</strong>n (dies gilt jedoch nur, wenn das<br />
Wasser aus <strong>de</strong>r Reaktionslösung entfernt wird).<br />
Bei <strong>de</strong>r Reaktion entstehen<strong>de</strong>s Wasser läßt sich durch Zusatz eines<br />
"Schleppers", eines Lösungsmittels, das mit Wasser ein azeotropes Gemisch<br />
bil<strong>de</strong>t (Methylenchlorid, Toluol u.a.), aus <strong>de</strong>m Reaktionsmedium entfernen<br />
(„Azeotrope Veresterung“).<br />
Man kann aber auch das Gleichgewicht dadurch „verschieben“, daß man gebil<strong>de</strong>ten<br />
Ester ab<strong>de</strong>stilliert o<strong>de</strong>r extraktiv durch Zusatz eines Lösungsmittels, das <strong>de</strong>n Ester gut,<br />
die Reaktionspartner aber nicht löst, aus <strong>de</strong>m Reaktionsgemisch entfernt („Extraktive<br />
Veresterung“).<br />
Praktikumsversuch 1: Azeotrope Veresterung o<strong>de</strong>r extraktive Veresterung<br />
Bei Säuren, die in α-Stellung verzweigt sind, z.B. Trimethylessigsäure<br />
(Pivalinsäure), verläuft die Veresterung wesentlich langsamer. Durch die<br />
Substituenten in α-Stellung wird <strong>de</strong>r nukleophile Angriff <strong>de</strong>s Alkohols sterisch<br />
behin<strong>de</strong>rt. Eine Veresterung gelingt in diesem Falle durch Lösen <strong>de</strong>r<br />
47
Carbonsäure in konzentrierter Schwefelsäure und Umsetzung dieser Lösung mit<br />
<strong>de</strong>m Alkohol. In <strong>de</strong>r Schwefelsäure liegt das Acylium-Ion vor, das ausgesprochen<br />
leicht nukleophil angegriffen wer<strong>de</strong>n kann:<br />
R C O<br />
OH<br />
R C O �<br />
+ 2 H2SO4 + H3O � �<br />
+ 2 HSO4 Acylium-Ion<br />
Aus <strong>de</strong>n gleichen Grün<strong>de</strong>n (sterische Hin<strong>de</strong>rung) ist auch die Veresterung mit<br />
sekundären o<strong>de</strong>r tertiären Alkoholen erschwert. Bei Veresterungereaktionen mit diesen<br />
Alkoholen erhält man leicht als Nebenprodukt ungesättigte Kohlenwasserstoffe, die sich<br />
durch H2O-Eliminierung bil<strong>de</strong>n, die durch die als Katalysator zugesetzte Säure (z.B.<br />
H2SO4) bewirkt wird (E1-Eliminierung).<br />
CH 3<br />
H3O C<br />
�<br />
H3C CH2 CH3 H3C CH2 C CH3+ H2O - H 2O<br />
OH<br />
H 2O<br />
H<br />
H H3C 3C CH<br />
CH 3<br />
- H3O C CH3 �<br />
�<br />
CH 3<br />
OH 2<br />
�<br />
H H3C 3C CH<br />
C<br />
CH 3<br />
CH 3<br />
Ester, die durch die beschriebene Veresterungsreaktion nur schwer herstellbar, sind,<br />
können auch durch Umsetzung von Carbonsäuresalzen mit Alkylhalogeni<strong>de</strong>n<br />
hergestellt wer<strong>de</strong>n (nukleophile Substitution).<br />
R C O<br />
O � Na �<br />
+R' X<br />
S N2<br />
R C<br />
O<br />
O R'<br />
X = Halogen, OSO 2R'', OSO 2OR''<br />
+ NaX<br />
48
2.3 Herstellung von Methylestern mit Diazomethan:<br />
Diazomethan ist durch Einwirkung von Alkali auf Nitrosomethylharnstoff herstellbar:<br />
O C<br />
H 3C<br />
NH 2<br />
N<br />
CH 3<br />
N O<br />
N N O �<br />
OH �<br />
�<br />
O<br />
HO<br />
+ 2 H 2O<br />
- 2 OH �<br />
C<br />
� � � �<br />
H 2C<br />
NH 2<br />
N<br />
CH 3<br />
H2C N N H2C N N<br />
N O<br />
�<br />
N N OH2 H OH �<br />
O C NH2 OH<br />
+<br />
H 3C<br />
- 2 H 2O<br />
Diazomethan (toxisch, cancerogen, explosiv)<br />
N N O<br />
Dabei greift das Alkali zunächst am Carbonylkohlenstoffatom an. Das so<br />
gebil<strong>de</strong>te Produkt zerfällt, wie in <strong>de</strong>n Formeln dargelegt, (im Falle <strong>de</strong>s N-Methyl-<br />
nitrosomethylharnstoffs entsteht Carbaminsäure, die weiter zu Ammoniak und<br />
CO2 gespalten wird).<br />
Anstelle <strong>de</strong>s unbeständigen und hochcancerogenen Nitrosomethylharnstoffs<br />
verwen<strong>de</strong>t man besser p-Tolylsulfonyl-methylnitrosamid, das mit KOH in<br />
prinzipiell gleicher Reaktion zu Diazomethan umgesetzt wird:<br />
�<br />
49
O<br />
N O<br />
H3C S N + KOH<br />
O<br />
O<br />
O<br />
CH 3<br />
H3C S O �<br />
K � +<br />
CH 2N 2 + H 2O<br />
Diazomethan reagiert von selbst mit Verbindungen, die genügend aci<strong>de</strong><br />
Wasserstoffatome enthalten, wie z.B. Säuren und Phenolen (mit Alkoholen aber nur<br />
unter beson<strong>de</strong>ren Bedingungen) unter Veresterung bzw. Veretherung:<br />
H2C N N<br />
� �<br />
R C O<br />
OH + �<br />
R COO + N N<br />
�<br />
H3C S N2<br />
R C<br />
O<br />
O CH 3<br />
�<br />
�<br />
+<br />
N N<br />
OH + H2C N N<br />
O + H3C N N<br />
OCH 3<br />
+ N 2<br />
Die Reaktion eignet sich hervorragend zur Herstellung kleiner und kleinster<br />
Methylestermengen (mikroanalytischer Maßstab).<br />
VORSICHT:<br />
�<br />
�<br />
50
Die Handhabung von N-Nitrosomethylharnstoff und beson<strong>de</strong>rs die von<br />
Diazomethan ist sehr gefährlich!!!<br />
N-Nitrosomethylharnstoff ist krebserzeugend, kann bei Licht- und Wärmeeinwirkung<br />
unter Feuererscheiniing verpuffen und muss <strong>de</strong>shalb in dunklen Flaschen in <strong>de</strong>r<br />
Tiefkühltruhe aufbewahrt wer<strong>de</strong>n.<br />
Diazomethan ist ein explosives und außeror<strong>de</strong>ntlich giftiges Gas (Kp –24°C). Es<br />
wird nur in Lösung (Ether) hergestellt und gehandhabt. Es ist auch in <strong>de</strong>r Kälte<br />
in Lösung nur einige Tage haltbar. Arbeiten mit Diazomethan dürfen nur unter<br />
einem speziellen Abzug mit beson<strong>de</strong>rs starker Absaugung hinter einem<br />
Schutzschild durchgeführt wer<strong>de</strong>n!!l<br />
Deshalb wird zur Herstellung größerer Estermengen die Veresterungsreaktion mit<br />
Alkoholen <strong>de</strong>r eleganteren und rascheren Metho<strong>de</strong> <strong>de</strong>r Veresterung mit Diazomethan<br />
vorgezogen.<br />
2.4 Veresterung mit Säurechlori<strong>de</strong>n:<br />
Im Prinzip können Säurechlori<strong>de</strong> mit Alkohol o<strong>de</strong>r Alkoholaten zu Estern<br />
umgesetzt wer<strong>de</strong>n:<br />
R C O + R'OH R C O<br />
+ HCl<br />
Cl<br />
OR'<br />
Im allgemeinen wer<strong>de</strong>n Säurechlori<strong>de</strong> jedoch bei Anwesenheit von geringsten<br />
Mengen Wasser sofort zu Carbonsäuren verseift, so daß diese Metho<strong>de</strong> zur<br />
Esterherstellung nur begrenzte Anwendung fin<strong>de</strong>t.<br />
Be<strong>de</strong>utung hat diese Metho<strong>de</strong> im analytischen Bereich zur Charakterisierung von<br />
Alkoholen mit aromatischen Säurechlori<strong>de</strong>n, die wegen vermin<strong>de</strong>rter<br />
Carbonylaktivität (Mesomerie!) nur langsam mit H20 reagieren.<br />
Verwen<strong>de</strong>t man ein Säurechlorid, das in Wasser nur schwer löslich ist, so kann<br />
die Veresterung mit diesem Säurechlorid auch dann vorgenommen wer<strong>de</strong>n, wenn<br />
<strong>de</strong>r Alkohol nicht wasserfrei ist.<br />
51
Bei dieser Reaktion wird <strong>de</strong>r Alkohol durch das Säurechlorid aus <strong>de</strong>r wäßrigen<br />
Phase herausextrahiert und kann in homogener Phase mit diesen zum<br />
entsprechen<strong>de</strong>n Ester reagieren. An<strong>de</strong>rerseits kann die Hydrolyse <strong>de</strong>s<br />
Säurechlorids zur Carbonsäure nur an <strong>de</strong>r Phasengrenzfläche stattfin<strong>de</strong>n, und<br />
diese Reaktion verläuft <strong>de</strong>mzufolge wesentlich langsamer als die Veresterung.<br />
C O<br />
Benzoesäurechlorid<br />
Cl<br />
+ R'OH C O<br />
- HCl<br />
NaOH/H2O OR'<br />
(Schotten-Baumann-Verfahren)<br />
o<strong>de</strong>r<br />
Pyridin (Einhorn-Verfahren)<br />
Wasserschwerlösliche Säurechlori<strong>de</strong> sind z.B. Benzoesäurechlorid und seine<br />
kermsubstituierten Derivate. Mit diesen Säurechlori<strong>de</strong>n kann ein Alkohol direkt<br />
aus <strong>de</strong>r wäßrigen Analysenlösung als Derivat einer Carbonsäure (Benzoesäure)<br />
abgeschie<strong>de</strong>n und charakterisiert wer<strong>de</strong>n, da die Benzoesäureester <strong>de</strong>r meisten<br />
Alkohole Feststoffe sind und einen <strong>de</strong>finierten Schmelzpunkt haben (Schotten-<br />
Baumann).<br />
2.5 Herstellung von Essigsäureestern durch Reaktion eines Alkohols mit Acetanhydrid<br />
(Acetylierung):<br />
Ester wer<strong>de</strong>n nicht nur, wie eben gezeigt wur<strong>de</strong> (Kap.: 2.4) zur Erhöhung <strong>de</strong>r<br />
Carbonylaktivität <strong>de</strong>r entsprechen<strong>de</strong>n Säure im Hinblick auf die weitere<br />
Umsetzung (hier zur Reduktion zu einem primären Alkohol) hergestellt. Ihre<br />
Herstellung ist weiterhin auch zum Schutze von OH-Funktionen einer<br />
mehrfunktionellen Verbindung gegen Oxidation von Be<strong>de</strong>utung. Durch<br />
Veresterung mit Essigsäureanhydrid kann eine solche "Schutzgruppe" in das<br />
betreffen<strong>de</strong> Molekül eingefügt wer<strong>de</strong>n.<br />
52
CH 2<br />
R OH<br />
H 3C<br />
H 3 C<br />
C<br />
O<br />
O<br />
C O<br />
-H �<br />
-H �<br />
+H �<br />
+H �<br />
R<br />
CH 2<br />
H 3 C<br />
H 3C<br />
O<br />
C OH<br />
O<br />
C<br />
O<br />
-H �<br />
-H �<br />
+H �<br />
+H �<br />
H 3C<br />
H 3C<br />
+<br />
C<br />
C<br />
O<br />
O<br />
O<br />
OH<br />
CH 2<br />
Die Carbonylaktivität von Säureanhydri<strong>de</strong>n ist vergleichbar mit <strong>de</strong>r von<br />
Säurechlori<strong>de</strong>n (vgl. Kap.: 2.1).<br />
Als Katalysator und zun Abfangen <strong>de</strong>r entstehen<strong>de</strong>n Essigsäure wird häufig Pyridin<br />
(Salzbildung) verwen<strong>de</strong>t.<br />
Diese "Derivatisierung" eines Alkohols wird auch benutzt, um Alkohole vor <strong>de</strong>r<br />
analytischen Trennung in einem Gaschromatographen flüchtiger zu machen.<br />
2.6 Nachweis von Carbonsäureestern<br />
Hinweise auf das Vorliegen eines Carbonsäureesters gibt eine positiv<br />
verlaufen<strong>de</strong> Prüfung auf alkalische Verseifbarkeit <strong>de</strong>r vorliegen<strong>de</strong>n Verbindung<br />
sowie <strong>de</strong>r positive Hydroxamsäuretest.<br />
Bei<strong>de</strong> Nachweisreaktionen sind nicht spezifisch für Ester, son<strong>de</strong>rn Lactone,<br />
Anhydri<strong>de</strong> und verseifbare Halogeni<strong>de</strong> (beim Hydroxamsäuretest nur<br />
Säurechlori<strong>de</strong> und geminale Trihalogeni<strong>de</strong>) sowie Ami<strong>de</strong> und Nitrile geben<br />
gleiche o<strong>de</strong>r ähnliche Reaktionen. Der sicherste Weg zur Charakterisierung ist<br />
daher die Verseifung <strong>de</strong>s Esters und <strong>de</strong>r Einzelnachweis <strong>de</strong>r Alkohol- und<br />
Säurekomponente nebeneinan<strong>de</strong>r.<br />
Bei <strong>de</strong>r Probe auf alkalische Verseifbarkeit wird wenig Substanzprobe mit<br />
alkoholischer Natronlauge unter Zusatz von Phenolphthalein versetzt. Dann wird<br />
beobachtet, ob die durch das zugefügte Phenolphthalein hervorgerufene<br />
Rotfärbung verschwin<strong>de</strong>t.<br />
Ester reagieren mit Hydroxylamin zu Hydroxamsäuren und Alkohol.<br />
R R C O<br />
- HOR'<br />
COOR' +H2N OH<br />
NH OH<br />
R<br />
53
Mit Eisen-(III)-Salzen geben die Hydroxamsäuren meist violett gefärbte Komplexe.<br />
Diese Reaktion ist für Enole typisch. Hydroxamsäuren können nämlich als Enole<br />
vorliegen.<br />
R C O<br />
N<br />
H<br />
OH<br />
R C<br />
3. Herstellung von primären Alkoholen durch Reduktion von Carbonsäureestern<br />
3.1 Reduktion mit Lithiumaluminiumhydrid:<br />
Die Reduktion von Carbonsäureesteim zu primären Alkoholen wird im Labor meist mit<br />
Hilfe komplexer Metallhydri<strong>de</strong> - vorzugsweise mit LiAlH4 - ausgeführt. Angreifen<strong>de</strong>s<br />
Agens ist ein Hydridion:<br />
R C O<br />
R C<br />
OR'<br />
O<br />
H<br />
H H<br />
Hydrolyse<br />
- 2 H 2<br />
H<br />
Al<br />
Al<br />
H<br />
Li �<br />
H R C<br />
H<br />
H<br />
�<br />
�<br />
OR'<br />
+ 4 H 2O<br />
- LiAl(OH) 4<br />
Li �<br />
OH<br />
N<br />
O<br />
H<br />
OR'<br />
H<br />
R C<br />
H<br />
OH<br />
Al<br />
O<br />
H<br />
H<br />
H<br />
�<br />
H<br />
Al<br />
O<br />
Li �<br />
H �<br />
R'<br />
Li �<br />
R CH 2 OH + R'OH<br />
54
Bei Verwendung von LiAlH4 gelingt es nicht, die Reaktion auf <strong>de</strong>r Stufe <strong>de</strong>r<br />
Al<strong>de</strong>hy<strong>de</strong> abzufangen, so daß die Alkohole direkt erhalten wer<strong>de</strong>n. Als<br />
Lösungsmittel dient im allgemeinen Diethylether, bei <strong>de</strong>r Reduktion<br />
reaktionsträger Verbindungen ist <strong>de</strong>r Einsatz von Tetrahydrofuran, das einen<br />
höheren Sie<strong>de</strong>punkt als Ether hat, vorzuziehen (höher sie<strong>de</strong>n<strong>de</strong> Lösungsmittel<br />
erlauben die Durchführung von Reaktionen bei höherer Temperatur, wodurch die<br />
Reaktionsgeschwindigkeit erheblich gesteigert wird).<br />
VORSICHT:<br />
LiAlH4 reagiert mit Wasser aber auch mit Alkohol unter Bildung von Wasserstoff<br />
(Knallgasbildung = Explosionsgefahr !!), <strong>de</strong>r zur Reduktion verwen<strong>de</strong>te Ether muß<br />
daher vor <strong>de</strong>r Reaktion von Wasserspuren und Alkohol befreit wer<strong>de</strong>n.<br />
Natriumborhydrid hingegen ist weniger reaktiv wie LiAlH4. Es kann zwar in wäßriger<br />
Lösung zur Reduktion von Al<strong>de</strong>hy<strong>de</strong>n und Ketonen verwen<strong>de</strong>t wer<strong>de</strong>n, greift aber Ester<br />
nicht an.<br />
Der Vorteil <strong>de</strong>r Reduktion mit komplexen Metallhydri<strong>de</strong>n gegenüber <strong>de</strong>r<br />
nachfolgend beschriebenen Anwendung von unedlen Metallen als<br />
Reduktionsmittel ist <strong>de</strong>r weitaus schonen<strong>de</strong>re Reaktionsverlauf und die<br />
wesentlich höhere Ausbeute.<br />
LiAlH4 ist jedoch ein teures Reagenz, <strong>de</strong>shalb verwen<strong>de</strong>t man im Labor sowie in <strong>de</strong>r<br />
Technik zur Reduktion größerer Ansätze unedle Metalle.<br />
3.2 Reduktion mit unedlen Metallen (Bouveault-Blanc):<br />
Die Reduktionskraft <strong>de</strong>r Metalle ist von ihrer Stellung in <strong>de</strong>r Spannungsreihe<br />
abhängig: Während Al<strong>de</strong>hy<strong>de</strong> und Ketone sowohl mit Alkalimetallen als auch mit<br />
Zn, Al und Mg reduzierbar sind, ist die Reduktion von Estern nur mit<br />
Alkalimetallen möglich. Meist wird hierfür Natrium verwen<strong>de</strong>t, das man in die<br />
alkoholische Lösung <strong>de</strong>s Esters einträgt (Bouveault-Blanc-Reduktion). Die freien<br />
Säuren selbst kann man so nicht reduzieren, weil diese mit Na-Metall (ähnlich wie<br />
Alkohole zu Alkoholat) unter Salzbildung reagieren wur<strong>de</strong>n:<br />
55
R C O<br />
OH<br />
+<br />
Na<br />
R C O<br />
O � Na �<br />
+ ½ H 2<br />
Bei dieser Reaktion entsteht Wasserstoff (sachgerecht ableiten), Reaktion im Abzug<br />
ausführen! ! !<br />
Man nimmt an, daß die Bouveault-Blanc-Reduktion in Gegenwart von Alkohol an<br />
<strong>de</strong>r Na-Oberfläche über Radikalanionen abläuft:<br />
R C O<br />
R<br />
H<br />
C O<br />
OR'<br />
R'<br />
�<br />
+ 2 Na<br />
O<br />
� + R''OH + 2 Na � + R''O �<br />
R C O<br />
H<br />
+ 2 Na �<br />
H<br />
R C<br />
O<br />
R C<br />
O �<br />
R'<br />
R C O<br />
H<br />
+ R'O �<br />
R C O �<br />
+ R''OH + 2 Na �<br />
H<br />
H<br />
O �<br />
+ H 2O<br />
H<br />
H<br />
- OH � R CH 2 OH<br />
+ R''O �<br />
Als Alkohol dient in <strong>de</strong>r Regel Isopropanol, da dieser weniger leicht ein Alkoholat bil<strong>de</strong>t<br />
als ein primärer Alkohol (induktive Wirkung <strong>de</strong>r Methylgruppen) und so weniger Natrium<br />
durch die Nebenreaktion <strong>de</strong>r Alkoholatbildung verlorengeht.<br />
In <strong>de</strong>r Technik wen<strong>de</strong>t man zur Reduktion von Estern oft auch katalytische Verfahren<br />
an, wobei <strong>de</strong>r Ester und Wasserstoff bei Temperaturen zwischen 100°C und 300°C<br />
über Kupferchromitkatalysatoren geleitet und dabei reduziert wird.<br />
3.3 Nachweis von Alkoholen:<br />
56
Substanzen, die eine Hydroxylfunktion enthalten, ergeben mit einer Lösung von<br />
Cerammoniumnitrat (NH4)2[Ce(NO3)6] in Salpetersäure farbige Komplex-Verbindungen.<br />
Phenole und Enole geben auch mit Eisen(IlI)-chlorid farbige Komplexe, nicht jedoch die<br />
aliphatischert Alkohole (Unterscheidungsmöglichkeit).<br />
Charakterisiert wer<strong>de</strong>n Alkohole u.a. durch die Schmelzpunkte <strong>de</strong>r Benzoesäure-, <strong>de</strong>r<br />
p-Nitrobenzoesäure- o<strong>de</strong>r <strong>de</strong>r 3,5-Dinitrobenzoesäureester, (Herstellung nach<br />
Schotten-Baumann, Kap. 2.4.). Sekundäre Alkohole, die nur schwer zu verestern sind,<br />
wer<strong>de</strong>n in die entsprechen<strong>de</strong>n Halogenverbindungen überführt und als solche<br />
nachgewiesen.<br />
4. Alkylhalogeni<strong>de</strong><br />
4.1 Nucleophile Substitution:<br />
Bei <strong>de</strong>r nukleophilen Substitution ersetzt ein nukleophiles Reagenz ein Atom o<strong>de</strong>r eine<br />
Atomgruppe <strong>de</strong>s Substrats und steuert dabei Elektronen zur Bindungsbildung bei. Zum<br />
Unterschied zur Basizität, die die Fähigkeit einer Base zur Reaktion mit einem Proton<br />
beschreibt, versteht man unter "Nucleophilie" die Fähigkeit eines Reagenz mit einem<br />
mehr o<strong>de</strong>r weniger positiven Kohlenstoffatom zu reagieren.<br />
R X + Y R<br />
�<br />
4.1.1 Merkmale <strong>de</strong>r monomolekularen Substitution (SN1):<br />
H 3C<br />
H 3C<br />
CH 3<br />
C<br />
CH 3<br />
C<br />
�<br />
CH 3<br />
X<br />
CH 3<br />
langsam<br />
+ Y �<br />
schnell<br />
H 3C<br />
H 3C<br />
Y + X �<br />
C<br />
CH 3<br />
C<br />
CH 3<br />
� + X �<br />
CH 3<br />
CH 3<br />
1) Die SN1-Reaktion verläuft nach einem Geschwindigkeitsgesetz 1. Ordnung. Der<br />
geschwindigkeitsbestimmen<strong>de</strong> Schritt ist <strong>de</strong>r Bindungsbruch zwischen Alkylrest und<br />
Y<br />
57
X. Daraus folgt weiterhin, daß eine Steigerung <strong>de</strong>r Konzentration von Y �<br />
zu keiner<br />
Geschwindigkeitserhöhung führt.<br />
2) Bei <strong>de</strong>r Bildung <strong>de</strong>s Carbenium-Ions geht <strong>de</strong>r zentrale Kohlenstoff <strong>de</strong>s Substrats aus<br />
<strong>de</strong>r tetraedischen Form in eine dreibindige planare Struktur über. Der nucleophile<br />
Angriff von Y �<br />
im zweiten Reaktionsschritt kann daher von bei<strong>de</strong>n Seiten <strong>de</strong>s<br />
Carbeniumions erfolgen. Bei chiralem Carbeniumion tritt <strong>de</strong>shalb Racemisierung ein<br />
(in Wirklichkeit nur partiell, da das Nukleophil vom Nukleofug sterisch behin<strong>de</strong>rt wird<br />
und <strong>de</strong>shalb eher auf <strong>de</strong>r an<strong>de</strong>ren Seite <strong>de</strong>s Carbeniumions angreift).<br />
3) Da bei <strong>de</strong>r SN1-Reaktion Ionen solvatisiert wer<strong>de</strong>n müssen, hat das<br />
Solvatationsvermögen <strong>de</strong>s Lösungsmittels großen Einfluß auf <strong>de</strong>n Ablauf <strong>de</strong>r<br />
Reaktion.<br />
4) Da das Carbenium-Ion auch Zwischenstufe von Eliminierungsreaktionen ist,<br />
bil<strong>de</strong>n sich als Nebenprodukte Olefine. Bei bestimmten strukturellen<br />
Gegebenheiten <strong>de</strong>s Substratmoleküls entstehen zusätzlich<br />
Umlagerungsprodukte.<br />
4.1.2 Merkmale <strong>de</strong>r SN2 Substitution:<br />
X<br />
+ Y �<br />
H<br />
H<br />
C Y C X<br />
H<br />
R<br />
R<br />
H<br />
H<br />
Y C + X<br />
H<br />
R<br />
�<br />
1) Bei dieser Reaktion erfolgen Bindungsbildung und Bindungslösung<br />
gleichzeitig. Im Übergangszustand, <strong>de</strong>r <strong>de</strong>n Zustand höchster Energie im<br />
Verlauf <strong>de</strong>r Reaktion darstellt, befin<strong>de</strong>n sich austreten<strong>de</strong> und eintreten<strong>de</strong><br />
Gruppen gleichzeitig an zentralen Kohlenstoffatom, Y ist noch nicht ganz<br />
gebun<strong>de</strong>n und X ist noch nicht ganz gelöst.<br />
2) Die Reaktion verläuft nach einem Geschwindigkeitsgesetz 2. Ordnung., <strong>de</strong>mzufolge<br />
bewirkt eine Konzentrationserhöhung von Y �<br />
eine Erhöhung <strong>de</strong>r Reaktionsgeschwindigkeit.<br />
3) Bei optisch aktiven Verbindungen kehrt sich die Konfiguration um (Wal<strong>de</strong>n-Umkehr).<br />
58
4) Eliminierungs- und Umlagerungsreaktionen lassen sich durch geeignete Wahl <strong>de</strong>r<br />
Reaktionsbedingungen vermei<strong>de</strong>n.<br />
5) Wegen <strong>de</strong>r hohen Ordnung <strong>de</strong>s Übergangszustan<strong>de</strong>s ist die Reaktionsentropie stark<br />
negativ.<br />
In <strong>de</strong>n folgen<strong>de</strong>n Anwendungsbeispielen wird auf <strong>de</strong>n Einfluß <strong>de</strong>r Struktur <strong>de</strong>s<br />
Substrates, <strong>de</strong>r austreten<strong>de</strong>n Gruppe, <strong>de</strong>s Lösungsmittels und an<strong>de</strong>rer Parameter auf<br />
<strong>de</strong>n Reaktionsverlauf eingegangen.<br />
4.2 Herstellung von Alkylhalogeni<strong>de</strong>n aus primären Alkoholen:<br />
Alkylhalogeni<strong>de</strong> sind wichtige Ausgangsstoffe für nucleophile<br />
Substitutionsreaktionen.<br />
Die Reaktivität <strong>de</strong>r Alkylhalogeni<strong>de</strong> im Zuge nucleophiler Substitutionsreaktionen nimmt<br />
von <strong>de</strong>n lodi<strong>de</strong>n über die Bromi<strong>de</strong> zu <strong>de</strong>n Chlori<strong>de</strong>n stark ab, <strong>de</strong>nn mit fallen<strong>de</strong>m<br />
lonenradius ist mehr Energie zur Bildung <strong>de</strong>s X �<br />
-Anions aufzuwen<strong>de</strong>n (geringere<br />
Polarisierbarkeit <strong>de</strong>r Bindung, Verteilung <strong>de</strong>r Ladung auf einem kleinen Raum).<br />
Leicht zugängliches Ausgangsmaterial zur Herstellung primärer<br />
Alkylhalogeni<strong>de</strong> sind die entsprechen<strong>de</strong>n Alkohole, die im Zuge einer<br />
nucleophilen SN2-Reaktion umgesetzt wer<strong>de</strong>n. Allerdings ist OH �<br />
eine so schlechte Abgangsgruppe, daß <strong>de</strong>r Ersatz gegen X � nicht<br />
freiwillig eintritt. Er kann erzwungen wer<strong>de</strong>n, in<strong>de</strong>m man <strong>de</strong>n Alkohol<br />
protoniert and damit eine Wasserabspaltung anstelle <strong>de</strong>r OH � -<br />
Eliminierung ermöglicht:<br />
[H<br />
OH<br />
�<br />
@<br />
R R O H �<br />
H<br />
+ X �<br />
R X + H 2O<br />
Im Prinzip stellt diese Reaktion die Veresterung einer anorganischen Säure mit einem<br />
Alkohol dar.<br />
59
Die Gleichgewichtsreaktion läßt sich durch Zusatz von Schwefelsäure als<br />
wasserentziehen<strong>de</strong>s Mittel auf die Seite <strong>de</strong>r Alkylhalogenidbildung drücken.<br />
Da HI bereits gebil<strong>de</strong>tes Alkyliodid zum Kohlenwasserstoff zu reduzieren vermag, HCl<br />
jedoch zu geringe Nukleophile besitzt, stellt man in <strong>de</strong>r Regel Alkylbromi<strong>de</strong> her, die im<br />
allgemeinen genügend Reaktivität besitzen, um für weitere Synthesen eingesetzt<br />
wer<strong>de</strong>n zu können.<br />
In <strong>de</strong>r Praxis führt man die Reaktion durch mehrstündiges Erhitzen <strong>de</strong>s primären<br />
Alkohols in 48 % HBr unter Zusatz von H2SO4 aus.<br />
Praktikumsversuch 2: Nucleophile Substitution eines primären Alkohols mit HBr<br />
Reicht die Reaktivität eines Alkylbromi<strong>de</strong>s für die nachfolgend geplante Umsetzung<br />
nicht aus, so kann aus ihnen das lodid nach Finkelstein hergestellt wer<strong>de</strong>n. Dazu wird<br />
das Bromid in Aceton gelöst und mit KI erhitzt. KI ist in Aceton gut löslich, KBr<br />
dagegen nur sehr schlecht (Gleichgewichtsverschiebung).<br />
(Aceton)<br />
R Br + KI<br />
R<br />
I + KBr<br />
schwerlöslich<br />
Die Austauschreaktion beruht zum Teil auch auf <strong>de</strong>r größeren<br />
Nukleophilie <strong>de</strong>s I � gegenüber <strong>de</strong>s Br � .<br />
lodi<strong>de</strong> sind außer<strong>de</strong>m direkt herstellbar aus <strong>de</strong>n Alkoholen durch Umsatz mit PI3, das<br />
im Zuge <strong>de</strong>r Reaktion aus I2 und Phosphor gebil<strong>de</strong>t wird.<br />
Im ersten Schritt reagiert <strong>de</strong>r Alkohol wahrscheinlich mit Pl3 zu<br />
R O P R<br />
I<br />
I bzw. O P<br />
O<br />
O<br />
R<br />
R<br />
60
I �<br />
greift dann dieses Zwischenprodukt im Zuge einer nukleophilen Substitutionsreaktion<br />
an:<br />
(RO) 3P + 3 H , 3 5 , + H 3 PO 3<br />
Diese Reaktion ist vor allem wichtig zur Herstellung sekundärer und tertiärer<br />
Alkylhalogeni<strong>de</strong>, (die über die Finkelstein-Reaktion nur mit schlechter Ausbeute<br />
zugänglich sind, weil eine SN2-Reaktion erschwert ist.<br />
Alkylchlori<strong>de</strong> erhält man aus primären Alkoholen, wenn man bei höheren Temperaturen<br />
<strong>de</strong>n Alkohol mit HCl-Gas sättigt.<br />
R OH<br />
+ HCl, Δ<br />
- H 2O<br />
R Cl<br />
Weiterhin entstehen Alkylchlori<strong>de</strong> bei <strong>de</strong>r Umsetzung von Alkoholen mit PCl3, PCl5 o<strong>de</strong>r<br />
SOCl2.<br />
3<br />
+ PCl3 R OH 3 R Cl<br />
- H3PO3 + PCl5 2 R OH 2 R Cl<br />
- POCl3 Primäre Alkylbromi<strong>de</strong> stellt man analog mit PBr3 her:<br />
3<br />
+ PBr3 R CH2 OH 3 R<br />
- H3PO3 CH 2<br />
Eine oft benutzte Möglichkeit, die Abgangsgruppen-Qualität <strong>de</strong>s Hydroxyls in Alkoholen<br />
zu verbessern, ist die Herstellung von Schwefelsäure- und Sulfonsäureestern.<br />
Beispiele:<br />
Br<br />
61
H 3 C<br />
O<br />
H3C S O<br />
O<br />
O<br />
O S O CH3+ Na �<br />
O<br />
CH CH 2 CH 3<br />
CH 3<br />
� ����<br />
�������� �����<br />
� ����� � ��� �<br />
����� �����<br />
� ������<br />
4.3 Herstellung sekundärer und tertiärer Alkylhalogeni<strong>de</strong>:<br />
Br<br />
CH 3<br />
�<br />
CH CH 2 CH 3<br />
Sekundäre und tertiäre Alkohole können nicht so einfach in entsprechen<strong>de</strong><br />
Alkylhalogeni<strong>de</strong> überführt wer<strong>de</strong>n wie primäre:<br />
Versucht man etwa mit 48 %iger Bromwasserstoffsäure (HBr) aus einem sekundären<br />
o<strong>de</strong>r tertiären Alkohol das Bromid herzustellen, so erhält man oft in überwiegen<strong>de</strong>r<br />
Menge Olefine. Grund für diese gegenüber primären Alkoholen an<strong>de</strong>rs verlaufen<strong>de</strong><br />
Reaktion ist <strong>de</strong>r Wechsel <strong>de</strong>s Reaktionmechanismus, wenn man von primären über<br />
sekundäre zu tertiären Alkoholen übergeht. Der gedrängte räumliche Bau verhin<strong>de</strong>rt<br />
<strong>de</strong>n Angriff <strong>de</strong>s Reagenz im Zuge einer SN2-Reaktion. An<strong>de</strong>rerseits wird durch<br />
Zunahme <strong>de</strong>s +I-Effektes vom primären zum tertiären C-Atom hin <strong>de</strong>r Bindungsbruch<br />
zur austreten<strong>de</strong>n Gruppe (-OH bzw. – �<br />
OH2) erleichtert:<br />
H 3C<br />
CH 2<br />
OH<br />
CH 3<br />
CH 3<br />
CH 3<br />
H3C CH OH H3C C OH<br />
CH 3<br />
Dies führt dazu, dass die Bindung zur austreten<strong>de</strong>n Gruppe schon vor <strong>de</strong>m Angriff von<br />
X �<br />
unter Bildung eines Carbenium-Ions gelöst wird (SN1-Mechanismus). Das gebil<strong>de</strong>te<br />
Carbenium-Ion wird mit steigen<strong>de</strong>m +I-Effekt stabilisiert.<br />
Während primäre Alkohole normalerweise bei Substitutionen nach <strong>de</strong>m SN2-<br />
Mechanismus reagieren, wer<strong>de</strong>n tertiäre Alkohole nach <strong>de</strong>m SN1-Mechanismus<br />
substituiert. Die Reaktion sekundärer Alkohole ist zumeist eine Mischung zwischen<br />
62
mono- und bimolekularer Umsetzung und kann durch geeignete Wahl <strong>de</strong>s<br />
Lösungsmittels in <strong>de</strong>n Bereich <strong>de</strong>s einen o<strong>de</strong>r an<strong>de</strong>ren Reaktionstyps gedrängt wer<strong>de</strong>n.<br />
Das im ersten Reaktionsschritt gebil<strong>de</strong>te Carbeniumion einer SN1-Reaktion hat zwei<br />
Möglichkeiten zum Endprodukt weiterzureagieren:<br />
H 2C<br />
C<br />
Wird es von Y �<br />
CH 3<br />
CH 3<br />
+ X �<br />
- HX<br />
Eliminierung<br />
H 3C<br />
CH 3<br />
C<br />
�<br />
CH 3<br />
+ X �<br />
Substitution<br />
CH 3<br />
H3C C X<br />
CH 3<br />
nucleophil angegriffen, so entsteht unter Bindungsknüpfung<br />
(Substitution) ein Halogenalkan. Das Carbenium-Ion ist sp 2 -hybridisiert und planar. Im<br />
Halogenalkan liegt wie<strong>de</strong>r ein tetraedrisches sp 3 -hybridisiertes Kohlenstoffatom vor, die<br />
Substituenten müssen im Zuge <strong>de</strong>r Substitution also wie<strong>de</strong>r enger zusammen rücken,<br />
was umso energieaufwendiger ist, je sperriger die Substituenten sind.<br />
Stabilisiert sich das Carbeniumion unter Eliminierung (in<strong>de</strong>m X �<br />
als Base wirkt und ein<br />
H-Atom aus <strong>de</strong>r β-Position abstrahiert, β Eliminierung), so bleiben die Substituenten<br />
weiterhin in planarer Anordnung (sp 2 Hybrid) und es braucht nicht wie bei <strong>de</strong>r<br />
Substitution, Energie zugeführt wer<strong>de</strong>n. In <strong>de</strong>r Regel läßt es sich aber nicht vermei<strong>de</strong>n,<br />
daß Substitutions- und Eliminierungsprodukte nebeneinan<strong>de</strong>r entstehen.<br />
Das Mengenverhältnis ist abhängig von <strong>de</strong>r Struktur <strong>de</strong>r Verbindung.<br />
Kompliziert wird die Reaktion noch durch die Möglichkeit, daß primär gebil<strong>de</strong>te<br />
Carbeniumionen in an<strong>de</strong>re stabilere Carbeniumionen umgelagert wer<strong>de</strong>n können, die<br />
ihrerseits im Zuge einer Substitutions- und Eliminierungsreaktion weiter reagieren<br />
können:<br />
63
R<br />
R<br />
R<br />
C OH H3O �<br />
R<br />
R<br />
CH2 +<br />
- H2O �<br />
C CH 2<br />
R<br />
>+ �<br />
@<br />
; �<br />
R<br />
R<br />
C CH 2<br />
R<br />
R<br />
R<br />
R<br />
C<br />
X<br />
C CH 2<br />
R<br />
� - H2O OH2 CH R<br />
R<br />
R<br />
C CH 2<br />
Da die SN1-Reaktion und damit die ungewünschte Olefinbildung (E1-Eliminierung)<br />
durch protische polare Lösungsmittel geför<strong>de</strong>rt wird (För<strong>de</strong>rung <strong>de</strong>r Solvatation von<br />
Kationen und Anionen, die Voraussetzung für die Bindungsspaltung ist), muß man zur<br />
Herbeiführung einer SN2-Reakzion ein aprotisches dipolares Lösungsmittel verwen<strong>de</strong>n.<br />
Diese för<strong>de</strong>rt zwar auch die Solvatation, da sie aber zum Anion keine<br />
Wasserstoffbrücke ausbil<strong>de</strong>n können, ist die primäre Abdissoziation von X �<br />
und damit auch die miteinan<strong>de</strong>r konkurrieren<strong>de</strong>n SN1- und E1-Reaktionen.<br />
R<br />
R<br />
�<br />
erschwert<br />
Da die sterisch weniger gespannten Olefine thermodynamisch stabiler, d.h. eine<br />
größere negative freie Bildungsenthalpie haben, wer<strong>de</strong>n sie bei höheren<br />
Temperaturen bevorzugt gebil<strong>de</strong>t. Der Grund dafür ist <strong>de</strong>r bei höheren<br />
Temperaturen größere Energieinhalt <strong>de</strong>r Ausgangsmoleküle.<br />
Will man sekundäre und tertiäre Alkohole in die Halogeni<strong>de</strong><br />
überführen, sollte man daher bei tiefen Temperaturen arbeiten.<br />
Damit allein kann die Ausbeutemin<strong>de</strong>rung zufolge Olefinbildung nur<br />
eingeschränkt, nicht aber vermie<strong>de</strong>n wer<strong>de</strong>n. Deshalb wählt man zur Herstellung<br />
sekundärer und tertiärer Alkylhalogeni<strong>de</strong> <strong>de</strong>n Umweg <strong>de</strong>r Umsetzung mit<br />
Phosphorhalogeni<strong>de</strong>n o<strong>de</strong>r Thionylchlorid.<br />
Br2 und I2 reagiert wie bereits früher ausgeführt, mit rotem Phosphor<br />
unter PX3 Bildung. Dieses Reagenz setzt sich mit Alkoholen zu einem<br />
64
Ester um, <strong>de</strong>r in das Alkylhalogenid überführbar ist. Thionylchlorid<br />
reagiert mit Alkohol zum Chlorsulfinsäureester, <strong>de</strong>r unter SO2 -<br />
R OH<br />
R Cl<br />
Eliminierung in das Alkylchlorid zerfällt.<br />
62&O� R O S Cl<br />
O<br />
H Cl H Cl<br />
O S Cl<br />
O H<br />
SO 2 + HCl<br />
Ein an<strong>de</strong>rer Weg zur Herstellung sekundärer Bromi<strong>de</strong> unter Ausschluß <strong>de</strong>r Gefahr <strong>de</strong>r<br />
Carbeniumionenbildung ist das Verfahren von Hunsdiecker:<br />
R CH<br />
R'<br />
C<br />
O<br />
OAg<br />
+ Br 2 R CH<br />
R'<br />
Br + CO 2 + AgBr<br />
Dabei wer<strong>de</strong>n die trockenen Silbersalze von Carbonsäuren in Fluor-<br />
kohlenwasserstoffen mit Br2 behan<strong>de</strong>lt. Aus <strong>de</strong>m zunächst gebil<strong>de</strong>ten<br />
Acylhypohalogenid entsteht unter CO2-Abspaltung neben einem Bromradikal ein<br />
Alkylradikal, das in einer radikalischen Kettenreaktion zum Endprodukt weiterreagiert<br />
(zum Mechanismus von Kettenreaktionen siehe auch Kap. 4.4).<br />
65
R C<br />
R C<br />
R C<br />
O<br />
OAg<br />
O<br />
O Br<br />
R �<br />
AgBr<br />
+ Br2 R C<br />
+ Br 2 R Br<br />
O<br />
+ Br<br />
O Br<br />
�<br />
R �<br />
O<br />
O Br<br />
R � + CO 2 + Br �<br />
R �<br />
+ Br 2 R Br<br />
+ CO 2<br />
+ Br �<br />
+ Br �<br />
+ Br 2<br />
usw.<br />
Bei Verwendung von CCl4 als Lösungsmittel entsteht als Nebenprodukt immer das<br />
entsprechen<strong>de</strong> Chlorid (Reaktion mit <strong>de</strong>m Lösungsmittel). In <strong>de</strong>n meisten Fällen kann<br />
aber das Chlorid/Bromid-Gemisch für die weiteren Umsetzungen eingesetzt wer<strong>de</strong>n.<br />
Da bereits geringe Feuchtigkeitsspuren die Ausbeute stark vermin<strong>de</strong>rn, wird meist <strong>de</strong>r<br />
gegenüber Wasser weniger empfindliche Cristol-Abbau vorgezogen. Dieser erlaubt<br />
<strong>de</strong>n Einsatz <strong>de</strong>r Carbonsäuren, die in Gegenwart von HgO durch Zutropfen von Br2 das<br />
Bromid liefern.<br />
4.4 Bromierung mit N-Bromsuccinimid:<br />
Unter Einhaltung bestimmter Reaktionsbedingungen können Olefine mit N-<br />
Bromsuccinimid (NBS) unter Beibehaltung <strong>de</strong>r Doppelbindung in Allylstellung<br />
(direkte Nachbarschaft zur Doppelbindung) bromiert wer<strong>de</strong>n.<br />
An<strong>de</strong>rs als bei <strong>de</strong>n bisher beschriebenen Reaktionen han<strong>de</strong>lt es sich hierbei nicht um<br />
eine nucleophile, son<strong>de</strong>rn um eine radikalische Substitution, die als<br />
Radikalkettenreaktion abläuft.<br />
66
Eine Radikalkettenreaktion wird durch einen homolytischen Bindungsbruch unter<br />
Bildung zweier Radikale, von <strong>de</strong>nen min<strong>de</strong>stens ein Radikal <strong>de</strong>r Kettenträger ist,<br />
gestartet. Dies geschieht in vielen Fällen durch Lichtenergie, wobei die Energie<br />
<strong>de</strong>s eingestrahlten Lichtes höher als die Bindungsenergie <strong>de</strong>r zu spalten<strong>de</strong>n<br />
Bindung sein muß.<br />
Bei <strong>de</strong>r Einwirkung von Licht auf N-Bromsuccinimnid (NBS) bil<strong>de</strong>t sich:<br />
CH 2<br />
CH 2<br />
C<br />
C<br />
O<br />
N<br />
O<br />
Br<br />
N-Bromsuccinimid<br />
(NBS)<br />
h•ν<br />
CH 2<br />
CH 2<br />
C<br />
C<br />
O<br />
N<br />
O<br />
• •<br />
Diese Reaktion kann auch mit in katalytischen Mengen zugesetzten "Initiatoren"<br />
eingeleitet wer<strong>de</strong>n. Initiatoren bil<strong>de</strong>n bereits bei geringerer Energiezufuhr<br />
Radikale, die dann ihre Radikal -Eigenschaften auf das Reagenz übertragen z.B.:<br />
C<br />
O O<br />
C<br />
O O<br />
Dibenzoylperoxid<br />
2<br />
2<br />
+<br />
� + 2 CO 2<br />
Das Bromradikal kann nun in einer ersten Kettenfortpflanzungsreaktion das Olefin<br />
radikalisch angreifen:<br />
Br<br />
C<br />
O<br />
O<br />
�<br />
67
R CH 2 CH CH R + Br �<br />
R CH CH CH R + HBr<br />
�<br />
Der Angriff erfolgt an einer <strong>de</strong>r Doppelbindung benachbarten C-H-Bindung, weil<br />
so ein mesomeriestabilisiertes Allylradikal gebil<strong>de</strong>t wer<strong>de</strong>n kann:<br />
R CH CH CH R<br />
�<br />
�<br />
R CH CH CH R<br />
Bei ungleichen Resten R entstehen <strong>de</strong>mzufolge zwei Allylbromi<strong>de</strong>. Durch Einwirkung<br />
eines weiteren Moleküls NBS auf <strong>de</strong>n entstan<strong>de</strong>nen Bromwasserstoff bil<strong>de</strong>t sich Brom,<br />
das eigentliche Agens, das mit <strong>de</strong>m Allylradikal weiterreagiert:<br />
CH 2<br />
CH 2<br />
C<br />
HBr + N Br<br />
NH<br />
+ Br Br<br />
C<br />
O<br />
O<br />
R CH CH CH R<br />
R CH CH CH R<br />
�<br />
Br Br + + Br �<br />
Das Bromradikal greift nun wie<strong>de</strong>r ein Olefinmolekül an und <strong>de</strong>r Reaktionsablauf<br />
beginnt von neuem.<br />
Greift man die mittlere Kettenfortpflanzungsreaktion heraus, so hat N-<br />
Bromsuccinimid nur die Aufgabe, das bei <strong>de</strong>r Substitution gebil<strong>de</strong>te HBr in Brom<br />
umzuwan<strong>de</strong>ln, wodurch eine gleichbleiben<strong>de</strong> Bromkonzentration eingestellt wird.<br />
Obwohl <strong>de</strong>r Mechanismus <strong>de</strong>r Reaktion noch nicht völlig geklärt ist, gibt es<br />
experimentelle Anhaltspunkte dafür, daß eine geringe Bromkonzentration<br />
entschei<strong>de</strong>nd für <strong>de</strong>n Ablauf <strong>de</strong>r Reaktion in die gewünschte Richtung ist.<br />
CH 2<br />
CH 2<br />
Br<br />
C<br />
C<br />
O<br />
O<br />
68
Wichtig ist auch, daß die Reaktion in Tetrachlorkohlenstoff, in <strong>de</strong>m NBS kaum<br />
löslich ist, durchgeführt wird. In polaren Lösungssmitteln wird die<br />
Doppelbindung unter Addition angegriffen. Schon polare Verunreinigungen<br />
(Säuren, Salze) begünstigen diese Nebenreaktion.<br />
4.5 Halogenierung in α-Stellung von Carbonylverbindungen:<br />
Eine Carbonylgruppe bewirkt die Aktivierung benachbarter C-H-Bindungen: Das<br />
positivierte Carbonylkohlenstoffatom versucht negative Ladungsteile aus benachbarten<br />
Bindungen abzuziehen und führt so zu einer partiellen Polarisierung benachbarter C-<br />
Atome, von <strong>de</strong>nen daher die Ablösung eines Protons leichter erfolgen kann<br />
(Aktivierung).<br />
Diese Reaktion wird durch Basen wie auch durch Säuren katalysiert.<br />
a) Basenkatalyse (Hydroxid-lonen, Acetat-Ionen):<br />
R CH 2 C<br />
O<br />
R OH�<br />
- H 2O<br />
R CH C<br />
�<br />
O<br />
R CH C<br />
O<br />
�<br />
R<br />
R<br />
praktisch<br />
nicht<br />
vorhan<strong>de</strong>n<br />
Durch die Base wird das α-ständige Wasserstoffatom abstrahiert und ein Carbanion<br />
gebil<strong>de</strong>t, das sich z.B. mit Brom sofort unter Bildung von α-Bromketon umsetzt:<br />
R CH C<br />
O<br />
�<br />
R<br />
Br Br<br />
R CH C<br />
Br<br />
O<br />
R<br />
+ Br �<br />
69
Diese Reaktion zeigt, daß Carbonylverbindungen neben <strong>de</strong>m<br />
positivierten, d.h. elektrophilen Carbonyl-C-Atom<br />
δ+ δ-<br />
C O<br />
formal ein weiteres, jedoch nucleophiles Reaktionszentrum am αα-C-<br />
b) Säurekatalyse (Säure = H-A):<br />
R CH 2 C<br />
O<br />
R CH 2 C<br />
OH<br />
�<br />
R<br />
R<br />
Atom besitzen:<br />
�<br />
CH C R<br />
O<br />
HA - A �<br />
+<br />
R CH 2 C<br />
OH<br />
+ A � - HA<br />
R CH C<br />
�<br />
OH<br />
Nach vorgeschalteter reversibler Protonierung <strong>de</strong>s Carbonylsauerstoffs wird hier<br />
(wie bei <strong>de</strong>r Basenkatalyse direkt) durch die konjugierte Base <strong>de</strong>r Säure ein H-<br />
Atom vom α-C-Atom unter Bildung eines Enols abgespalten. Dieses Enol reagiert<br />
ebenfalls rasch mit einem Halogenmolekül:<br />
Br<br />
Br<br />
R CH C<br />
O<br />
R<br />
H<br />
Br �<br />
Br<br />
R CH C<br />
O<br />
R<br />
H �<br />
R<br />
R<br />
70
Die α-Halogenketone und Säure<strong>de</strong>rivate sind außeror<strong>de</strong>ntlich reaktive Verbindungen,<br />
die wegen <strong>de</strong>s Vorhan<strong>de</strong>nseins von 2 verschie<strong>de</strong>nen funktionellen Gruppen sehr<br />
wertvoll für <strong>de</strong>n Aufbau komplexer Moleküle sind.<br />
Allerdings reicht die Carbonylaktivität freier Säuren noch nicht zu einer α-Halogenierung<br />
aus. α-Halogencarbonsäuren lassen sich aber über die reaktiveren Säurehalogeni<strong>de</strong><br />
nach <strong>de</strong>m oben zur Herstellung α-bromierter Ketone dargelegten Mechanismus<br />
erhalten. In <strong>de</strong>r Praxis braucht man die Säurebromi<strong>de</strong> nicht herzustellen, wenn man<br />
sich <strong>de</strong>r Metho<strong>de</strong> von Hell-Volhard-Zelinsky bedient: Man läßt auf die vorgelegte<br />
Carbonsäure und roten Phosphor Br2 einwirken. Dabei entsteht zunächst PBr3, das als<br />
Bromierungsreasenz (ähnlich wie bei <strong>de</strong>r Herstellung von sekundären und tertiären<br />
Bromi<strong>de</strong>n diskutiert, Kap.4.3), Über die Phosphorsäureester mit <strong>de</strong>r Carbonsäure das<br />
Säurebromid bil<strong>de</strong>t. Dieses wird in <strong>de</strong>r Folge durch weiteres Br2 zu <strong>de</strong>m α-<br />
Halogencarbonsäurebromid umgesetzt, das durch Reaktion mit überschüssiger Säure<br />
die freie α-Halogencarbonsäure bil<strong>de</strong>t:<br />
R CH 2<br />
R CH 2 C O<br />
2 P, 3 Br2 COOH R CH2C O<br />
- H3PO Br<br />
3<br />
Br<br />
R C O<br />
CH<br />
Br<br />
Br Br<br />
R C O<br />
CH<br />
Br<br />
Br<br />
+<br />
H<br />
R C O<br />
CH<br />
OH<br />
Br<br />
R CH 2 COOH<br />
+<br />
R C O<br />
CH<br />
Br<br />
R C O<br />
CH<br />
Br<br />
Br<br />
R CH 2 C O<br />
Br<br />
H<br />
+ HBr<br />
71
4.6 Nachweisreaktionen:<br />
Halogenverbindungen lassen sich durch die Beilsteinprobe nachweisen: Am<br />
glühen<strong>de</strong>n Kupferdraht wird die Halogenverbindung unter Bildung von<br />
Kupferhalogenid zersetzt, das sich durch charakteristische Grünfärbung zu<br />
erkennen gibt.<br />
Die Reaktion versagt oft, falls die Halogenverbindung zu flüchtig ist<br />
(Wegdampfen <strong>de</strong>r Verbindung vor Zersetzung) o<strong>de</strong>r bei Gegenwart von<br />
Stickstoffverbindungen, die durch Zersetzung Nitrile bil<strong>de</strong>n) die ebenfalls als<br />
Pseudohalogeni<strong>de</strong> mit Cu unter grüner Flammenfärbung reagieren.<br />
Der Nachweis <strong>de</strong>r Halogeni<strong>de</strong> gelingt ferner nach Aufschluß <strong>de</strong>r organischen<br />
Substanz mit metallischem Natrium im Glühröhrchen durch Fällen mit AgNO3 in<br />
salpetersaurer Lösung.<br />
Durch Hydrolyse-Versuche kann die Substanzklasse, in die die Halogenverbindung<br />
gehört, ermittelt wer<strong>de</strong>n: Es wird in wäßriger Lösung unter Zusatz von AgNO3 zunächst<br />
bei Raumtemperatur und schließlich in <strong>de</strong>r Wärme hydrolysiert. Je nach<strong>de</strong>m, ob in <strong>de</strong>r<br />
Kälte o<strong>de</strong>r erst nach Erwärmung ein Nie<strong>de</strong>rschlag zu beobachten ist, kann eine<br />
Unterteilung nach Substanzgruppen erfolgen.<br />
In <strong>de</strong>r Kälte: Säurechlori<strong>de</strong>, tert. Alkylhalogeni<strong>de</strong>, Allylhalogeni<strong>de</strong>,<br />
geminale Dibromi<strong>de</strong>.<br />
In <strong>de</strong>r Wärme: Primäre und sekundäre Alkylchlori<strong>de</strong>, (Arylhalogeni<strong>de</strong> geben keine<br />
Fällung<br />
5. Herstellung von Ethern, Nitrilen und Nitroverbindungen aus primären<br />
Alkylhalogeni<strong>de</strong>n:<br />
Primäre AlkyIhalogeni<strong>de</strong> sind i<strong>de</strong>ale Ausgangsverbindungen zur Herstellung von<br />
Ethern, Thioethern, Nitroalkanen und Nitrilen, aber auch von Thiolen und Aminen.<br />
Will man Thiole und primäre bzw. sekundäre Amine herstellen, muß man<br />
allerdings durch Verwendung von Schutzgruppen gegen eine weitergehen<strong>de</strong><br />
Alkylierung Vorkehrungen treffen. Im Falle <strong>de</strong>r Thiole wählte man daher <strong>de</strong>n Weg<br />
72
über S-Alkyl-isothiuronium-Salze, die aus Alkylhalogenid und Thioharnstoff<br />
zugänglich sind:<br />
S C NH 2<br />
NH 2<br />
+ RX<br />
R<br />
�<br />
X �<br />
S C NH 2<br />
NH 2<br />
R SH + CO 2 + 2 NH 3 + HX<br />
(OH �<br />
+ 2 H2O Primäre Amine sind über die N-Alkylphthalimi<strong>de</strong> zugänglich (Gabriel-Synthese):<br />
+ R X<br />
- KX<br />
O<br />
C<br />
C<br />
O<br />
Phthalimid<br />
NH<br />
+ KOH<br />
- H2O O<br />
C<br />
C<br />
O<br />
N<br />
N-Alkyl-Phthalimid<br />
O<br />
C<br />
C<br />
O<br />
Kalium-Phthalimid<br />
(Hydrazin)<br />
R H 2 N NH 2<br />
N<br />
�<br />
K �<br />
+ R NH 2<br />
O<br />
C<br />
C<br />
O<br />
primäres Amin<br />
NH<br />
NH<br />
Phthalhydrazid<br />
Die Umsetzungen primärer Alkylhalogeni<strong>de</strong> verlaufen überwiegend nach einer SN2-<br />
Reaktion: Das angreifen<strong>de</strong> Agens wird we<strong>de</strong>r durch räumliche Faktoren an <strong>de</strong>r<br />
Reaktion mit <strong>de</strong>m positivierten, das Halogenatom tragen<strong>de</strong>n Kohlenstoff behin<strong>de</strong>rt,<br />
73
noch besteht die Möglichkeit zur Ausbildung eines stabilen Carbeniumions, das eine<br />
SN1-Reaktion begünstigen wur<strong>de</strong>.<br />
För<strong>de</strong>rlich ist <strong>de</strong>r SN2-Reaktion die Verwendung eines dipolaren aprotischen<br />
Lösungsmittels wie Dimethylsulfoxid o<strong>de</strong>r Dimethylformamid.<br />
Die Herstellung von Ethern und Thioethern im Zuge einer Williamson-schen<br />
Ethersynthese ist unproblematisch:<br />
R X + Na �<br />
R X + Na �<br />
� - NaX<br />
O R'<br />
R<br />
� - NaX<br />
S R'<br />
R S<br />
Praktikumsversuch 3: Methylether nach Williamson<br />
O R'<br />
Beim Umsatz eines Alkylhalogenids mit einem Nitrit- o<strong>de</strong>r Cyanidion muß beachtet<br />
wer<strong>de</strong>n, daß es sich hierbei um ambi<strong>de</strong>nte Anionen han<strong>de</strong>lt, die je nach<br />
Reaktionsbedingungen und Reagenz verschie<strong>de</strong>n reagieren können:<br />
In Nitrit-Ionen verfügen nicht nur die bei<strong>de</strong>n Sauerstoffatome über<br />
"nucleophile Kräfte<br />
� �<br />
O N O O N O<br />
son<strong>de</strong>rn auch das Stickstoffatom, da es ein freies Elektronenpaar besitzt. In<br />
gleicher Weise ist auch das Cyanidion - das ebenfalls 2 reaktive Zentren trägt - zu<br />
<strong>de</strong>n "ambi<strong>de</strong>nten" Anionen zu rechnen:<br />
�<br />
C<br />
N<br />
C<br />
�<br />
N<br />
R'<br />
74
Je nach<strong>de</strong>m welches Zentrum <strong>de</strong>s ambi<strong>de</strong>nten Anions reagiert, erhält man durch<br />
Umsatz von Alkylhalogeni<strong>de</strong>n mit Nitrit entwe<strong>de</strong>r Nitroverbindungen o<strong>de</strong>r<br />
Salpetrigsäureester:<br />
R X + NO �<br />
2<br />
mit Cyanidionen Nitrile o<strong>de</strong>r Isonitrile:<br />
R X<br />
�<br />
C<br />
C<br />
N<br />
�<br />
N<br />
R N O<br />
�<br />
O �<br />
Nitroalkan<br />
R O N O<br />
Salpetrigsäureester<br />
R C<br />
Nitril<br />
R<br />
N<br />
N O<br />
Isonitril<br />
(S N2)<br />
(S N1)<br />
Die Reaktionsweise ambi<strong>de</strong>nter Anionen ist von verschie<strong>de</strong>nen Faktoren<br />
abhängig. Bei einem SN2-Mechanismus reagiert bevorzugt das Atom mit höchster<br />
nucleophiler Kraft (das am leichtesten polarisierbare Atom), d..h. beim Umsatz<br />
mit Nitrit wer<strong>de</strong>n Nitroalkane, mit Cyanid Cyani<strong>de</strong> entstehen. Verläuft die<br />
Reaktion nach einem SN1-Mechanismus, wird bevorzugt das Atom höchster<br />
Elektronendichte angegriffen<br />
(Bildung von Salpetrigsäureestern, bzw. Isonitrilen). Ob SN1- o<strong>de</strong>r SN2-Reaktion<br />
vorliegt ist, wie bereits diskutiert, hauptsächlich abhängig von <strong>de</strong>r Struktur <strong>de</strong>s<br />
Alkylhalogenids und <strong>de</strong>n Eigenschaften <strong>de</strong>s Lösungsmittels.<br />
Je leichter polarisierbar die Abgangsgruppe ist, umso eher reagiert <strong>de</strong>r daran<br />
gebun<strong>de</strong>ne Alkylrest mit <strong>de</strong>m leichter polarisierbaren Zentrum <strong>de</strong>s ambi<strong>de</strong>nten Agens<br />
(SN2). Die Bildung <strong>de</strong>r Nitroverbindung erfolgt also leichter mit Iodi<strong>de</strong>n als mit<br />
Bromi<strong>de</strong>n o<strong>de</strong>r gar mit Chlori<strong>de</strong>n.<br />
75
Die nucleophile Kraft für SN2-Reaktionen wird überdies stark durch Verwendung eines<br />
dipolaren aprotischen Lösungsmittels gesteigert. Deshalb erhält man bei <strong>de</strong>r<br />
Umsetzung primärer Iodi<strong>de</strong> mit NO2 �<br />
Nitroverbindung und nicht <strong>de</strong>n Salpetrigsäureester.<br />
5.1 Nachweisreaktionen:<br />
5.1.1 Ether<br />
in Dimethylformamid fast ausschließlich die<br />
Ether sind meistens sehr beständige Verbindungen und geben keine typischen<br />
Nachweisreaktionen, die auf die funktionelle Gruppe R-O-R hin<strong>de</strong>uten.<br />
Deswegen sind sie mit gesättigten Kohlenwasserstoffen verwechselbar. Die<br />
meisten aliphatischen Ether sind jedoch in konzentrierter Salzsäure unter<br />
Oniumsalzbildung löslich:<br />
Cl<br />
�<br />
R O R'<br />
�<br />
Diese Salze zerfallen beim Verdünnen wie<strong>de</strong>r (Metho<strong>de</strong> zur Abtrennung).<br />
H<br />
Zum ein<strong>de</strong>utigen Nachweis müssen Ether mit Säure (HI, HBr) gespalten wer<strong>de</strong>n<br />
und die entstehen<strong>de</strong>n Alkylhalogeni<strong>de</strong> als solche i<strong>de</strong>ntifiziert wer<strong>de</strong>n.<br />
5.1.2 Nitroalkane:<br />
R O R' + H I R I + R O H<br />
In primären und sekundären Nitroalkanen bewirkt die Nitrogruppe eine leichte<br />
"Beweglichkeit" <strong>de</strong>r am gleichen C-Atom gebun<strong>de</strong>nen H-Atome, so daß folgen<strong>de</strong><br />
Tautomerie ermöglicht wird:<br />
76
R<br />
CH<br />
H<br />
�<br />
N<br />
O<br />
O �<br />
R<br />
R<br />
�<br />
CH<br />
CH<br />
�<br />
N<br />
�<br />
N<br />
aci-Form<br />
In wäßriger Natronlauge gehen daher primäre und sekundäre Nitroalkane unter<br />
Salzbildung in Lösung, aus alkoholischer Natronlauge wer<strong>de</strong>n die Natriumsalze<br />
abgeschie<strong>de</strong>n.<br />
Als Nachweis und Unterscheidungsreaktion von Nitroalkanen verwen<strong>de</strong>t man die<br />
Umsetzung mit salpetriger Säure. Diese Reaktion beruht ebenfalls auf <strong>de</strong>r<br />
aktivieren<strong>de</strong>n Wirkung <strong>de</strong>r Nitrogruppe auf benachbarte H-Atome. Mit primären<br />
Nitroalkanen wer<strong>de</strong>n die sogenannten Nitrolsäuren erhalten, <strong>de</strong>ren Alkalisalze<br />
blutrot gefärbt sind.<br />
R CH2NO2 R C NO2 N OH<br />
Nitrolsäure<br />
R C NO2 N OH<br />
+ NaOH<br />
R<br />
R<br />
C<br />
N<br />
C<br />
�<br />
N<br />
O �<br />
�<br />
N<br />
N O<br />
O<br />
O<br />
O<br />
O<br />
�<br />
H<br />
H<br />
+ H 2O<br />
O �<br />
O<br />
O �<br />
O �<br />
Sekundäre Nitroalkane ergeben blaugrün gefärbte Pseudonitrole.<br />
+ Na �<br />
77
R � O �<br />
R<br />
CH<br />
N<br />
O<br />
+ HNO2 - H2O R<br />
R<br />
C<br />
�<br />
N<br />
N O<br />
O �<br />
O<br />
Pseudonitrol<br />
Tertiäre Nitroalkane sind dagegen nicht in <strong>de</strong>r Lage, mit salpetriger Säure zu<br />
reagieren.<br />
5.1.3 Nitrile<br />
Nitrile ergeben bei basischer Hydrolyse die entsprechen<strong>de</strong> Carbonsäure und<br />
Ammoniak:<br />
H2O R CH2COOH (OH �<br />
R CH2CN + NH3 Der Nachweis <strong>de</strong>s gasförmig entweichen<strong>de</strong>n Ammoniaks mit Indikatorpapier<br />
dient als Nachweis auf das Vorhan<strong>de</strong>nsein von Nitrilen. Es ist jedoch zu<br />
beachten, daß auch Säureami<strong>de</strong> bei <strong>de</strong>r Hydrolyse Ammoniak entwickeln. Die<br />
Hydrolyse wird mit konzentrierter Kalilauge in <strong>de</strong>r Sie<strong>de</strong>hitze durchgeführt.<br />
Zur I<strong>de</strong>ntifizierung wer<strong>de</strong>n die Nitrile durch Reduktion mit Natrium in Amine überführt<br />
und als solche z.B. durch Umsetzung mit Benzoylchlorid nachgewiesen:<br />
R NH 2 +<br />
R C N R CH2NH2 O<br />
C<br />
Cl<br />
+<br />
N<br />
(Pyridin)<br />
- Pyridin �HCl<br />
C<br />
O<br />
NH R<br />
ein N-Alkylbenzamid<br />
78
6. Herstellung eines sekundären o<strong>de</strong>r tertiären Alkohols bzw. einer Säure durch<br />
Grignardreaktion:<br />
Alkylhalogeni<strong>de</strong> können infolge ihrer Polarisation nicht direkt mit Carbonylgruppen in<br />
Reaktion gebracht wer<strong>de</strong>n:<br />
δ+ δ− R δ+ δ−<br />
R CH2I + C O<br />
R<br />
Will man eine solche Reaktion erzwingen, so muss man vorher das Alkylhalogenid<br />
umpolarisieren (Umpolung). Dies gelingt über metallorganische Verbindungen:<br />
Alkylhalogeni<strong>de</strong> setzen sich in ",absolutem", d.h. wasserfreiem Ether langsam mit<br />
Magnesiumspänen formal unter Einschub <strong>de</strong>s Metalls zwischen Alkylrest und<br />
Halogenatom um. Die so gebil<strong>de</strong>te Grignardverbindling steht im Gleichgewicht mit <strong>de</strong>m<br />
Dialkylmagnesium:<br />
2<br />
R Mg X<br />
R X + Mg R Mg X<br />
X<br />
Mg<br />
R<br />
X<br />
Die Aufgabe <strong>de</strong>s Lösungsmittels ist es, das Grignard-Reagenz komplex zu bin<strong>de</strong>n:<br />
H 3C<br />
H 3C<br />
CH 2<br />
CH 2<br />
Mg<br />
O<br />
R<br />
R Mg X<br />
O<br />
X<br />
CH 2 CH 3<br />
CH 2 CH 3<br />
Mg<br />
R<br />
+<br />
X<br />
Mg<br />
R<br />
79
Zur besseren Aktivierung kann <strong>de</strong>r Ether nach Bildung <strong>de</strong>r Grignard-Verbindung<br />
ab<strong>de</strong>stilliert und durch ein an<strong>de</strong>res Lösungsmittel ersetzt wer<strong>de</strong>n. Die<br />
„metallorganische“ Verbindung kann eine polarisierbare Doppelbindung, z.B. C=O o<strong>de</strong>r<br />
-C≡NI am Kohlenstoffatom nucleophil angreifen:<br />
R<br />
R<br />
δ+<br />
C<br />
H 2O<br />
δ−<br />
O<br />
+<br />
R<br />
R<br />
δ− δ+ δ−<br />
R' Mg X R C O Mg X<br />
R C OH + HO Mg X<br />
R'<br />
Je nach Art <strong>de</strong>r Carbonylgruppe wer<strong>de</strong>n erhalten:<br />
R<br />
R<br />
R<br />
C<br />
C<br />
O 1. R'MgX<br />
H<br />
aus Al<strong>de</strong>hy<strong>de</strong>n<br />
O<br />
aus Ketonen<br />
2.<br />
1.<br />
2.<br />
H 2 O<br />
R'MgX<br />
H 2 O<br />
R<br />
R<br />
H<br />
C<br />
R<br />
C<br />
R'<br />
C O H<br />
H<br />
1. R'MgX<br />
2. H2O H<br />
H<br />
C<br />
R'<br />
OH<br />
aus Formal<strong>de</strong>hyd primäre Alkohole<br />
OH<br />
R'<br />
sekundäre Alkohole<br />
OH<br />
R'<br />
tertiäre Alkohole<br />
80
Der Angriff <strong>de</strong>r Alkylgruppe auf die Carbonylverbindung erfolgt innerhalb eines<br />
cyclischen Komplexes mit einem zweiten Molekül <strong>de</strong>r Grignard-Verbindung. Die relativ<br />
geringe nucleophile Kraft <strong>de</strong>r magnesiumorganischen Verbindung wird auf diese Weise<br />
verstärkt:<br />
R<br />
C<br />
O<br />
R<br />
R'<br />
Mg<br />
X<br />
Mg<br />
R<br />
X<br />
Statt einer zweiten Grignard-Verbindung kann auch eine Lewis-Säure wie<br />
Magnesiumbromid diese Wirkung ausüben:<br />
R<br />
C<br />
O<br />
R<br />
R'<br />
Mg<br />
Br<br />
R<br />
R<br />
C<br />
O<br />
R'<br />
Mg<br />
X<br />
+<br />
Mg<br />
R<br />
R<br />
R R'<br />
Mg<br />
Br<br />
X C<br />
O<br />
+<br />
Mg<br />
Mg<br />
Br<br />
Setzt man Grignard-Reagenzien mit stark raumbeanspruchen<strong>de</strong>n Gruppen um, so<br />
verläuft die Reaktion vorwiegend unter Hydridionenübertragung an das Kohlen-<br />
stoffatom <strong>de</strong>r Carbonylgruppe, weil eine zweite Grignardverbindung aus sterischen<br />
Grün<strong>de</strong>n nicht an <strong>de</strong>m für die Reaktion notwendigen cyclischen Übergangszustand<br />
teilnehmen kann.<br />
Br<br />
X<br />
X<br />
81
R<br />
R<br />
R<br />
R<br />
C<br />
C<br />
H<br />
Mg<br />
X<br />
R R<br />
C<br />
O<br />
R<br />
R<br />
C<br />
R<br />
C R<br />
R<br />
R<br />
+<br />
H<br />
Mg<br />
X<br />
CH<br />
C<br />
O<br />
R<br />
R<br />
+ H2O - Mg(OH)X<br />
Aus <strong>de</strong>m Grignardreagenz entsteht so ein Olefin, aus <strong>de</strong>r Carbonylverbindung ein<br />
Alkohol. Durch Zusatz von Magnesiumbromid kann diese Nebenreaktion unterdrückt<br />
wer<strong>de</strong>n.<br />
Aus Carbonsäureestern entstehen zunächst Ketone:<br />
R C O<br />
R''MgX<br />
OR'<br />
R''MgX<br />
O<br />
R C<br />
R''<br />
MgX<br />
R''<br />
O<br />
MgX<br />
R C O R'<br />
R''<br />
H 2O<br />
- Mg(OH)X<br />
- R'OMgX<br />
OH<br />
R C R''<br />
R''<br />
OH<br />
O<br />
R C<br />
Die Reaktion ist jedoch auf <strong>de</strong>r Stufe <strong>de</strong>r Ketone nicht anhaltbar, da diese wegen ihrer<br />
hohen Carbonylaktivität eher reagieren als die Ester, so dass diese mit überschüssiger<br />
Grignardverbindung weiter tertiäre Alkohole bil<strong>de</strong>n.<br />
Mit CO2 entstehen Carbonsäuren:<br />
O C O + R Mg X O C<br />
O Mg X H2O R<br />
R''<br />
R C O<br />
OH<br />
82
Die Carbonylaktivität <strong>de</strong>r so gebil<strong>de</strong>ten Säureanionen reicht nicht mehr für eine weitere<br />
Umsetzung mit noch vorhan<strong>de</strong>nem Grignardreagenz aus.<br />
Metallorganische Verbindungen reagieren mit allen Stoffen, die aktive Wasserstoffe<br />
enthalten, also mit Wasser, Alkoholen, Mercaptanen, Säuren, Ami<strong>de</strong>n und Aminen<br />
unter Bildung eines Kohlenwasserstoffs:<br />
H 3C Mg Br + HO CH 2 R CH 4 + Br Mg OCH 2R<br />
Aus <strong>de</strong>m Grignardreagenz <strong>de</strong>s Methylbromids wird Methan gebil<strong>de</strong>t, das<br />
gasvolumetrisch bestimmbar ist. Somit kann die Anzahl aktiver Wasserstoffe bestimmt<br />
wer<strong>de</strong>n (Zerewitinow-Reaktion).<br />
Stark CH-aci<strong>de</strong> Stoffe wie Acetylene reagieren ebenfalls mit Grignardreagenz:<br />
R C C H + R' Mg X R C C Mg X + R' H<br />
Dieser Weg wird oft zur Herstellung sonst nicht zugänglicher Grignard-Verbindungen<br />
beschritten.<br />
Wegen <strong>de</strong>r Zersetzbarkeit von Grignard-Verbindungen durch Verbindung mit aktiven<br />
Wasserstoffatomen sind vor allem Wasser- o<strong>de</strong>r Alkoholspuren aus <strong>de</strong>m als<br />
Lösungsmittel fungieren<strong>de</strong>n Ether vor <strong>de</strong>r Reaktion vollständig zu entfernen.<br />
Alkylhalogeni<strong>de</strong> reagieren mit Grignard-Verbindungen ähnlich <strong>de</strong>r Wurtz'schen<br />
Synthese zu Alkanen:<br />
R X + R' Mg X R R' + MgX2 Wichtig ist die Austauschreaktion <strong>de</strong>s Magnesium-Atoms gegen Cadmium bzw.<br />
allgemein gegen edlere Metalle:<br />
83
2 RMgX + CdCl 2<br />
R 2Cd + MgX 2 + MgCl 2<br />
Die Cadmium-organischen Verbindungen sind weniger reaktiv als die Grignard-<br />
Verbindungen. Setzt man sie mit Säurechlori<strong>de</strong>n um, so bleibt die Reaktion auf <strong>de</strong>r<br />
Stufe <strong>de</strong>r Ketone stehen:<br />
R C O<br />
O<br />
R C<br />
Cl + CdR''2 R'' + CdCl2 Der Nachweis von Alkoholen ist im Kapitel 3.3 beschrieben, <strong>de</strong>r von Ketonen im Kapitel<br />
7.<br />
Praktikumsversuch 4: Grignard-Reaktion zum sekundären Alkohol.<br />
7. Oxidation primärer und sekundärer Alkohole zu Al<strong>de</strong>hy<strong>de</strong>n bzw. Ketonen:<br />
Primäre Alkohole sind über die Stufe <strong>de</strong>r Al<strong>de</strong>hy<strong>de</strong> zu Carbonsäuren oxidierbar:<br />
R CH 2 OH<br />
R C<br />
O<br />
O<br />
R C<br />
H OH<br />
Es ist schwierig, die Reaktion auf <strong>de</strong>r Stufe <strong>de</strong>r Al<strong>de</strong>hy<strong>de</strong> anzuhalten, da diese - als<br />
Al<strong>de</strong>hydhydrate - leicht zu Carbonsäuren oxidiert wer<strong>de</strong>n können. Da Alkohole höhere<br />
Sie<strong>de</strong>punkte als die Al<strong>de</strong>hy<strong>de</strong> haben (Wasserstoffbrückenbindungen), kann man <strong>de</strong>n<br />
entstan<strong>de</strong>nen Al<strong>de</strong>hyd durch rasche Destillation aus <strong>de</strong>m Reaktionsmedium entfernen.<br />
Als Oxidationsmittel dient meist Chromsäure, die man durch Zusatz von Schwefelsäure<br />
aus Dichromat in Freiheit setzt.<br />
H 3C<br />
CH 2<br />
CH 2<br />
OH<br />
H 2Cr 2O 7<br />
H 3C<br />
CH 2<br />
C O<br />
H<br />
84
Als Nebenprodukt entsteht <strong>de</strong>r Ester : Gebil<strong>de</strong>ter Al<strong>de</strong>hyd und Alkohol setzen sich zum<br />
Halbacetal um, das dann mit Chromsäure zum Ester oxidiert wird:<br />
H 3C<br />
H 3C<br />
CH 2<br />
H 3C<br />
CH 2<br />
CH 2<br />
CH 2<br />
C O<br />
C<br />
H<br />
OH<br />
O<br />
O<br />
CH 2 CH 2<br />
H 3C<br />
H 3C<br />
CH 3<br />
CH 2<br />
CH 2<br />
C<br />
CH 2<br />
OH<br />
H<br />
O<br />
H 2Cr 2O 7<br />
Diese Reaktion tritt vor allem dann ein, wenn man höhere Al<strong>de</strong>hy<strong>de</strong> herstellen will.<br />
In <strong>de</strong>r Technik wen<strong>de</strong>t man vorzugsweise katalytische Oxidationsverfahren an, bei<br />
<strong>de</strong>nen <strong>de</strong>r Alkohol über einen Kupfer-Chromoxid-Katalysator geleitet wird.<br />
Nach einem neueren Verfahren führt man <strong>de</strong>n Alkohol in das Tosylat über und oxidiert<br />
dieses mit Dimethylsulfoxid o<strong>de</strong>r geht vom entsprechen<strong>de</strong>n Alkylchlorid aus und oxidiert<br />
mit Trimethylamin-N-oxid:<br />
R CH 2 OH<br />
R CH O<br />
H<br />
+ TosCl<br />
- HCl<br />
� - S(CH 3) 2<br />
S(CH 3) 2<br />
�<br />
HCO3 R CH 2 O SO 2 CH 3<br />
- H 2CO 3<br />
R C<br />
O<br />
H<br />
�<br />
Ox.<br />
- TosOH<br />
O S CH 3<br />
�<br />
CH 3<br />
85
R CH 2<br />
O N(CH3) 3<br />
�<br />
�<br />
Cl<br />
7.1 Oppenauer-Oxidation:<br />
Cl �<br />
R CH<br />
H O<br />
H H<br />
O N(CH3) 3<br />
�<br />
R C<br />
O<br />
H<br />
+<br />
�<br />
Cl �<br />
HN(CH 3) 3<br />
Ein sehr schonen<strong>de</strong>s und spezifisches Oxidationsverfahren ist die Oppenauer-<br />
Oxidation, die vorzugsweise zur Oxidation von Naturstoffen eingesetzt wird. In <strong>de</strong>r<br />
Regel wird ein sekundärer Alkohol über das Aluminiumalkoholat in das Keton überführt.<br />
Zunächst wird aus <strong>de</strong>m Alkohol mit Aluminium-t-butylat das Aluminiumalkoholat<br />
hergestellt:<br />
R<br />
3 R CH<br />
OH + (H 3C) 3C O 3 Al R CH<br />
R<br />
O Al + 3 (H<br />
3<br />
3C) 3C OH<br />
Das Alkoholat reagiert weiter mit zugesetztem Cyclohexanon in einem Redox-Prozess<br />
zum entsprechen<strong>de</strong>n Keton:<br />
R<br />
R CH O Al + 3 O<br />
3<br />
3<br />
R<br />
R<br />
C<br />
O<br />
+<br />
H<br />
Al<br />
O<br />
3<br />
Die Oxidation von sekundären Alkoholen zu Ketonen ist in <strong>de</strong>r Regel aber auch mit<br />
Chromsäure durchführbar, weil die Ketone nicht mehr weiter oxidierbar sind:<br />
R<br />
R CH<br />
OH<br />
H 2CrO 4<br />
R<br />
R<br />
C<br />
O<br />
86
Die erhaltenen Al<strong>de</strong>hy<strong>de</strong> und Ketone können im Zuge von Grignard-Reaktionen unter<br />
Bildung von C-C-Bindungen zu sekundären bzw. tertiären Alkoholen umgesetzt wer<strong>de</strong>n<br />
(siehe vorn).<br />
7.2 Nachweis von Al<strong>de</strong>hy<strong>de</strong>n und Ketonen:<br />
Al<strong>de</strong>hy<strong>de</strong> und Ketone gehen zahlreiche Kon<strong>de</strong>nsations- bzw. Additionsreaktionen ein,<br />
die man direkt für Nachweisreaktionen und zur I<strong>de</strong>ntifizierung verwen<strong>de</strong>n kann.<br />
Am gebräuchlichsten ist die Umsetzung mit 2,4-Dinitrophenylhydrazin zu 2,4-Dinitrophenylhydrazonen:<br />
R<br />
R<br />
C O + H2N NH<br />
R<br />
R<br />
C N NH<br />
NO 2<br />
NO 2<br />
NO 2<br />
NO 2<br />
- H 2O<br />
8. Herstellung ungesättigter und gesättigter Kohlenwasserstoffe:<br />
8.1 Herstellung ungesättigter Kohlenwasserstoffe:<br />
Als Ausgangsmaterialien zur Herstellung ungesättigter Kohlenwasserstoffe dienen<br />
Verbindungen, die funktionelle Gruppen enthalten. Die funktionelle Gruppe wird im<br />
Zuge einer Eliminierungsreaktion mit einem Wasserstoffatom aus einer benachbarten<br />
CH-Bindung abgespalten.<br />
R CH 2 CH R'<br />
X<br />
- HX<br />
R CH CH R'<br />
Wie bei <strong>de</strong>n Substitutionsreaktionen unterschei<strong>de</strong>t man nach <strong>de</strong>r Art <strong>de</strong>s<br />
Eliminierungsmechanismus E1- und E2-Reaktionen.<br />
87
8.1.1 E1-Eliminierung:<br />
Bei <strong>de</strong>r E1-Eliminierung wird wie bei <strong>de</strong>r SN1-Reaktion im geschwindig-<br />
keitsbestimmen<strong>de</strong>n Schritt <strong>de</strong>r Reaktion die Bindung zwischen <strong>de</strong>m Substituenten X<br />
und <strong>de</strong>m damit verbun<strong>de</strong>nen Kohlenstoffatom gelöst, so dass sich als Zwischenprodukt<br />
das gleiche Carbeniumion wie bei <strong>de</strong>r SN1-Substitution bil<strong>de</strong>t. Dementsprechend wird<br />
auch die E1-Reaktion durch protische polare Lösungsmittel begünstigt, die befähigt<br />
sind, durch Wasserstoffbrückenbindungen zum austreten<strong>de</strong>n Ion X �<br />
dieses zu<br />
solvatisieren und gleichzeitig in <strong>de</strong>r Lage sind, durch vorhan<strong>de</strong>ne freie Elektronenpaare<br />
an Heteroatomen das gebil<strong>de</strong>te Carbeniumion zu stabilisieren.<br />
Der Bau <strong>de</strong>s Carbeniumions ist ausschlaggebend dafür, in welchem Ausmaß<br />
Substitution o<strong>de</strong>r Eliminierung erfolgt: Tertiäre Carbeniumionen (beson<strong>de</strong>rs mit<br />
voluminösen Substituenten) erschweren <strong>de</strong>n Angriff <strong>de</strong>s nucleophilen Teilchens, so<br />
dass die Eliminierung begünstigt ist. Auch die Möglichkeit, durch Eliminierung sterische<br />
Spannung abzubauen ("sterische Beschleunigung"), begünstigt die Olefinbildung,<br />
ebenso wie Temperaturerhöhung (vergl. Kap.4. SN1-Substitution).<br />
Typische Beispiele für <strong>de</strong>rartige Eliminierungsreaktionen sind die säurekatalysierte<br />
Wasserabspaltung aus tertiären Alkoholen und die Solvolyse von Schwefelsäure- o<strong>de</strong>r<br />
Sulfonsäureestern in Alkohol.<br />
R<br />
R<br />
C<br />
OH<br />
CH 2 R + H 3O �<br />
- 2 H 2O<br />
R CH 2 CH<br />
8.1.2 E2-Eliminierung:<br />
R<br />
R<br />
R<br />
�<br />
C<br />
O SO 3H<br />
CH 2 R<br />
(EtOH)<br />
- [H �<br />
@<br />
R CH<br />
Bei <strong>de</strong>r E2-Reaktion erfolgt die Abstraktion <strong>de</strong>s Protons vom β-Kohlenstoffatom und die<br />
Eliminierung <strong>de</strong>s Substituenten X nahezu gleichzeitig. Beson<strong>de</strong>rs geeignet als<br />
(H �<br />
R<br />
R<br />
C<br />
C<br />
R<br />
H<br />
CH<br />
R<br />
88
angreifen<strong>de</strong>s Agens sind voluminöse Basen, die durch ihre Raumbeanspruchung<br />
schlecht in <strong>de</strong>r Lage sind, in einer Nebenreaktion das <strong>de</strong>n Substituenten tragen<strong>de</strong><br />
Kohlenstoffatom nucleophil anzugreifen (Unterschied Basizität und Nucleophilie vergl.<br />
Kap.4). Als Basen fungieren beispielsweise Chinolin o<strong>de</strong>r Dicyclohexylamin zur<br />
Abspaltung von Halogenwasserstoff aus primären Alkylhalogeni<strong>de</strong>n:<br />
H<br />
R<br />
H<br />
H<br />
N<br />
C<br />
X<br />
C H<br />
H<br />
H<br />
R<br />
C<br />
C<br />
H<br />
H<br />
X �<br />
�<br />
+ (C 6H 11) 2NH 2<br />
Stark ausgeprägt ist die Neigung zur E2-Eliminierung bei quartären Ammoniumbasen<br />
(Hofmann-Eliminierung), die schon beim Erhitzen dieser Basen eintritt:<br />
H 3C<br />
CH CH<br />
vN(CH3)<br />
3<br />
w<br />
OH<br />
CH 3<br />
CH 3<br />
Hitze<br />
Sterischer Verlauf <strong>de</strong>r E2-Eliminierung:<br />
H 2C<br />
H 3C<br />
CH CH<br />
+<br />
CH<br />
C<br />
CH 3<br />
CH 3<br />
CH 3<br />
CH 3<br />
> 98%<br />
< 2%<br />
Voraussetzung für die bimolekulare Eliminierung ist, dass <strong>de</strong>r abzuspalten<strong>de</strong><br />
Substituent zu einem am benachbarten C-Atom gebun<strong>de</strong>nen Wasserstoff die anti-<br />
Konformation einnimmt (anti-Eliminierung - Ingold-Regel).<br />
89
X C<br />
C<br />
Während sich bei aliphatischen Verbindungen diese anti-Lage leicht einzustellen<br />
vermag (freie Drehbarkeit), ist dies bei höher substituierten alicyclischen Verbindungen<br />
nicht mehr <strong>de</strong>r Fall. Betrachten wir beispielsweise ein Cyclohexan<strong>de</strong>rivat mit einer<br />
raumerfüllen<strong>de</strong>n Gruppe einmal trans-ständig (a) und einmal cis-ständig (b) zu einem<br />
am benachbarten C-Atom gebun<strong>de</strong>nen Halogenatom (X), so sind folgen<strong>de</strong><br />
Reaktionsabläufe möglich.<br />
a) R und X trans-ständig<br />
R<br />
X<br />
R e<br />
H X<br />
3 5<br />
1<br />
e<br />
Im energetischen Grundzustand nimmt die raumerfüllen<strong>de</strong> Gruppe die äquatoriale Lage<br />
ein. Da X trans-ständig zu R angeordnet ist, befin<strong>de</strong>t sich auch X in dieser Lage (e,e).<br />
Eine anti-Eliminierung ist jedoch nur aus <strong>de</strong>r diaxialen trans-Stellung (a,a) möglich.<br />
Diese Konformation kann durch "Umklappen" <strong>de</strong>r Sesselform (über die Wannenform)<br />
eingenommen wer<strong>de</strong>n. Wie man sieht, gibt es neben <strong>de</strong>m <strong>de</strong>n Substituenten X<br />
tragen<strong>de</strong>n Kohlenstoff nur ein β-C-Atom, das ein zu X trans-ständiges H-Atom besitzt,<br />
so dass die Eliminierung nur in einer Richtung unter Bildung eines einheitlichen<br />
Endproduktes abläuft:<br />
H<br />
H<br />
H<br />
H<br />
R a<br />
1<br />
X<br />
a<br />
3<br />
H<br />
H<br />
5<br />
90
H<br />
H<br />
R a<br />
X<br />
a<br />
H<br />
a<br />
w<br />
OH<br />
H<br />
- X �<br />
- H 2O<br />
b) Betrachten wir nun die Verbindung, in <strong>de</strong>r X und R zueinan<strong>de</strong>r cis-ständig sind, so<br />
befin<strong>de</strong>n sich bereits im Grundzustand (<strong>de</strong>r raumerfüllen<strong>de</strong> Substituent in äquatorialer<br />
Lage) zwei transaxiale H-Atome in Nachbarschaft zum Substituenten X und es wird bei<br />
<strong>de</strong>r E2-Eliminierung <strong>de</strong>mzufolge ein Olefingemisch gebil<strong>de</strong>t:<br />
R<br />
R<br />
o<strong>de</strong>r<br />
X<br />
X<br />
R<br />
R<br />
H<br />
H<br />
a<br />
H<br />
a<br />
H<br />
X<br />
X<br />
a<br />
a<br />
a<br />
H<br />
w<br />
OH<br />
a<br />
H<br />
w<br />
OH<br />
H<br />
H<br />
R<br />
R<br />
- X �<br />
- H 2O<br />
- X �<br />
- H 2O<br />
Wovon das Produktverhältnis <strong>de</strong>r bei<strong>de</strong>n Verbindungen im allgemeinen abhängig ist,<br />
wird in <strong>de</strong>n folgen<strong>de</strong>n Abschnitten besprochen.<br />
R<br />
R<br />
91
Die überwiegen<strong>de</strong> Eliminierungsrichtung ist bei unsymmetrisch gebauten R-X-<br />
Molekülen durch die Saytzeff- und Hofmann-Regel vorhersagbar. Bei sekundären und<br />
tertiären Alkylhalogeni<strong>de</strong>n und Alkoholen <strong>de</strong>r folgen<strong>de</strong>n Struktur kann z.B. die<br />
Eliminierung in zwei Richtungen laufen:<br />
R CH 2 CH<br />
OH<br />
CH 3<br />
- H 2O<br />
- H 2O<br />
R CH CH<br />
(Saizew-Produkt)<br />
(Saytzeff)<br />
CH 3<br />
R CH 2 CH CH 2<br />
(Hofmann-Produkt)<br />
Das Olefin mit <strong>de</strong>r höchsten Alkylsubstitution bezeichnet man als Saytzeff-Produkt, das<br />
Olefin, das die geringste Anzahl Alkylgruppen an <strong>de</strong>n Doppelbindungskohlenstoffen<br />
trägt, als Hoffmannprodukt. Das Saytzeff-Produkt ist das thermodynamisch stabilere.<br />
Bei monomolekularen Eliminierungen (z.B. <strong>de</strong>r säurekatalysierten Dehydratisierung von<br />
tertiären Alkoholen) entsteht überwiegend das Saytzeff-Produkt, da das im<br />
Übergangszustand vorhan<strong>de</strong>ne Carbeniumion schon weitgehend Olefinstruktur besitzt,<br />
sind für die Bildung <strong>de</strong>s Endproduktes allein energetische Grän<strong>de</strong> maßgebend. Nur<br />
wenn <strong>de</strong>r Angriff <strong>de</strong>r Base auf das Proton am β-C-Atom, <strong>de</strong>ssen Ablösung zum<br />
Saytzeff-Produkt aus sterischen Grün<strong>de</strong>n erschwert wird, bil<strong>de</strong>t sich auch bei <strong>de</strong>r E1-<br />
Eliminierung das Hofmann-Produkt:<br />
92
R<br />
CH 2<br />
H 3 C<br />
R '<br />
C<br />
CH<br />
R ''<br />
CH<br />
CH 3<br />
CH 3<br />
C<br />
OH<br />
CH 3<br />
H �<br />
- H 2 O<br />
R C C<br />
CH 2<br />
H 3 C<br />
R '<br />
CH<br />
R ''<br />
CH 3<br />
R<br />
C<br />
Saizew-Produkt =<br />
Nebenprodukt<br />
CH 2<br />
H 3 C<br />
R '<br />
C<br />
- H 3 O �<br />
CH 3<br />
CH 3<br />
CH<br />
CH 3<br />
R ''<br />
C<br />
H<br />
C<br />
�<br />
O<br />
H H<br />
sterisch<br />
behin<strong>de</strong>rt<br />
R '<br />
CH 3<br />
CH 2<br />
R ''<br />
H<br />
O<br />
H<br />
leicht<br />
CH 3<br />
H<br />
R CH2 C C C CH2 H<br />
H 3 C<br />
CH<br />
CH 3<br />
Hofmann-Produkt =<br />
Hauptprodukt<br />
Bei <strong>de</strong>r bimolekularen Eliminierung ist die Produktbildung abhängig von<br />
1) <strong>de</strong>r austreten<strong>de</strong>n Gruppe X<br />
- H 3 O �<br />
2) <strong>de</strong>n sterischen Verhältnissen, insbeson<strong>de</strong>re <strong>de</strong>r Substitution am α- und β-C-Atom<br />
<strong>de</strong>s Substrates<br />
3) <strong>de</strong>m Lösungsmittel und <strong>de</strong>r Stärke, <strong>de</strong>r auf das H-Atom einwirken<strong>de</strong>n Base<br />
Je leichter <strong>de</strong>r Substituent -X abgelöst wer<strong>de</strong>n kann (-I leichter als -Cl), umso mehr<br />
Saytzeff-Produkt wird gebil<strong>de</strong>t.<br />
Positiv gela<strong>de</strong>ne Gruppen (- �<br />
NR3), - �<br />
SR2) in sogenannten Oniumverbindungen, bil<strong>de</strong>n<br />
überwiegend das Hofmann-Produkt.<br />
Die Eliminierung von tertiären Aminen aus quartären Ammoniumsalzen stellt die<br />
Hofmann-Eliminierung dar. Diese Reaktion hatte große Be<strong>de</strong>utung bei <strong>de</strong>r<br />
Strukturermittlung von Alkaloi<strong>de</strong>n durch chemischen Abbau.<br />
Entschei<strong>de</strong>nd für diese Orientierung bei <strong>de</strong>r Produktbildung sind zwei Grün<strong>de</strong>:<br />
1) die positive Gruppe erhöht durch <strong>de</strong>n Induktionseffekt die Acidität <strong>de</strong>r β-H-Atome<br />
stärker als an<strong>de</strong>re austreten<strong>de</strong> Gruppen<br />
93
2) Durch die räumliche Größe <strong>de</strong>r austreten<strong>de</strong>n Gruppen kann nur <strong>de</strong>r<br />
Übergangszustand mit <strong>de</strong>r geringsten Gruppenhäufung durchlaufen wer<strong>de</strong>n, dies<br />
ist <strong>de</strong>r Übergangszustand, <strong>de</strong>r zum Hofmann-Produkt führt. An einem Beispiel<br />
soll dies veranschaulicht wer<strong>de</strong>n:<br />
R<br />
C<br />
H3C C<br />
CH3 N v<br />
C C<br />
H H<br />
'<br />
R ''<br />
H H<br />
H H<br />
|B<br />
H H<br />
geringere Gruppenhäufung<br />
�<br />
- HB<br />
R ' R '' CH CH 2 N(CH 3) 2 + H 2C CH 2<br />
H 3C<br />
H 3C<br />
H 3C<br />
CH 3<br />
C<br />
CH 3<br />
v<br />
C<br />
H<br />
C<br />
OH<br />
H<br />
C<br />
CH 3<br />
CH 3<br />
CH 3<br />
+ H<br />
- H2O �<br />
- H �<br />
Hofmann-Produkt<br />
H 3C<br />
H 3C<br />
H 3C<br />
CH 3<br />
C<br />
CH 3<br />
C<br />
H<br />
C<br />
v<br />
C<br />
CH 3<br />
CH 3<br />
CH 3<br />
Eine ganz ähnliche Wirkung geht auch von <strong>de</strong>r Base aus. Je stärker raumerfüllend<br />
diese ist, <strong>de</strong>sto mehr Hofmann-Produkt entsteht, da <strong>de</strong>r Angriff auf die durch die<br />
Alkylgruppe bereits abgeschirmten β-H-Atome zusätzlich erschwert ist.<br />
Das Lösungsmittel ist wie bei <strong>de</strong>r Substitution dafür verantwortlich, ob die Reaktion<br />
mono- o<strong>de</strong>r bimolekular abläuft. Um schließlich bei bimolekularem Reaktionsablauf die<br />
Eliminierung gegenüber <strong>de</strong>r Substitution zu begünstigen, müssen möglichst starke<br />
Basen eingesetzt wer<strong>de</strong>n.<br />
94
In <strong>de</strong>r Praxis wird die Bildung einheitlicher Produkte noch zusätzlich durch mögliche<br />
Umlagerungsreaktionen erschwert. Beispielsweise erhält man bei <strong>de</strong>r Elininierung von<br />
Wasser aus Pinakolylalkohol nicht das erwartete Olefin, son<strong>de</strong>rn ein<br />
Umlagerungsprodukt, das im Zuge einer Wagner-Meerwein-Umlagerung entsteht:<br />
H 3C<br />
H 3C<br />
H 3C<br />
CH 3<br />
C<br />
CH 3<br />
v<br />
C<br />
H<br />
C<br />
OH<br />
H<br />
C<br />
CH 3<br />
CH 3<br />
CH 3<br />
+ H<br />
- H2O �<br />
- H �<br />
H 3C<br />
H 3C<br />
H 3C<br />
CH 3<br />
C<br />
CH 3<br />
C<br />
H<br />
C<br />
v<br />
C<br />
CH 3<br />
CH 3<br />
CH 3<br />
Ein weiteres Beispiel stellt die Möglichkeit zur Bildung cis/trans-Isomeren Verbindungen<br />
dar, die bei E1-Reaktion etwa mit gleichen Wahrscheinlichkeiten entstehen, während<br />
bei <strong>de</strong>r sterisch besser kontrollierten E2-Reaktion je nach Art zusätzlicher Substituenten<br />
das eine o<strong>de</strong>r an<strong>de</strong>re überwiegt (Kap. 8.1.2).<br />
Will man daher reine Olefine herstellen, so ist <strong>de</strong>r Einsatz dieser Metho<strong>de</strong> stark<br />
beschränkt, oft strebt man aber die Entfernung <strong>de</strong>r funktionellen Gruppe an, um in<br />
einem zweiten Schritt durch Hydrierung einen gesättigten Kohlenwasserstoff<br />
herzustellen.<br />
Für diese Zwecke können die Gemische <strong>de</strong>r Olefine katalytisch zu einheitlichen<br />
Kohlenwasserstoffen hydriert wer<strong>de</strong>n (dies gilt streng, nur für aliphatische<br />
Verbindungen).<br />
Als Katalysatoren wer<strong>de</strong>n im Labor vorzugsweise Palladiumkohle o<strong>de</strong>r PtO2 verwen<strong>de</strong>t,<br />
das mit Wasserstoff zu Pt mit großer Oberfläche (beson<strong>de</strong>rs gute Aufnahme von H2)<br />
reduzierbar ist.<br />
95
R CH 2 CH<br />
OH<br />
CH 2<br />
R '<br />
R CH2 CH2 R '<br />
CH2 - H 2O<br />
- H 2O<br />
R CH CH<br />
R CH 2 CH<br />
CH 2<br />
CH<br />
R '<br />
R '<br />
+ H 2<br />
Katalysator<br />
Nach Beendigung <strong>de</strong>r Wasserstoffaufnahme wird <strong>de</strong>r Katalysator abfiltriert und die<br />
Lösung eingeengt - <strong>de</strong>r Kohlenwasserstoff fällt meist in sehr reiner Form an.<br />
8.1.3 Thermische syn-Eliminierung:<br />
Neben E1- und E2-Eliminierung von HX aus Alkohol, Alkylhalogenid und <strong>de</strong>r<br />
Zersetzung von Oniumsalzen spielen thermische Zersetzungsreaktionen eine wichtige<br />
Rolle zur Herstellung von Olefinen.<br />
Xanthogensäurealkylester, die aus Schwefelkohlenstoff und Alkohol bei Gegenwart von<br />
Alkalihydroxid und nachfolgen<strong>de</strong>m Umsatz mit R‘X (meistens verwen<strong>de</strong>t man CH3I)<br />
herstellbar sind,<br />
R CH 2 CH 2 OH + S C S NaOH<br />
- H 2O<br />
R CH 2 CH 2<br />
R CH 2 CH 2<br />
S<br />
O C S Na �<br />
�<br />
+ CH3 I<br />
- NaI<br />
O<br />
S<br />
C S<br />
zerfallen beim Erhitzen über einen 6-gliedrigen Übergangszustand in Olefin, Mercaptan<br />
und COS (Tschugaeff-Reaktion):<br />
CH 3<br />
96
H H<br />
R '<br />
R<br />
O<br />
H<br />
C<br />
S<br />
SCH 3<br />
Hitze<br />
H H<br />
R '<br />
C<br />
C<br />
R<br />
+<br />
O C<br />
H<br />
S<br />
SCH 3<br />
O C S<br />
+<br />
CH 3SH<br />
Wegen <strong>de</strong>s bei <strong>de</strong>r Reaktion entstehen<strong>de</strong>n Mercaptans (Geruch) zieht man heute die<br />
bei mil<strong>de</strong>ren Temperaturen verlaufen<strong>de</strong> Cope-Eliminierung von Aminoxi<strong>de</strong>n vor:<br />
R CH 2 CH 2 NR '<br />
2<br />
H 2O 2<br />
H<br />
H<br />
R R<br />
H<br />
H H<br />
N C<br />
+<br />
H<br />
O C<br />
�<br />
R'<br />
R '<br />
�<br />
H<br />
R CH2CH2 N R'<br />
�<br />
R '<br />
2NOH<br />
Die thermische Zersetzung <strong>de</strong>r Ester, die ebenfalls eine cis-Eliminierung darstellt ,<br />
erfor<strong>de</strong>rt sehr hohe Temperaturen und wird daher nicht viel verwen<strong>de</strong>t:<br />
H H<br />
H<br />
R<br />
O<br />
H<br />
C<br />
O<br />
R<br />
Hitze<br />
H H<br />
R<br />
O C<br />
Von beson<strong>de</strong>rer Be<strong>de</strong>utung zur Herstellung von Olefinen ist heute die Wittig-Reaktion.<br />
Hierbei setzt man einen Al<strong>de</strong>hyd mit einem Phosphorylid um:<br />
H<br />
C<br />
C<br />
+<br />
H<br />
O<br />
R<br />
�<br />
O<br />
R '<br />
97
R C<br />
O<br />
H<br />
O<br />
+ H 2C PPh 3 R CH<br />
CH 2<br />
R CH + O<br />
PPh 3<br />
PPh 3<br />
CH 2<br />
ein Oxaphosphetan<br />
Das Zwischenprodukt zerfällt zu Triphenylphosphinoxid und einem Olefin, so dass im<br />
En<strong>de</strong>ffekt die Carbonylgruppe durch eine Methylengruppe ersetzt wird.<br />
Die Phosphoryli<strong>de</strong> (Phosphorane) sind durch Umsatz von Triphenylphosphin mit CH3I<br />
leicht zugänglich:<br />
Ph3P| + CH3 I Ph3P CH3 � �<br />
Ph3P CH2 Phosphor-Ylid<br />
8.1.4. Nachweis von Olefinen:<br />
�<br />
I<br />
Ph 3P CH 2<br />
Ylen<br />
�<br />
Li �<br />
Ph �<br />
o<strong>de</strong>r NaH<br />
Zum Nachweis von Olefinen macht man sich ihre große Neigung zu<br />
Anlagerungsreaktionen zunutze:<br />
KMnO4 wird sofort entfärbt:<br />
�<br />
C MnO4 C<br />
O<br />
O<br />
�<br />
MnO 2<br />
H 2O<br />
(OH �<br />
Allerdings ist diese Reaktion nicht spezifisch für Olefine, da alle leicht oxidierbaren<br />
Substanzen (Alkohole, Al<strong>de</strong>hy<strong>de</strong>, Amine, Thiole, Enole usw.) einen positiven Test<br />
ergeben.<br />
OH<br />
OH<br />
98
In gleicher Weise kann die Reaktion mit molekularem Brom - erkenntlich ebenfalls an<br />
<strong>de</strong>r Entfärbung <strong>de</strong>s zugesetzten Broms - als Nachweisreaktion dienen. Brom wird<br />
elektrophil an <strong>de</strong>r Doppelbindung addiert.<br />
Br<br />
C C + Br 2 C C<br />
Es ist zu beachten, das Brom C-H-aci<strong>de</strong> Verbindungen (z.B. Ketone) auch substituieren<br />
kann:<br />
O<br />
+ Br 2<br />
in CCl 4 O<br />
Br<br />
Br<br />
+ HBr<br />
Diese Reaktion führt ebenfalls zur Entfärbung <strong>de</strong>s Broms. Arbeitet man in CCl4 statt in<br />
CHCl3, in <strong>de</strong>m das entstan<strong>de</strong>ne HBr nicht löslich ist und daher am Entweichen aus <strong>de</strong>r<br />
Lösung erkenntlich ist (Indikatorpapier), so kann man entschei<strong>de</strong>n, ob ein Olefin o<strong>de</strong>r<br />
eine substituierbare Verbindung vorliegt.<br />
Mit Olefinen, die elektronenziehen<strong>de</strong> Gruppen an <strong>de</strong>r Doppelbindung tragen, reagiert<br />
Brom nur langsam. Hier ist die Prüfung mit KMnO4 angebracht.<br />
8.2 Herstellung gesättigter Kohlenwasserstoffe:<br />
Neben <strong>de</strong>r Hydrierung von Olefinen bzw. Olefingemischen sind gesättigte<br />
Kohlenwasserstoffe aus Carbonylverbindungen zugänglich:<br />
8.2.1 Clemmensen-Reduktion:<br />
Im allgemeinen führt die Reduktion von Al<strong>de</strong>hy<strong>de</strong>n und Ketonen zur Bildung von<br />
Alkoholen, die nicht mehr weiter reduzierbar sind. Clemmensen stellte fest, dass die<br />
Reduktion bis zum Kohlenwasserstoff unter Überspringen <strong>de</strong>r Zwischenstufe <strong>de</strong>s<br />
99
Alkohols verläuft, wenn man als Reduktionsmittel amalgamiertes Zink (Zn/Hg) in<br />
salzsaurer Lösung einsetzt:<br />
R<br />
R<br />
C<br />
O +<br />
8.2.2 Wolff-Kishner-Reduktion:<br />
2 Zn + 4 [H �<br />
@ CH2 + 2 Zn 2�<br />
R<br />
R<br />
+ �2<br />
Ergänzt wird dieses Verfahren durch die Metho<strong>de</strong> von Wolff-Kishner in <strong>de</strong>r Variante von<br />
Huang-Minlon. Ein Keton, das in einem hochsie<strong>de</strong>n<strong>de</strong>n Lösungsmittel (Ethylenglycol)<br />
gelöst ist, reagiert in Gegenwart von KOH und Hydrazin nach Bildung <strong>de</strong>s Hydrazons<br />
unter N2-Abspaltung:<br />
R<br />
R<br />
R<br />
R<br />
C<br />
C<br />
R<br />
R<br />
O<br />
O<br />
+ H 2N NH 2<br />
CH<br />
H<br />
O<br />
H<br />
H2N NH2 KOH<br />
- H2O 140°C<br />
N N H<br />
R<br />
R<br />
OH<br />
�<br />
C<br />
KOH<br />
- H 2O<br />
- H 2O<br />
N<br />
- N 2<br />
- OH �<br />
NH 2<br />
R<br />
R<br />
R<br />
R<br />
C<br />
KOH<br />
- N2 200°C<br />
CH 2<br />
N<br />
R<br />
R<br />
NH 2<br />
CH 2<br />
Ein dritter Weg zur Herstellung von Kohlenwasserstoffen aus Carbonylverbindungen<br />
besteht im Umsatz <strong>de</strong>r Carbonylverbindung zu einem Dithioacetal (meist<br />
Ethylendithioacetal), das an schließend mit Raney-Nickel entschwefelt wird:<br />
100
R<br />
R<br />
R<br />
R<br />
C<br />
CH2 SH<br />
S<br />
CH2 SH R<br />
O C<br />
- H2O R<br />
S<br />
CH 2<br />
+<br />
CH 2<br />
CH 2<br />
SH<br />
SH<br />
CH 2<br />
CH 2<br />
(Ni)<br />
+ H2 Raney-Nickel erhält man aus einer Aluminium-Nickel-Legierung durch Herauslösen <strong>de</strong>s<br />
Aluminiums mit Alkali.<br />
Vorsicht: Raney-Nickel ist pyrophor, d.h. an <strong>de</strong>r Luft selbstentzündlich,<br />
Filterpapiere mit Raney-Nickel dürfen daher keinesfalls achtlos weggeworfen<br />
wer<strong>de</strong>n, son<strong>de</strong>rn müssen unmittelbar nach Abfiltrieren durch gezieltes<br />
Abbrennen mit <strong>de</strong>m Bunsenbrunner unschädlich gemacht wer<strong>de</strong>n.<br />
Symmetrische gesättigte Kohlenwasserstoffe sind ferner nach Wurtz aus<br />
Alkylhalogeni<strong>de</strong>n durch Behandlung mit Na zugänglich:<br />
H3C (CH2 ) n CH2 I + 2 Na H3C (CH2 ) n CH2 Na + Na I<br />
H 3 C (CH 2 ) n CH 2 Na<br />
+<br />
H 3 C (CH 2 ) n CH 2<br />
I<br />
H 3C (CH 2) n CH 2<br />
H 3 C (CH 2 ) n CH 2<br />
+ NaI<br />
Corey und House entwickelten unabhängig voneinan<strong>de</strong>r eine sehr vielseitige<br />
Kohlenwasserstoffsynthese, die die Herstellung längerkettiger (auch verzweigter und<br />
unsymmetrischer) Alkane erlaubt. Sie setzen das Alkylhalogenid mit Lithium zur<br />
Alkyllithiumverbindung um. Mit Kupfer-(I)-iodid entsteht die Lithium-dialkylkupferverbindung,<br />
die schließlich mit weiterem Alkylhalogenid <strong>de</strong>n Kohlenwasserstoff<br />
ergibt.<br />
101
CH 3<br />
2 R CH 2 CH<br />
CH 3<br />
R CH 2 CH<br />
Cl<br />
2 Li<br />
- LiCl<br />
CH 3<br />
2 R CH2CHLi CH 3<br />
2 CuLi R' CH2 Br<br />
R CH2CH - LiBr<br />
+<br />
CH 3<br />
R CH2CHCu Cu I<br />
- LiI<br />
CH 2<br />
Auch durch Zersetzung von Grignard-Verbindungen mit Wasser erhält man<br />
Kohlenwasserstoffe:<br />
R Mg X + H 2 O R H + Mg(OH)X<br />
Aus diesem Grun<strong>de</strong> ist bei Grignard-Reaktionen die Gegenwart von Wasser o<strong>de</strong>r<br />
an<strong>de</strong>ren Verbindungen mit aci<strong>de</strong>n Wasserstoffen (Phenolen, Säuren, Alkoholen,<br />
Aminen) peinlichst auszuschließen!!<br />
Praktikumsversuch 5: Oxidation o<strong>de</strong>r Reduktion nach einem <strong>de</strong>r erwähnten o<strong>de</strong>r<br />
analogen Verfahren.<br />
9. Herstellung von Aminen:<br />
Bei <strong>de</strong>r Einwirkung von NH3 auf Alkylhalogeni<strong>de</strong> entstehen Gemisch primärer,<br />
sekundärer und tertiärer Amine sowie das quartäre Ammoniumsalz. Die Trennung<br />
dieser Verbindungen nach Hinsberg ist relativ zeitaufwendig. Es ist daher eleganter<br />
und zweckmäßiger, die Herstellung reiner Verbindungen anzustreben:<br />
9.1 Herstellung primärer Amine:<br />
Reine Primäre Amine sind über die Gabrielsynthese zugänglich:<br />
R '<br />
102
O<br />
C<br />
C<br />
O<br />
N �<br />
K �<br />
+ RCl<br />
O<br />
C<br />
C<br />
O<br />
N<br />
R + KCl<br />
Die so erhältlichen N-alkylsubstituierten Phthalimi<strong>de</strong> sind durch Hydrazinolyse in<br />
primäres Amin und Phthalsäurehydrazid spaltbar:<br />
O<br />
C<br />
C<br />
O<br />
N<br />
R H 2 N NH 2<br />
Vorsicht: Hydrazin ist ein starkes Nervengift und cancerogen.<br />
O<br />
O<br />
NH<br />
NH<br />
+ R NH 2<br />
Primäre Amine sind auch durch Reduktion <strong>de</strong>r Oxime von Al<strong>de</strong>hy<strong>de</strong>n o<strong>de</strong>r Ketonen<br />
zugänglich:<br />
R<br />
R<br />
C<br />
O<br />
H 2N<br />
- H 2O<br />
OH<br />
R<br />
R<br />
C<br />
N<br />
OH<br />
H 2/Ni<br />
EtOH<br />
R<br />
R<br />
CH NH 2<br />
Die theoretisch mögliche Reduktion von aliphatischen Nitroverbindungen zu Aminen hat<br />
in <strong>de</strong>r Praxis kaum Be<strong>de</strong>utung, da diese im allgemeinen schwerer zugänglich sind als<br />
die Amine.<br />
Dagegen spielt die Reduktion <strong>de</strong>r Nitrile zu primären Aminen eine große Rolle,<br />
insbeson<strong>de</strong>re in <strong>de</strong>r Technik. (Herstellung von Nylon, Reduktion von Adipinsäuredinitril).<br />
103
Als Zwischenprodukte entstehen zunächst Aldimine, die entwe<strong>de</strong>r zum primären Amin<br />
weiter hydriert wer<strong>de</strong>n o<strong>de</strong>r aber mit bereits gebil<strong>de</strong>tem primären Amin unter<br />
Ammoniakabspaltung zu Azomethinen weiter reagieren, die bei <strong>de</strong>r Hydrierung<br />
sekundärer Amine ergeben.<br />
R CH 2 C N<br />
H 2<br />
Ni<br />
δ+ δ-<br />
R CH2CH NH<br />
+<br />
R CH 2 CH 2 NH 2<br />
R CH 2<br />
- NH 3<br />
H 2<br />
CH NH R CH2 CH2 NH2 Ni<br />
R CH 2 CH N CH 2 CH 2 R<br />
H 2/Ni<br />
R CH2CH2 NH CH2 CH2 R<br />
Um die Bildung <strong>de</strong>s als Nebenprodukt entstehen<strong>de</strong>n sekundären Amins zu<br />
unterdrücken, fügt man <strong>de</strong>r Reaktionslösung einen grossen Überschuß Ammoniak zu<br />
(Gleichgewichtsverschiebung).<br />
Weitere wichtige Metho<strong>de</strong>n zur Herstellung von Aminen gehen von Säuren aus:<br />
Hofmann-Abbau:<br />
Beim Hofmann-Abbau stellt man über das Säurechlorid das Säureamid her, das mit Br2<br />
in alkalischer Lösung umgesetzt wird.<br />
Dabei bil<strong>de</strong>t sich Hypobromit, das das Säureamid am Stickstoff bromiert:<br />
R<br />
C<br />
O<br />
NH 2<br />
+ HOBr<br />
- H 2O<br />
R<br />
C<br />
O<br />
N H<br />
Br<br />
104
Die N-Bromverbindung spaltet formal HBr ab und lagert sich sofort unter<br />
Restwan<strong>de</strong>rung zum Isocyanat um:<br />
R<br />
C<br />
O<br />
N H<br />
�<br />
OH<br />
Br<br />
- H 2O<br />
R<br />
C<br />
�<br />
O<br />
N Br<br />
- Br �<br />
R N<br />
C O<br />
Die in manchen Lehrbüchern erwähnte Nitrenzwischenstufe mit einem<br />
Elektronensextett am Stickstoff konnte noch niemals nachgewiesen wer<strong>de</strong>n:<br />
Es entsteht so ein Isocyanat, das in <strong>de</strong>r wässrigen Lösung H2O addiert:<br />
R<br />
+ H2O R N C O<br />
R NH C<br />
Die entstehen<strong>de</strong> Carbaminsäure zerfällt in primäres Amin und CO2:<br />
Curtius-Abbau:<br />
R<br />
NH<br />
C<br />
O<br />
OH<br />
C<br />
O<br />
N<br />
- CO 2<br />
R NH 2<br />
Sehr ähnlich ist <strong>de</strong>r Curtius-Abbau, bei <strong>de</strong>m man von Säureazi<strong>de</strong>n ausgeht, die wie<strong>de</strong>r<br />
über Säurechlori<strong>de</strong> durch Umsatz mit NaN3 erhältlich sind. Die Säureazi<strong>de</strong> zerfallen<br />
beim Erhitzen unter Stickstoffabspaltung zu <strong>de</strong>m gleichen Addukt, das man beim<br />
Hofmann-Abbau erhält:<br />
O<br />
OH<br />
105
R C<br />
O<br />
Cl<br />
NaN3 R C<br />
�<br />
O<br />
N<br />
N N<br />
�<br />
- N 2<br />
R N<br />
C O<br />
Wenn z.B. in wasserfreiem Benzol als Lösungsmittel gearbeitet wird, kann man die<br />
Isocyanate isolieren. Bei Gegenwart von kleinen Mengen Wasser entsteht aus <strong>de</strong>m<br />
Isocyanat über das Carbaminsäure<strong>de</strong>rivat wie beim Hofmann-Abbau primäres Amin,<br />
das sich mit noch unumgesetzten Isocyanaten zum Harnstoff<strong>de</strong>rivat umsetzt<br />
(Nebenreaktion):<br />
R NH2 + R N C O R NH C<br />
O<br />
NH R<br />
Zur Herstellung primärer Amine zersetzt man daher das Säureazid in alkoholischer<br />
Lösung. Hier bil<strong>de</strong>t sich aus <strong>de</strong>m zunächst entstehen<strong>de</strong>n Isocyanat ein Urethan<strong>de</strong>rivat,<br />
das bei <strong>de</strong>r sauren Hydrolyse zum primären Amin, Alkohol und CO2 zerfällt:<br />
O - N2 R C<br />
R N C O<br />
R NH<br />
Schmidt-Abbau:<br />
N 3<br />
C<br />
ein Urethan<br />
O<br />
OC 2H 5<br />
+ C 2H 5OH<br />
R NH 2 + C 2H 5OH + CO 2<br />
Beim Schmidt-Abbau setzt man die Säure mit HN3 (Stickstoffwasserstoffsäure) –<br />
VORSICHT, EXPLOSIV - in Gegenwart von Schwefelsäure um:<br />
106
R<br />
R<br />
C<br />
C<br />
O<br />
OH<br />
OH OH<br />
+ H �<br />
N<br />
H<br />
N<br />
�<br />
N<br />
R<br />
- H 3O �<br />
C<br />
R<br />
�<br />
O<br />
OH<br />
H<br />
C<br />
O<br />
+ HN 3<br />
� N N N<br />
�<br />
Unter Stickstoffverlust entsteht das gleiche Zwischenprodukt wie bei <strong>de</strong>n übrigen<br />
Abbaureaktionen, das schließlich das primäre Amin liefert.<br />
9.2 Herstellung sekundärer Amine:<br />
Sekundäre Amine sind erhältlich durch katalytische Reduktion von Iminen, die ihrerseits<br />
aus Al<strong>de</strong>hyd und primären Amin zugänglich sind:<br />
R NH 2 + O C<br />
H<br />
R '<br />
R R '<br />
NH CH2 R N C<br />
Ein weiterer Weg besteht in <strong>de</strong>r Acylierung eines primären Amins, das dann durch<br />
LiAlH4-Reduktion in das entsprechen<strong>de</strong> sekundäre Amin überführbar ist:<br />
R NH2 + O C R '<br />
Cl<br />
R R '<br />
NH CH2 9.3 Herstellung tertiärer Amine:<br />
- HCl<br />
O<br />
H<br />
R '<br />
R R '<br />
NH C<br />
H 2<br />
LiAlH 4<br />
Tertiäre Amine mit verschie<strong>de</strong>nen Alkylsubstituenten sind erhältlich durch Acylierung<br />
entsprechen<strong>de</strong>r sekundärer Amine und nachfolgen<strong>de</strong>r LiAlH4-Reduktion:<br />
107
R R '<br />
NH<br />
R<br />
R '<br />
N<br />
+ O C<br />
Cl<br />
CH 2<br />
Leuckart-Wallach-Reaktion:<br />
R NH 2<br />
R ''<br />
R ''<br />
9.4. Nachweisreaktionen von Aminen:<br />
9.4.1 Isonitril-Reaktion:<br />
- HCl<br />
HCHO / HCOOH<br />
- CO 2 - H 2O<br />
R<br />
R '<br />
N<br />
O<br />
C<br />
R ''<br />
R N CH 3<br />
CH 3<br />
LiAlH 4<br />
Eine empfindliche Nachweisreaktion für primäre Amine ist die Isonitril-Reaktion. Bei<br />
<strong>de</strong>r Umsetzung mit Chloroform und Alkalilauge entstehen die wi<strong>de</strong>rlich riechen<strong>de</strong>n<br />
giftigen Isonitrile:<br />
- 3 NaCl<br />
� �<br />
R NH2+ CHCl3 + 3 NaOH R N C<br />
- 3 H2O Bei <strong>de</strong>r Isonitrilreaktion entsteht aus CHCl3 zunächst im Zuge einer α-Eliminierung<br />
Dichlorcarben:<br />
Cl<br />
Cl C H<br />
Cl<br />
OH �<br />
- HCl<br />
Cl<br />
Cl<br />
C x<br />
108
(Als Carben bezeichnet man eine Methylengruppe mit zwei Elektronen :CH2. Carbene<br />
sind außeror<strong>de</strong>ntlich reaktive Verbindungen).<br />
Mit primären Aminen reagiert das Dichlorcarben zum entsprechen<strong>de</strong>n Isonitril:<br />
H<br />
Cl<br />
R NH x<br />
2 +<br />
xC<br />
R N<br />
Cl<br />
� �<br />
R N C<br />
H<br />
C Cl<br />
Cl<br />
- 2 HCl<br />
9.4.2. Umsetzungen mit salpetriger Säure, Reaktionen zur Unterscheidung<br />
primärer, sekundärer und tertiärer Amine:<br />
Primäre aliphatische Amine wer<strong>de</strong>n in saurer Lösung von NO �<br />
, (entsteht aus NaNO2<br />
und Säure) am Stickstoffatom (Ort größter Elektronendichte) angegriffen:<br />
R N<br />
H<br />
H<br />
+ NO �<br />
R N N �<br />
OH 2<br />
R<br />
�<br />
N<br />
N<br />
H<br />
H<br />
Durch Deprotonierung-Protonierung entsteht ein protoniertes Diazoniumhydroxid,<br />
woraus nach Wasserabspaltung ein Diazoniumsalz entsteht:<br />
R N N �<br />
OH 2<br />
R N<br />
�<br />
N<br />
- H 2O<br />
�<br />
R N N<br />
Das Diazoniumsalz ist unbeständig, solange nicht eine Stabilisierungsmöglichkeit durch<br />
Mesomerie mit Elektronen <strong>de</strong>s Restes R gegeben ist und spaltet N2 ab:<br />
O<br />
109
Der Rest R �<br />
� - N2 �<br />
R N N<br />
R<br />
+ H 2O<br />
- H � R OH<br />
reagiert mit einem vorhan<strong>de</strong>nem Nukleophil (z.B. Lösungsmittel) o<strong>de</strong>r<br />
spaltet im Zuge einer Eliminierung H �<br />
ab.<br />
Sekundäre Amine wer<strong>de</strong>n in gleicher Weise wie primäre Amine von NO �<br />
am Stickstoff<br />
angegriffen. In diesem Falle resultiert aber eine N-Nitrosoverbindung:<br />
R NH R<br />
NO �<br />
R<br />
R N N O<br />
H<br />
�<br />
- H �<br />
Nitrosamine sind gelbe bis orangefarbene, in Wasser wenig lösliche Öle.<br />
R<br />
R<br />
N N O<br />
VORSICHT: Nitrosamine sind krebserregend. - Beim Arbeiten mit diesen Substanzen<br />
äußerste Vorsicht walten lassen: Abzug, Schutzhandschuhe!ll<br />
R<br />
N<br />
Tertiäre Amine reagieren ebenso zu Nitrosaminen<br />
R<br />
R<br />
NO �<br />
X �<br />
R<br />
�<br />
R N N O<br />
R X�<br />
O<br />
H H<br />
- ROH<br />
- HX<br />
R<br />
R<br />
N N O<br />
9.4.2. Trennung von primären, sekundären und tertiären Aminen (Hinsberg-Trennung):<br />
Mit Benzolsulfochlorid bzw. p-Toluolsulfochlorid reagieren primäre und sekundäre<br />
Amine in <strong>de</strong>r folgen<strong>de</strong>n Weise:<br />
110
O<br />
S<br />
O<br />
O<br />
S<br />
O<br />
Cl<br />
Cl<br />
Tertiäre Amine reagieren nicht.<br />
O<br />
+ H2N R<br />
- HCl<br />
S<br />
+ H<br />
R<br />
N R<br />
- HCl<br />
H<br />
N<br />
O<br />
löslich in Alkali<br />
R<br />
O<br />
S N<br />
R<br />
O<br />
R<br />
unlöslich in Alkali<br />
Einige primäre Amine reagieren zum Teil zu Disulfonyl<strong>de</strong>rivaten, die ebenfalls in<br />
alkalischer Lösung unlöslich sind (Verwechselungsmöglichkeit mit sekundären<br />
Aminen). Durch Kochen mit Natriumethylat kann die Disulfonylverbindung zerstört<br />
wer<strong>de</strong>n:<br />
O<br />
O<br />
2 S Cl + 2H2N<br />
R<br />
- 2 HCl<br />
S<br />
O<br />
O<br />
S<br />
O<br />
O<br />
R<br />
N<br />
O<br />
S<br />
O<br />
N R EtO S<br />
� �<br />
Na ���<br />
Praktikumsversuch 6: Herstellung eines aliphatischen Amins nach einer <strong>de</strong>r<br />
erwähnten o<strong>de</strong>r analogenVerfahren<br />
10. Herstellung einfacher aromatischer Verbindungen<br />
10.1. Die elektrophile Substitution:<br />
�<br />
Na �<br />
O<br />
O<br />
111
Im Gegensatz zu substituierten aliphatischen Verbindungen, die vielfach über<br />
nucleophile Reaktionen zugänglich sind, spielen solche Reaktionen in <strong>de</strong>r Chemie <strong>de</strong>r<br />
Aromaten nur eine geringe Rolle: Das aromatische Ringsystem ist relativ reich an<br />
Elektronen und daher eher von positiv gela<strong>de</strong>nen Partikelchen im Zuge elektrophiler<br />
Substitutionsreaktionen angreifbar.<br />
In <strong>de</strong>r Regel bil<strong>de</strong>t sich zunächst mit <strong>de</strong>m angreifen<strong>de</strong>n positiv gela<strong>de</strong>nen Agens ein loser<br />
Komplex - <strong>de</strong>r π-Komplex - unter Beteiligung negativer Ladungsteile <strong>de</strong>s aromatischen<br />
Ringsystems. Dieser entwickelt sich zu einem σ-Komplex, in <strong>de</strong>m bereits eine σ-<br />
Bindung zwischen einem Kohlenstoffatom <strong>de</strong>s Aromaten und <strong>de</strong>m elektrophilen<br />
Reagens ausgebil<strong>de</strong>t ist. Obwohl noch 5 Kohlenstoffatome an <strong>de</strong>m Mesomeriesystem<br />
im σ-Komplex beteiligt sind, ist durch die Aufhebung <strong>de</strong>s aromatischen Zustan<strong>de</strong>s<br />
hoher Energieaufwand nötig.<br />
+ X � X �<br />
π -Komplex<br />
�<br />
H<br />
X<br />
σ -Komplex<br />
Bis hierher gleicht die Reaktion völlig <strong>de</strong>r Additionsreaktion an Doppelbindungen. Der<br />
aus <strong>de</strong>m Aromaten gebil<strong>de</strong>te σ-Komplex hat aber das Bestreben, wie<strong>de</strong>r <strong>de</strong>n<br />
energetisch günstigen Zustand <strong>de</strong>s Aromaten zu erreichen. Dies ist nur möglich, wenn<br />
das Wasserstoffatom von <strong>de</strong>m sp 3 -hybridisierten Kohlenstoffatom - <strong>de</strong>r<br />
Unterbrechungsstelle <strong>de</strong>s mesomeren Systems - als Proton eliminiert wird.<br />
Auf diese Weise lassen sich aus Aromaten durch Nitrierung Nitroverbindungen,<br />
durch Alkylierung o<strong>de</strong>r Acylierung im Zuge von Frie<strong>de</strong>l-Crafts-Reaktionen<br />
Kohlenwasserstoffe bzw. aromatische Ketone, durch Halogenierung Bromi<strong>de</strong> und<br />
Iodi<strong>de</strong> und durch Sulfonierung Sulfonsäuren gewinnen. Alle diese Verbindungen<br />
sind wie<strong>de</strong>rum wertvolle Ausgangsstoffe zur Überführung in an<strong>de</strong>re Derivate bzw.<br />
zur Einführung weiterer Substituenten.<br />
112
Die Alkylhalogeni<strong>de</strong> spielen in <strong>de</strong>r Chemie <strong>de</strong>r Aromaten als Zwischenprodukte zur<br />
Synthese weiterer Derivate eine wesentlich geringere Rolle als die Alkylhalogeni<strong>de</strong> in<br />
<strong>de</strong>r Chemie <strong>de</strong>r Aliphaten, weil eine direkte nucleophile Substitution am Aromaten sehr<br />
erschwert ist:<br />
Das Halogenatom ist an <strong>de</strong>r Mesomerie beteiligt, wodurch die C-Halogenbindung<br />
partiellen Doppelbindungscharakter erhält und damit fester als in aliphatischen<br />
Verbindungen gebun<strong>de</strong>n ist (verhin<strong>de</strong>rt SN1-Reaktion).<br />
Cl Cl<br />
Außer<strong>de</strong>m ist an <strong>de</strong>m Kohlenstoffatom, das das Halogen trägt, die negative<br />
Ladungsdichte im Vergleich zu analogen Kohlenstoffatomen aliphatischer<br />
Verbindungen viel höher. Damit ist <strong>de</strong>r Angriff eines Nucleophils auch im Zuge<br />
einer SN2-Reaktion erschwert.<br />
Die Rolle <strong>de</strong>r Alkylhalogeni<strong>de</strong> in <strong>de</strong>r Aliphatenchemie kommt in <strong>de</strong>r Chemie <strong>de</strong>r<br />
Aromaten <strong>de</strong>n Aminen zu, die über Sandmeyer-Reaktionen in eine große Zahl<br />
von Verbindungen mit an<strong>de</strong>ren Substituenten überführbar sind. Sie sind erhältlich<br />
durch Reduktion von Nitroverbindungen.<br />
Enthält eine aromatische Verbindung bereits einen Substituenten, so übt dieser<br />
entschei<strong>de</strong>n<strong>de</strong>n Einfluß darauf aus, welche Position <strong>de</strong>r neu einzutreten<strong>de</strong> Substituent<br />
angreift:<br />
Substituenten, die durch einen induktiven o<strong>de</strong>r mesomeren Effekt elektronendrückend<br />
wirken, erhöhen die negative Ladungsdichte in 2- und 4-Stellung (Substituenten 1.<br />
Ordnung). Insgesamt wird dadurch die elektrophile Substitution erleichtert und in diese<br />
Stellungen gelenkt:<br />
�<br />
�<br />
113
CH 3<br />
O<br />
�<br />
CH 3<br />
O<br />
Anisol<br />
Substituent 1. Ordnung<br />
�<br />
�<br />
CH 3<br />
Elektronenziehen<strong>de</strong> Substituenten vermin<strong>de</strong>rn die Elektronendichte im Kern und damit<br />
die Neigung zur weiteren Substitution (Substituenten 2. Ordnung). Relativ am größten<br />
ist die Elektronendichte noch in 3-Stellung und daher erfolgt, wenn überhaupt, ein<br />
Angriff in dieser Position:<br />
H 3C<br />
C<br />
O<br />
H 3C<br />
�<br />
C<br />
O<br />
�<br />
H 3C<br />
Acetophenon<br />
Substituent 2. Ordnung<br />
Entfaltet ein Substituent gleichzeitig induktive und mesomere Effekte, so ist für<br />
die Orientierung <strong>de</strong>s Zweitsubstituenten immer <strong>de</strong>r mesomere Effekt<br />
verantwortlich:<br />
Zum Beispiel wirkt im Anisol (Ph-O-CH3) und Anilin (Ph-NH2) <strong>de</strong>r induktive Effekt in<br />
Richtung <strong>de</strong>s Substituenten, da Sauerstoff und auch Stickstoff elektronegativer als<br />
Kohlenstoff sind. Wür<strong>de</strong> man diesen induktiven Effekt allein betrachten, so wür<strong>de</strong> sich<br />
eine Vermin<strong>de</strong>rung <strong>de</strong>r Elektronendichte im aromatischen Kern ergeben.<br />
C<br />
O<br />
�<br />
�<br />
O<br />
�<br />
114
Da sowohl Sauerstoff als auch Stickstoff über freie Elektronenpaare verfügen,<br />
üben sie gleichzeitig einen mesomeren Effekt aus, <strong>de</strong>r in die an<strong>de</strong>re Richtung<br />
wirkt.<br />
NH 2<br />
-I-Effekt<br />
(σ -Acceptor-Effekt)<br />
NH 2<br />
�<br />
+M-Effekt<br />
( π -Donor-Effekt)<br />
NH 2<br />
Dipolmoment<br />
�<br />
NH 2<br />
Aus <strong>de</strong>r experimentellen Ermittlung <strong>de</strong>r Größe und <strong>de</strong>r Richtung <strong>de</strong>s<br />
Dipolmomentes weiß man, dass <strong>de</strong>r resultieren<strong>de</strong> Gesamteffekt von –OCH3 und –<br />
NH2 eine Erhöhung <strong>de</strong>r Elektronendichte im aromatischen Kern bewirkt, diese<br />
Substituenten also elektronendrückend wirken.<br />
Dies hat weiterhin zur Folge, dass die Zweitsubstituenten in 2- und 4-Stellung<br />
eintreten. Da Sauerstoff und Stickstoff relativ leicht ihr Elektronenpaar zur<br />
Verfügung stellen, überwiegt hier <strong>de</strong>r mesomere Effekt gegenüber <strong>de</strong>m<br />
induktiven Effekt.<br />
An<strong>de</strong>rs sind die Verhältnisse beim Chlorbenzol. Chlor ist elektronegativer als<br />
Sauerstoff und Stickstoff und übt einen starken -I-Effekt aus. Chlor hat ebenfalls<br />
ein freies Elektronenpaar, ist aber im Gegensatz zu Sauerstoff und Stickstoff weit<br />
weniger bereit, dieses zur Verfügung zu stellen.<br />
115
Das Dipolmoment ist im Chlorbenzol daher an<strong>de</strong>rs als im Anisol o<strong>de</strong>r Anilin zum<br />
Chlor hin gerichtet. Chlorbenzol vermin<strong>de</strong>rt also die Elektronendichte im<br />
aromatischen Kern und erschwert damit die Zweitsubstitution.<br />
Cl<br />
Dipolmoment<br />
Wie ist es nun mit <strong>de</strong>r Orientierung <strong>de</strong>r neu eintreten<strong>de</strong>n Substituenten? Oben wur<strong>de</strong><br />
erwähnt, dass elektronenziehen<strong>de</strong> Gruppen, die die Elektronendichte im Kern<br />
vermin<strong>de</strong>rn, dies am wenigsten in <strong>de</strong>r 3-Stellung bewirken können und dass ein Angriff,<br />
wenn er überhaupt erfolgt, in dieser Position stattfin<strong>de</strong>t.<br />
Die Praxis zeigt jedoch, dass Chlorbenzol in 2- und 4-Stellung substituiert wird.<br />
Das be<strong>de</strong>utet, dass die bisherige Deutung zu vereinfacht ist,und dass<br />
an<strong>de</strong>rerseits <strong>de</strong>r mesomere Effekt trotz<strong>de</strong>m bei <strong>de</strong>r Richtung <strong>de</strong>r Substitution in<br />
Rechnung zu stellen ist, auch wenn <strong>de</strong>r induktive Effekt bezüglich <strong>de</strong>r Richtung<br />
<strong>de</strong>r Polarisierung ein an<strong>de</strong>res Substitutionsmuster erwarten lassen wür<strong>de</strong>.<br />
Die bisherige Vorhersage über <strong>de</strong>n Angriffspunkt <strong>de</strong>s Zweitsubstituenten (s.o.)<br />
basiert ausschließlich auf <strong>de</strong>r Betrachtung <strong>de</strong>s Ausgangsmoleküls. Entschei<strong>de</strong>nd<br />
für <strong>de</strong>n Reaktionsablauf ist aber <strong>de</strong>r Übergangszustand.<br />
Die Struktur, die <strong>de</strong>m Übergangszustand recht nah sein sollte, ist <strong>de</strong>r σ-Komplex<br />
(dafür spricht u.a. die Beobachtung, dass die Bildung <strong>de</strong>s σ-Komplexes bei vielen<br />
elektrophilen Substitutionsreaktionen <strong>de</strong>r geschwindigkeitsbestimmen<strong>de</strong> Schritt<br />
ist).<br />
116
Cl<br />
�<br />
Cl �<br />
NO 2<br />
H<br />
NO 2<br />
H<br />
Cl Cl<br />
�<br />
NO 2<br />
H<br />
H<br />
H<br />
Cl �<br />
�<br />
NO 2<br />
NO 2<br />
2-Substitution 3-Substitution 4-Substitution<br />
Bei vergleichen<strong>de</strong>r Betrachtung <strong>de</strong>s σ-Komplexes <strong>de</strong>r drei gedachten<br />
Angriffspunkte eines Zweitsubstituenten (Nitrogruppe) wird <strong>de</strong>utlich, dass nur bei<br />
2- und 4-Stellung eine Stabilisierung durch Mesomerie möglich ist. Dies ist <strong>de</strong>r<br />
Grund für die Bildung von z.B. 2- und 4-Nitrochlorbenzol, obwohl <strong>de</strong>r Angriff <strong>de</strong>s<br />
Zweitsubstituenten im Vergleich zum Benzol im Chlorbenzol wegen <strong>de</strong>s<br />
elektronenziehen<strong>de</strong>n Effektes <strong>de</strong>s Chlors erschwert ist.<br />
Ähnlich sind die Verhältnisse beim Styrol. Obwohl die Vinylgruppe elektronenziehend<br />
ist, erfolgt 2-und 4-Substitution. Auch hier kann im σ-Komplex nur die 2- und 4-Stellung<br />
stabilisiert wer<strong>de</strong>n:<br />
CH<br />
�<br />
CH 2<br />
NO 2<br />
CH<br />
H NO2 H<br />
�<br />
CH 2<br />
H<br />
CH<br />
�<br />
NO 2<br />
CH 2<br />
117
Die Orientierung <strong>de</strong>s Zweitsubstituenten ist also ein<strong>de</strong>utig nur aus <strong>de</strong>r<br />
Betrachtung <strong>de</strong>s <strong>de</strong>m Übergangszustand <strong>de</strong>r Reaktion sehr ähnlichen σ-<br />
Komplexes abzuleiten. Die Betrachtung nur <strong>de</strong>s Grundzustan<strong>de</strong>s ist eine<br />
vereinfachte Interpretation, die zu Fehlschlüssen führen kann.<br />
Man sollte erwarten, dass das Verhältnis von 2- zu 4-Substitutionsprodukten etwa<br />
2:1 beträgt (zwei 2-Stellungen gegenüber einer 4-Stellung). In <strong>de</strong>r Regel wird<br />
jedoch hauptsächlich das 4-Produkt gebil<strong>de</strong>t. Ausschlaggebend hierfür sind<br />
sterische Faktoren (<strong>de</strong>r Angriff <strong>de</strong>s Elektrophils ist in unmittelbarer<br />
Nachbarschaft zur bereits vorhan<strong>de</strong>nen Gruppe räumlich erschwert) und die<br />
höhere Stabilität <strong>de</strong>r parachinoi<strong>de</strong>n Struktur bei Entstehung <strong>de</strong>s 4-Produktes.<br />
�<br />
O<br />
�<br />
CH 3<br />
bzw.<br />
�<br />
O<br />
CH 3<br />
H NO 2<br />
parachinoi<strong>de</strong> Struktur<br />
11. Herstellung von Nitroverbindungen:<br />
�<br />
O<br />
CH 3<br />
�<br />
bzw.<br />
�<br />
O<br />
orthochinoi<strong>de</strong> Struktur<br />
CH 3<br />
NO 2<br />
Das aktive Agens <strong>de</strong>r Nitrierung ist das NO2 �<br />
Ion (Nitronium-Ion). In Salpetersäure wird<br />
dieses Ion nur in ganz geringer Menge durch Eigenprotonierung gebil<strong>de</strong>t:<br />
HO NO 2 + HNO 3 H 2O NO 2<br />
�<br />
�<br />
NO2 - H 2O<br />
�<br />
+ NO3 Die Konzentration reicht aber aus, um reaktive aromatische Verbindungen wie z.B.<br />
Phenol o<strong>de</strong>r Anisol zu nitrieren:<br />
H<br />
118
CH 3<br />
O<br />
�<br />
CH 3<br />
O<br />
�<br />
�<br />
+ NO2 �<br />
CH 3<br />
O<br />
- H �<br />
OCH 3<br />
H NO 2 NO 2<br />
Zur Nitrierung unsubstituierter aromatischer Kohlenwasserstoffe o<strong>de</strong>r gar von<br />
solchen, die elektronenziehen<strong>de</strong> Gruppen tragen, ist die Konzentration an NO2 �<br />
in<br />
<strong>de</strong>r Salpetersäure nicht ausreichend. Um diese zu erhöhen, setzt man<br />
Schwefelsäure zu:<br />
HNO 3 + 2 H 2SO 4<br />
�<br />
NO2 + H 3O �<br />
�<br />
+ 2 HSO4 Die Nitrierkraft <strong>de</strong>r so erhältlichen Nitriersäure kann gegebenenfalls noch durch<br />
Zusatz von Stickoxi<strong>de</strong>n (rote rauchen<strong>de</strong> Salpetersäure) und Erhitzen gesteigert<br />
wer<strong>de</strong>n.<br />
Da Salpetersäure auch oxidieren<strong>de</strong> Wirkung entfaltet, die zu einem Abbau <strong>de</strong>s<br />
Aromaten führen könnte, ist beson<strong>de</strong>rs bei <strong>de</strong>r Nitrierung von Phenolen und<br />
Aminen genaue Temperaturkontrolle nötig. Zweckmäßig ist ein vorhergehen<strong>de</strong>n<br />
Schutz durch Acylierung. Nach <strong>de</strong>r Reaktion kann die Schutzgruppe wie<strong>de</strong>r<br />
entfernt wer<strong>de</strong>n.<br />
Ähnliches gilt für die Nitrierung von Aromaten mit Seitenketten, die durch Oxidation zu<br />
entsprechen<strong>de</strong>n aromatischen Garbonsäuren abgebaut wer<strong>de</strong>n:<br />
NO 2<br />
CH 2 R CH 2 R<br />
NO 2<br />
COOH<br />
119
In <strong>de</strong>r Regel enstehen bei <strong>de</strong>r Nitrierumg substituierter Aromaten<br />
Isomerengemische, <strong>de</strong>ren Trennung im Labor nicht immer einfach ist. In <strong>de</strong>r<br />
Technik wer<strong>de</strong>n diese Gemische durch Ausfrieren o<strong>de</strong>r Destillation getrennt.<br />
In manchen Fällen ist die Trennung im Labor durch Wasserdampf<strong>de</strong>stillation<br />
möglich, wie z.B. von 2- und 4-Nitrophenol: Nur das 2-Isomere ist<br />
wasserdampfflüchtig, nicht aber das 4-, und auch nicht das 3-Nitrophenol.<br />
Maßgebend für diesen drastischen Unterschied in <strong>de</strong>n physikalischen<br />
Eigenschaften ist <strong>de</strong>r sogenannte ortho-Effekt.<br />
Befin<strong>de</strong>n sich in ortho-Stellung eine OH-Gruppe und eine Gruppe mit einem<br />
freien Elektronenpaar, so kann es über eine quasi Sechsringstruktur zur<br />
Ausbildung einer intramolekularen Wasserstoffbrücke kommen. Da <strong>de</strong>shalb<br />
Wasserstoffbrücken nicht zu an<strong>de</strong>ren Molekülen geschlagen wer<strong>de</strong>n können,<br />
ergeben sich starke Unterschie<strong>de</strong> von 2- und 3- bzw. 4-Isomeren in <strong>de</strong>n<br />
physikalischen Eigenschaften.<br />
In manchen Fällen ist auch eine oxidative Herstellung von Nitroverbindungen aus<br />
Aminoverbindungen durch Reaktion mit Caro-scher Säure angebracht:<br />
NH 2<br />
NO 2<br />
�<br />
H 2SO 5<br />
N<br />
O<br />
O<br />
O<br />
H<br />
�<br />
NO 2<br />
NO 2<br />
120
11.1 Herstellung von 3-Nitro<strong>de</strong>rivaten aus Verbindungen, die einen Substituenten 1.<br />
Ordnung tragen:<br />
Will man von Verbindungen mit Substituenten erster Ordnung 3-Nitroverbindungen<br />
erhalten, so muß man Umwege gehen. Beispielsweise kann man durch vorgeschaltete<br />
Nitrierung in 4-Stellung und anschließen<strong>de</strong> Reduktion <strong>de</strong>r NO2-Gruppe zur -NH2-<br />
Gruppe, diese -NH2-Gruppe durch Acetylierung schützen und die<br />
Acetylaminoverbindung in 2-Stellung nitrieren, was eine Nitrierung in 3-Stellung <strong>de</strong>r<br />
ursprünglichen Verbindung be<strong>de</strong>utet. Zur Entfernung <strong>de</strong>r Acetylaminogruppe wird <strong>de</strong>r<br />
Acetylrest abhydrolisiert, die Aminogruppe in die Diazoniumverbindung überführt und<br />
dann reduktiv entfernt (Kap. 12.2.1).<br />
O 2 N<br />
CH3 CH 3 CH 3 CH 3<br />
CH 3<br />
NHCOCH 3<br />
O 2N<br />
NO 2 NH 2 NH<br />
CH 3<br />
NH 2<br />
O 2N<br />
CH 3<br />
�<br />
N2 Cl �<br />
O 2N<br />
C CH3 C<br />
O<br />
CH3 O<br />
Die Herstellung von 2- und 4-Nitro<strong>de</strong>rivaten von Verbindungen mit Substituenten<br />
zweiter Ordnung gelingt wie<strong>de</strong>r nur auf Umwegen. Beispielsweise ist 2- und 4-<br />
Nitrobenzoesäure durch Oxidation <strong>de</strong>s leicht erhältlichen 2- und 4-Nitrotoluols<br />
herstellbar:<br />
CH 3<br />
121
CH 3<br />
NO 2<br />
COOH<br />
NO 2<br />
In manchen Fällen gelingt die Einführung von Nitrogruppen durch Austausch gegen die<br />
Sulfonsäuregruppe:<br />
OH OH<br />
SO 3H<br />
SO 3H<br />
11.2 Nachweis von aromatischen Nitroverbindungen:<br />
O 2N NO 2<br />
NO 2<br />
Pikrinsäure<br />
Die Nitroverbindung wird mit Zinkstaub in saurer Lösung zum entsprechen<strong>de</strong>n<br />
aromatischen Amin reduziert. Durch Behan<strong>de</strong>ln mit NaNO2-Lösung in schwach saurem<br />
Medium erhält man das Diazoniumsalz, das mit β-Naphthol in schwach alkalischer<br />
Lösung zu einem roten Farbstoff gekuppelt wer<strong>de</strong>n kann (Kap. 12.2.2).<br />
Zur Charakterisierung dienen die Säureami<strong>de</strong> <strong>de</strong>r Benzoesäure <strong>de</strong>r Benzol-<br />
sulfonsäure o<strong>de</strong>r <strong>de</strong>r 4-Toluolsulfonsäure.<br />
12. Herstellung aromatischer Amine<br />
Aromatische Amine erhält man in hervorragen<strong>de</strong>n Ausbeuten durch Reduktion von<br />
Nitroverbindungen.<br />
Die gebräuchlichsten Reduktionsmittel sind:<br />
122
a) Zinn in salzsaurer Lösung<br />
NO 2<br />
Sn/HCl<br />
b) bessere Ausbeuten liefert SnCl2 in konzentrierter Salzsäure:<br />
� + Sn 2�<br />
Ph N O<br />
Ph N<br />
Gesamt:<br />
Ph NO 2<br />
O �<br />
OH<br />
H<br />
- Sn 4�<br />
NH 2<br />
+ 2 H �<br />
- H2O Ph N O + Sn 2�<br />
+ 2 H �<br />
- Sn 4�<br />
+ Sn 2�<br />
+ 2 H �<br />
- Sn 4�<br />
+ 3 Sn 2�<br />
- 3 Sn 4�<br />
- H 2O<br />
+ 6 H �<br />
- 2 H 2O<br />
Ph NH 2<br />
Ph NH 2<br />
c) Reduziert man mit Zink in Eisessig/Essigsäureanhydrid, so erhält man direkt das<br />
acetylierte Amin:<br />
NO 2<br />
3 Zn<br />
Ac 2O / HOAc<br />
NH<br />
O<br />
C<br />
CH 3<br />
d) In <strong>de</strong>r Technik wird das billigere Eisen in Wasser als Reduktionsmittel verwen<strong>de</strong>t.<br />
Salzsäure und Essigsäure dienen als Katalysator (Bechamp-Verfahren):<br />
4<br />
+ 9 Fe + 4 H2O / HCl<br />
Ph NO2 4 Ph NH2 - 3 Fe3O4 Das entstehen<strong>de</strong> Eisenoxid wird als Farbpigment ebenfalls verwen<strong>de</strong>t.<br />
123
e) Die Nitrogruppe kann auch durch katalytische Hydrierung in die Aminogruppe<br />
überführt wer<strong>de</strong>n. In <strong>de</strong>r Regel verwen<strong>de</strong>t man hierfür Platin-Aktivkohle (10 % Pt)<br />
o<strong>de</strong>r Raney-Nickel in neutraler, meist alkoholischer Lösung.<br />
Zur Herstellung von Raney-Nickel wird aus einer Aluminium-Nickel-Legierung durch<br />
Lauge das Aluminium herausgelöst und so Nickel mit einer sehr großen Oberfläche<br />
erhalten. VORSICHT: Raney-Nickel ist in trockenem Zustand pyrophor, also<br />
selbstentzündlich. Es muss nach <strong>de</strong>m Abfiltrieren durch gezieltes Abbrennen<br />
vernichtet wer<strong>de</strong>n (Einziger Einsatz <strong>de</strong>s Bunsenbrenners im OC-Grundpraktikum).<br />
Der Vorteil <strong>de</strong>r katalytischen Hydrierung gegenüber <strong>de</strong>n vorher erwähnten<br />
Metho<strong>de</strong>n für die Synthese liegt unter an<strong>de</strong>rem darin, dass bei <strong>de</strong>r Reduktion von<br />
Nitroverbindungen, die zusätzlich eine Acetylaminogruppe tragen, die<br />
Schutzgruppe nicht, wie bei <strong>de</strong>r Reduktion in saurem Medium, abhydrolysiert<br />
wird:<br />
NHCOCH 3<br />
NO 2<br />
Pt / H2 EtOH<br />
NHCOCH 3<br />
NH 2<br />
Bei <strong>de</strong>r Reduktion mit Raney-Nickel kann die Anwendung von H2 dadurch<br />
umgangen wer<strong>de</strong>n, dass man Hydrazin als wasserstoffliefern<strong>de</strong>s Reagens<br />
einsetzt.<br />
VORSICHT: Hydrazin ist jedoch ein Plasmagift und ruft Krämpfe und<br />
Herzschä<strong>de</strong>n hervor. Auf <strong>de</strong>r Haut wirkt es stark ätzend. - Verätzte Hautstellen<br />
wer<strong>de</strong>n mit verdünnter Essigsäure gewaschen.<br />
f) Die selektive Reduktion nur einer Nitrogruppe in Polynitroverbindungen gelingt<br />
mit <strong>de</strong>r berechneten Menge von Natrium- o<strong>de</strong>r Ammoniumhydrogensulfid:<br />
124
NO 2<br />
NO 2<br />
NH 4<br />
SH<br />
NH 2<br />
NO 2<br />
Solange man in saurer Lösung arbeitet, verläuft die Reduktion glatt. In neutraler<br />
o<strong>de</strong>r alkalischer Lösung kann die Reaktion auf Zwischenstufen stehen bleiben,<br />
so dass man je nach Reaktionsbedingungen.auch Nitrosoverbindungen,<br />
aromatische Hydroxyl-amine, Azoxyverbindungen, Azoverbindungen und<br />
Hydrazoverbindungen erhalten kann:<br />
Nitrosobenzol<br />
Phenylhydroxylamin<br />
Anilin<br />
Ph NO 2<br />
Ph N O<br />
Ph NH OH<br />
H �<br />
Ph NH 2<br />
OH �<br />
OH �<br />
O<br />
�<br />
Ph N N Ph<br />
�<br />
Azoxybenzol<br />
Ph<br />
Ph<br />
N N Ph<br />
Azobenzol<br />
NH NH Ph<br />
Hydrazobenzol<br />
Die Nitrogruppe ist im Vergleich zu an<strong>de</strong>ren reduzierbaren Stoffen beson<strong>de</strong>rs<br />
leicht angreifbar, so dass es in vielen Fällen entsprechen<strong>de</strong>r Umwege o<strong>de</strong>r<br />
Vorkehrungen bedarf, um in ihrer Gegenwart an<strong>de</strong>re Gruppen zu reduzieren.<br />
Ein spezielles Verfahren zur Herstellung von β-Naphthylamin und analogen<br />
Verbindungen - vor allem in <strong>de</strong>r Technik - ist die Bucherer-Reaktion: Setzt man<br />
β-Naphthol in ammomiakalischer Lösung mit Ammoniumhydrogensulfit bei 150°C<br />
(Druckgefäß) um, so erhält man β-Naphthylamin:<br />
125
OH OH<br />
NH4HSO3 NH<br />
H SO 3 NH 4<br />
H SO 3NH 4 H SO 3NH 4<br />
NH 2<br />
H SO 3NH 4<br />
- NH4HSO3 O + NH 3<br />
- H 2O<br />
VORSICHT: β-Naphthylamin ist ein starkes Cancerogen, beim Umgang mit dieser<br />
Verbindung ist daher höchste Vorsicht geboten. Auch an<strong>de</strong>re Amine haben häufig<br />
cancerogene Eigenschaften, daher immer mit Gummihandschuhen und im Abzug<br />
arbeiten!!!<br />
Gemischt aromatisch-aliphatische sekundäre Amine sind zugänglich durch<br />
Acylierung <strong>de</strong>s betreffen<strong>de</strong>n primären aromatischen Amins und nachfolgen<strong>de</strong><br />
Reduktion durch ein komplexes Metallhydrid:<br />
NH 2<br />
NHCOCH 3<br />
LiAlH 4<br />
NH<br />
NH 2<br />
C 2H 5<br />
Aus Carbonsäuren sind primäre Amine durch Abbaureaktionen erhältlich (z.B.<br />
Hofmann-Abbau, siehe dazu Kapitel 9.1).<br />
12.1 Bildung von Diazoniumsalzen<br />
Primäre aromatische Amine reagieren im Gegensatz zu primären aliphatischen Aminen<br />
(die unter N2-Abspaltung in die entsprechen<strong>de</strong>n Alkohole übergehen, Kap. 9.4.1) mit<br />
salpetriger Säure in mineralsaurem (meist salzsaurem) Medium zu Diazoniumsalzen:<br />
126
Die Mineralsäure setzt aus salpetriger Säure bzw. Natriumnitrit das Nitrosonium-<br />
Ion frei, das die Aminogruppe zunächst nitrosiert.<br />
NH 2 + N O �<br />
NH N<br />
� - H2O OH2 + H 2O<br />
- H 3O �<br />
�<br />
N<br />
NH N O<br />
N<br />
+ 2 H 3O �<br />
- 2 H 2O<br />
Das im weiteren Verlauf <strong>de</strong>r Reaktion entstehen<strong>de</strong> Diazoniumion wird durch <strong>de</strong>n<br />
Benzolring zusätzlich stabilisiert (Beteiligung an <strong>de</strong>r Mesomerie) und ist daher im<br />
Gegensatz zu <strong>de</strong>n aliphatischen Diazoniumionen in Lösung bei tiefen Temperaturen<br />
beständig.<br />
12.2 Reaktionen <strong>de</strong>r Diazoniumsalze<br />
Die Be<strong>de</strong>utung <strong>de</strong>r aromatischen Amine in <strong>de</strong>r synthetischen Chemie beruht unter<br />
an<strong>de</strong>rem auf <strong>de</strong>r Überführbarkeit in Diazoniumsalze, die zu einer Anzahl weiterer<br />
Reaktionen befähigt sind (man informiere sich darüber im Lehrbuch).<br />
In diesem Rahmen soll nur auf zwei wichtige Reaktionstypen eingegangen wer<strong>de</strong>n, die<br />
Desaminierung und die sogenannte Kupplungsreaktion. Die Sandmeyer Reaktion und<br />
ähnliche Umsetzungen, die ebenfalls von Diazoniumsalzen ausgehen, wer<strong>de</strong>n im Kap.<br />
13 behan<strong>de</strong>lt.<br />
12.2.1 Desaminierung<br />
Diese Reaktion dient zur Entfernung <strong>de</strong>r NH2-Gruppe aus einem Aromaten im Verlauf<br />
einer Synthese.<br />
Bei Behandlung <strong>de</strong>s aus <strong>de</strong>m Amin hergestellten Diazoniumsalzes mit<br />
Reduktionsmitteln wie unterphosphoriger bzw. phosphoriger Säure, alkalischer<br />
Natriumstannitlösung o<strong>de</strong>r Ameisensäure wird unter Abspaltung von Stickstoff<br />
127
<strong>de</strong>r entsprechen<strong>de</strong> Kohlenwasserstoff gewonnen, d.h. die ursprüngliche<br />
Aminogruppe entfernt:<br />
NH 2<br />
CH 3<br />
Cl<br />
NaNO 2<br />
(HCl)<br />
12.2.2 Kupplungsreaktionen<br />
�<br />
N N<br />
CH 3<br />
Cl �<br />
Cl<br />
+ H 3PO 4 + H 2O<br />
- H 3PO 3 - N 2 - HCl<br />
Das Diazoniumkation ist ebenso wie an<strong>de</strong>re positiv gela<strong>de</strong>ne Reagenzien<br />
befähigt, aromatische Systeme elektrophil anzugreifen. Diese Reaktion nennt<br />
man Azokupplung.<br />
Das Diazoniumkation ist, verglichen mit an<strong>de</strong>ren Ionen (z.B. NO �<br />
), nur ein schwaches<br />
elektrophiles Reagens und kann <strong>de</strong>mzufolge nur mit reaktionsfähigen aromatischen<br />
Verbindungen reagieren (Phenolen, Aminen, aber nicht mehr mit Anisol).<br />
Durch elektronenziehen<strong>de</strong> Gruppen wird die positive Ladung <strong>de</strong>s<br />
Diazoniumkations verstärkt und seine Reaktivität erhöht.<br />
In saurer und auch in schwach alkalischer Lösung sind Diazoniumsalze<br />
beständig und liegen in dissoziierter Form vor. Im stark alkalischen Milieu bil<strong>de</strong>n<br />
sich dagegen Diazotat-Anionen.<br />
� + OH�<br />
�<br />
N N Cl<br />
- Cl �<br />
N N O �<br />
N<br />
OH<br />
CH 3<br />
+ OH �<br />
- H 2O<br />
Es gibt daher für je<strong>de</strong> Kupplungsreaktion einen optimalen pH-Wert. Bei <strong>de</strong>r<br />
Reaktion mit Phenolen arbeitet man im schwach alkalischem Medium, weil das<br />
N<br />
Cl<br />
128
Phenolatanion eine größere Elektronendichte als das Phenol selbst aufweist und<br />
daher elektrophil leichter angreifbar ist.<br />
Obwohl <strong>de</strong>r Angriff am Sauerstoff und am Kohlenstoff erfolgen könnte, erhält<br />
man bei Phenolen nur das kohlenstoffsubstituierte Produkt. Entschei<strong>de</strong>nd dafür<br />
ist die Bindungsstärke <strong>de</strong>r neugebil<strong>de</strong>ten Bindung und nicht die<br />
Elektronendichte.<br />
+ OH �<br />
- H 2O<br />
�<br />
O �<br />
N N<br />
O �<br />
+ N N<br />
O<br />
N<br />
N<br />
Amine reagieren langsamer als Phenole. Um eine hohe Diazoniumkation-<br />
Konzentration zu erzielen, arbeitet man in saurem Medium. Ist die Lösung jedoch<br />
zu sauer, so wird an<strong>de</strong>rerseits das Amin in das wesentlich reaktionsträgere<br />
Kation umgewan<strong>de</strong>lt:<br />
NH 2<br />
+ H 3O �<br />
- H 2 O<br />
O �<br />
�<br />
NH3 Es muß also in schwach saurem Bereich gearbeitet wer<strong>de</strong>n. Der optimale pH-<br />
Wert liegt etwa beim pKA-Wert <strong>de</strong>s eingesetzten Amins.<br />
H<br />
129
An<strong>de</strong>rs als Phenole kuppeln primäre und sekundäre Amine, nicht tertiäre Amine,<br />
am Stickstoff <strong>de</strong>r Amingruppe und nicht am Kohlenstoff. Daher wer<strong>de</strong>n<br />
Diazoamino-verbindungen gebil<strong>de</strong>t:<br />
- H �<br />
�<br />
H<br />
N N + N<br />
N N<br />
H<br />
N<br />
N<br />
NH<br />
Beim Erwärmen in saurer Lösung lagern die Diazoaminoverbindungen jedoch in<br />
die Aminoazoverbindungen um:<br />
N N NH<br />
�<br />
N N +<br />
+ H �<br />
NH 2<br />
N N<br />
NH2 H<br />
N<br />
H<br />
H<br />
N N N<br />
Ein Beispiel für die Kupplungsreaktion ist die Bildung von Methylorange durch<br />
Kupplung von p-Sulfonyldiazoniumchlorid mit N,N-Dimethylanilin in schwach<br />
saurem Medium.<br />
- H �<br />
H<br />
�<br />
�<br />
130
HO 3S<br />
HO 3S<br />
�<br />
N N Cl +<br />
�<br />
N<br />
N<br />
Methylorange<br />
N<br />
N<br />
CH 3<br />
CH 3<br />
CH 3<br />
CH 3<br />
- HCl<br />
In saurer Lösung liegt Methylorange in Form eines rotgefärbten chinoi<strong>de</strong>n Salzes vor.<br />
In basischer Lösung bil<strong>de</strong>t sich das gelbgefärbte Natriumsalz <strong>de</strong>r Azoform. Deshalb<br />
fin<strong>de</strong>t Methylorange als Indikator Anwendung.<br />
Na �<br />
�<br />
O3S �<br />
�<br />
Na O3S �<br />
N N<br />
N<br />
H<br />
CH 3<br />
CH 3<br />
N N<br />
N<br />
gelb<br />
rot<br />
Na �<br />
�<br />
O3S CH 3<br />
CH 3<br />
H �<br />
OH �<br />
N N<br />
N<br />
Der Nachweis primärer aromatischer Amine erfolgt durch Diazotierung und Kupplung<br />
mit β-Naphthol (siehe Kap. 11)<br />
13. Herstellung aromatischer Halogenverbindungen und Nitrile<br />
Während die Anlagerung eines Halogenmoleküls an Doppelbindungen so rasch und<br />
leicht erfolgt, dass diese Reaktion für <strong>de</strong>n qualitativen Nachweis von Doppelbindungen<br />
nutzbar ist, erfor<strong>de</strong>rt die Halogenierung eines aromatischen Systems meist die<br />
Gegenwart von Katalysatoren (eine Ausnahme bil<strong>de</strong>t die Reaktion von Halogen mit<br />
H<br />
CH 3<br />
�<br />
CH 3<br />
131
Phenolen und Aminen, die durch die funktionelle Gruppe beson<strong>de</strong>rs stark für<br />
elektrophile Angriffe aktiviert sind).<br />
Als Katalysatoren dienen Lewis Säuren, wie FeCl3 o<strong>de</strong>r ZnCl2. In <strong>de</strong>r Regel genügt eine<br />
kleine Menge an Fe-Pulver, um die Reaktion einzuleiten. Dieses reagiert mit Halogen<br />
und bil<strong>de</strong>t FeX3, das nun die eigentliche Reaktion in Gang setzt, die meist bereits bei<br />
Raumtemperatur abläuft (KKK-Regel: Kälte, Katalysator, Kern).<br />
Da Chlor ein Substituent 1. Ordnung ist und <strong>de</strong>mzufolge <strong>de</strong>r Eintritt von Zweit-<br />
substituenten in 2- und 4-Stellung erfolgt, könnte man weiterhin annehmen, dass<br />
<strong>de</strong>r für die Orientierung maßgeben<strong>de</strong> Mesomerieeffekt (Kap. 10.1) auch <strong>de</strong>n<br />
weiteren Angriff eines zweiten Chloratoms an das zunächst gebil<strong>de</strong>te<br />
Chlorbenzol för<strong>de</strong>rt. Dies ist aber nicht <strong>de</strong>r Fall, da <strong>de</strong>r Chlorsubstituent<br />
insgesamt die Elektronendichte im Kern vermin<strong>de</strong>rt (Kap.10.1).<br />
Die Chlorierung von Benzol kann also auf <strong>de</strong>r Stufe <strong>de</strong>s monohalogenierten<br />
Produktes abgestoppt wer<strong>de</strong>n. Disubstitutionsprodukte, die vor allem bei <strong>de</strong>r<br />
Halogenierung <strong>de</strong>s reaktionsfähigeren Naphthalins entstehen, können durch<br />
Destillation leicht abgetrennt wer<strong>de</strong>n.<br />
13.1 Herstellung aromatischer Halogenverbindungen und Nitrile durch Sandmeyer-<br />
Reaktion<br />
Als Ausgangsmaterial dienen primäre aromatische Amine. Bei <strong>de</strong>r Umsetzung <strong>de</strong>r<br />
durch Diazotierung (Kap. 12.1) zugänglichen Diazoniumsalze, z.B. Benzol-<br />
diazoniumchlorid mit Kupfer(I)chlorid in salzsaurer Lösung und anschließen<strong>de</strong>r<br />
Erwärmung <strong>de</strong>r Lösung, bil<strong>de</strong>t sich Chlorbenzol, das durch Wasserdampf<strong>de</strong>stillation<br />
aus <strong>de</strong>r Reaktionslösung isoliert wer<strong>de</strong>n kann.<br />
�<br />
CuCl<br />
�<br />
N N Cl<br />
Cl + N 2<br />
Im Einzelnen läuft die Reaktion folgen<strong>de</strong>rmaßen ab: Kupfer-(I)-chlorid bil<strong>de</strong>t in<br />
salzsaurer Lösung einen Komplex:<br />
132
CuCl + Cl �<br />
[CuCl 2] �<br />
In zu stark saurer Lösung entsteht ein Tetrakomplex, <strong>de</strong>r nicht mehr in <strong>de</strong>r<br />
gewünschten Weise reagiert; in zu stark salzsauren Lösungen verläuft die<br />
Umsetzung daher wesentlich langsamer:<br />
CuCl + 3 Cl �<br />
[CuCl 4 ] 3�<br />
Der [CuCl2] �<br />
-Komplex reagiert mit <strong>de</strong>m Diazoniumsalz unter Abspaltung von Stickstoff<br />
und Bildung eines Arylradikals. Kupfer gibt dabei ein Elektron ab und wird zum<br />
Kupfer(II) oxidiert.<br />
�<br />
N N [CuCl2 ] + N2 �<br />
+ � + CuCl2 Diese Reaktion ist geschwindigkeitsbestimmend für <strong>de</strong>n Ablauf <strong>de</strong>r Gesamtreaktion.<br />
Der Elektronenübergang vom Kupfer-(I)-Komplex erfolgt vermutlich in einem aktivierten<br />
Komplex über eine „Chlorid-Brücke“.<br />
�<br />
N N Cl Cu Cl �<br />
In einer nachfolgen<strong>de</strong>n schnelleren Reaktion überträgt das Kupfer-(II)-chlorid ein<br />
Chlorradikal auf das Arylradikal und wird dabei wie<strong>de</strong>r zum Kupfer-(I)-chlorid reduziert.<br />
� + Cl Cu Cl<br />
Cl + CuCl<br />
In gleicher Weise sind Bromi<strong>de</strong> und Chlori<strong>de</strong> herstellbar.<br />
133
�<br />
N<br />
N<br />
- N 2<br />
[CuBr 2] �<br />
+ CN �<br />
Cu �<br />
Br<br />
C N<br />
Bei <strong>de</strong>r Herstellung von lodi<strong>de</strong>n sind Kupfersalze als Katalysatoren nicht erfor<strong>de</strong>rlich, da<br />
das lodid-Ion selbst reversibel oxidierbar ist und somit seinen eigenen Katalysator<br />
darstellt, kann Kaliumiodid für die Umsetzung eingesetzt wer<strong>de</strong>n.<br />
�<br />
N N Cl �<br />
+ K ,<br />
- KCl<br />
,<br />
+ N 2<br />
Fluorbenzol läßt sich in analoger Weise nicht herstellen, ist aber durch die Balz-<br />
Schiemann-Reaktion zugänglich, bei <strong>de</strong>r trockenes Benzoldiazonium-<br />
Tetrafluoroborat erhitzt wird.<br />
�<br />
N N [BF4] F<br />
� Hitze<br />
- N2 + BF 3<br />
Der Vorteil dieser Reaktionen zur Herstellung von aromatischen<br />
Halogen<strong>de</strong>rivaten liegt vor allem darin, dass auf diese Weise auch in solchen<br />
Positionen Halogenatome eingebaut wer<strong>de</strong>n können, die sonst nicht zugänglich<br />
sind.<br />
m-Dichlorbenzol ist durch direkte Chlorierung nicht herstellbar, da Chlor in 2- und 4-<br />
Stellung dirigiert. Seine Herstellung gelingt aber auf folgen<strong>de</strong> Weise über die<br />
Sandmeyer-Reaktion:<br />
134
NO �<br />
NO 2<br />
�<br />
N 2<br />
NO 2<br />
�<br />
N 2<br />
Sn/HCl<br />
CuCl<br />
HCl<br />
NH 2<br />
13.2 Herstellung aromatischer Nitrile durch Sulfonsäuresalzschmelze<br />
Cl<br />
NH 2<br />
Bei größeren Diazotierungsansätzen steigt die Gefahr, die Temperatur nicht mehr<br />
kontrollieren zu können, so dass sie nur schlecht im industriellen Maßstab<br />
durchzuführen sind. Man wen<strong>de</strong>t daher zur Einführung <strong>de</strong>r Cyanidgruppe anstelle <strong>de</strong>s<br />
Sandmeyerverfahrens die KCN-Schmelze von Sulfonsäuren an:<br />
SO 3H<br />
13.2.2 Herstellung von Sulfonsäuren<br />
KCN<br />
CN<br />
+ KHSO 3<br />
Die als Ausgangsmaterial zur Nitrilherstellung benötigten Sulfonsäuren sind durch<br />
Sulfonierung zugänglich: Die Sulfonierung aromatischer Verbindungen erfor<strong>de</strong>rt je nach<br />
<strong>de</strong>r Aktivierung <strong>de</strong>s Aromaten unterschiedliche Reaktionsbedingungen: Phenole lassen<br />
sich bereits mit 70-100 % H2SO4 sulfonieren, Naphthalin erst mit Schwefelsäure, <strong>de</strong>r<br />
noch SO3 zugesetzt wird. Das angreifen<strong>de</strong> Agens bei <strong>de</strong>r Sulfonierung ist SO3.<br />
Cl<br />
135
O<br />
+ δ+ S<br />
δ−<br />
O<br />
O<br />
�<br />
H<br />
O<br />
S O<br />
O<br />
�<br />
- H �<br />
O<br />
S O<br />
Als Nebenprodukte bil<strong>de</strong>n sich Sulfone. Sie entstehen aus <strong>de</strong>n Sulfonsäuren, die<br />
durch Protonierung ihrerseits wie<strong>de</strong>r elektrophile Reagentien bil<strong>de</strong>n können, die<br />
die Ausgangsmoleküle angreifen:<br />
O<br />
O<br />
S<br />
OH<br />
+ H �<br />
- H2O Weitere Nebenprodukte können durch die oxidative Wirkung <strong>de</strong>r Schwefelsäure<br />
gebil<strong>de</strong>t wer<strong>de</strong>n. Die Isolierung <strong>de</strong>r entstehen<strong>de</strong>n Säuren ist wegen ihrer hohen<br />
Wasserlöslichkeit schwierig. Meist gelingt sie durch Aussalzen (Zusatz von festem<br />
NaCl).<br />
Um leichter isolierbare Verbindungen zu erhalten, stellt man vielfach anstelle <strong>de</strong>r<br />
Sulfonsäuren <strong>de</strong>ren Sulfochlori<strong>de</strong> her, die durch Umsatz <strong>de</strong>r Aromaten mit<br />
Chlorsulfonsäuren erhältlich sind:<br />
O<br />
O<br />
O<br />
S<br />
O<br />
S<br />
�<br />
O<br />
�<br />
136
Cl<br />
+ O S O<br />
OH<br />
- HCl<br />
SO 3 H<br />
Cl SO 3H<br />
- H 2SO 4<br />
SO 2 Cl<br />
Die Sulfonierung ist wie die Frie<strong>de</strong>l-Crafts-Reaktion reversibel. Durch kinetische<br />
Kontrolle gebil<strong>de</strong>te Produkte können daher bei Temperaturerhöhung in die<br />
thermodynamisch stabileren umgelagert wer<strong>de</strong>n, so dass dadurch die<br />
Möglichkeit besteht, je nach Reaktionsbedingungen verschie<strong>de</strong>ne<br />
Substitutionsprodukte zu erhalten:<br />
SO 3H<br />
SO 3H<br />
13.3 Nachweis aromatischer Halogen<strong>de</strong>rivate<br />
Die Beweglichkeit von Halogenen, die an einem Aromaten gebun<strong>de</strong>n sind, ist - wie<br />
bereits früher eingehend dargelegt - bei weitem nicht so groß wie die aliphatischer<br />
Halogeni<strong>de</strong>. Dies zeigt sich beispielsweise in <strong>de</strong>r Reaktionsfähigkeit gegenüber<br />
alkoholischer Silbernitratlösung: Während aliphatische Halogeni<strong>de</strong> relativ rasch unter<br />
Bildung von AgX reagieren, beobachtet man bei Umsatz von aromatischen<br />
Halogeni<strong>de</strong>n auch nach mehrstündigen Stehgn keine Trübung <strong>de</strong>r Reaktionslösung<br />
durch ausfallen<strong>de</strong>s Silberhalogenid.<br />
Als Nachweisreaktion ist die Beilsteinprobe geeignet sowie <strong>de</strong>r Aufschluß <strong>de</strong>r<br />
aromatischen Verbindung mit Natrium und <strong>de</strong>r Nachweis <strong>de</strong>r Chlorionen mit<br />
Silbernitrat.<br />
Eine Charakterisierung ist meist durch Nitrierung über <strong>de</strong>n Schmelzpunkt <strong>de</strong>r<br />
Nitro<strong>de</strong>rivate o<strong>de</strong>r durch Sulfonamidbildung möglich.<br />
14. Herstellung aromatischer Ketone und Al<strong>de</strong>hy<strong>de</strong><br />
14.1 Die Frie<strong>de</strong>l-Crafts-Acylierung<br />
137
Acylhalogeni<strong>de</strong> (Säurechlori<strong>de</strong>) sind befähigt, aromatische Verbindungen in Gegenwart<br />
von Lewis-Säuren im Zuge einer elektrophilen Substitutionsreaktion zu acylieren<br />
(Frie<strong>de</strong>l-Crafts-Acylierung).<br />
H 3C C<br />
O<br />
Cl<br />
H<br />
�<br />
+ AlCl3 H3C C<br />
�<br />
O<br />
O<br />
C<br />
�<br />
AlCl4 CH 3<br />
- HCl<br />
�<br />
AlCl4 O<br />
C<br />
AlCl 3<br />
CH 3<br />
Die Reaktion wird offenbar durch Komplexbildung am Sauerstoffatom (Erhöhung<br />
<strong>de</strong>r Carbonylaktivität) eingeleitet. Das so gebil<strong>de</strong>te Elektrophil greift in üblicher<br />
Weise die aromatische Verbindung an. AlCl3 bil<strong>de</strong>t auch mit <strong>de</strong>m entstehen<strong>de</strong>n<br />
Keton eine Komplexverbindung, die unter <strong>de</strong>n gegebenen Reaktionsbedingungen<br />
beständig ist. AlCl3 muß daher in einer Menge, die über einem Mol liegt,<br />
zugesetzt wer<strong>de</strong>n.<br />
Aromaten, die über elektronenziehen<strong>de</strong> Substituenten verfügen, haben zu geringe<br />
negative Ladungsdichte, um eine Frie<strong>de</strong>l-Crafts-Reaktion einzugehen. Da zu<br />
diesen Substituenten auch Ketone zählen, bleibt die Reaktion nach <strong>de</strong>r erfolgten<br />
Mono-Acylierung stehen.<br />
Eine Umsetzung von Säure<strong>de</strong>rivaten und Nitroverbindungen gelingt aus <strong>de</strong>m<br />
gleichen Grun<strong>de</strong> nicht, es sei <strong>de</strong>nn, noch zusätzlich vorhan<strong>de</strong>ne<br />
elektronendrücken<strong>de</strong> Gruppen (z.B. Methoxylgruppen) heben <strong>de</strong>n<br />
reaktionsbehin<strong>de</strong>rn<strong>de</strong>n Einfluß dieser Substituenten zweiter Ordnung auf.<br />
�<br />
�<br />
138
Als Lösungsmittel für die Reaktion dient Nitrobenzol, das wegen seiner Trägheit<br />
selbst nicht reagiert und wegen seiner hohen Polarität zur Lösung <strong>de</strong>s benötigten<br />
AlCl3 gut geeignet ist. Ebenso geeignet ist 1,2-Dichlorethan (Vorsicht: Sehr giftig,<br />
cancerogen).<br />
Der Ausschluss von Wasser und an<strong>de</strong>ren Verbindungen mit aktiven<br />
Wasserstoffatomen (Säuren) ist erfor<strong>de</strong>rlich, um eine Hydrolyse <strong>de</strong>r<br />
Säurechlori<strong>de</strong> zu vermei<strong>de</strong>n.<br />
Anstelle von Säurechlori<strong>de</strong>n können auch die etwas trägeren Anhydri<strong>de</strong><br />
eingesetzt wer<strong>de</strong>n. In diesem Falle ist aber min<strong>de</strong>stens eine 2 molare Menge an<br />
Katalysator erfor<strong>de</strong>rlich, ein Mol <strong>de</strong>s Katalysators wird hierbei zur<br />
Komplexbildung an <strong>de</strong>r Ketofunktion, das zweite zur Bindung <strong>de</strong>r entstehen<strong>de</strong>n<br />
Carbonsäure benötigt.<br />
Da die Reaktion reversibel ist, kann durch längere Reaktionszeit und verschärfte<br />
Reaktionsbedingungen (höhere Temperatur) eine zunächst im Zuge kinetischer<br />
Reaktionskontrolle überwiegend gebil<strong>de</strong>te Verbindung zum thermodynamisch<br />
stabileren Isomeren umgelagert wer<strong>de</strong>n, beispielsweise α-Acetylnaphthalin in<br />
das β-Acetylnaphthalin.<br />
H 3C<br />
C<br />
O<br />
Hitze<br />
AlCl 3<br />
O<br />
C<br />
CH 3<br />
Phenole wür<strong>de</strong>n mit <strong>de</strong>m Katalysator Salze bil<strong>de</strong>n. Daher setzt man in diesem<br />
Falle die Phenolester ein und lagert diese nach Zusatz.von AlCl3 in Nitrobenzol<br />
zum aromatischen Hydroxyketon um (Fries-Verschiebung).<br />
139
O C CH 3<br />
O<br />
Hitze<br />
AlCl 3<br />
HO C CH 3<br />
Bei höheren Temperaturen (150°C) bil<strong>de</strong>t sich überwiegend das o-Produkt.<br />
14.1.1 Frie<strong>de</strong>l-Crafts-Reaktion mit Alkylhalogeni<strong>de</strong>n<br />
Frie<strong>de</strong>l-Crafts-Reaktionen sind auch mit Alkylhalogeni<strong>de</strong>n durchführbar. Die<br />
dabei entstehen<strong>de</strong>n Alkylaromaten för<strong>de</strong>rn zufolge <strong>de</strong>s Elektronendrucks <strong>de</strong>r<br />
Alkylgruppe weitere elektrophile Substitutionsreaktionen, so dass<br />
Mehrfachsubstitutionsprodukte entstehen.<br />
Abgesehen davon läßt es sich nicht vermei<strong>de</strong>n. dass unter <strong>de</strong>r Einwirkung <strong>de</strong>s<br />
Katalysator die Alkylketten so rasch umgelagert wer<strong>de</strong>n, dass bevorzugt<br />
Reaktionsprodukte mit Verzweigung in <strong>de</strong>r Seitenkette gebil<strong>de</strong>t wer<strong>de</strong>n:<br />
H 3C CH 2 CH 2 Cl<br />
AlCl 3<br />
�<br />
AlCl4 H 3C CH 2 CH 2 Cl CH 2 CH 2 CH 3<br />
�<br />
�<br />
AlCl4 O<br />
CH 3<br />
H3C �<br />
CH Cl CH<br />
H3C CH3 Dieser Reaktion kommt daher zur Herstellung von aromatischen<br />
Kohlenwasserstoffen mit aliphatischer Seitenkette nur in Son<strong>de</strong>rfällen Be<strong>de</strong>utung<br />
zu. Statt Alkylhalogeni<strong>de</strong>n kann man bei dieser Reaktion auch Alkene einsetzen.<br />
Aromatische Kohlenwasserstoffe mit unverzweigten Seitenketten stellt man<br />
durch Acylierung nach Frie<strong>de</strong>l-Crafts- und nachfolgen<strong>de</strong> Clemmenson-Reduktion:<br />
140
C 2H 5<br />
AlCl 3<br />
C<br />
O<br />
Cl<br />
O<br />
C<br />
C 2H 5<br />
Red.<br />
CH 2<br />
C 2H 5<br />
Die Herstellung von Ketonen nach <strong>de</strong>r Houben-Hoesch-Synthese durch Umsetzung<br />
<strong>de</strong>s Aromaten mit einem Nitril bei Anwesenheit von Aluminiumchlorid wird im Kapitel<br />
14.2.2 gesprochen.<br />
14.2 Herstellung aromatischer Al<strong>de</strong>hy<strong>de</strong><br />
14.2.1 Gattermann-Koch-Synthese<br />
Zur Herstellung aromatischer Al<strong>de</strong>hy<strong>de</strong> könnte man in Analogie zur Herstellung von<br />
Ketonen, Aromaten mit Formylchlorid nach Frie<strong>de</strong>l-Grafts umsetzen. Formylchlorid<br />
selbst ist aber unbeständig, es zerfällt zu HCl und CO.<br />
Die Reaktion gelingt aber, wenn man Aromaten mit HCl und CO unter hohem<br />
Druck mit AlCl3 zusammenbringt. Die Verwendung <strong>de</strong>s Druckgefäßes läßt sich<br />
vermei<strong>de</strong>n, wenn <strong>de</strong>r Reaktion CuCl zugesetzt wird, das offensichtlich CO zu<br />
komplexieren und damit reaktionsfähiger zu machen vermag (Gattermann-Koch-<br />
Synthese).<br />
CH 3<br />
14.2.2 Gattermann-Synthese<br />
+ CO + HCl AlCl 3, CuCl<br />
Elektrophil:<br />
H C O �<br />
�<br />
AlCl4 H<br />
CH 3<br />
Als Formylierungsreagens sind aber auch wasserfreie Blausäure und HCl einsetzbar:<br />
Dabei erfolgt zunächst Addition von HCl, an die Blausäure unter Bildung <strong>de</strong>s<br />
unbeständigen Formimidchlorid, das <strong>de</strong>m Formylchlorid analog gebaut ist. Dieses<br />
C<br />
O<br />
141
eagiert nun unter Komplexbildung mit <strong>de</strong>m AlCl3, das elektrophil <strong>de</strong>n Aromaten angreift<br />
(Gattermann-Synthese):<br />
H C N + HCl H C NH<br />
H C NH<br />
Cl<br />
� �<br />
AlCl3 Cl<br />
� �<br />
AlCl 3<br />
bzw. H C N AlCl3 + HCl<br />
Das Hydrochlorid <strong>de</strong>s entstehen<strong>de</strong>n Aldimins zerfällt bei Säurebehandlung unter<br />
Hydrolyse zum Al<strong>de</strong>hyd:<br />
H 3CO<br />
+ H C NH<br />
H3CO H 3CO<br />
Cl<br />
� �<br />
AlCl3 C<br />
O<br />
H<br />
Setzt man anstelle <strong>de</strong>r HCN Nitrile ein, so erhält man aromatische Ketone<br />
(Houben-Hoesch-Synthese).<br />
+<br />
H �<br />
R C N + HCl<br />
C<br />
O<br />
R<br />
AlCl 3<br />
C<br />
C<br />
�<br />
H<br />
NH 2<br />
�<br />
NH 2<br />
R<br />
Cl<br />
�<br />
Cl<br />
�<br />
142
Das gefährliche Arbeiten mit wasserfreier Blausäure läßt sich<br />
vermei<strong>de</strong>n, wenn man <strong>de</strong>n nötigen Cyanwasserstoff aus Zn(CN)2<br />
durch Einleiten von Chlorwasserstoffgas in Freiheit setzt<br />
(Gattermann-Synthese).<br />
Die Gattermann-Synthese dient vorzugsweise zur Herstellung von Al<strong>de</strong>hy<strong>de</strong>n aus<br />
Phenolethern und Phenolen. Die Größe <strong>de</strong>s Reagens bedingt eine nahezu ausschließliche<br />
Formylierung in <strong>de</strong>r 4-Stellung.<br />
14.2.3 Vilsmeyer-Synthese<br />
Phenolether, Phenole, tertiäre aromatische Amine und beson<strong>de</strong>rs reaktive Aromaten<br />
können auch mit Hilfe <strong>de</strong>r Vilsmeyer-Synthese formyliert wer<strong>de</strong>n. Das<br />
Formylierungsreagenz ist in diesem Falle ein formyliertes sekundäres Amin<br />
(Dimethylformamid und N-Methyl-formanilid sind am gebräuchlichsten), <strong>de</strong>ssen<br />
Formylgruppe durch Umsatz mit Phosphoroxychlorid aktiviert wird:<br />
H 3 C<br />
H 3 C<br />
N<br />
C<br />
O<br />
H<br />
H 3 C<br />
H 3 C<br />
N<br />
+ POCl 3<br />
�<br />
C<br />
O<br />
H<br />
O Cl<br />
P<br />
Cl �<br />
Cl<br />
H 3 C<br />
H 3 C<br />
N<br />
�<br />
H 3 C<br />
H 3C<br />
H 3C<br />
H 3C<br />
C<br />
N<br />
N<br />
�<br />
O<br />
H<br />
C<br />
Cl<br />
C<br />
O Cl<br />
P<br />
Cl<br />
O<br />
H<br />
H<br />
�<br />
Cl<br />
Cl<br />
O Cl<br />
P<br />
Cl<br />
�<br />
PO2Cl2 Das so gebil<strong>de</strong>te Reagens mit positiver Partialladung am Formylkohlenstoffatom<br />
reagiert als Elektrophil mit <strong>de</strong>r aromatischen Verbindung zu einem<br />
143
Al<strong>de</strong>hydammoniak<strong>de</strong>rivat, das - wie für solche Verbindungen üblich - leicht einer<br />
Hydrolyse unterliegt:<br />
H 3C<br />
H 3C<br />
N<br />
�<br />
C<br />
�<br />
PO2Cl2 (H 3C) 2N<br />
H<br />
Cl<br />
+<br />
CH<br />
NR 2<br />
Cl<br />
NR 2<br />
H 2O<br />
-HCl<br />
- HN(CH 3) 2<br />
(H 3C) 2N<br />
H<br />
NR 2<br />
14.2.4 Weitere Herstellungsmetho<strong>de</strong>n von Al<strong>de</strong>hy<strong>de</strong>n und Ketonen<br />
H<br />
C<br />
O<br />
CH<br />
�<br />
NR 2<br />
Aromatische Al<strong>de</strong>hy<strong>de</strong> und Ketone sind überdies durch Oxidation entsprechen<strong>de</strong>r<br />
Alkohole zugänglich. Da Al<strong>de</strong>hy<strong>de</strong> leicht zu entsprechen<strong>de</strong>n Benzoesäure<strong>de</strong>rivaten<br />
weiter oxidiert wer<strong>de</strong>n, sind Umwege notwendig:<br />
Radikalische Dihalogenierung von Toluol und Derivaten, und anschließen<strong>de</strong><br />
Hydrolyse <strong>de</strong>r Reaktionsprodukte:<br />
Cl<br />
144
Cl Cl Cl �<br />
CH 3<br />
+ Cl �<br />
+ Cl �<br />
- HCl � Cl Cl<br />
CH2 - Cl �<br />
CH<br />
Cl<br />
Cl<br />
+ Cl �<br />
Cl Cl<br />
+ Cl<br />
- HCl<br />
�<br />
CH 2Cl<br />
Die Benzylstellung ist in aromatischen Verbindungen durch <strong>de</strong>n Aromaten<br />
aktiviert. Sie ist daher bevorzugt radikalisch angreifbar. Durch Lichteinwirkung<br />
ist Chlor spaltbar, das gebil<strong>de</strong>te Chloratom reagiert mit einer benzylständigen<br />
C-H-Bindung unter Abstraktion eines Wasserstoffatoms und eines durch<br />
Mesomerie stabilisierten Benzylradikals, das nun seinerseits wie<strong>de</strong>r mit einem<br />
Halogemolekül unter Bildung von Benzylchlorid weiterreagieren kann. Die<br />
Reaktion läßt sich nach Austausch von 2 Halogenatomen stoppen. Das<br />
Benzalchlorid ist im Zuge einer nukleophilen Substitutionsreaktion in <strong>de</strong>n<br />
Al<strong>de</strong>hyd überführbar.<br />
CH<br />
Cl<br />
Cl<br />
H 2O<br />
C O<br />
H<br />
Zur Überführung einer am aromatischen kernbstituierten Methylgruppe in eine<br />
Al<strong>de</strong>hydruppe kann eine verbesserte Variante <strong>de</strong>r veralteten Etard-Reaktion<br />
(Oxidation mit CrO2Cl2 in Schwefelkohlenstoff) dienen:<br />
Aktivierte benzylische C-H-Bindungen können oxidativ durch<br />
Chromsäureanhydrid in Essigsäureanhydrid/Essigsäure angegriffen wer<strong>de</strong>n. Der<br />
sich bil<strong>de</strong>n<strong>de</strong> Al<strong>de</strong>hyd wird sofort in das geminale Diacetat überführt und so vor<br />
weiterer Oxidation bewahrt. Das Diacetat ist leicht zum Al<strong>de</strong>hyd hydrolisierbar:<br />
CH<br />
�<br />
Cl<br />
145
CH 3<br />
Ac 2O<br />
in HOAc<br />
H2SO4 CrO 3<br />
CH C O<br />
OAc<br />
H2O OAc<br />
Blanc-Reaktion mit nachfolgen<strong>de</strong>r Sommelet-Reaktion<br />
Aromaten reagieren mit <strong>de</strong>m reaktivsten Al<strong>de</strong>hyd, <strong>de</strong>m Formal<strong>de</strong>hyd, in Gegenwart von<br />
Chlorwasserstoff und ZnCl2, AlCl3 o<strong>de</strong>r H3PO4 unter Chlormethylierumg (Blanc-sche<br />
Reaktion). Der protonierte Formal<strong>de</strong>hyd greift elektrophil <strong>de</strong>n Aromaten an:<br />
H C<br />
O<br />
H<br />
+ H �<br />
H C<br />
OH<br />
�<br />
OH<br />
+ H C<br />
H<br />
�<br />
H H<br />
�<br />
CH 2 OH<br />
+ H �<br />
- H2O H<br />
CH 2<br />
�<br />
CH2 OH<br />
+ Cl �<br />
Der so gebil<strong>de</strong>te Benzylalkohol neigt nach Protonierung am Sauerstoffatom zur<br />
Wasserabspaltung. Das entstehen<strong>de</strong> Benzylcarbenium-Ion (SN1-Reaktion) bil<strong>de</strong>t<br />
mit vorhan<strong>de</strong>nen Chloridionen das Benzylchlorid.<br />
Das reaktionsfreudige Benzylhalogenid setzt sich mit Hexamethylentetramin zu<br />
Benzylamin um.<br />
- H �<br />
CH 2<br />
H<br />
Cl<br />
146
CH 2<br />
CH 2<br />
Cl<br />
N<br />
N<br />
N<br />
N<br />
CH 2<br />
N CH2 CH N CH3 NH 2 H C<br />
+ H2O - CH3NH2 O<br />
H<br />
C O<br />
H<br />
Wahrscheinlich reagiert <strong>de</strong>r ebenfalls bei <strong>de</strong>r Hydrolyse von Hexamethylentetramin<br />
entstehen<strong>de</strong> Formal<strong>de</strong>hyd mit Benzylamin zu einer Schiff‘schen Base, aus <strong>de</strong>r nach<br />
Umlagerung und Hydrolyse Benzal<strong>de</strong>hyd entsteht.<br />
Nachweisreaktionen: Siehe Nachweis aliphatischer Ketone und Al<strong>de</strong>hy<strong>de</strong> (Kap. 7).<br />
15. Herstellung aromatischer Carbonsäuren<br />
15.1 Be<strong>de</strong>utung von Carbonsäuren für die Synthese<br />
Aromatische Carbonsäuren können in Form ihrer Derivate zur Einleitung von<br />
Aufbaureaktionen unter Bildung von C-C-Bindungen verwen<strong>de</strong>t wor<strong>de</strong>n.<br />
Beispielsweise läßt sich ein aromatisches Säurechlorid im Zuge einer Frie<strong>de</strong>l-Crafts-<br />
Acylierung mit einem zweiten aromatischen Rest verknüpfen:<br />
O<br />
C<br />
Cl +<br />
AlCl 3<br />
Die Acylgruppe kann aber auch im Zuge von Kon<strong>de</strong>nsationsreaktionen<br />
(Esterkon<strong>de</strong>nsation) zum Anbau einen aliphatischen Restes verwen<strong>de</strong>t wer<strong>de</strong>n:<br />
O<br />
C<br />
147
O<br />
C<br />
OR<br />
+<br />
H 3C C<br />
O<br />
OCH 3<br />
O<br />
C<br />
CH 2<br />
COOCH 3<br />
Aromatische Carbonsäuren sind also wichtige Vor- und Zwischenstufen für<br />
Synthesen.<br />
15.2 Herstellung aromatischer Säuren durch Grignard-Reaktion<br />
Ähnlich wie aliphatische Carbonsäuren können auch aromatische Carbonsäuren über<br />
eine Grignard-Reaktion hergestellt wer<strong>de</strong>n (Kap. 6). Die dazu benötigten aromatischen<br />
Halogeni<strong>de</strong> sind in <strong>de</strong>r Regel weniger reaktiv als aliphatische, weil das Halogenatom an<br />
<strong>de</strong>m aromatischen Rest fester gebun<strong>de</strong>n ist. Die Einleitung <strong>de</strong>r Reaktion bedarf daher<br />
vielfach <strong>de</strong>r Starthilfe, die durch Zusatz einer Spur von Methyliodid o<strong>de</strong>r<br />
Tetrachlorkohlenstoff gewährt wer<strong>de</strong>n kann. (Peinlicher Ausschluß von Wasser und<br />
Alkoholen ist selbstverständlich).<br />
In <strong>de</strong>r Regel wer<strong>de</strong>n die Bromi<strong>de</strong> <strong>de</strong>n Chlori<strong>de</strong>n vorgezogen, weil sie leichter erhältlich<br />
sind und außer<strong>de</strong>m höhere Reaktivität besitzen. Wenn ihre Reaktivität nicht ausreicht,<br />
muß man auf die schwerer zugänglichen lodi<strong>de</strong> zurückgreifen.<br />
15.3 Herstellung aromatischer Säuren durch Verseifung von Nitrilen<br />
Nur in Son<strong>de</strong>rfällen spielt die Verseifung <strong>de</strong>r Nitrile als Herstellungsverfahren<br />
aromatischer Säuren eine Rolle, <strong>de</strong>nn es muß dabei berücksichtigt wer<strong>de</strong>n, dass die<br />
Nitrile selbst meist nur in mäßigen Ausbeuten über die Sandmeyer-Reaktion o<strong>de</strong>r die<br />
Sulfonsäuren zugänglich sind.<br />
O<br />
C N C<br />
H2O OH<br />
15.4 Herstellung durch oxidativen Abbau von Seitenketten<br />
148
Das wohl wichtigste Verfahren zur Herstellung aromatischer aber auch von<br />
heterocyclischen Carbonsäuren - ist <strong>de</strong>r oxidative Abbau von Seitenketten:<br />
Die Benzylstellung ist wegen ihrer hohen Aktivität leicht oxidativ angreifbar, nicht aber<br />
<strong>de</strong>r aromatische Kern. So können Alkylbenzole in guten Ausbeuten mit Permanganat<br />
zu entsprechen<strong>de</strong>n Benzoesäure<strong>de</strong>rivaten abgebaut wer<strong>de</strong>n:<br />
CH 2 CH 2 CH 3<br />
KMnO 4<br />
O<br />
C<br />
OH<br />
+ H 3C C<br />
Das Naphthalinsystem ist ebenfalls oxidativ unter Abbau eines Ringes angreifbar:<br />
O 2<br />
V 2 O 5<br />
COOH<br />
COOH<br />
Diese Metho<strong>de</strong> ist ein geeignetes Verfahren zur Herstellung substituierter<br />
Phthalsäuren, mit elektronenziehen<strong>de</strong>n Substituenten, <strong>de</strong>nn <strong>de</strong>r oxidative Angriff<br />
erfolgt bevorzugt im unsubstituierten Ring:<br />
O 2N<br />
Ox.<br />
O 2N<br />
COOH<br />
COOH<br />
Will o<strong>de</strong>r muß man schonen<strong>de</strong>r oxidieren, z.B. bei Anwesenheit<br />
elektronendrücken<strong>de</strong>r Substituenten, so ist in <strong>de</strong>n Fällen, in <strong>de</strong>nen eine COCH3-<br />
Seitenkette vorhan<strong>de</strong>n ist, <strong>de</strong>r Abbau über die Haloform-Reaktion mit Vorteil<br />
anwendbar. Hierbei wird zunächst die Methylgruppe halogeniert, <strong>de</strong>r hohe<br />
Elektronenzug <strong>de</strong>r Trihalogenmethylgruppe bewirkt die durch Alkali katalysierte<br />
Bindungsspaltung:<br />
O<br />
OH<br />
149
O<br />
Ar C CH 3<br />
2 Br 2 + 2 OH �<br />
OH �<br />
- H 2O<br />
O<br />
Ar C<br />
- 2 H 2O - 2 Br � Ar C<br />
- �<br />
,&%U� Ar C<br />
O<br />
O<br />
OH<br />
�<br />
C<br />
CH 2<br />
Br<br />
Br<br />
Br<br />
+ �<br />
,&%U� Br Br<br />
- Br �<br />
OH �<br />
O<br />
Ar C<br />
O �<br />
CH 2<br />
Br<br />
Ar C C Br<br />
Ar C<br />
OH<br />
Br<br />
Br<br />
O + HCBr3<br />
O �<br />
Beispielsweise gelingt auf diesem Wege die Herstellung von β-Naphthoesäure:<br />
O<br />
C<br />
CH 3<br />
COOH<br />
Diese Reaktion ist nicht nur auf aromatische Methylketone<br />
beschränkt, son<strong>de</strong>rn auf alle Verbindungen, die die CH3-CO- Gruppe<br />
enthalten, anwendbar.<br />
Entsprechen<strong>de</strong> Alkohole wer<strong>de</strong>n durch das in <strong>de</strong>r Lösung vorhan<strong>de</strong>ne Hypohalogenit<br />
zunächst zum Keton aufoxidiert, das dann die Haloformspaltung eingeht.<br />
15.5 Nachweis und Charakterisierung<br />
150
Aromatische Carbonsäuren wer<strong>de</strong>n wie aliphatische Carbonsäuren am besten durch<br />
Überführung in ein Säureamid o<strong>de</strong>r -anilid charakterisiert.<br />
Das Äquivalentgewicht kann durch Titration ermittelt wer<strong>de</strong>n.<br />
16. Herstellung aromatischer Phenole und Chinone<br />
Im Gegensatz zu aliphatischen Alkoholen sind aromatische Alkohole (Phenole) aus<br />
entsprechen<strong>de</strong>n Halogeni<strong>de</strong>n nur unter sehr verschärften Bedingungen durch Umsatz<br />
mit Alkali erhältlich. Dies beruht darauf, dass aromatisch gebun<strong>de</strong>nes Halogen <strong>de</strong>m<br />
Angriff eines Nucleophils erheblichen Wi<strong>de</strong>rstand entgegensetzt:<br />
Cl<br />
hohe<br />
Elektronendichte<br />
�<br />
Cl<br />
�<br />
partielle<br />
Doppelbindung<br />
Elektronenziehen<strong>de</strong> Substituenten in o- und p-Stellung führen zu einer relativen<br />
Elektronenverarmung an <strong>de</strong>m Kohlenstoffatom, an <strong>de</strong>m das Halogen gebun<strong>de</strong>n<br />
ist. Damit wird ein nucleophiler Angriff erleichtert. Wenn zwei <strong>de</strong>rartige Gruppen<br />
vorhan<strong>de</strong>n sind, erfolgt bereits relativ bereitwillig ein Austausch gegen ein<br />
an<strong>de</strong>res Nucleophil, z.B. OH; drei Nitrogruppen machen das aromatisch<br />
gebun<strong>de</strong>ne Halogen bereits so beweglich, dass es nahezu ähnlich leicht<br />
austauschbar ist wie in einem Säurechlorid:<br />
151
�<br />
O �<br />
N<br />
Cl<br />
�<br />
N<br />
�<br />
O<br />
�<br />
O �<br />
N<br />
Cl<br />
O<br />
O O<br />
�<br />
O<br />
O 2N<br />
N<br />
Cl<br />
O<br />
OH<br />
NO 2<br />
�<br />
N<br />
O<br />
O<br />
�<br />
�<br />
- Cl �<br />
�<br />
O<br />
O 2N<br />
N<br />
O<br />
�<br />
N<br />
OH<br />
NO 2<br />
O<br />
O<br />
�<br />
�<br />
NO 2<br />
+ OH �<br />
Bei <strong>de</strong>r Herstellung von Phenol aus Chlorbenzol im sogenannten Raschig-<br />
Verfahren erfolgt kein nucleophiler Austausch, son<strong>de</strong>rn die Reaktion läuft über<br />
die Zwischenstufe <strong>de</strong>r Arine: Hierbei wird durch das Alkali aus <strong>de</strong>m Benzol unter<br />
Ausbildung von Dehydrobenzol HCl eliminiert. Das so gebil<strong>de</strong>te Arin reagiert<br />
sofort weiter unter Wasseranlagerung:<br />
H<br />
Cl<br />
*<br />
- HCl<br />
*<br />
+ H 2O<br />
+ H 2O<br />
HO<br />
OH<br />
*<br />
*<br />
152
Der-Reaktionsverlauf ließ sich durch Markierung <strong>de</strong>s Kohlenstoffatoms<br />
nachweisen, <strong>de</strong>r ursprünglich das Halogenatom trug: Im gebil<strong>de</strong>ten Phenol<br />
verteilte sich die Markierung sowohl auf das C-Atom, das die OH-Gruppe trägt als<br />
auch auf, die benachbarten C-Atome (Nachweis durch Abbaureaktionen).<br />
Das Verfahren ist zwar zur Herstellung von Phenol in industriellem Maßstab<br />
anwendbar, nicht aber zur Synthese von Phenolen im Labor:<br />
Hier benutzt man in <strong>de</strong>r Regel zur Herstellung komplexer Phenole <strong>de</strong>n Weg über die<br />
Nitro-Verbindungen, die zu <strong>de</strong>n Aminen reduziert wer<strong>de</strong>n und dann nach Diazotierung<br />
zum Phenol verkocht wer<strong>de</strong>n: Das Diazoniumsalz ist in <strong>de</strong>r Hitze unbeständig und<br />
zerfällt beim Erwärmen zu einem Carbenium-Ion, das sofort mit vorhan<strong>de</strong>nem Wasser<br />
o<strong>de</strong>r an<strong>de</strong>ren Nucleophilen in Reaktion tritt. Erhitzt man daher das Diazoniumsalz in<br />
wäßriger Lösung, erhält man im wesentlichen nur das Phenol:<br />
� Hitze<br />
N N<br />
- N2 �<br />
H 2O<br />
- H �<br />
Ein weiterer, teilweise im Labor, hauptsächlich aber industriell angewandtes<br />
Verfahren zur Herstellung von Phenolen besteht in <strong>de</strong>r KOH-Schmelze <strong>de</strong>r<br />
Sulfonsäuren:<br />
SO 3H<br />
KOH<br />
Hock'sche Phenolsynthese:<br />
Cumolhydroperoxid zerfällt beim Behan<strong>de</strong>ln mit verdünnten Mineralsäuren zu Aceton<br />
und Phenol:<br />
OH<br />
OH<br />
153
H 3C<br />
C<br />
CH 3<br />
O OH<br />
H �<br />
OH<br />
+ H 3C<br />
O<br />
C<br />
CH 3<br />
In Westeuropa wer<strong>de</strong>n mehr als 90 % <strong>de</strong>s benötigten Phenols nach diesem, erst in <strong>de</strong>n<br />
50er Jahren in <strong>de</strong>r Technik eingeführten Verfahren hergestellt. Cumolhydroperoxid<br />
entsteht bereits durch Autoxidation im Zuge einer Radikalkettenreaktion. In <strong>de</strong>r<br />
Technik erfolgt die Oxidation katalytisch an Kupfer-, Mangan- o<strong>de</strong>r Kobaltsalzen.<br />
H 3C<br />
CH<br />
CH 3<br />
O O �<br />
�<br />
H 3C<br />
C<br />
CH 3<br />
O OH<br />
Cumolhydroperoxid wird bei <strong>de</strong>r Zersetzung an <strong>de</strong>r Peroxidgruppe protoniert,<br />
spaltet Wasser ab, lagert sich unter Wan<strong>de</strong>rung <strong>de</strong>s Phenylrestes um und lagert<br />
wie<strong>de</strong>r Wasser an:<br />
H 3C<br />
CH 3<br />
C<br />
O<br />
O<br />
H3C H A C<br />
H<br />
- A �<br />
- H 2O<br />
Dieses Halbacetal zerfällt zu Aceton und Phenol.<br />
�<br />
O<br />
CH 3<br />
+ H 2O<br />
- HA<br />
H 3C<br />
C<br />
O<br />
CH 3<br />
OH<br />
154
H 3C<br />
C<br />
O<br />
CH 3<br />
OH<br />
OH<br />
+<br />
H 3C<br />
O<br />
C<br />
CH 3<br />
Das gleichzeitig entstehen<strong>de</strong> Aceton ist ebenfalls ein willkommenes Produkt<br />
(Lösungsmittel, Syntheseausgangsstoff).<br />
Phenole sind äußerst oxidationsempfindlich, vor allem in alkalischer Lösung. Die<br />
Oxidationsempfindlichkeit wird durch zusätzlich vorhan<strong>de</strong>ne OH- und NH2-Gruppen<br />
noch weiter gesteigert, vor allem, wenn diese in 2- o<strong>de</strong>r 4-Stellung stehen Dabei wird<br />
z.B. aus <strong>de</strong>m 4-Dihydroxybenzol (Hydrochinon) p-Chinon gebil<strong>de</strong>t, während aus <strong>de</strong>m<br />
entsprechen<strong>de</strong>n 2-Dihydroxybenzol (Brenzkatechin) das entstehen<strong>de</strong> o-Chinon so<br />
leicht weiter oxidativ abgebaut wer<strong>de</strong>n kann, dass es lange Zeit für nicht herstellbar<br />
galt.<br />
OH<br />
OH<br />
Ox.<br />
O<br />
O<br />
Hydrochinon p-Benzochinon Brenzkatechin o-Benzochinon<br />
Wegen ihrer hohen Oxidationsempfindlichkeit wer<strong>de</strong>n daher Verbindungen dieses Typs<br />
als photographische Entwickler eingesetzt.<br />
In mehrkernigen kon<strong>de</strong>nsierten Aromaten ist <strong>de</strong>r aromatische Charakter <strong>de</strong>r<br />
mittleren Ringe eingeschränkt. Durch Oxidation <strong>de</strong>r mittleren<br />
Ringkohlenstoffatome unter Bildung von Chinonen behalten die äußeren Ringe<br />
OH<br />
OH<br />
Ox.<br />
O<br />
O<br />
155
ihren vollen aromatischen Charakter bei. Solche Systeme sind daher ebenfalls<br />
oxidativ angreifbar:<br />
Ox.<br />
O<br />
Anthracen Anthrachinon<br />
o-chinoi<strong>de</strong> Verbindungen erlei<strong>de</strong>n allerdings leicht Weiteroxidation unter<br />
Ringöffnung:<br />
Ox.<br />
O<br />
O<br />
O<br />
COOH<br />
COOH<br />
Will man mit Phenolen arbeiten, so müssen daher vielfach die vorhan<strong>de</strong>nen OH-<br />
Gruppen geschützt wer<strong>de</strong>n. Dies gelingt durch Veretherung o<strong>de</strong>r Veresterung.<br />
Zur Veretherung verwen<strong>de</strong>t man meist Diazomethan, das mit einem Phenol<br />
wegen seines sauren Charakters unter Etherbildung reagiert:<br />
OH<br />
� �<br />
+ N N<br />
CH 2<br />
- N 2<br />
O CH 3<br />
156
Schutz durch Acylierung wird durch Umsatz mit einem Säureanhydrid o<strong>de</strong>r noch<br />
besser mit einem Säurehalogenid erreicht. Derivate, die durch Acylierung<br />
erhältlich sind, kristallisieren im allgemeinen gut und sind daher wichtige<br />
Reagenzien zur Charakterisierung von Phenolen.<br />
16.1 Nachweis von Phenolen<br />
Der qualitative Phenolnachweis ist durch die Fe 3�<br />
-chlorid-Reaktion zu führen: Eine<br />
winzige Probe <strong>de</strong>s Phenols, in einem Tropfen Alkohol gelöst, verfärbt sich nach Zusatz<br />
von Alkali und einem Tropfen Fe 3�<br />
, weil das Enolsystem mit <strong>de</strong>m Eisen einen<br />
Farbkomplex bil<strong>de</strong>n kann.<br />
Praktikumsversuche 7-10: Halogenierung am Aromaten, Sandmeyer-Reaktion,<br />
Vilsmeier-Formylierung, Frie<strong>de</strong>l-Crafts-Acylierung, Haloform-Reaktion,<br />
Herstellung eines aromatischen Amins.<br />
17. Knüpfen von Kohlenstoff-Kohlenstoff-Bindungen<br />
1 Einleitung<br />
Bisher haben wir uns im wesentlichen mit <strong>de</strong>m Austausch o<strong>de</strong>r <strong>de</strong>r Einführung<br />
funktioneller Gruppen in organische Moleküle beschäftigt. Die organische Synthese<br />
beruht aber hauptsächlich auf <strong>de</strong>m Aufbau komplexer Moleküle durch Knüpfen von<br />
Kohlenstoff-Kohlenstoff-Bindungen.<br />
Die Grignard-Reaktion, die wir bereits kennenlernten, ist eine solche vielfach<br />
angewandte Aufbaureaktion. Auch <strong>de</strong>r Austausch eines Halogenatoms gegen eine<br />
Nitrilgruppe ist als Aufbaureaktion zu werten, weil so ein zusätzliches Kohlenstoffatom<br />
in die Verbindung eingeführt wird.<br />
In diesem Kapitel sollen weitere Aufbaureaktionen besprochen wer<strong>de</strong>n.<br />
18. Aufbaureaktionen, die die Kohlenstoffkette um 1 C-Atom verlängern<br />
157
Aus Vollständigkeitsgrün<strong>de</strong>n wollen wir unter diesem Gesichtspunkt (Einführung eines<br />
zusätzlichen C-Atoms in das Molekül), zunächst die bereits besprochenen Reaktionen<br />
noch einmal kurz anführen:<br />
a) Grignard-Reaktion mit CO2:<br />
R X + Mg<br />
RCOOMgX<br />
Ether<br />
H �<br />
RMgX<br />
R COOH<br />
b) Ersatz eon Halogen gegen CN (Kolbe-Synthese):<br />
c) Wittig-Reaktion:<br />
R CH 2 C<br />
R CH 2<br />
d) Chlormethylierung:<br />
R<br />
CN<br />
R X R CN<br />
�<br />
O<br />
H<br />
CH CH 2<br />
O<br />
+ H 2C P(C 6H 5) 3<br />
P(C 6H 5) 3<br />
H C<br />
O<br />
H<br />
HCl / H 3PO 4<br />
e) Formylierung von aromatischen Verbindungen:<br />
e1) Vilsmeyer-Synthese:<br />
CO 2<br />
R CH 2 CH CH 2<br />
R<br />
CH 2Cl<br />
158
N<br />
CH 3<br />
CH 3<br />
H 3C<br />
H 3C<br />
POCl 3<br />
e2) Gattermann- und Gattermann/Koch-Synthese:<br />
N<br />
C<br />
CO / HCl<br />
bzw.<br />
HO<br />
HCN / HCl<br />
HO<br />
Folgen<strong>de</strong> Metho<strong>de</strong>n <strong>de</strong>r Kettenverlängerung um ein C-Atom wur<strong>de</strong>n noch nicht<br />
diskutiert:<br />
Bei <strong>de</strong>r Arndt-Eistert Reaktion wird ein Saurechlorid mit Diazomethan zu einem<br />
Diazoketon umgesetzt, wobei das nucleophile Kohlenstoffatom <strong>de</strong>s Diazomethans am<br />
Carbonylkohlenstoffatom <strong>de</strong>r Säure angreift. Im Reaktionsprodukt drängt das negativ<br />
gela<strong>de</strong>ne Sauerstoffatom das Halogenatom aus <strong>de</strong>m Molekülverband. In <strong>de</strong>r Folge<br />
kommt es zur Abspaltung eines Protons und damit zur Ausbildung <strong>de</strong>s Diazoketons.<br />
Dieses zerfällt in Gegenwart von Silber unter Stickstoffabspaltung. In <strong>de</strong>m nicht<br />
fafbaren Reaktionsprodukt ist am Kohlenstoff ein Elektronensextett. Solche<br />
Zwischenprodukte mit "Carben"-Struktur neigen zu einer Wolff-Umlagerung, bei <strong>de</strong>r <strong>de</strong>r<br />
Alkylrest an das Kohlenstoffatom wan<strong>de</strong>rt, wobei sich ein Keten ausbil<strong>de</strong>t; dieses<br />
reagiert sofort mit Lösungsmittel (H20 o<strong>de</strong>r Alkohol) zu einer Saure bzw. einem Ester:<br />
O<br />
H<br />
O<br />
C<br />
H<br />
C<br />
N<br />
O<br />
H<br />
CH 3<br />
CH 3<br />
159
R C<br />
O<br />
Cl<br />
+ H 2C<br />
O<br />
H<br />
N N � �<br />
�<br />
R C CH N N<br />
R C<br />
Cl �<br />
O<br />
CH<br />
ein Carben<br />
R CH C O<br />
ein Keten<br />
- HCl<br />
- N 2<br />
R C<br />
O<br />
R C<br />
O<br />
O<br />
Cl<br />
�<br />
CH 2<br />
CH N N � �<br />
�<br />
R C CH N N<br />
�<br />
+ H 2O<br />
�<br />
N N<br />
R CH 2 COOH<br />
In ähnlicher Weise lassen sich auch Methylgruppen in Al<strong>de</strong>hy<strong>de</strong> o<strong>de</strong>r Ketone<br />
einschieben:<br />
R C<br />
O<br />
H<br />
+ H2C N N � �<br />
O<br />
�<br />
�<br />
R C N N<br />
H<br />
CH 2<br />
In <strong>de</strong>m primären Reaktionsprodukt ist im Gegensatz zu <strong>de</strong>m Produkt, das aus<br />
Säurechlorid und Diazomethan entsteht, keine gut eliminierbare Gruppe (H �<br />
kann im<br />
Gegensatz zu Cl �<br />
nicht abgespalten wer<strong>de</strong>n) vorhan<strong>de</strong>n. Eine Stabilisierung ist daher<br />
nicht möglich, <strong>de</strong>shalb erfolgt Stickstoffabspaltung. Das entstan<strong>de</strong>ne Produkt lagert<br />
sich unter Wan<strong>de</strong>rung <strong>de</strong>s Restes R um:<br />
160
�<br />
R<br />
O<br />
CH<br />
�<br />
N N<br />
- N2 R CH2 C<br />
CH 2<br />
Es entsteht so ein um ein C-Atom längerer Al<strong>de</strong>hyd.<br />
Be<strong>de</strong>utung hat diese Reaktion vor allem zur Ringerweiterung gewonnen, da<br />
hierbei einheitliche Produkte entstehen, während bei Ketonen mit verschie<strong>de</strong>n<br />
langen Alkylresten schwer trennbare Gemische erhalten wer<strong>de</strong>n, so dass die<br />
Reaktion für synthetische Zwecke nur beschränkt brauchbar ist.<br />
O<br />
Cyclohexanon<br />
Cyanhydrin-Synthese:<br />
+ H2C N N � �<br />
Al<strong>de</strong>hy<strong>de</strong> reagieren mit Cyanid-Ionen unter Addition:<br />
R C<br />
O<br />
H<br />
O<br />
�<br />
CH 2<br />
O<br />
H<br />
- N 2<br />
O<br />
Cycloheptanon<br />
O<br />
+ HCN R C C N<br />
H<br />
H<br />
Cyanhydrin<br />
�<br />
N N<br />
161
Blausäure ist nur wenig dissoziiert und es müssen daher zur Freisetzung <strong>de</strong>r<br />
Cyanidionen basische Katalysatoren zugesetzt wer<strong>de</strong>n (Alkalicyani<strong>de</strong>,<br />
Alkalicarbonate usw.). Üblicherweise verwen<strong>de</strong>t man daher Cyanidsalze, aus<br />
<strong>de</strong>nen man durch Zutropfen von Säure die Cyanidionen freisetzt und gera<strong>de</strong> <strong>de</strong>n<br />
zur Reaktion optimalen pH-Wert einstellt (durch Protonenzusatz wird die<br />
Carbonylaktivität erhöht, Anlagerung von H �<br />
an das Carbonylsauerstoffatom).<br />
Die Reaktion ist reversibel. Insbeson<strong>de</strong>re sind Cyanhydrine empfindlich gegen<br />
Basen und thermische Beanspruchung. Sie wer<strong>de</strong>n daher nur als<br />
Zwischenprodukt verwen<strong>de</strong>t, aus <strong>de</strong>nen man durch saure Verseifung α-Hydroxy-<br />
Carbonsäuren herstellt.<br />
O<br />
H<br />
R C C N<br />
H<br />
Cyanhydrin<br />
H 2O (H �<br />
OH<br />
R CH<br />
COOH<br />
Vorsicht!!! Unter gut ziehen<strong>de</strong>m Abzug arbeiten, Handschuhe tragen,<br />
Entsorgung sichern (Cyanid-Abfallflasche, pH basisch).<br />
Umsatz von Formal<strong>de</strong>hyd mit Acetyli<strong>de</strong>n (Ethinylierung):<br />
Acetyli<strong>de</strong> reagieren mit Formal<strong>de</strong>hyd unter Bildung von Derivaten <strong>de</strong>s<br />
Propargylalkohols:<br />
R C C �<br />
Na �<br />
Na-Acetylenid<br />
+ H C<br />
O<br />
H<br />
R C C Na �<br />
CH2 O �<br />
Das Acetylenid wird durch Eintragen <strong>de</strong>r Acetylenverbindung in ein Gefäß, in <strong>de</strong>m<br />
man flüssigen Ammoniak mit metallischem Natrium versetzt hat (Bildung von<br />
162
Natriumamid) erhalten. Dabei entzieht das Natriumamid <strong>de</strong>r Acetylverbindung<br />
unter Ammoniak-bildung ein Proton. Das Anion kann nun mit zugesetztem<br />
Formal<strong>de</strong>hyd zur Reaktion gebracht wer<strong>de</strong>n.<br />
Diese Reaktion hat vorzugsweise Be<strong>de</strong>utung für Synthesen im technischen<br />
Maßstab. Beispielsweise kann man auf diese Weise durch Umsatz von Acetylen<br />
mit 2 Mol Formal<strong>de</strong>hyd und nachfolgen<strong>de</strong> Hydrierung 1,4-Butandiol gewinnen:<br />
Na + NH 3<br />
NaNH 2 + ½ H 2<br />
HC CH + 2 NaNH 2 Na �<br />
Na �<br />
�<br />
O<br />
HO<br />
CH 2<br />
CH 2<br />
CH 2<br />
� �<br />
C C<br />
Na �<br />
+ 2 H 2C=O<br />
+ 2 NH 3<br />
C C Na �<br />
CH2 O �<br />
+ H 2O<br />
C C CH 2<br />
OH<br />
HO CH 2 OH<br />
CH 2<br />
+ 2 H 2<br />
CH 2<br />
Daraus ist durch Wasserabspaltung Butadien herstellbar. Allerdings ist dieses<br />
Verfahren heute zur Butadien-Herstellung nicht mehr konkurrenzfähig.<br />
Aminomethylierung (Mannich-Reaktion):<br />
Als Mannich-Reaktion bezeichnet man die Umsetzung von Formal<strong>de</strong>hyd und einem<br />
sekundären Amin mit einer C-H-aci<strong>de</strong>n Verbindung (z.B. Keton), dabei wird die C-Haci<strong>de</strong><br />
Verbindung aminomethyliert.<br />
163
Sekundäre Amine setzen sich mit Formal<strong>de</strong>hyd folgen<strong>de</strong>rmaßen um:<br />
R<br />
R<br />
�<br />
NH 2<br />
Cl<br />
�<br />
+<br />
H<br />
C<br />
O<br />
H<br />
R<br />
�<br />
R<br />
�<br />
Cl<br />
NH<br />
OH<br />
C<br />
H<br />
H<br />
- H 2O<br />
R<br />
R<br />
�<br />
N CH 2<br />
Das entstehen<strong>de</strong> Kation, das ein N-analoges Formal<strong>de</strong>hyd<strong>de</strong>rivat darstellt, besitzt<br />
wie Formal<strong>de</strong>hyd eine starke Neigung mit nucleophilen Reagenzien in Reaktion<br />
zu treten. Als nucleophiles Reagens kann z.B. ein in <strong>de</strong>r Enolform vorliegen<strong>de</strong>s<br />
Keton (C-H-aci<strong>de</strong> Verbindung) wirken:<br />
O<br />
C<br />
R<br />
R<br />
C H<br />
R<br />
+ �<br />
O C C CH2 NH<br />
R<br />
R<br />
R<br />
Cl �<br />
HO<br />
R<br />
R<br />
6DO] GHU 0DQQLFK %DVH<br />
�<br />
C<br />
R<br />
R<br />
C H<br />
R<br />
R<br />
R<br />
�<br />
Cl<br />
N CH 2<br />
Als C-H-aci<strong>de</strong> Verbindungen sind Al<strong>de</strong>hy<strong>de</strong>, Ketone, aber auch aliphatische<br />
Nitroverbindungen und Acetylen einsetzbar. Verbindungen mit beson<strong>de</strong>rs hoher<br />
C-H-Acidität wie Malonester reagieren mit Formal<strong>de</strong>hyd unter Aldolkon<strong>de</strong>nsation,<br />
weil in diesem Falle sich <strong>de</strong>r Formal<strong>de</strong>hyd bevorzug mit <strong>de</strong>m stärker<br />
nucleophilen Partner (Malonester) umsetzt.<br />
Merke: Mannich-Basen kann man nur erhalten, wenn das eingesetzte Amin eine<br />
höhere nucleophile Kraft besitzt als die C-H-aci<strong>de</strong> Verbindung!<br />
Da in zu stark saurer Lösung das freie Amin<br />
+ �<br />
+ �<br />
�<br />
Cl<br />
�<br />
164
R<br />
R<br />
�<br />
NH 2<br />
R<br />
R<br />
NH +�<br />
aufgrund obiger Gleichgewichtsbedingungen nur in geringer Konzentration vorliegt,<br />
aber an<strong>de</strong>rerseits die Aktivität <strong>de</strong>r C-H-aci<strong>de</strong>n Verbindung mit zunehmen<strong>de</strong>r H �<br />
-<br />
Ionenkonzentration ansteigt, gibt es für je<strong>de</strong> Mannich-Reaktion ein pH-Optimum.<br />
Primäre Amine reagieren unter Ersatz aller am Stickstoff befindlichen<br />
Wasserstoffatome:<br />
Cl<br />
�<br />
R<br />
O C CH2 NH<br />
R<br />
�<br />
CH2 H<br />
6DO] GHU 0DQQLFK %DVH<br />
Bei Umsatz mit einem primären Amin:<br />
O C CH2 NH R<br />
R<br />
+<br />
CH 2<br />
R<br />
HO C C<br />
+<br />
H<br />
C<br />
O<br />
H<br />
+ H � �� ��<br />
O C CH2 R<br />
CH 2<br />
O C CH2 R<br />
CH 2<br />
R<br />
�<br />
O C CH2 NH R<br />
R<br />
CH 2<br />
+ H � + Cl �<br />
O C CH2 CH2 N CH2 R<br />
R<br />
CH 2<br />
R<br />
N CH 2 C<br />
CH 2<br />
CH 2<br />
R<br />
NH C O<br />
R<br />
�<br />
OH<br />
�<br />
165
Hat eine Methylenkomponente mehr als eine reaktionsfähige Methyl- o<strong>de</strong>r<br />
Methylengruppe, so erhält man oft Bis-Mannich-Basen, weil doppelter Umsatz möglich<br />
ist:<br />
O<br />
H3C CH3 HNR2 ,H2C O<br />
CH2 C CH2 - H2O H 3 C<br />
CH<br />
O<br />
C<br />
CH<br />
CH 3<br />
R2N CH2 CH NR 2 2<br />
In diesen Fällen muß man zur Vermeidung <strong>de</strong>s doppelten Umsatzes mit einem<br />
großen Überschuß an C-H-aci<strong>de</strong>r Verbindung arbeiten.<br />
Auch Phenole und manche Heterocyclen (Indol, Thiophen), die mit hoher Neigung<br />
im Zuge elektrophiler Substitution angegriffen wer<strong>de</strong>n, bil<strong>de</strong>n Mannichprodukte:<br />
N<br />
H<br />
+ HNMe 2 + HCHO<br />
- H 2O<br />
N H<br />
CH 2<br />
NMe 2<br />
Mannich-Basen von Carbonylverbindungen gehen bereits beim Erhitzen unter<br />
Eliminierung in entsprechen<strong>de</strong> α,β−ungesättigte Verbindungen über.<br />
Glyci<strong>de</strong>stersynthese zur Herstellung von Al<strong>de</strong>hy<strong>de</strong>n:<br />
In α-halogenierten Fettsäureestern sind die anständigen Wasserstoffatome durch <strong>de</strong>n<br />
induktiven Effekt <strong>de</strong>s Halogenatoms und <strong>de</strong>n Elektronenzug <strong>de</strong>r Carbonylgruppe<br />
beson<strong>de</strong>rs aktiviert. Solche Verbindungen können sich mit Al<strong>de</strong>hy<strong>de</strong>n o<strong>de</strong>r Ketonen<br />
nach <strong>de</strong>m Prinzip einer Aldolkon<strong>de</strong>nsation umsetzen:<br />
166
H CH COOR + O R<br />
Cl<br />
O<br />
R<br />
C CH COOR<br />
R<br />
2,3-Epoxyester<br />
(Glyci<strong>de</strong>ster)<br />
�<br />
- Cl �<br />
R<br />
R<br />
R<br />
�<br />
O<br />
C<br />
R<br />
�<br />
CH<br />
Cl<br />
C O<br />
CH<br />
Cl<br />
COOR<br />
COOR<br />
+ ROH<br />
Die so gebil<strong>de</strong>ten Epoxi<strong>de</strong> <strong>de</strong>carboxylieren bei <strong>de</strong>r Verseifung unter Bildung eines<br />
Al<strong>de</strong>hyds.<br />
R<br />
R<br />
O<br />
C<br />
H<br />
CH<br />
O<br />
C<br />
O<br />
19. Einführung von 2 Kohlenstoffatomen<br />
Ethinylierung:<br />
R<br />
R<br />
C<br />
R<br />
CH<br />
R<br />
In Acetylen ist <strong>de</strong>r Wasserstoff etwas aci<strong>de</strong> und daher mit Basen ablösbar. Das so<br />
gebil<strong>de</strong>te nucleophile Reagens kann mit einem Keton unter Ethinylierung in Reaktion<br />
treten:<br />
CH<br />
C<br />
O<br />
O<br />
H<br />
H<br />
+<br />
O<br />
C<br />
O<br />
167
Als Base wird meistens Natriumamid in flüssigem Ammoniak angewandt<br />
(metallisches Natrium wird in flüssigen Ammoniak gegeben und dann die<br />
Carbonylverbindung zugefügt).<br />
Na + NH 3<br />
Na �<br />
�<br />
NH2 HC CH + Na � �<br />
C<br />
NH 2<br />
R OH<br />
C<br />
R C CH<br />
H �<br />
R<br />
R<br />
R<br />
R<br />
�<br />
+ ½<br />
C O<br />
C<br />
O<br />
H 2<br />
CH<br />
�<br />
C CH<br />
+ NH 3<br />
Natriumamid muß in min<strong>de</strong>stens molaren Mengen vorliegen, da das entstehen<strong>de</strong><br />
Ethinylcarbinol-Anion erst nach been<strong>de</strong>ter Reaktion und Verdampfen <strong>de</strong>s<br />
Ammoniaks mit angesäuertem Wasser zersetzt wird.<br />
Aliphatische Ketone reagieren auch schon mit Ätzkali als Katalysator, wobei man<br />
meist in schwer flüchtigen Ethern, wie Diethylenglycoldimethylether<br />
H3CO-CH2-CH2-O-CH2-CH2-OCH3 („diglyme“) arbeitet.<br />
HC CH + OH C<br />
�<br />
R OH<br />
C<br />
R C CH<br />
H2O - OH �<br />
R<br />
R<br />
R<br />
R<br />
�<br />
C O<br />
C<br />
O<br />
CH<br />
�<br />
C CH<br />
+ H 2O<br />
168
Al<strong>de</strong>hy<strong>de</strong> lassen sich auf diese Weise nicht „ethinylieren“, weil die zur Reaktion<br />
benötigte Base eine Aldolkon<strong>de</strong>nsation zweier Al<strong>de</strong>hydmoleküle so begünstigen<br />
wür<strong>de</strong>, dass die Ethinylierung praktisch nicht eintreten könnte.<br />
Bei <strong>de</strong>r Verwendung von Kupferacetylenid statt Acetylen gelingt jedoch auch eine<br />
Umsetzung mit Al<strong>de</strong>hy<strong>de</strong>n.<br />
Die Metho<strong>de</strong> hat industrielle Be<strong>de</strong>utung, beispielsweise stellt man auf diese<br />
HO<br />
Weise Derivate von Steroidhormonen (Verhütungsmittel) her:<br />
Östron<br />
Malonesterkon<strong>de</strong>nsation:<br />
O<br />
HC CH<br />
+ Na + NH 3<br />
HO<br />
17α -Ethinyl<br />
Östradiol<br />
OH<br />
C CH<br />
In Malonestern sind die Wasserstoffatome <strong>de</strong>r zwischen <strong>de</strong>n Carbonylgruppen<br />
sitzen<strong>de</strong>n Methylengruppen durch zwei Carbonylgruppen aktiviert und daher beson<strong>de</strong>rs<br />
leicht unter Basenkatalyse (Zusatz von Alkoholat) entfernbar, weil so ein durch<br />
Mesomerie sehr gut stabilisiertes Anion entstehen kann:<br />
COOR<br />
C<br />
H<br />
H<br />
COOR<br />
+ B �<br />
- HB<br />
C<br />
C<br />
�<br />
O<br />
OR<br />
H<br />
COOR<br />
C<br />
C<br />
O<br />
OR<br />
H<br />
COOR<br />
�<br />
COOR<br />
Der so herstellbare Natriummalonester ist ein starkes nucleophiles Reagens, das<br />
mit Alkylhalogeni<strong>de</strong>n und Acylhalogeni<strong>de</strong>n in üblicher Weise reagiert:<br />
C<br />
C<br />
H<br />
O<br />
�<br />
OR<br />
169
COOR<br />
C<br />
��<br />
H<br />
COOR<br />
+ R X<br />
- X �<br />
R C<br />
O<br />
X<br />
COOR<br />
CH R C<br />
COOR<br />
+ C<br />
COOR<br />
��<br />
H<br />
COOR<br />
COOR<br />
��<br />
H<br />
COOR<br />
- X �<br />
+<br />
R<br />
R C<br />
R C<br />
O<br />
C<br />
�<br />
O<br />
X<br />
COOR<br />
CH<br />
COOR<br />
- X �<br />
COOR<br />
C H<br />
COOR<br />
COOR<br />
O<br />
CH<br />
COOR<br />
Durch Verseifung <strong>de</strong>r Estergruppen entsteht eine β-Carbonylverbindung, die<br />
Decarboxylierung erlei<strong>de</strong>t:<br />
R<br />
O<br />
C<br />
HO<br />
CH<br />
O<br />
C<br />
C<br />
O<br />
O<br />
H<br />
- CO 2<br />
O<br />
X<br />
R C CH C<br />
R<br />
O<br />
O<br />
C<br />
CH 2<br />
Die Malonestersynthese stellt somit eine Metho<strong>de</strong> dar, um eine Carbonsäure nach<br />
LiAlH4-Reduktion ihres Esters zum entsprechen<strong>de</strong>n primären Alkohol über das<br />
primäre Alkylhalogenid um zwei Kohlenstoffatome zu verlängern:<br />
C<br />
OH<br />
OH<br />
O<br />
OH<br />
C<br />
R<br />
170
R C<br />
HBr<br />
H 2O<br />
O<br />
OH<br />
ROH<br />
H �<br />
R CH 2 Br<br />
R C<br />
�<br />
CH<br />
O<br />
COOR<br />
COOR<br />
- Br �<br />
R CH 2 CH 2 C<br />
OR<br />
¼ LiAlH 4<br />
R CH 2 CH<br />
R CH 2 OH<br />
COOR<br />
COOR<br />
Da die nucleophile Kraft <strong>de</strong>s Malonesteranions durch Einführung einer<br />
Alkylgruppe durch <strong>de</strong>n +I-Effekt dieser Gruppe noch erhöht wird, wird bei <strong>de</strong>r<br />
Alkylierung meistens Mehrfachumsetzung beobachtet. Monoalkylmalonester<br />
sind auf diese Weise nicht rein herstellbar.<br />
Zur Herstellung dieser Produkte verwen<strong>de</strong>t man daher häufig die<br />
Esterkon<strong>de</strong>nsation mit Oxalsäurediestern.<br />
Beispiel: Herstellung von Propylmalonester.<br />
O<br />
OH<br />
171
H 7C 3 CH COOR<br />
COOR<br />
COOR<br />
H<br />
H 7C 3<br />
H 7C 3<br />
O<br />
H 7C 3<br />
O<br />
C<br />
RO<br />
C<br />
RO<br />
C<br />
C<br />
C<br />
CH<br />
O<br />
OR<br />
COOR<br />
OH �<br />
�<br />
C O<br />
OR<br />
C O<br />
C O<br />
�<br />
O R<br />
OR<br />
C O<br />
C O<br />
�<br />
H<br />
H<br />
�<br />
H7C3 CH COOR<br />
- �<br />
25<br />
H 7C 3<br />
H 7C 3<br />
H 7C 3<br />
O<br />
C<br />
RO<br />
C<br />
CH<br />
O<br />
OR<br />
C O<br />
COOR<br />
C<br />
OR<br />
C O<br />
C O<br />
COOR<br />
CH<br />
COOR<br />
Der bei <strong>de</strong>r Kon<strong>de</strong>nsation von Valeriansäureester mit Oxalsäurediester zunächst<br />
entstehen<strong>de</strong> β-Carbonyloxalester erlei<strong>de</strong>t bereits bei geringer Wärmezufuhr<br />
Decarbonylierung.<br />
H<br />
172
Acetessigestersynthese:<br />
Eine gleichartige Kettenverlängerung gelingt, wenn man an Stelle <strong>de</strong>s Malonesters<br />
Acetessigester einsetzt und diesen dann <strong>de</strong>r Säurespaltung (Hauptprodukt ist eine<br />
Säure) mit Alkali untewirft:<br />
R' X +<br />
�<br />
COOR<br />
CH<br />
C<br />
CH 3<br />
O<br />
- X �<br />
COOR<br />
R' CH OH �<br />
C<br />
CH 3<br />
O<br />
R' CH 2 COOH<br />
+<br />
CH 3<br />
COOH<br />
Starkes Alkali greift am Carbonylkohlenstoffatom an, so dass in Umkehr <strong>de</strong>r<br />
Bildungsreaktion <strong>de</strong>s Acetessigesters <strong>de</strong>r nunmehr am Methylenkohlenstoff<br />
substituierte Acetessigester in eine Alkylcarbonsäure und Essigsäure gespalten<br />
wird:<br />
H 3C C<br />
R'<br />
�<br />
O<br />
CH COOR<br />
R'<br />
CH COOR<br />
OH �<br />
H 2 O<br />
OH �<br />
H 3C C<br />
OH<br />
O<br />
�<br />
CH COOR<br />
R'<br />
R' CH 2 COOH<br />
- CH 3COOH<br />
Wen<strong>de</strong>t man zur Verseifung Alkali o<strong>de</strong>r Säure in <strong>de</strong>r Kälte an, so erfolgt zuerst eine<br />
Verseifung <strong>de</strong>r Estergruppierung. Die so gebil<strong>de</strong>te β-Ketosäure erlei<strong>de</strong>t<br />
Decarboxylierung unter Bildung eines Methylketons. Diese sogenannte Ketonspaltung<br />
(Hauptprodukt ist ein Keton) ist daher ein interessanter Zugangsweg zu Methylketonen:<br />
173
R'<br />
COOR<br />
CH<br />
C<br />
CH 3<br />
O<br />
H �<br />
E]Z<br />
OH �<br />
(verdünnt)<br />
Kälte<br />
R'<br />
O<br />
CH<br />
C<br />
C<br />
CH 3<br />
O<br />
O<br />
H - CO2 R' CH<br />
CH 3<br />
CH<br />
O<br />
R' CH 2 C<br />
Knoevenagel-Reaktion:<br />
Verbindungen mit aktiven Methylengruppen, wie z.B. Malonester reagieren mit<br />
Al<strong>de</strong>hy<strong>de</strong>n in Gegenwart von Piperidinacetat (Piperidin katalysiert als Base die<br />
Abspaltung eines Protons aus <strong>de</strong>r Methylengruppe <strong>de</strong>s Malonesters) unter Knüpfung<br />
einer C-C-Bindung. Nach Wasserabspaltung (Chance zur Ausbildung eines<br />
konjugierten Systems) und Decarboxylierung entsteht eine α,β-ungesättigte<br />
Carbonsäure:<br />
COOR<br />
C<br />
��<br />
H<br />
COOR<br />
+ H �<br />
- H2O +<br />
O<br />
R' C<br />
R' CH<br />
H<br />
CH<br />
�<br />
R' CH<br />
H<br />
C<br />
COOR<br />
COOR<br />
H �<br />
-<br />
O<br />
�<br />
COOR<br />
COOR<br />
R'<br />
ROOC<br />
CH<br />
C<br />
H �<br />
COOR<br />
R' CH<br />
CH<br />
+ H �<br />
O<br />
O<br />
- CO 2<br />
- 2 ROH<br />
H<br />
CH 3<br />
H<br />
COOR<br />
COOR<br />
R' CH CH COOH<br />
174
Reformatsky-Rektion:<br />
Eine weitere Metho<strong>de</strong> zur Herstellung ungesättigter Fettsäuren ausgehend von<br />
Al<strong>de</strong>hy<strong>de</strong>n und <strong>de</strong>r Kettenverlängerung um 2 C-Atome ist die Reformatsky-Reaktion.<br />
Bromessigester reagiert mit Zink unter Bildung einer metallorganischen<br />
Verbindung, die Al<strong>de</strong>hy<strong>de</strong>, nicht aber Ester (geringere Carbonyaktivität) ähnlich<br />
wie eine Grignardverbindung anzugreifen vermag:<br />
Br CH 2 COOR<br />
OH<br />
R' CH CH 2 COOR<br />
Zn<br />
H 2O<br />
BrZn<br />
R'<br />
C<br />
R' CH<br />
CH 2<br />
O<br />
H<br />
OZnBr<br />
CH 2<br />
COOR<br />
COOR<br />
Die so gebil<strong>de</strong>ten β-Hydroxyester sind sehr leicht unter Bildung eines α,β-ungesättigten<br />
Esters <strong>de</strong>hydratisierbar (treiben<strong>de</strong> Kraft: Ausbildung eines mesomerie-stabilisierten<br />
Systems).<br />
OH<br />
R' CH CH 2 COOR<br />
- H 2O<br />
R' CH CH<br />
COOR<br />
Wer<strong>de</strong>n anstelle <strong>de</strong>r Al<strong>de</strong>hy<strong>de</strong> Ketone eingesetzt, so erhält man Ester, die in β-Stellung<br />
verzweigt sind.<br />
Die Metho<strong>de</strong> ist allerdings nur zur Herstellung nie<strong>de</strong>rmolekularer β-Hydroxyester<br />
geeignet, höhermolekulare Hydroxyester entstehen nur in sehr geringer Ausbeute.<br />
Perkin-Reaktion:<br />
175
Im Acetanhydrid sind die zur funktionellen Gruppe α-ständigen C-H-Bindungen so weit<br />
aktiviert, dass unter schwacher Basenkatalyse (z.B. Natriumacetat) die Ablösung eines<br />
Protons erfolgen kann. Die so erhaltene reaktive Spezies setzt sich mit aromatischen<br />
Al<strong>de</strong>hy<strong>de</strong>n zu α,β-ungesättigten Säuren um:<br />
H 3 C<br />
H 3 C<br />
Ph<br />
Ph<br />
H<br />
C<br />
O<br />
O<br />
C<br />
CH<br />
O<br />
O<br />
C O<br />
O<br />
C<br />
C<br />
O<br />
Aldol-Kon<strong>de</strong>nsation:<br />
CH 2<br />
��<br />
CH 2<br />
+ CH 3 COO �<br />
CH 3<br />
C O<br />
O<br />
CH 3<br />
COO �<br />
+<br />
- AcO �<br />
Ph<br />
H 2 C �<br />
H 3C<br />
C<br />
H<br />
C<br />
O<br />
��<br />
O<br />
H<br />
C<br />
CH 2<br />
H 3C<br />
O<br />
O<br />
C O<br />
C O<br />
O<br />
C O<br />
Ph CH CH COOH<br />
176
Acetal<strong>de</strong>hyd kann unter schwacher Basenkatalyse ein aktiviertes Proton<br />
abspalten:<br />
B �<br />
+<br />
H<br />
CH 2<br />
C<br />
O<br />
H<br />
- HB<br />
�<br />
CH2 C<br />
O<br />
H<br />
CH 2<br />
Das mesomeriestabilisierte Anion vermag mit <strong>de</strong>m Carbonylkohlenstoffatom eines<br />
zweiten Moleküls unter Bindungsspaltung zu reagieren:<br />
CH 3<br />
C<br />
+ H �<br />
- H 2O<br />
O<br />
H<br />
H B<br />
+<br />
CH 2<br />
C<br />
H 3C CH CH<br />
O<br />
H<br />
�<br />
C<br />
O<br />
H<br />
H 3C<br />
O H<br />
C<br />
H<br />
B �<br />
CH 2<br />
Das so gebil<strong>de</strong>te Alkoholatanion nimmt ein Proton auf und reagiert unter<br />
Wasserabspaltung zu einem α,β-ungesättigten Al<strong>de</strong>hyd. Bei Gegenwart stärkerer<br />
Basen kann das Reaktionsprodukt, ein „vinyloger“ Acetal<strong>de</strong>hyd, unter<br />
neuerlichem Umsatz mit einem Acetal<strong>de</strong>hydmolekül weiter reagieren, so dass<br />
Kon<strong>de</strong>nsationsprodukte entstehen:<br />
H3C CH CH C + CH3COO H<br />
�<br />
O<br />
+<br />
�<br />
CH 3<br />
CH 2<br />
C<br />
H<br />
O<br />
C<br />
C<br />
O<br />
H<br />
O<br />
H<br />
CH<br />
O<br />
CH C<br />
H<br />
+ CH3COOH +H �<br />
- H 2 O<br />
H3C CH CH CH CH C<br />
+<br />
CH 3<br />
C<br />
O<br />
H<br />
usw.<br />
+H �<br />
- H 2 O<br />
O<br />
H<br />
�<br />
177
Die Reaktion ist nicht auf Acetal<strong>de</strong>hyd beschränkt. Höhere Al<strong>de</strong>hy<strong>de</strong> bil<strong>de</strong>n<br />
Verbindungen, die am α-C-Atom verzweigt sind.<br />
Ester-Kon<strong>de</strong>nsation (Claisen-Kon<strong>de</strong>nsation):<br />
Wird an Stelle von Acetal<strong>de</strong>hyd Essigester mit einer starken Base behan<strong>de</strong>lt, so erfolgt<br />
ebenfalls Abstraktion eines Protons:<br />
H CH2 C<br />
Na<br />
O<br />
�<br />
+ O C2H5 OC2H5 �<br />
CH2 C<br />
�<br />
Na �<br />
(1) (2) (3)<br />
O<br />
OC 2H 5<br />
+ C 2H 5OH<br />
Das Anion reagiert wie das aus Acetal<strong>de</strong>hyd entstan<strong>de</strong>ne Reaktionsprodukt mit <strong>de</strong>m<br />
Carbonylkohlenstoffatom eines zweiten Moleküls:<br />
C<br />
O<br />
OC2H5 Na<br />
�<br />
CH2 C<br />
O<br />
OC2H5 �<br />
H3C +<br />
Na<br />
O<br />
H3C C CH2 OC2H5 C<br />
�<br />
�<br />
(3) (4)<br />
O<br />
OC 2 H 5<br />
In diesem Zwischenprodukt ist eine relativ leicht als Anion abspaltbare OR �<br />
-Gruppe<br />
vorhan<strong>de</strong>n, die von <strong>de</strong>m negativ gela<strong>de</strong>nen Sauerstoffatom aus <strong>de</strong>m Molekülverband<br />
herausgedrängt wird.<br />
�<br />
O<br />
Na �<br />
H3C C C<br />
CH 2<br />
OC 2H 5<br />
(4)<br />
O<br />
OC 2H 5<br />
O<br />
H3C C<br />
�<br />
CH C<br />
O<br />
OC 2H 5<br />
+<br />
O<br />
H3C C C<br />
+<br />
CH 2<br />
�<br />
Na O C2H5 �<br />
Na �<br />
O<br />
(5)<br />
O<br />
H3C C C<br />
CH 2<br />
+ EtOH<br />
OC 2H 5<br />
O<br />
�<br />
OC 2H 5<br />
178
Die zunächst gebil<strong>de</strong>te β-Dicarbonylverbindung (5) reagiert als die schwächere Base<br />
mit <strong>de</strong>r Alkoholat-Base (H5C2O �<br />
) unter Protonenabgabe. Dabei entsteht ein<br />
mesomeriestabilisiertes Anion (6) <strong>de</strong>s β-Ketosäureesters, d.h. es entsteht bei <strong>de</strong>r<br />
Reaktion sofort die Natriumverbindung <strong>de</strong>s β-Ketosäureester, so dass ein Äquivalent<br />
Natrium eingesetzt wer<strong>de</strong>n muß. Alkohol braucht nur in geringeren Mengen zum<br />
Starten <strong>de</strong>r Reaktion eingesetzt zu wer<strong>de</strong>n, da er im Laufe <strong>de</strong>r Reaktion gebil<strong>de</strong>t wird.<br />
Die Bildung <strong>de</strong>s mesomeriestabilisierten Enolatanions (6) ist be<strong>de</strong>utend für <strong>de</strong>n<br />
gesamten Reaktionsablauf, da dadurch das Gleichgewicht nach rechts<br />
verschoben wird. Die Gleichgewichtsreaktion zur Bildung <strong>de</strong>s Anions (3) liegt<br />
nämlich stärker auf <strong>de</strong>r linken Seite.<br />
Daher reagieren Ester <strong>de</strong>r Formel R2CH-COOC2H5 nicht, obwohl ein α-ständiges<br />
H-Atom zur Bildung <strong>de</strong>s Anions (3) vorhan<strong>de</strong>n ist, <strong>de</strong>nn im Kon<strong>de</strong>nsationsprodukt<br />
R 2CH<br />
O<br />
C<br />
CR 2<br />
C<br />
O<br />
OC 2H 5<br />
ist keine Möglichkeit zur Bildung eines Enolations gegeben (Fehlen von α-ständigen H-<br />
Atomen).<br />
Einwirkung von Ethylenoxid auf Grignardverbindungen:<br />
Grignardverbindungen reagieren mit Ethylenoxid unter Bildung primärer Alkohole.<br />
C 4 H 9 Mg Br + H 2 C CH 2<br />
H 2O<br />
C 4H 9<br />
CH 2<br />
O<br />
CH 2<br />
OH<br />
C 4 H 9<br />
CH 2<br />
CH 2<br />
OMgBr<br />
Die Reaktion verläuft nur mit schlechter Ausbeute. Sie hat daher wenig praktische<br />
Be<strong>de</strong>utung.<br />
179
20. Kettenverlängerung um drei und mehr C-Atome:<br />
In <strong>de</strong>n voangegangenen Kapiteln wur<strong>de</strong>n bereits folgen<strong>de</strong> Synthesemöglicbkeiten<br />
beschrieben:<br />
1. Die Grignard-Reaktion, mit <strong>de</strong>r aus Carbonylverbindungen und Alkyl- o<strong>de</strong>r<br />
Arylhalogeni<strong>de</strong>n Verbindungen variabler C-Zahl synthetisierbar sind.<br />
2. Die Wurtz‘sche Kohlenwasserstoffe-Synthese<br />
3. Die Acylierung von Aromaten nach Frie<strong>de</strong>l-Crafts und anschließen<strong>de</strong><br />
Clemmensen- o<strong>de</strong>r Wolff-Kishner-Reduktion zur Einführung von<br />
Alkylketten in Aromaten.<br />
20.1 Michael-Addition:<br />
In α,β-ungesättigten Carbonylverbindungen bil<strong>de</strong>n die π-Elektronen eine sich über das<br />
ganze ungesättigte System erstrecken<strong>de</strong> Elektronenwolke. Die Eigenschaften <strong>de</strong>s<br />
Carbonylkohlenstoffatoms wer<strong>de</strong>n dadurch nahezu ungeschwächt auf das β-C-Atom<br />
übertragen:<br />
β<br />
R C<br />
H<br />
H<br />
α<br />
C C<br />
R<br />
O<br />
�<br />
R C<br />
H<br />
H<br />
δ+<br />
H<br />
δ−<br />
R C C C O<br />
H<br />
C C<br />
Diese Verbindungen wer<strong>de</strong>n als Vinyloge (Vinyl-Homologe) <strong>de</strong>r entsprechen<strong>de</strong>n<br />
Carbonylverbindung bezeichnet. Mit nucleophilen Reagenzien (Basen) reagieren<br />
vinyloge Carbonylverbindungen unter Addition an <strong>de</strong>r C=C-Doppelbindung:<br />
R<br />
R<br />
O<br />
�<br />
180
R<br />
R CH CH C O<br />
B �<br />
HB<br />
B �<br />
-<br />
R<br />
B<br />
CH<br />
CH<br />
R<br />
C O<br />
R<br />
B<br />
CH<br />
CH<br />
R<br />
C O<br />
R<br />
H<br />
R<br />
B<br />
CH CH2 C O<br />
Im Prinzip liegen in vinylogen Verbindungen zwei Reaktionszentren vor: Die C=O-<br />
Gruppe und die vinyloge C=C-Doppelbindung. Mit wenig polarisierbaren Nucleophilen<br />
(sogenannten „harten“ Nucleophilen) erhält man tatsächlich überwiegend einen Angriff<br />
an die C=O-Bindung.<br />
Mit gut polarisierbaren Nucleophilen ("weichen Nucleophilen") erfolgt <strong>de</strong>r Angriff am<br />
vinylogen C-Atom.<br />
Insbeson<strong>de</strong>re <strong>de</strong>r basekatalysierte Angriff von C-H-aci<strong>de</strong>n 'Verbindungen an<br />
vinyloge Carbonylverbindungen wird als Michael-Addition im engeren Sinne<br />
bezeichnet. Die Michael-Addition hat einen weiten Anwendungsbereich in <strong>de</strong>r<br />
organischen Synthese. Als C-H-aci<strong>de</strong> Verbindungen wer<strong>de</strong>n Ester, Ketone, Nitrile<br />
und Nitroverbindungen verwen<strong>de</strong>t, hauptsächlich:<br />
β-Dicarbonylverbindungen (z.B. Malonester)<br />
Cyanessigester (N≡CH2-COOR)<br />
Benzylcyanid (Ph-CH2-C≡N)<br />
Gebräuchliche vinyloge Carbonylverbindungen sind<br />
Acrylsäuremethylester (H2C=CH-COOCH3)<br />
Methylvinylketon<br />
H 2C<br />
CH<br />
O<br />
C<br />
CH 3<br />
usw.<br />
Malonester reagiert z.B. mit Acrylsäureester (vinyloge Carbonylverbindung) in <strong>de</strong>r<br />
folgen<strong>de</strong>n Weise:<br />
�<br />
181
ROOC<br />
ROOC<br />
ROOC<br />
ROOC<br />
CH 2<br />
CH CH 2<br />
+ OR �<br />
- ROH<br />
CH<br />
ROOC<br />
ROOC<br />
C<br />
OR<br />
CH<br />
�<br />
H 2C<br />
� O + ROH<br />
- OR �<br />
CH<br />
ROOC<br />
ROOC<br />
C<br />
O<br />
OR<br />
CH CH 2<br />
CH 2<br />
Nach Hydrolyse <strong>de</strong>s Esters kann das entstan<strong>de</strong>ne β-Dicarbonyl<strong>de</strong>rivat durch Erhitzen<br />
(ca. 160°C) <strong>de</strong>carboxyliert wer<strong>de</strong>n und es bil<strong>de</strong>t sich Glutarsäure:<br />
ROOC<br />
ROOC<br />
CH CH 2<br />
Hitze<br />
- CO 2<br />
CH 2<br />
C<br />
O<br />
OR<br />
ROOC<br />
ROOC<br />
CH CH 2<br />
HOOC CH2 CH2 CH2 COOH<br />
Glutarsäure<br />
Beim Einsatz von alkylsubstituierten Malonestern wer<strong>de</strong>n α,β-alkylverzweigte<br />
Glutarsäure<strong>de</strong>rivate erhalten.<br />
Bei <strong>de</strong>r Umsetzung α,β-ungesättigter Ketone mit Malonester reagiert das entstan<strong>de</strong>ne<br />
Michael-Additionsprodukt im Zuge einer Esterkon<strong>de</strong>nsation unter Ringschluß weiter:<br />
Aus Mesityloxid (1) und Malonester (2) bil<strong>de</strong>t sich auf diese Weise 4-<br />
Carboxyethyl-5,5-dimethyl-cyclohexan-1,3-dion (3).<br />
CH 2<br />
C<br />
O<br />
OH<br />
C<br />
O<br />
OR<br />
182
ROOC<br />
CH 2<br />
ROOC<br />
Malonester<br />
ROOC<br />
ROOC<br />
H 3 C<br />
H 3C<br />
CH<br />
CH 2<br />
C<br />
+<br />
CH 3<br />
H 3 C<br />
H 3 C<br />
C CH 2<br />
CH 3<br />
O<br />
C<br />
CH<br />
COOR<br />
�<br />
CH2 C<br />
C<br />
O<br />
C<br />
CH<br />
CH 3<br />
O<br />
C<br />
Mesityloxid<br />
O<br />
OR<br />
- OR �<br />
(1)<br />
CH 3<br />
+ OR �<br />
+ OR �<br />
Esterkon<strong>de</strong>nsation<br />
H 3C<br />
H 3C<br />
CH 2<br />
C<br />
O<br />
C<br />
CH<br />
C<br />
COOR<br />
CH 2<br />
Durch Decarboxylierung wird aus (3) Dimedon (4) (5,5-Dimethyldihydresorcin) erhalten:<br />
H 3C<br />
H 3C<br />
CH 2<br />
C<br />
O<br />
C<br />
CH<br />
COOR<br />
CH 2<br />
C<br />
O<br />
(3)<br />
1. Verseifung<br />
2. Hitze<br />
- CO 2<br />
O<br />
C<br />
O<br />
(3)<br />
C<br />
Dimedon<br />
Dimedon besitzt eine hohe C-H-Aktivität und reagiert mit Formal<strong>de</strong>hyd in folgen<strong>de</strong>r<br />
Weise:<br />
O<br />
183
OH<br />
C<br />
Dimedon<br />
Enol<br />
O<br />
O<br />
C<br />
H H<br />
- H 2 O<br />
O<br />
O<br />
CH 2<br />
Diese Reaktion kann zur gravimetrischen Bestimmung von Formal<strong>de</strong>hyd<br />
verwen<strong>de</strong>t wer<strong>de</strong>n.<br />
Die Kombination von Michael-Addition und Ester-o<strong>de</strong>r Aldolkon<strong>de</strong>nsation wird häufig<br />
bei Naturstoff-Synthesen angewandt, z.B. bei <strong>de</strong>r Robinson-Synthese zum Aufbau <strong>de</strong>s<br />
Steroidgrundgerüsts:<br />
CH 2<br />
O CH 3<br />
OR �<br />
+<br />
O<br />
H<br />
O<br />
CH 3<br />
CH 2<br />
CH 2<br />
O<br />
CH 3<br />
OH<br />
O<br />
OR �<br />
- H 2O<br />
Bei Verbindungen mit zwei konjugierten Doppelbindungen zur Carbonylgruppe<br />
überwiegt die 1,6-Addition gegenüber <strong>de</strong>r 1,4-Addition:<br />
O<br />
O<br />
O<br />
CH 2<br />
CH 3<br />
O<br />
O<br />
CH 3<br />
O<br />
CH 3<br />
O<br />
184
H 3C<br />
H 3C<br />
EtOOC<br />
H H3C 3C<br />
CH CH CH CH C<br />
O<br />
OCH 3<br />
CH CH CH C<br />
CH<br />
CH 2<br />
COOEt<br />
CH CH CH C<br />
EtOOC<br />
CH<br />
+<br />
CH 2<br />
COOEt<br />
O<br />
O<br />
OCH 3<br />
OCH 3<br />
CH 2<br />
COOEt<br />
COOEt<br />
72 %<br />
Häufig ist die Michael-Addition auch Folgereaktion z.B. einer Knoevenagel-Reaktion:<br />
O<br />
COOEt<br />
H3C CH2 C +<br />
H<br />
CH2 COOEt<br />
CH 2<br />
COOEt<br />
COOEt<br />
Michaeladdition<br />
EtOOC<br />
EtOOC<br />
HOOC<br />
CH<br />
CH 2<br />
CH<br />
OR �<br />
CH 2<br />
CH 3<br />
CH<br />
CH 2<br />
CH 3<br />
CH<br />
CH 2<br />
H 3 C<br />
COOEt<br />
COOEt<br />
CH 2<br />
COOH<br />
8 %<br />
C<br />
C<br />
1. Verseifung<br />
2. Hitze<br />
- CO 2<br />
3-Ethylpentandisäure<br />
(β<br />
-Ethylglutarsäure)<br />
COOEt<br />
COOEt<br />
185
20.2. Stobbe-Kon<strong>de</strong>nsation:<br />
Aus Bernsteinsäureestern kann durch Einwirkung von Alkoholat (z.B. Kalium-t-butylat)<br />
ein Proton eliminiert wer<strong>de</strong>n. Setzt man ein Keton zu, so reagiert dieses über ein<br />
isolierbares Paraconsäure<strong>de</strong>rivat zu einem Alkyli<strong>de</strong>nbernsteinsäure-Halbester:<br />
COOEt<br />
CH 2<br />
CH 2<br />
COOEt<br />
R<br />
R<br />
R<br />
O<br />
R<br />
O<br />
K � �<br />
O C(CH3) 3<br />
COOEt<br />
H<br />
O<br />
�<br />
COOEt<br />
�<br />
OEt<br />
O<br />
COOEt<br />
�<br />
CH<br />
CH 2<br />
- OEt �<br />
COOEt<br />
R<br />
R<br />
R<br />
H 3C<br />
R<br />
O<br />
C<br />
O<br />
CH 3<br />
COOEt<br />
H<br />
Paraconsäure<strong>de</strong>rivat<br />
C C<br />
R<br />
O<br />
COOEt<br />
CH 2<br />
R<br />
C<br />
O<br />
�<br />
O<br />
COOEt<br />
C<br />
CH 2<br />
C<br />
KO t Bu<br />
COO �<br />
K �<br />
Dieser Halbester liefert bei <strong>de</strong>r Verseifung unter Decarboxylierung die β,γ-ungesättigte<br />
Carbonsäure im Gleichgewicht mit <strong>de</strong>m entsprechen<strong>de</strong>n γ-Lacton, das mit<br />
Katalysatoren und Wasserstoff zur gesättigten Carbonsäure reduziert wird:<br />
OEt<br />
186
R<br />
R<br />
R<br />
R<br />
C C<br />
COOEt<br />
CH 2<br />
COO �<br />
K �<br />
C CH CH2COOH HBr / HOAc<br />
H2O - CO2 - EtOH<br />
- KBr<br />
Kat.<br />
20.3 Hünigsynthese (Enamin-Synthese):<br />
H 2<br />
R<br />
R<br />
R<br />
CH<br />
R<br />
O<br />
CH 2<br />
O<br />
CH COOH<br />
Eine wichtige Metho<strong>de</strong> zur gleichzeitigen Einführung von 5 und 6 C-Atomen ist die<br />
Hünig-Synthese. Zunächst wird aus Cyclohexanon o<strong>de</strong>r Cyclopentanon und Morpholin<br />
das Enamin hergestellt:<br />
O<br />
- H 2O<br />
[H �<br />
@<br />
HN<br />
O<br />
N<br />
O<br />
Morpholinocyclohexen<br />
Dieses Enamin kann acyliert (Elektrophiler Angriff eines Säurechlorids) wer<strong>de</strong>n und<br />
durch Verseifung entsteht aus dieser Verbindung ein β-Diketon, das wie<strong>de</strong>rum durch<br />
Säurespaltung in eine 6- bzw. 7-Ketosäure überführbar ist.<br />
OH<br />
N<br />
O<br />
187
-<br />
N<br />
+<br />
O<br />
Cl<br />
H2O / [H �<br />
@<br />
HN<br />
C<br />
R<br />
O<br />
O<br />
C<br />
��<br />
�<br />
N<br />
R<br />
Cl �<br />
Cl �<br />
Cl �<br />
O<br />
C<br />
OH �<br />
R<br />
O<br />
R C<br />
(CH 2) 5<br />
COOH<br />
Die endständige Ketofunktion läßt sich durch Wolff-Kishner-Reduktion entfernen, so<br />
dass auf diese Weise - ausgehend von einem Säurechlorid - eine um 5 bzw. 6 C-<br />
Atome längere Carbonsäure zugänglich ist.<br />
O<br />
R C<br />
(CH2) 5 COOH R (CH2) 6 COOH<br />
20.4 Umsetzung von Cyclopentanon o<strong>de</strong>r Cyclohexanon mit Grignard-Verbindungen:<br />
In Cyclohexanon und Cyclopentanon können durch Grignard-Reaktion beliebige<br />
Alkylreste eingeführt wer<strong>de</strong>n. Die so gebil<strong>de</strong>ten tertiären Alkohole sind durch<br />
Chromsäure in Eisessig oxidativ zu Ketosäuren spaltbar:<br />
O<br />
HO R<br />
RMgX CrO3 AcOH<br />
O<br />
R C<br />
(CH 2) 4<br />
COOH<br />
188
In Analogie zur Hünig-Synthese erhält man in diesem Falle ausgehend von einem<br />
Halogenalkan eine entsprechen<strong>de</strong> Kettenverlängerung.<br />
20.5 Oxidative Veknüpfung von Monoacetylenen (Glaser-Synthese):<br />
Bei <strong>de</strong>r Untersuchung <strong>de</strong>r Eigenschaften von Phenylacetylen (Ph-C≡C-H) fand Glaser<br />
(1869), dass sich diese Verbindung beim Durchleiten von Sauerstoff durch eine<br />
alkoholisch-ammoniakalische Lösung bei Anwesenheit äquivalenter Mengen Kupfer(I)chlorid<br />
zu Diphenyldiacetylen dimerisiert; daneben entsteht Kupfer(I)-oxid:<br />
2 Ph C CH + CuCl<br />
½ O 2<br />
ammoniakalische<br />
Lösung<br />
Ph C C C C Ph + Cu 2O<br />
2Ph C C Cu<br />
Der Mechanismus dieser Reaktion wird so ge<strong>de</strong>utet, dass intemediär gebil<strong>de</strong>te Radikal<br />
(Ph-C≡C • ) unter Bildung <strong>de</strong>s Endproduktes rekombiniert.<br />
Diese Synthese wur<strong>de</strong> mehrfach modifiziert und verbessert:<br />
2<br />
1. Bei Verwendung von Pyridin/Methanol als Lösungsmittel genügen<br />
katalytische Mengen Kupfer(I)-chlorid. Bei <strong>de</strong>r Umsetzung von 2-Methyl-3-butin-2ol<br />
wur<strong>de</strong> eine Ausbeute von 90 % erzielt:<br />
H 3C<br />
CH 3<br />
C<br />
OH<br />
C CH<br />
½ O 2<br />
[CuCl]<br />
Pyridin/MeOH<br />
CH 3<br />
H3C C C C C C C<br />
OH<br />
CH 3<br />
OH<br />
90 %<br />
CH 3<br />
2. Bei <strong>de</strong>r Umsetzung von 1-Alkinen mit <strong>de</strong>m entsprechen<strong>de</strong>n Brom<strong>de</strong>rivat<br />
(R-C≡C-Br), das aus ersterem mit Hypobromit zugänglich ist, wer<strong>de</strong>n ebenfalls<br />
nur katalytische Mengen Kupfersalz benötigt:<br />
189
NaOBr<br />
Ph C CH Ph C C<br />
Ph C CH<br />
- HBr<br />
Br<br />
Ph C C C C Ph<br />
Diese Reaktion wird in einer wäßrigen Ethylaminlösung durchgeführt.<br />
20.6 Kolbe-Synthese:<br />
Nach Kolbe (1849) sind symmetrische Kohlenwasserstoffe durch Elektrolyse <strong>de</strong>r<br />
Alkalisalze von Carbonsäuren zugänglich:<br />
2 H 3C CH 2 COONa 2 CH 3CH 2COO �<br />
Katho<strong>de</strong>: 2 H �<br />
2 H 2O 2 H �<br />
H �<br />
Ano<strong>de</strong>: 2 CH 3CH 2COO �<br />
H 2<br />
2+ �<br />
2 CH 3 CH 2 C<br />
2 CH3CH2COO � �<br />
2 CH3CH2 �<br />
2 CH3CH2 + 2 Na �<br />
O<br />
O�<br />
+ 2 CO 2<br />
H 3C CH 2 CH 2 CH 3<br />
2H 3C CH 2 COONa + 2 H 2O H 3C CH 2 CH 2 CH 3<br />
+ 2 e �<br />
+ 2 NaOH + H 2 € + 2 CO 2 €<br />
Das Carboxylat-Anion wird an <strong>de</strong>r Ano<strong>de</strong> entla<strong>de</strong>n. Das zunächst entstehen<strong>de</strong><br />
Carboxyl-Radikal bil<strong>de</strong>t unter CO2-Abspaltung ein Alkylradikal, das zum<br />
Kohlenwasserstoff dimerisiert.<br />
Der Einsatz von Salzgemischen (RCOONa / R´COONa) führt zu schwer trennbaren<br />
Gemischen von R-R, R-R´ und R´-R´, so dass - wie bei <strong>de</strong>r Wurtz'schen Synthese - nur<br />
die Herstellung symmetrischer Kohlenwasserstoffe sinnvoll ist.<br />
21. Aufbau mehrkerniger aromatischer Verbindungen<br />
190
21.1 Einleitung und Nomenklatur<br />
Mehrkernige Kohlenwasserstoffe können jeweils über eine Einfachbindung<br />
miteinan<strong>de</strong>r verknüpft sein o<strong>de</strong>r aber über jeweils zwei gemeinsame<br />
Kohlenstoffatome. Die letztere <strong>de</strong>r bei<strong>de</strong>n Verknüpfungsmöglichkeiten nennt<br />
man Anellierung.<br />
7<br />
6<br />
7<br />
6<br />
8<br />
5<br />
1<br />
4<br />
Naphthalin<br />
8<br />
5<br />
9<br />
Fluoren<br />
2<br />
3<br />
1<br />
4<br />
2<br />
3<br />
7<br />
6<br />
8<br />
5<br />
Biphenyl<br />
In<strong>de</strong>n Chrysen<br />
6<br />
7<br />
p-Terphenyl<br />
9<br />
10<br />
Anthracen<br />
5<br />
4<br />
1<br />
4<br />
3<br />
10<br />
8 9<br />
Phenanthren<br />
2<br />
3<br />
2<br />
1<br />
191
Zur Benennung <strong>de</strong>r über eine Einfachbindung verknüpften mehrkernigen Aromaten<br />
wer<strong>de</strong>n die Präfixe Bi, Ter-, Quater-, usw. vor <strong>de</strong>n Namen <strong>de</strong>s Kohlenwasserstoffrestes<br />
gestellt. Die anellierten mehrkernigen Ringe haben zumeist Trivialnamen.<br />
Eine weitere wichtige Verbindungsgruppe stellen die Phenylmethan<strong>de</strong>rivate dar, die<br />
durch Frie<strong>de</strong>l-Crafts-Alkylierung herstellbar sind.<br />
Benzylchlorid<br />
CH 2Cl +<br />
2 + CH2Cl2 AlCl 3<br />
AlCl 3<br />
AlCl 3<br />
CH 2<br />
Diphenylmethan<br />
CH 2<br />
Diphenylmethan<br />
3 + HCCl3CH Triphenylmethan<br />
Vom Triphenylmethan leitet sich eine Reihe von Farbstoffen ab (Malachitgrün;<br />
Kristallviolett).<br />
Das Triphenylmethylradikal (Tritylradikal) war das erste hergestellte freie organische<br />
Radikal (Gomberg, 1900):<br />
192
C �<br />
�<br />
Wegen <strong>de</strong>r vielfältigen Mesomeriemöglichkeiten ist dieses Radikal sehr beständig. In<br />
<strong>de</strong>r Lösung es im Gleichgewicht mit <strong>de</strong>m dimeren Produkt, das sich beim Eindampfen<br />
<strong>de</strong>r Lösung abschei<strong>de</strong>t. Das Dimere hat nicht die Struktur <strong>de</strong>s 1,1,1,2,2,2-<br />
Hexaphenylethans, son<strong>de</strong>rn:<br />
C<br />
C C<br />
21.2 Frie<strong>de</strong>l-Crafts-Acylierung zum Aufbau annellierter Aromaten<br />
Viele Verbindungen dieser Reihe können mit <strong>de</strong>r bekannten Frie<strong>de</strong>l-Crafts-Reaktion<br />
hergestellt wer<strong>de</strong>n.<br />
21.2.1 Naphthalin<strong>de</strong>rivate<br />
Durch Succinoylierung (Umsetzung mit Bernsteinsäureanhydrid) von Benzol entsteht<br />
Naphthalin. Diese auch als Haworth-Synthese bekannte Umsetzung wird zur<br />
Herstellung von Naphthalin selbst natürlich nicht angewandt, stellt aber eine wichtige<br />
Metho<strong>de</strong> zur Herstellung substituierter Naphthaline dar.<br />
β-substituierte Naphthaline sind z.B. durch folgen<strong>de</strong> Syntheseschritte zugänglich:<br />
C<br />
�<br />
193
X<br />
X<br />
X<br />
X = Halogen<br />
Alkyl<br />
OCH 3<br />
O<br />
+ O<br />
O<br />
AlCl 3<br />
HO O HF o<strong>de</strong>r<br />
C Polyphosphorsäure<br />
Pd, Hitze<br />
X<br />
Dehydrierung<br />
(Aromatisierung)<br />
X<br />
HO<br />
O<br />
C<br />
O<br />
O<br />
α− Tetralon<strong>de</strong>rivat<br />
Clemmensen-<br />
Reduktion<br />
Clemmensen-<br />
Reduktion<br />
Hydroaromaten lassen sich am Palladium-Kontakt in <strong>de</strong>r Wärme zu Aromaten<br />
<strong>de</strong>hydrieren.<br />
Durch Grignard-Umsetzung <strong>de</strong>s α-Tetralons o<strong>de</strong>r <strong>de</strong>ssen Derivate sind in 1-Stellung<br />
substituierte Naphthaline bzw. zusätzlich in β‘-Stellung <strong>de</strong>s zweiten Ringes<br />
disubstituierte Derivate herstellbar.<br />
X<br />
194
O<br />
1) Dehydratisierung<br />
2) Aromatisierung<br />
C 2H 5MgBr<br />
CH 2<br />
HO CH 2 CH 3<br />
Nach Veresterung <strong>de</strong>r im ersten Schritt entstehen<strong>de</strong>n Ketosäure gelingt auch auf<br />
dieser Stufe eine Umsetzung mit Grignard-Verbindungen. Da durch die Grignard-<br />
Verbindung auch die Esterfunktion angegriffen wer<strong>de</strong>n kann, müssen exakt<br />
äquimolare Mengen eingesetzt wer<strong>de</strong>n und möglichst die Grignard-Verbindung<br />
zugetropft wer<strong>de</strong>n, damit diese nicht im Überschuß vorliegt. Auf diese Weise<br />
sind ausgehend von mono-substituierten Benzol<strong>de</strong>rivaten 1,6-disubstituierte<br />
Naphthaline zugänglich.<br />
CH 3<br />
195
H 3C<br />
H 3C<br />
H 3C<br />
O<br />
+ O<br />
O OR<br />
C<br />
O<br />
O<br />
C<br />
R'<br />
21.2.2 Phenanthren<strong>de</strong>rivate<br />
O<br />
R'MgX<br />
AlCl 3<br />
H 3C<br />
H 3C<br />
OH 1) HF<br />
2) Clemmensen-<br />
Reduktion<br />
3) Aromatisierung<br />
O<br />
C<br />
O<br />
HO R'<br />
OH<br />
+ ROH<br />
H �<br />
O OR 1) Dehydratisierung<br />
C 2) Hydrolyse<br />
3) Hydrierung<br />
Durch Succinoylierung von Naphthalin bil<strong>de</strong>t sich entsprechend Phenanthren:<br />
H 3C<br />
R'<br />
196
O<br />
C<br />
O<br />
OH<br />
Phenanthren<br />
O<br />
+ O<br />
AlCl 3<br />
Durch Variation <strong>de</strong>r Synthese gelingt auch hier die Herstellung substituierter Derivate.<br />
21.2.3 Anthracen<strong>de</strong>rivate.<br />
Die Umsetzung von Phthalsäureanhydrid mit Benzol<strong>de</strong>rivaten liefert<br />
Anthrachinon<strong>de</strong>rivate:<br />
O<br />
O<br />
HO<br />
C<br />
O<br />
197
H 2SO 4<br />
O<br />
O<br />
O<br />
+<br />
O<br />
O<br />
CH 3 AlCl3<br />
CH 3<br />
Zn/OH �<br />
O OH<br />
Die Anthrachinone sind durch Reduktion mit Zink und Alkali in Anthracen<strong>de</strong>rivate<br />
überführbar:<br />
9-substituierte Anthracene wer<strong>de</strong>n folgen<strong>de</strong>rmaßen gewonnen:<br />
Zn/OH �<br />
O<br />
O<br />
O<br />
HO R<br />
+<br />
COOH<br />
- H 2O<br />
AlCl 3<br />
HF<br />
C<br />
O<br />
O OH<br />
O<br />
R<br />
C<br />
O<br />
CH 3<br />
RMgX<br />
CH 3<br />
198
21.3 Verknüpfung zu Biphenyl<strong>de</strong>rivaten<br />
Die Einwirkung von metallischem Natrium auf Arylhalogeni<strong>de</strong> ergibt in einer <strong>de</strong>r Wurtz-<br />
Reaktion analogen Umsetzung nur geringe Ausbeuten an Biphenyl:<br />
2 Cl + 2 Na<br />
21.3.1 Ullmann-Reaktion<br />
- 2 NaCl<br />
Ullmann fand, dass die Ausbeuten durch Verwendung von Kupferpulver o<strong>de</strong>r<br />
Kupferbronze bei höheren Temperaturen wesentlich verbessert wer<strong>de</strong>n können:<br />
[Cu]<br />
2 H3C Cl<br />
H3C CH3 21.3.2 Gomberg-Bachmann-Reaktion:<br />
Hierbei gibt man zu einem Gemisch bestehend aus einer wäßrigen<br />
Diazoniumsalzlösung und <strong>de</strong>m aromatischen Kohlenwasserstoff unter kräftigem<br />
Rühren (Zweiphasensystem) Natronlauge.<br />
�<br />
Br N N<br />
Cl �<br />
+<br />
NaOH<br />
Im Gegensatz zur Ullmann-Reaktion können mit <strong>de</strong>r Gomberg-Bachmann-Reaktion<br />
auch unsymmetrische Biphenyle hergestellt wer<strong>de</strong>n. Die Ausbeuten sind, bedingt<br />
durch das Arbeiten in einem zweiphasigen System, nur gering.<br />
Die Reaktion verläuft nach einem radikalischen Mechanismus. Das Arylradikal bil<strong>de</strong>t<br />
sich aus Diazohydroxid, das mit Natronlauge aus <strong>de</strong>m Diazoniumsalz entsteht:<br />
Br<br />
199
�<br />
Br N N<br />
Cl �<br />
NaOH<br />
- NaBr<br />
Br<br />
- N 2<br />
N N OH<br />
Br � + OH<br />
�<br />
Die Reaktion <strong>de</strong>s Radikals mit <strong>de</strong>n aromatischen Kohlenwasserstoff erfolgt<br />
wahrscheinlich in zwei Stufen.<br />
� Br +<br />
Br<br />
�<br />
- H �<br />
Br<br />
Das H-Radikal wird durch ein an<strong>de</strong>res Radikal abgefangen (HO • , Ph • ).<br />
Bei Angriff eines ungela<strong>de</strong>nen Radikals ist eigentlich keine dirigieren<strong>de</strong> Wirkung durch<br />
Erstsubstituenten zu erwarten, <strong>de</strong>nnoch wird die bevorzugte Bildung von 2- und 4-<br />
Produkten beobachtet. Dies muß damit erklärt wer<strong>de</strong>n, dass eine Stabilisierung <strong>de</strong>r<br />
radikalischen Übergangsverbindung nur von 2- und 4-ständigen Substituenten (sowohl<br />
von Substituenten 1. Ordnung als auch von Substituenten 2. Ordnung) ermöglicht wird.<br />
Ausgehend von 2-Nitrodiphenylmethan kann auch <strong>de</strong>r Fluoren-Grundkörper aufgebaut<br />
wer<strong>de</strong>n:<br />
H<br />
200
Cu, Zn<br />
O 2N<br />
1) Reduktion<br />
2) Diazotierung<br />
Wird die Verknüpfung eines Diazoniumsalzes mit Kupfer- o<strong>de</strong>r Zinkpulver vorgenommen,<br />
so bezeichnet man diesen Reaktionsschritt auch als Gattermann-Reaktion.<br />
21.3.3 Pschorr Synthese<br />
Die Pschorr-Synthese stellt eine interessante Anwendung <strong>de</strong>r Arylverknüpfung dar. Sie<br />
dient zum Aufbau <strong>de</strong>s Phenanthrengerüstes:<br />
H<br />
C O<br />
NO 2<br />
+<br />
CH 2<br />
COONa<br />
�<br />
N2 Cl �<br />
NO 2<br />
COOH<br />
2-Nitrobenzal<strong>de</strong>hyd wird mit <strong>de</strong>m Natriumsalz <strong>de</strong>r Phenylessigsäure in Gegenwart von<br />
Essigsäureanhydrid analog <strong>de</strong>r Perkin-Synthese umgesetzt. Statt <strong>de</strong>r genannten<br />
Verbindungen können auch jeweils substituierte Derivate eingesetzt wer<strong>de</strong>n. Bei dieser<br />
Umsetzung entsteht hauptsächlich die α-Phenyl-2-nitrozimtsäure, aus <strong>de</strong>r durch<br />
Reduktion <strong>de</strong>r Nitrogruppe und Diazotierung <strong>de</strong>s so gebil<strong>de</strong>ten Amino<strong>de</strong>rivates<br />
schließlich durch Arylverknüpfung die 9-Phenanthrencarbonsäure entsteht:<br />
201
Cu<br />
NO 2<br />
COOH<br />
1) Reduktion<br />
2) Diazotierung<br />
COOH<br />
Weiterhin seien folgen<strong>de</strong> Verknüpfungsreaktionen genannt:<br />
�<br />
N2 Cl �<br />
COOH<br />
1. lodaryle wer<strong>de</strong>n in einer photochemischen Reaktion mit flüssigen aromatischen<br />
Kohlenwasserstoffen verknüpft:<br />
h � ν<br />
H3C , + H3C 2. Aromatische Grignard-Verbindungen reagieren mit Kupfer(II)-halogeni<strong>de</strong>n zu<br />
Biarylverbindungen.<br />
MgX + XMg<br />
CuX 2<br />
+ 2 MgX 2 + Cu<br />
202